Etyn
|
Algemeen | |
|---|---|
| Naam | Etyn |
| Ander name | asetileen |
 |
 |
| Chemiese formule | C2H2 |
| Molêre massa | 26,0 [g/mol] |
| CAS-nommer | 74-86-2[1] |
| Voorkoms | kleurlose gas |
| Reuk | Nie sterk nie; knoffelrig[2] |
| Fasegedrag | |
| Smeltpunt | -80,8 °C[1] |
| Kookpunt | (sublimeer)[1] |
| Digtheid | 1,17 [g/L] (vastestof)[1] |
| Oplosbaarheid | 1.185 [g/L] (water)[2] |
| Dampdruk | 44 [bar] (by 20 °C)[2] |
| Kritieke temperatuur | 35.6 °C[2] |
| Henry se konstante | 4,0 x 10-2[L/mol.atm] 1800 [K][3] |
|
Suur-basis eienskappe | |
| pKa | 15.74 |
|
Veiligheid | |
| Flitspunt | -18 °C[2] |
| Selfontbrandingspunt | 325 °C[2] |
|
Tensy anders vermeld is alle data virstandaardtemperatuur en -druktoestande. | |
| Portaal | |
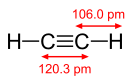
Etynofasetileenmet formuleC2H2is die eenvoudigstealkyn,'n koolstofverbinding met 'n drievoudige C≡C binding.
Dit is 'n gas wat met 'n baie warm vlam kan brand en daarom in branders gebruik word.
Soos ander ongesubstitueerde alkyne het die eindstandige proton die eienskappe van 'n swak suur. Daar is selfs soute wat afgelei is wat hierdie suur, soos kalsiumkarbiedCaC2wat die karbiedioonC2−2([C≡C]2-) bevat. Kalsiumkarbied reageer metwateren stel daarby etyn vry:
Asetileen is 'n kleurlose, ontvlambare gas wat uit kalsiumkarbied en water verkry word. 'n Kilogramkarbiedlewer sowat 300 liter asetileengas. Wanneer asetileen in suurstof brand, word 'n baie warm vlam met 'ntemperatuurvan 3 000 °C verkry, wat deur die hardstestaalkan sny.
Dit word derhalwe ook vir daardie doel en sweiswerk gebruik. Asetileen is 'n giftige gas met ʼn heelwat grotermassaas lug. Saamgepers of verhit, is dit 'n hoogs ontplofbare stof. Dit is 'n baie belangrike grondstof in die chemiese nywerheid en word baie gebruik in die vervaardiging van vinielchloriede vir plastiekgoedere, sintetieserubber,akrilonitriel, kunsvesel- en kleefstof enverf.
Dit word ook gebruik omvitamien Asinteties te berei. Asetileenswart, 'nkoolstofwat verkry word deur die onvolledige verbranding van asetileen, word in droëselbatterye gebruik.
Demonstrasie
[wysig|wysig bron]Verwysings
[wysig|wysig bron]- ↑1,01,11,21,3"Richard L. MyersThe 100 Most Important Chemical Compounds, 2007, "(PDF)(in Engels). p. 52.ISBN978-0-313-33758-1.Besoek op18 Januarie2016.[dooie skakel]
- ↑2,02,12,22,32,42,5"Air products Sout Africa"(PDF)(in Engels).Geargiveer(PDF)vanaf die oorspronklike op 8 Oktober 2018.Besoek op19 Januarie2016.
- ↑Sander.
Bron
[wysig|wysig bron]- Wêreldspektrum,1982,ISBN 0908409435,volume 2, bl. 80

