Енантиомер
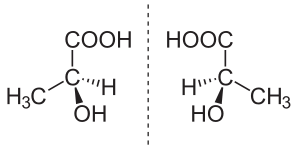
Вхимиятаенантиомер(отгръцки:ἐνάντιος,„противоположен “, иμέρος,„част “) е всеки един от двастереоизомера,демонстриращихиралност:т.е., които са огледални образи един на друг, без да са идентични (например лявата ръка е огледална на дясната, но не е същата, тоест лявата ръкавица не става на дясната ръка).[1]
Органичните съединения, които имат асиметричен хирален въглероден атом, обикновено имат две огледални една на друга структури, наречениенентиоморфи(енентио= противоположен;морф= форма). Оттук този вид оптичнаизомерияе позната катоенантиомерияи играе важна роля въвфармацията,тъй като различни енантиомери на лекарствените субстанции като правило имат различна биологична активност.Енантиочисти съединениясе отнася до вещества, коитов границите на детекциясъдържатмолекулисамо на единия енантиомер.
При еднакви условия енантиомерите имат еднакви физични и химични свойства с изключение на това, че въртятполяризиранатасветлина в еднаква степен, но в различни посоки (проявяват противоположнаоптична активност). Смес отравни частиот оптично активен изомер и неговия енантиомер се наричарацемична смеси не оказва оптично въртене на поляризирана светлина.
Болшинството хирални природни съединения (аминокиселини,монозахариди) съществуват само във вид на един енантиомер. Енантиомерите често показват различно поведение при реакции със субстанции, които също са енантиомери. Тъй като молекулите в живите организми често са енантиомери, то при действието на двата енантиомера върху организма също често се наблюдава различен биологичен ефект. Прилекарстватаобикновено само единият енантиомер допринася за желания физиологичен ефект, докато другият енантиомер е по-слабо активен, неактивен или дори има нежелани или вредни странични ефекти.
Критерии за енантиомер[редактиране|редактиране на кода]
Повечето съединения, които съдържат един или повече асиметричнивъглеродниатома,демонстрират енантиомерия, но се срещат и изключения.
Познати са малко на брой изключения, които иматасиметричен въглерод:който образува химични връзки с четири други атома или групи атоми така, че е възможно тези групи да се подредят по два различни начина. Присъствието на такъв асиметричен въглерод представлява често срещана хиралност, която се наричаточкова хиралностилицентрална хиралност.[2]:pg. 2Асиметричният атом се наричацентър на хиралност.Съединения с един (или нечетен брой) асиметрични атоми са винаги хирални. Обратното, съединения с четен брой асиметрични атоми не винаги са хирални, защото са подредени в огледално-симетрични двойки. Те са известни катомезо съединения.Така напримермезотартаратът имадваасиметрични въглерода, но все пак еоптично неактивен.По подобен начинтранс-циклохексан – 1,4 – дикарбоксилната киселина има асиметрични въглеродни атоми, но притежава вътрешенцентър на симетрия,поради което няма енантиомери.
Примери[редактиране|редактиране на кода]


Вхербицидамецорп (2-(4-хлоро-2-метилфенокси)пропанова киселина),карбоксилната групаи водородния атом при централния C-атом са разменени (екрана ни служи като равнина на симетрията). След завъртането на изомерите на 180 градуса (в същата равнина), двата продължават да са огледални един на друг.
Друг пример е антидепресантът есциталопрам и циталопрам. Циталопрамът е рацемична смес (1:1 (S)-циталопрам и (R)-циталопрам; докато есциталопрамът е чист (S)-енантиомер на циталопрама. Дозите за есциталопрама са 1/2 от тези за циталопрама.
Квазиенантиомери[редактиране|редактиране на кода]
Квазиенантиомерите не са точно енантиомери, но имат такова поведение.[3]
Вижте също[редактиране|редактиране на кода]
Източници[редактиране|редактиране на кода]
- ↑IUPAC, Compendium of Chemical Terminology, 2nd ed. (theGold Book) (1997). Online corrected version: (2006–)enantiomer.
- ↑Karras, Manfred."Synthesis of Enantiomerically Pure Helical Aromatics Such As NHC Ligands and Their Use in Asymmetric Catalysis, PhD Thesis.Charles University, 2018. Посетен на 6 August 2021.
- ↑G.S. Coumbarides, M. Dingjan, J. Eames, A. Flinn, J. Northen and Y. Yohannes, Tetrahedron Lett. 46 (2005), p. 2897er
| Тази страница частично или изцяло представлявапреводна страницатаEnantiomerв Уикипедия на английски. Оригиналният текст, както и този превод, са защитени отЛиценза „Криейтив Комънс – Признание – Споделяне на споделеното “,а за съдържание, създадено преди юни 2009 година – отЛиценза за свободна документация на ГНУ.Прегледайтеисторията на редакциитена оригиналната страница, както и напреводната страница,за да видите списъка на съавторите.
ВАЖНО:Този шаблон се отнася единствено доавторските прававърху съдържанието на статията. Добавянето му не отменя изискването да се посочватконкретни източници на твърденията,които да бъдатблагонадеждни. |
