Alanin
Izgled
| Alanin | |
|---|---|
| Općenito | |
| Hemijski spoj | Alanin |
| Druga imena | 2-Aminopropanska kiselina |
| Molekularna formula | C=3H=7N=1O=2 |
| CAS registarski broj | 206-126-4 |
| Kratki opis | Bijeli prah |
| Osobine1 | |
| Molarna masa | 60,07 g/mol |
| Agregatno stanje | čvrsto |
| Gustoća | 1.424 g/cm3 |
| Tačka topljenja | 258 °C (sublimira) |
| Rastvorljivost | Rastvorljiv |
| 1Gdje god je moguće korištene su SI jedinice. Ako nije drugačije naznačeno, dati podaci vrijede pri standardnim uslovima. | |
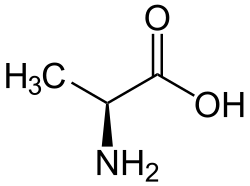


Alanin(al[dehid] + -anin), 2-aminopropionska kiselina – skraćeniceAlaiA– je neesencijalnaaminokiselinasa. Njekovu ugradnju uproteinskilanac kodirajutripletiGCU i GCC.[1][2][3]
Alanin se javlja u vidu dva enantiomera:
- α-alanin – hemijska formula: CH3CH(NH2)COOH jedna je od najčeščih aminokiselina koja gradi molkekuleproteina.Uključen je umetabolizamšećerai organskih kiselina, a jedan je od glavnih sastojaka svilenog vlakna. U slobodnom obliku se javlja ukrvnoj plazmi;
- β-alanin – NH2CH2CH2COOH – se javlja kodbakterijaućelijskom zidui nekim peptidnimantibioticima.Nije proteogen, ali ulazi u sastavkoenzimaA i prirodnih peptida. U nevezanom obliku se nalazi umozgu.
Biosinteza
[uredi|uredi izvor]U procesu biosinteze obično nastaje redukcijskom aminacijompiruvata.Transaminacijaje reverzibilna reakcija pa se alanin vrlo lahko stvara od piruvata; zato sudjeluje u metaboličkim putevimaglikolize,glukoneogenezeiciklusa limunske kiseline.
Također pogledajte
[uredi|uredi izvor]Reference
[uredi|uredi izvor]- ^Doolittle R. F. (1989): Redundancies in protein sequences, in Fasman, G. D., Prediction of Protein Structures and the Principles of Protein Conformation, New York: Plenum, pp. 599–623,ISBN0-306-43131-9.
- ^http://drugsynthesis.blogspot.co.uk/2011/11/laboratory-synthesis-of-l-alanine.html.
- ^Nelson, David L.; Cox, Michael M. (2005), Principles of Biochemistry (4th ed.), New York: W. H. Freeman, pp. 684–85,ISBN0-7167-4339-6.
