Etanol
| Etanol | |
|---|---|
 | |
| Općenito | |
| Hemijski spoj | Etanol |
| Druga imena | Etil-alkohol, špirit |
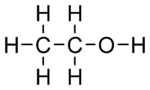
| Molekularna formula | C2H5OH |
| CAS registarski broj | 64-17-5 |
| Kratki opis | bezbojna tekućina karakterističnog mirisa |
| Osobine1 | |
| Molarna masa | 46,07 g/mol |
| Agregatno stanje | tekuće |
| Gustoća | 0,7894 g/cm3 |
| Tačka topljenja | −114,4 °C |
| Tačka ključanja | 78,37 °C |
| Pritisak pare | 58,7 hPa pri 20 °C |
| Rastvorljivost | neograničena u vodi |
| Dipolni moment | 1,69 D (gas) |
| 1Gdje god je moguće korištene su SI jedinice. Ako nije drugačije naznačeno, dati podaci vrijede pri standardnim uslovima. | |
Etanol(poznat još i kaoetilni alkohol,etil-alkohol,špiritili u narodu jednostavnoalkohol) je bezbojna, zapaljiva tekućina karakterističnog mirisa na vino i oštrog ukusa.[1][2].Koristi se umedicinikao sredstvo za sterilizaciju (u koncentracijama od 70-80%), kao komponenta ualkoholnimpićima (obično manje koncentracije) i kao pogonskogorivo(obično veće koncentracije tj preko 80%).
Smatra se da je etanolopijatjer izaziva ovisnost, iako je njegova konzumacija dozvoljena u gotovo svim zemljama svijeta. Međutim, upravljanje prevoznim sredstvima (automobil,avionilibrod) pod uticajem alkohola uglavnom je zakonski zabranjeno.
Etanol se prirodno proizvodi procesomfermentaciješećerapomoćukvascaili petrokemijskim procesima kao što je hidratacija etilena. Ima medicinsku primjenu kaoantiseptikidezinfekciono sredstvo.Koristi se kao hemijski rastvarač i u sintezi organskih jedinjenja, i kao izvor goriva. Etanol se takođe može dehidrirati da bi se dobioetilen,važna hemijska sirovina. Od 2006. godine svjetska proizvodnja etanola iznosila je 51 gigalitra, uglavnom iz Brazila i SAD-a.[3]
Hemijska struktura
[uredi|uredi izvor]Etanol (formula: C2H5OH) spada u n-alkanole. Izveden je izalkanaetana(C2H6) u kojem je jedan atomvodikazamijenjen hidroksilnom funkcionalnom grupom (OH). Zbog toga je imenuetandodan sufiks-olu skladu sa nomenklaturomIUPAC.Nazivetanolse koristi konkrentno za ovaj hemijski spoj, dok sealkoholmože odnositi na cjelokupnu grupu hemijskih spojevaalkoholau koju spadaju, između ostalih,metanol,propanol,butanoli mnogi drugi.
Upotreba
[uredi|uredi izvor]Etanol ima široku primjenu i to u slijedećim oblastima:
- Medicina
- Antiseptic
- Protuotrov
- Medicinski rastvarač
- Farmakologiji
- Rekreacijski
- Gorivo
- Motorno gorivo
- Raketno gorivo
- Grijanje i kuhanje domaćinstva
- Sirovina
- Rastvarač
- Tečnost na niskim temperaturama
Historija
[uredi|uredi izvor]Prvi put čisti etanol je dobioperzijskiliječnik, naučnik, filozof i pisacAbu Bekr Muhammed Ibn Zekerijja al-Raziputemdestilacijevina. Nazvao ga jeAl-Kuhl(cijelo). Ukazao je na sterilizirajuće i dezinfekcijske osobine alkohola i upotrebljavao ga u medicinske svrhe. Uarapskom jezikuالكحلal-kuhlse doslovno koristio kao naziv za šminku (za oči) i prah (antimona), a koristio se kao otapalo.[4]Kasnije je ovaj naziv došao uEvropuprekoŠpanijetokom arapskog osvajanja. U španskom jeziku riječalcoholالكحول se prvobitno koristila za fini, suhi prah, koji su upotrebljavali alhemičari.
Naziv etanol nastao je kao rezultat rezolucije o imenovanju alkohola i fenola koja je usvojena na Međunarodnoj konferenciji o hemijskoj nomenklaturi koja je održana u aprilu 1892. godine uŽenevi,uŠvicarskoj.[5]
Alkohol u ishrani
[uredi|uredi izvor]Alkohol se može pronaći prirodno u zrelomvoćukao proizvod alkoholnog vrenja voćnogšećera. Količine alkohola u različitim proizvodima (u volumenskom udjelu):
- kruh/hljeb: do 0,3 %
- sok odjabuke:do 0,4 %
- bezalkoholno pivo: do 0,5 %
- sok odgrožđa:do 0,6 %
- zrelabanana:do 1 %
- kefir:do 1 %
- pivo
- svijetlo pivo: 1-2,5 %
- puno pivo: 3-5 %
- jako pivo: 6-12 %
- vino:uglavnom od 7-14 %
- vino od meda: 5-15 %
- vino od jabuke: 5,5-7 %
- liker:15-75 %, većinom ispod 30 %
- špirit:od 30-80 %, većinom oko 40 %
Tehnička primjena
[uredi|uredi izvor]Najzanimljivija tehnička primjena je kao pogonsko gorivo. Postoji nekoliko klasa goriva koje sadrže etanol:
- E5 sadrži 5% etanola i 95% benzina. Ima oktansku vrijednost od RON95 oktana. Koristi se bez ikakvih izmjena na benzinskim automobilima.
- E85 sadrži 85% etanola, 14% benzina i 1% aditiva koji izazivaju povraćanje. Ima oktansku vrijednost od RON104 oktana. Da bi se koristilo u automobilima potrebno je dodati motoru 40% više E85 u odnosu na benzin. Ovo se postiže stavljanjem većih brizgaljki umjesto originalnih. Radni opseg goriva je -25oC do +78oC vanjsketemperature.Kod nas ga još nema na pumpama zbog neizgrađene infrastrukture. Cijena u EU je oko 0,7€/litri goriva, što odgovara cijeni od ca 1€/litri. Mana: veća potrošnja E85 ca 30% u odnosu na gorivo.
- E96 sadrži 96% etanola i 4% vode. Ima oktansku vrijednost od RON118 oktana. Da bi se koristilo u automobilima potrebno je dodati motoru 50% više E96 u odnosu na benzin. Ovo se postiže stavljanjem većih brizgaljki umjesto originalnih. Radni opseg goriva je +13oC do +78oC vanjske temperature, dakle zimi je potrebno predzagrijavanje i vazduha i goriva te se u praksi koristi samo kao ljetno gorivo. Ima odlična rashladna svojstva, bolji stepen iskorištenja i čistije izduvne gasove u odnosu na benzin. Cijena u EU je oko 5€/litar. Mana: veća potrošnja od ca 40% u odnosu na gorivo te je akcioni radius automobila kraći.
Etanol kvaliteta E96 se može dobiti na više načina i to:
- Destilacijomifermentacijomvoća, povrća i biološkog otpada (neefikasno i skupo). Ovaj proces je u narodu dobro poznat kao tradicionalno pečenje rakije tj prepečenice.
- Ekstrakcijom iz zemnog gasametanaCH4(industrijska primjena korištena niz godina).
- Sintezom ugljen dioksida i hidrogenskog gasa uz pomoć MoS2ili sličnog katalizatora.
- 2CO2+6H2=C2H5OH
Ovaj proces se vrši na temperaturama preko 255oC.
Također pogledajte
[uredi|uredi izvor]Vanjski linkovi
[uredi|uredi izvor]- Leksikon alkohola (njem.)Arhivirano12. 10. 2007. naWayback Machine
- Uticaj etanola na ljudsko tijelo
- Etanol kao izvor energije
Reference
[uredi|uredi izvor]- ^"Ethanol".PubChem. National Library of Medicine.Pristupljeno 28. 9. 2021.
- ^"Ethyl Alcohol"(PDF).Hazardous Substance Fact Sheet. New Jersey Department of Health.Pristupljeno 28. 9. 2021.
- ^"2008 World Fuel Ethanol Production".Ellisville, Missouri: Renewable Fuels Association. Arhivirano soriginala,24. 9. 2015.Pristupljeno 21. 2. 2011.
- ^Multhauf, Robert P.(1966).The Origins of Chemistry.London: Oldbourne.ISBN9782881245947.p. 205;OED;etymonline
- ^For a report on the 1892 International Conference on Chemical Nomenclature, see:
- Armstrong H (1892)."The International Conference on Chemical Nomenclature".Nature.46(1177): 56–59.Bibcode:1892Natur..46...56A.doi:10.1038/046056c0.
- Armstrong's report is reprinted with the resolutions in English in:Armstrong H (1892)."The International Conference on Chemical Nomenclature".The Journal of Analytical and Applied Chemistry.6(1177): 390–400 (398).Bibcode:1892Natur..46...56A.doi:10.1038/046056c0.
The alcohols and the phenols will be called after the name of the hydrocarbon from which they are derived, terminated with the suffixol(ex. pentanol, pentynol, etc.)

