Dimetilamina
 | |
| Substància química | tipus d'entitat química |
|---|---|
| Massa molecular | 45,058 Da |
| Trobat en el tàxon | |
| Estructura química | |
| Fórmula química | C₂H₇N |
 | |
| SMILES canònic | |
| Identificador InChI | Model 3D |
| Propietat | |
| Densitat | 0,67 g/cm³ (a 44 °F,líquid) |
| PKa | 10,64 (a valor desconegut) |
| Solubilitat | 24 g/100 g (aigua,60 °C) |
| Moment dipolar elèctric | 1,01 D |
| Punt de fusió | −92 °C −92,2 °C |
| Punt d'ebullició | 7 °C (a 760 Torr) 6,88 °C (a 101,325 kPa) |
| Moment dipolar elèctric | 1,01 D |
| Pressió de vapor | 1,7 atm (a 20 °C) |
| Perill | |
| Límit inferior d'explosivitat | 2,8 vol% |
| Límit superior d'explosivitat | 14,4 vol% |
| Límit d'exposició mitjana ponderada en el temps | 18 mg/m³ (10 h,Estats Units d'Amèrica) |
| Punt d'inflamabilitat | 20 °F |
| IDLH | 925 mg/m³ |
| NFPA 704: Standard System for the Identification of the Hazards of Materials for Emergency Response() | |
| Altres | |
| gas inflamable | |
LadimetilaminaoN-metilmetanaminaoDMAés uncompost orgànici unaamina.És ungasincolor,liquat iinflamablederivat de l'amoníacque fa olor depeix.La dimetilamina s'utilitza generalment diluït enaiguaa concentracions fins al 40%.
Química
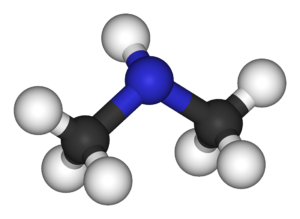
[modifica]La dimetilamina és unaamina secundària.Lamolèculaconsta d'unàtomdenitrogenamb dos substituentsmetilihidrogen.La dimetilamina és unabasei elpKade lasald'amoniCH₃-NH₂+-CH₃ és 10,73, la metilamina té un valor inferior (10,64) i la trimetilamina encara més (9,79). La dimetilamina reacciona ambàcidsper formar sals. L'hidroclorit de dimetilamina és un sòlid blanc inodor amb un punt de fusió de 171,5 °C. La dimetilamina és produïda per reacció catalítica demetanoliamoníacatemperaturesipressióelevades.[1]
Bioquímica
[modifica]Lapanerola germànicautilitza ladimetilaminacom aferomonaper a la comunicació.
LaDMAsofreixnitrosaciósota condicions d'àcid dèbilsde donardimetilnitrosamina.Aquesta substànciacarcinògenaanimal s'ha detectat i s'ha quantificat en mostres d'orinahumanes i també pot sorgir de nitrosació de DMA peròxids de nitrogenpresents enpluja àcidaals països altament industrialitzats[2]
Usos
[modifica]La dimetilamina s'utilitza com a agent de dehairing bronzejant-se, en tints, en accelerants de goma, en sabons i compostos de neteja i com afungicidaagrícola. En indústria la dimetilamina es converteix endimetilformamidai l'òxid de lauril dimetilaminad'agenttensioactiu.És primera matèria en la producció de moltsfàrmacscom ladifenhidraminai també del tabun usat com aarma química.
Referències
[modifica]- ↑Corbin D.R.; Schwarz S.; Sonnichsen G.C. «Methylamines synthesis: A review».Catalysis Today,37, 2, 1997, pàg. 71-102.DOI:10.1016/S0920-5861(97)00003-5.
- ↑Zhang AQ, Mithchell SC, Smith RL (1998) Dimethylamine formation in the rat from various related amine precursors. Food Chem Toxicol 36(11):923-7
Enllaços externs
[modifica]- PropietatsArxivat2013-01-02 atArchive.issegons Air Liquide.com.
- MSDS a airliquide.comArxivat2005-02-06 aWayback Machine.
- MSDS aphyschem.ox.ac.ukArxivat2004-08-18 aWayback Machine.
- methylamines.comArxivat2002-06-19 atArchive.is
- Pherobase.comArxivat2005-05-10 aWayback Machine.
