Aromaticitat

L'aromaticitatés el fenomen en virtut del qual certes substàncies orgàniques cícliques, la composició ponderal de les quals indicainsaturació—tals com elbenzèi els seus derivats—, tenen un conjunt de propietats especials característiques que les distingeixen de les substàncies alifàtiques o alicícliques i en particular de lesolefines,amb les quals, a jutjar per la composició ponderal, haurien d'assemblar-se.
Les propietats que caracteritzen els composts orgànics que presenten aromaticitat són, essencialment:
- una estabilitat termodinàmica elevada, que les entalpies de combustió i d'hidrogenació posen de manifest;
- característiques espectrals peculiars, molt distintes de les de les olefines;
- en uncamp magnètic,existència d'un corrent d'electrons en el cicle, detectable, per exemple, perressonància magnètica nuclear;
- distàncies carboni-carboni intermèdies entre les d'un simple i d'un doble enllaç;
- escassa reactivitat química (per comparació amb les olefines) i en particular gran predomini de les reaccions de substitució respecte a les d'addició.
Evolució històrica
[modifica]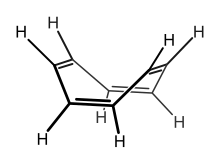

L'aromaticitat o caràcter aromàtic fou atribuïda primerament a la pre sắc ncia d'un sistema tancat d'enllaços dobles conjugats, però la descoberta feta perRichard Willstätter,el 1911, que el ciclooctatetraè té propietats olefíniques normals i la impossibilitat de preparar el ciclobutadiè demostraren que aquesta tesi era inexacta.Robert Robinsonel 1925 suggerí que l'aromaticitat anava lligada a la pre sắc ncia de 6 electrons π i predigué encertadament el caràcter aromàtic de l'anióciclopentadienil.
Així i tot l'aromaticitat no trobà explicació teòrica fins que el físic alemanyErich Hückelaplicà el mètode dels orbitals moleculars el 1931.[1][2]Hückel es dedicà a estudiar la situació general dels anells monocíclics coplanars on cada àtom de l'anell té un orbital p disponible com en el cas del benzè. Els seus càlculs indicaren que els anells coplanars que contenen (4n + 2) electrons π, on n = 0, 1, 2... tenen capes d'electrons tancades com el benzè i, per això, les seves energies de ressonància o deslocalització són altes. En altres paraules, els anells monocíclics coplanars amb 2, 6, 10, 14, 18 i 22 electrons deslocalitzats han de ser aromàtics. És l'anomenadaregla de Hückel.[3]
Compostos heterocíclics
[modifica]En el cas delscomposts heterocíclics,l'aromaticitat de lapiridina,delfurani delpirroleés coneguda des de fa molt de temps, però altres composts heterocíclics amb caràcter aromàtic, que contenen també 10 electrons π, tals com el borazolè i el dibenzotetraazapentalè, han estat preparats posteriorment. Correlativament a la noció d'aromaticitathom ha introduït també les de pseudoaromaticitat i d'antiaromaticitat, la primera aplicada als composts cíclics amb enllaços dobles conjugats que no manifesten estabilització, i la segona a aquells en els quals hi ha desestabilització, és a dir, energia de ressonància negativa.
Referències
[modifica]- ↑Hückel,Erich«Quantentheoretische Beiträge zum Benzolproblem I. Die Elektronenkonfiguration des Benzols und verwandter Verbindungen».Z. Phys.,70, 3/4, 1931, pàg. 204–86..Hückel,Erich«Quanstentheoretische Beiträge zum Benzolproblem II. Quantentheorie der induzierten Polaritäten».Z. Phys.,72, 5/6, 1931, pàg. 310–37..Hückel,Erich«Quantentheoretische Beiträge zum Problem der aromatischen und ungesättigten Verbindungen. III».Z. Phys.,76, 9/10, 1932, pàg. 628–48.
- ↑Hückel,E.Grundzüge der Theorie ungesättiger und aromatischer Verbindungen(en alemany). Berlin: Verlag Chem, 1938, p. 77–85.
- ↑Solomons,T.W.G.Química orgánica(en castellà). Mèxic: Limusa, 1982.ISBN 968-18-0982-3.


