Kyselina šťavelová
| Kyselina šťavelová | |
|---|---|
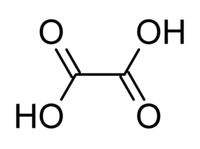 Strukturní vzorec kyseliny šťavelové | |
 | |
| Obecné | |
| Systematický název | ethandiová kyselina |
| Triviální název | kyselina šťavelová |
| Ostatní názvy | kyselina oxalová |
| Latinský název | acidum oxalicum |
| Anglický název | oxalic acid |
| Německý název | Oxalsäure |
| Funkční vzorec | (COOH)2 |
| Sumární vzorec | C2H2O4 |
| Vzhled | bílá krystalická látka |
| Identifikace | |
| Registrační číslo CAS | 144-62-7 |
| EC-no (EINECS/ELINCS/NLP) | 205-634-3 |
| Indexové číslo | 607-006-00-8 |
| Vlastnosti | |
| Molární hmotnost | 90,03 g/mol, 126,07 g/mol (dihydrát) |
| Teplota sublimace | 157 °C |
| Hustota | 1,9 g/cm³ |
| Disociační konstanta pKa | pKa1=1,27, pKa2=4,27 |
| Rozpustnost ve vodě | rozpustná |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H312 H302 H318[2] |
| P-věty | P280 P302+352 P305+351+338[2] |
| R-věty | R21/22 |
| S-věty | (S2) S24/25 |
| NFPA 704 |  1
3
0
|
Některá data mohou pocházet z datové položky. | |
Kyselina šťavelová je karboxylová (organická) kyselina. Jedná se o nejjednodušší dikarboxylovou kyselinu, její systematický název je kyselina ethandiová. Lidový název je „jetelová sůl“. Je obsažena prakticky ve veškerém ovoci a zelenině a způsobuje jejich kyselost. Nachází se například v jahodách, ve větším množství je obsažená ve šťavelu, šťovíku a rebarboře. Soli kyseliny šťavelové se nazývají šťavelany nebo oxaláty. Odtud je také možno vysvětlit název intermediátu Krebsova cyklu, oxalacetátu.
Fyzikální a chemické vlastnosti
[editovat | editovat zdroj]Kyselina šťavelová je pevná, bezbarvá, ve vodě rozpustná, krystalická látka. Je jedovatá a má leptavé účinky. Kyselina šťavelová disociuje ve dvou stupních. V porovnání s monokarboxylovými kyselinami je v prvním stupni kyselina šťavelová kyselejší. Naopak do druhého stupně disociuje neochotně.
| Název | pKa1 | pKa2 |
|---|---|---|
| kyselina mravenčí | 3,75 | – |
| kyselina šťavelová | 1,27 | 4,27 |
| kyselina malonová | 2,85 | 5,70 |
Z tabulky je také vidět, že kyselina šťavelová je z dikarboxylových kyselin nejsilnější. Způsobuje to záporný indukční efekt druhé karboxylové skupiny.
Využití
[editovat | editovat zdroj]Kyselina šťavelová se používá v analytické chemii při titracích jako primární standard, tedy látka, podle níž se určuje přesná koncentrace titračních činidel.[3] Umožňují to její vlastnosti: je to chemicky stálá látka, nereaktivní, neabsorbuje vzdušnou vlhkost, nerozkládá se účinkem světla. Používá se ve včelařství jako akaricid proti roztoči kleštíku včelímu. Dále se používá k bělení dřeva a odstraňování skvrn od rzi z kamene, dřeva, textilu ap. Používá se také do eloxovacích lázní pro dosažení žlutavého odstínu.[4]
Příprava oxidu uhelnatého
[editovat | editovat zdroj]Rozkladem kyseliny šťavelové se připravuje oxid uhelnatý, vedle něj vzniká i oxid uhličitý:
(COOH)2 → CO + CO2 + H2O
Místo kyseliny šťavelové lze pro přípravu oxidu uhelnatého použít kyselinu mravenčí nebo mravenčan barnatý.
Koordinační chemie
[editovat | editovat zdroj]V koordinačních sloučeninách (komplexech) se vyskytuje jako dvouvazný kyslíkatý ligand C2O 2−
4 s předponou oxalato-.
Bezpečnost
[editovat | editovat zdroj]Kyselina šťavelová je zdraví škodlivá. Orální LD50 pro potkany je 475 mg/kg (samci), resp. 375 mg/kg (samice). Hlavním toxickým účinkem je tvorba krystalů šťavelanu vápenatého v ledvinách, což vede k jejich selhání. Vyvázáním vápníku však také může nastat hypokalcémie. Může dojít k neurotoxickým účinkům a/nebo k zástavě srdce. Kyselina šťavelová dráždí kůži, oči a dýchací cesty.[5] Expoziční limit OEL v EU je 1 mg/m3 (TWA).[6]
Člověk denně vyloučí močí několik miligramů kyseliny šťavelové.[7]
Kyselina šťavelová se za horka rozkládá na kyselinu mravenčí a oxid uhelnatý. S některými sloučeninami stříbra reaguje za vzniku výbušného šťavelanu stříbrného.[6]
Odkazy
[editovat | editovat zdroj]Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Oxalic acid na anglické Wikipedii.
- ↑ a b Oxalic acid. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ a b Bezpečnostní list. www.pentachemicals.eu [online]. [cit. 2022-03-09]. Dostupné v archivu pořízeném z originálu dne 2022-12-19.
- ↑ DRBAL, Karel; KŘÍŽEK, Martin. Analytická chemie. 1. vyd. České Bdějovice: Jihočeská univerzita, 1999. 185 s. ISBN 80-7040-352-7. S. 69.
- ↑ ŠKEŘÍK, Jan. Receptář pro elektrotechnika. 1. vyd. Praha: Státní nakladatelství technické literatury, 1966. 219 s. S. 54.
- ↑ Oxalic Acid - Committee for Veterinary Medicinal Products - The European Agency for the Evaluation of Medicinal Products. www.ema.europa.eu [online]. [cit. 2010-12-13]. Dostupné v archivu pořízeném z originálu dne 2014-03-03.
- ↑ a b Oxalic acid - ICSC
- ↑ Wilhelm Riemenschneider, Minoru Tanifuji "Oxalic Acid" in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim.
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu kyselina šťavelová na Wikimedia Commons
Obrázky, zvuky či videa k tématu kyselina šťavelová na Wikimedia Commons

