Aconitsäure
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
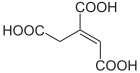
| ||||||||||||||||
| Strukturformeln voncis- undtrans-Aconitsäure | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Aconitsäure | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C6H6O6 | |||||||||||||||
| Kurzbeschreibung | ||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 174,11 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
0,56 g·cm−3(trans)[3] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| pKS-Wert | ||||||||||||||||
| Löslichkeit |
sehr gut in Wasser (400 g·l−1bei 20 °C,trans)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werdenSI-Einheitenverwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten beiStandardbedingungen(0 °C, 1000 hPa). | ||||||||||||||||
Aconitsäureist der Trivialname für1,2,3-Propentricarbonsäure,eineungesättigteorganische Verbindung mit dreiCarbonsäurefunktionen.Ihre Salze heißen Aconitate.
Isomere
[Bearbeiten|Quelltext bearbeiten]Die Aconitsäure kann alscis- oder alstrans-Isomervorliegen.
| Isomere von Aconitsäure | ||
| Name | cis-Aconitsäure | trans-Aconitsäure |
| Andere Namen | (Z)-Aconitsäure | (E)-Aconitsäure |
| Strukturformel | 
| |
| CAS-Nummer | 585-84-2 | 4023-65-8 |
| 499-12-7(unspez.) | ||
| EG-Nummer | 209-564-4 | 223-688-6 |
| 207-877-0 (unspez.) | ||
| ECHA-Infocard | 100.008.697 | 100.021.536 |
| 100.007.162(unspez.) | ||
| PubChem | 643757 | 444212 |
| 309(unspez.) | ||
| Wikidata | Q27104226 | Q27104227 |
| Q288782(unspez.) | ||
Vorkommen
[Bearbeiten|Quelltext bearbeiten]In der Natur kommen beide Isomere der Aconitsäure vor.[4]
Diecis-Aconitsäure ist ein Zwischenprodukt bei der Umsetzung von Citrat zu Isocitrat durch dieAconitaseimCitratzyklusundGlyoxylatzyklus.[4]
Sie kommt in freier Form in der BlumeBlauer Eisenhut[4](Aconitum napellus), aber auch in anderen Pflanzen wie derGemeinen Schafgarbe(Achillea millefolium) und derChristrosevor.
Darstellung
[Bearbeiten|Quelltext bearbeiten]Aconitsäure lässt sich durchDehydratisierungvonCitronensäureunter dem Einfluss von konzentrierter Schwefelsäure herstellen:[7]
Erstmals wurde sie 1875 thermisch bei 170 °C aus Citronensäure hergestellt.[8]
Eigenschaften
[Bearbeiten|Quelltext bearbeiten]Dascis-Isomer bildet sehr leicht einAnhydrid,cis-Aconitanhydrid[9]mit einem Schmelzpunkt von 75 °C.
Siehe auch
[Bearbeiten|Quelltext bearbeiten]Einzelnachweise
[Bearbeiten|Quelltext bearbeiten]- ↑Datenblattcis-AconitsäurebeiAlfa Aesar,abgerufen am 8. Mai 2010(Seite nicht mehr abrufbar).
- ↑Datenblatttrans-AconitsäurebeiAlfa Aesar,abgerufen am 8. Mai 2010(Seite nicht mehr abrufbar).
- ↑abDatenblatttrans-Aconitsäure(PDF) beiCarl Roth,abgerufen am 8. Mai 2010.
- ↑abcdefghEintrag zuAconitsäure.In:Römpp Online.Georg Thieme Verlag, abgerufen am 10. November 2014.
- ↑abcPfendt, L., Dražić, B., Popović, G., Drakulić, B., Vitnik, Ž, Juranić, I.:Determination of all pKavalues of some di- and tri-carboxylic unsaturated and epoxy acids and their polylinear correlation with the carboxylic group atomic charges.In:Journal of Chemical Research.Band2003,S.247–248,doi:10.3184/030823403103173732.
- ↑abDatenblattcis-Aconitic acidbeiSigma-Aldrich,abgerufen am 1. April 2022 (PDF).
- ↑Bruce, W. F.:Aconitic acidIn:Organic Syntheses.17, 1937, S. 1,doi:10.15227/orgsyn.017.0001;Coll. Vol. 2, 1943, S. 12 (PDF).
- ↑B. Pawolleck:Substitutionsproducte der Citronensäure und ein Versuch zur Synthese der letzteren.In:Justus Liebig's Annalen der Chemie.178, 1875, S. 150,doi:10.1002/jlac.18751780203.
- ↑Externe Identifikatoren von bzw. Datenbank-Links zucis-Aconitanhydrid:CAS-Nr.:6318-55-4,EG-Nr.:228-663-3,ECHA-InfoCard:100.026.058,PubChem:65163,Wikidata:Q55972704.


![{\displaystyle \mathrm {C_{6}H_{8}O_{7}\ {\xrightarrow[{}]{H_{2}SO_{4}}}\ C_{6}H_{6}O_{6}\ +\ H_{2}O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/97821ad9295bf688aafbc92ccadb7d1773ec54af)