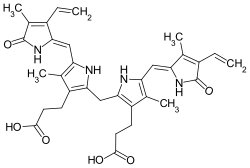
Bilirubin
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Bilirubin | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C33H36N4O6 | ||||||||||||||||||
| Kurzbeschreibung |
rot-oranger Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 584,66 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werdenSI-Einheitenverwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten beiStandardbedingungen(0 °C, 1000 hPa). | |||||||||||||||||||
DasBilirubin(lateinischbilis„Galle “undruber„rot “) ist ein rot-oranges Abbauprodukt desHäm-Anteils des rotenBlutfarbstoffesHämoglobinund damit einGallenfarbstoff.DasPigmentkommt in der Natur nicht nur in Tieren, sondern auch in Pflanzen vor; 2009 wurde es erstmals im Samen vonBaum-Strelitziennachgewiesen.[3] Bilirubin wurde erstmals 1942 durchHans Fischererfolgreich synthetisiert.
Stoffwechsel
[Bearbeiten|Quelltext bearbeiten]Rote Blutkörperchen (Erythrozyten) leben etwa 120 Tage, danach werden sie inLeberundMilzabgebaut. Aus Hämb,dem roten Blutfarbstoff, der beim Abbau anfällt, wird über Zwischenstufen die rot-orange Substanz Bilirubin gebildet. Täglich entstehen ca. 300 mg Bilirubin im menschlichen Organismus, davon rund 70 Prozent aus dem Abbau gealterter Erythrozyten, der Rest aus dem Stoffwechsel anderer Hämoproteine,[4]überschüssig gebildetem Hämoglobin oder aus Vorläuferzellen im Knochenmark.[5]Bilirubin ist gut in Fett (lipophil), aber sehr schlecht in Wasser löslich. Zum Transport im Blut muss es deshalb durch eine lockere, nicht kovalente Bindung anAlbumin,ein Bluteiweiß, gekoppelt werden und wird dannunkonjugiertes Bilirubin(Synonym: indirektes Bilirubin) genannt. Bilirubin kann auch eine kovalente, also feste Bindung mit Albumin eingehen. Diese Form wird dann als Delta-Bilirubin bezeichnet.[6]
Unkonjugiertes Bilirubin wird anschließend in der Leber durch das EnzymUDP-GlucuronosyltransferaseanGlucuronsäuregekoppelt (konjugiert) und in dieser wasserlöslichen Form als „konjugiertes Bilirubin “bezeichnet; dieses hat dann auch eine gelbe Farbe. Konjugiertes Bilirubin und Delta-Bilirubin werden zusammen als „direktes Bilirubin “bezeichnet. Direktes Bilirubin kann mit derGallein denDarmausgeschieden werden. Im Darm wird konjugiertes Bilirubin dann über die ZwischenstufenMesobilirubinogenundStercobilinogen(lateinischstercus„Stuhl “) zuStercobilinüberführt, welches mit für die braunrote Farbe desKotesverantwortlich ist. Etwa 20 Prozent[7]des in den Darm abgegebenen Bilirubins unterliegen alsUrobilinogenund Stercobilinogen einementerohepatischen Kreislauf,werden also nochmals aufgenommen. Der Hauptanteil dagegen wird mit dem Stuhl ausgeschieden. Ein geringer Teil des resorbierten Urobilinogens wird über dieHarnwegeeliminiert. Bei Leberfunktionsstörungen werden diese Produkte vermehrt über denUrinausgeschieden (Bilirubinurie). Hohe Konzentrationen an Bilirubin wirken toxisch.[8]
Ursachen eines abweichenden Bilirubinspiegels
[Bearbeiten|Quelltext bearbeiten]DerNormalwertdes Gesamtbilirubins imSerumliegt unter 21 µmol/l (1,2 mg/dl), bei Neugeborenen dagegen sind Werte bis 340 µmol/l (20 mg/dl) normal. Ist der Serumbilirubinspiegel erhöht (Hyperbilirubinämie), kommt es zurGelbsucht(Ablagerung des Bilirubins in der Haut, griechisch Ikterus), wobei sich ab einem doppelten Normalwert zuerst dieSclera(die weiße Augenhaut) und später die restlicheHautgelb verfärben. Bei ausgeprägter Hyperbilirubinämie verfärben sich durch die massive Einlagerung insGewebeschließlich nahezu alle Organe gelb. Je nach Ursache und Art des angestiegenen Bilirubins gibt es auch andere Symptome, wieHautjucken(lateinisch Pruritus).
BeiMorbus Meulengrachtkann durch eine Abbaustörung des Bilirubins eine Gelbsucht fast ohne Krankheitswert auftreten. DasRotor-SyndromundDubin-Johnson-Syndromsind seltene erbliche Störungen des Bilirubinstoffwechsels.
Auch eineCholestase(Rückstau von Gallenflüssigkeit durchGallensteineoder andere Hindernisse in oder an den Gallenwegen) kann zu einer Erhöhung des Bilirubinwerts führen.[9]
BeiNeugeborenenist ein erhöhter Bilirubinspiegel normal, da das fetale Hämoglobin abgebaut wird, die Leber noch nicht voll arbeitet und die Ausscheidung noch nicht ausreicht (bis zur 30. Schwangerschaftswoche erreicht die Aktivität des Enzyms Glucuronyltransferase, das die Umwandlung in das direkte Bilirubin katalysiert, 0,1 Prozent des Erwachsenenwertes, am Geburtstermin ca. 1 Prozent). So kommt es bei etwa 60 Prozent zu einerNeugeborenengelbsucht.[10]Auf Grund der noch nicht vollständig ausgereiftenBlut-Hirn-Schrankekann es bei Überschreiten alters- und gewichtsabhängiger Grenzwerte zu Entwicklungsstörungen aufgrund einesKernikterus(Ablagerung in denBasalganglienimGroßhirn) kommen. Das in der Haut abgelagerte Bilirubin kann mittelsPhototherapiezum wasserlöslichen Lumirubin umgewandelt und so ausgeschieden werden.
Aber auch der Abbau der Inhaltsstoffe von Medikamenten in der Leber kann zu Erhöhungen des Bilirubinspiegels führen.
Isomere
[Bearbeiten|Quelltext bearbeiten]Die quantitativ vorherrschende Form entsteht durch Aufspaltung des Häm-Rings in der IX-α Position und wird deshalb als (Z,Z)-Bilirubin IX-α bezeichnet. Es liegen jedoch auch andereIsomerevor, die durch Aufspaltung des Häm-Rings in der β-, γ- oder δ-Position generiert werden. Bilirubin IX-α ist bei physiologischempH-Wertnahezu wasserunlöslich, da seineCarboxy-undAminogruppendurch intramolekulareWasserstoffbrückenfixiert sind. Für den Transport in der Zirkulation ist es deshalb nicht-kovalentan Albumin gebunden. Durch die intramolekularen Wasserstoffbrücken entsteht zudem die wannenförmige räumliche Struktur des Bilrubins. Die β-, γ- oder δ-Isomere können keine Wasserstoffbrücken ausbilden. Sie sind daher besser wasserlöslich und könnenrenalausgeschieden werden. Weitere Isomere, z. B. Bilirubin III-α und Bilirubin XIII-α, kommen zwar im Plasma nicht vor, können jedoch in Standardpräparationen in größeren Mengen vorhanden sein.[11]
DieFototherapie,bei der mit sichtbarem Licht im Wellenlängenbereich 420–470 nm bestrahlt wird, ist heute die Standardtherapie für mittelschwere Hyperbilirubinämien bei Neugeborenen. Neben Fotooxidationsprodukten, d. h. Bruchstücken des Moleküls, entstehen dabei durch einecis-trans-Isomerisierung(Z→E) zwei neue Fraktionen: dasStereoisomer(4Z,15E)-Bilirubin IX-α und in geringerem Umfang das (4E,15Z)-CyclobilirubinIX-α. Durch das Umklappen einer Doppelbindung wird einer der äußeren Ringe des Moleküls so gedreht, dass die Ausbildung von Wasserstoffbrücken nicht mehr möglich ist. Die Moleküle sind deshalb polarer und besser wasserlöslich und werden in der Hauptsache ohne Konjugation über Leber und Galle ausgeschieden.[11][12]
Literatur
[Bearbeiten|Quelltext bearbeiten]- Gerd Herold:Innere Medizin.2005.
- Georg Löffler, Petro E. Petrides, Peter C. Heinrich:Biochemie & Pathobiochemie.8. Auflage. Springer-Verlag, Heidelberg 2007,ISBN 978-3-540-32680-9.
- Stefan Silbernagl, Agamemnon Despopoulos:Color Atlas of Physiology.6. Auflage. Thieme, 2009,ISBN 978-3-13-545006-3.
Weblinks
[Bearbeiten|Quelltext bearbeiten]Einzelnachweise
[Bearbeiten|Quelltext bearbeiten]- ↑abDatenblattBilirubinbeiSigma-Aldrich,abgerufen am 25. Mai 2011 (PDF).
- ↑abcEintrag zuBilirubin.In:Römpp Online.Georg Thieme Verlag, abgerufen am 29. Mai 2014.
- ↑C. Pirone u. a.:Animal Pigment Bilirubin Discovered in Plants.In:J. Am. Chem. Soc.Band 131 (8), 2009, S. 2830–2831,doi:10.1021/ja809065g.
- ↑Henryk Dancygier:Klinische Hepatologie: Grundlagen, Diagnostik und Therapie hepatobiliärer Erkrankungen.Springer-Verlag, 2013,ISBN 978-3-642-55902-0,S.347(google.de).
- ↑Karen Marcdante, Robert M. Kliegman:Nelson Essentials of Pediatrics.Elsevier Health Sciences, 2014,ISBN 978-0-323-22698-1,S.219(google.de).
- ↑Gabriele Halwachs-Baumann:Labormedizin. Klinik – Praxis – Fallbeispiele.Springer-Verlag, Wien 2006,ISBN 3-211-25291-6.
- ↑Melanie Königshoff, Timo Brandenburger:Kurzlehrbuch Biochemie.2. Auflage. Georg-Thieme-Verlag, Stuttgart / New York 2007,ISBN 978-3-13-136412-8.
- ↑Guido Majno:Cells, Tissues, and Disease.Oxford University Press, 2004,ISBN 978-0-19-974892-1,S. 118.
- ↑Hilmar Burchardi:Die Intensivmedizin.Springer-Verlag, 2011,ISBN 978-3-642-16929-8,S. 568 (eingeschränkte Vorschauin der Google-Buchsuche).
- ↑C. Bührer u. a.:Hyperbilirubinämie des Neugeborenen – Diagnostik und Therapie.AWMF-Leitlinie. AWMF, Düsseldorf 2015.
- ↑abMarkus Thaler, Peter B. Luppa, Harald Schlebusch:Die Bilirubinbestimmung – Eine aktuelle Übersicht / Bilirubin measurement – An updated survey.In:LaboratoriumsMedizin.Band32,Nr.1,2008,S.1–10,doi:10.1515/JLM.2008.005.
- ↑V. Yu Plavskiĭ, V. A. Mostovnikov, A. I. Tret’yakova, G. R. Mostovnikova:Photophysical processes that determine the photoisomerization selectivity of Z,Z-bilirubin IXα in complexes with albumins.In:Journal of Optical Technology.Band74,Nr.7,2007,S.446–454,doi:10.1364/JOT.74.000446(osapublishing.org).