Butene
Butene(auchButylene) sind eine Gruppe von vierisomerenKohlenwasserstoffenmit der allgemeinen Summenformel C4H8,die über eine C=C-Doppelbindungverfügen. Sie zählen damit zu denAlkenen.Zwei der Isomere unterscheiden sich durchcis-trans-Isomerie.
Butene sind unterStandardbedingungenfarblose, brennbare Gase mit einer größerenDichteals Luft. Unter Druck lassen sich die Isomere verflüssigen. Sie wirken in höheren Konzentrationen narkotisierend und erstickend. Mit Luft bilden sie explosive Gemische.
Struktur und Eigenschaften
[Bearbeiten|Quelltext bearbeiten]| Eigenschaften der Butene | ||||||||||||
| Name | But-1-en | (Z)-But-2-en | (E)-But-2-en | 2-Methylprop-1-en | ||||||||
| Andere Namen | 1-Buten n-Buten 1-Butylen α-Butylen BUTENE(INCI)[1] |
cis-2-Buten (Z)-2-Buten cis-But-2-en |
trans-2-Buten (E)-2-Buten trans-But-2-en |
2-Methyl-1-propen Isobuten i-Butylen | ||||||||
| Struktur | 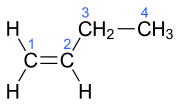
|
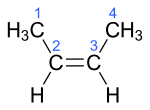
|

|
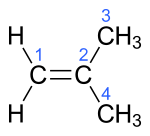
| ||||||||
| CAS-Nummer | 106-98-9 | 590-18-1 | 624-64-6 | 115-11-7 | ||||||||
| 107-01-7(EZ)-2-Buten | ||||||||||||
| 25167-67-3(Isomerengemisch) | ||||||||||||
| Summenformel | C4H8 | |||||||||||
| Molare Masse | 56,11 g·mol−1 | |||||||||||
| Kurzbeschreibung | farblose Gase[2] | |||||||||||
| Schmelzpunkt | −185,4 °C[3] | −138,9 °C[4] | −105,5 °C[5] | −140,4 °C[6] | ||||||||
| Siedepunkt | −6,2 °C[3] | 3,7 °C[4] | 0,9 °C[5] | −7,1 °C[6] | ||||||||
| molareVerdampfungsenthalpieam Siedepunkt | 22,07 kJ·mol−1[7] | 23,34 kJ·mol−1[7] | 22,72 kJ·mol−1[7] | 24,03 kJ·mol−1[8] | ||||||||
| Dampfdruck | 2,545 bar (20 °C) | 1,813 bar (20 °C) | 1,991 bar (20 °C) | 2,59 bar (20 °C) | ||||||||
| Untere Explosionsgrenze(20 °C / 1,013 bar)[9] | 1,2 Vol.‑% / 28 g·m3 | 1,6 Vol.‑% / 37 g·m3 | 1,6 Vol.‑% / 37 g·m3 | 1,6 Vol.‑% / 37 g·m3 | ||||||||
| Obere Explosionsgrenze(20 °C / 1,013 bar)[9] | 10,6 Vol.‑% / 252 g·m3 | 10,0 Vol.‑% / 235 g·m3 | 10,0 Vol.‑% / 235 g·m3 | 10,0 Vol.‑% / 235 g·m3 | ||||||||
| Zündtemperatur/Temperaturklasse[9] | 360 °C / T2 | 324 °C / T2 (E/Z-Isomerengemisch)[10] | 324 °C / T2 (E/Z-Isomerengemisch)[10] | 465 °C / T1 | ||||||||
| Löslichkeit | praktisch unlöslich in Wasser,[3][4][5][6]leichtlöslich in Ethanol und Ether | |||||||||||
| GHS- Kennzeichnung |
ausVerordnung (EG) Nr. 1272/2008 (CLP),[11]ggf. erweitert
|
ausVerordnung (EG) Nr. 1272/2008 (CLP),[12]ggf. erweitert
|
ausVerordnung (EG) Nr. 1272/2008 (CLP),[13]ggf. erweitert
|
ausVerordnung (EG) Nr. 1272/2008 (CLP),[14]ggf. erweitert
| ||||||||
| H-Sätze | 220‐280[3] | 220[4] | 220[5] | 220‐280[6] | ||||||||
| EUH-Sätze | keine EUH-Sätze | |||||||||||
| P-Sätze | 210‐377‐381‐403[3] | 210[4] | 210[5] | 210‐377‐381‐403[6] | ||||||||
Thermodynamische Eigenschaften
[Bearbeiten|Quelltext bearbeiten]Butene sind leicht zu verflüssigende Gase, deren Anwendung und Umsetzung oft unter erhöhtem Druck als Flüssigkeit oder im überkritischen Zustand erfolgt.
| Dampf-Flüssig-Gleichgewichte | ||||
|---|---|---|---|---|
| Name | But-1-en | (Z)-But-2-en | (E)-But-2-en | 2-Methylprop-1-en |
| DampfdruckfunktionnachAntoine | Parameter nach log10(P) = A−(B/(T+C)) (P in bar, T in K) | |||
| A | 4,24696 | 3,98744 | 4,04360 | 3,64709 |
| B | 1099,207 | 957,060 | 982,166 | 799,055 |
| C | −8,265 | −36,504 | −30,775 | −46,615 |
| Temperaturbereich | 195,6 K – 269,4 K | 203,06 K – 295,91 K | 201,70 K – 274,13 K | 216,40 K – 273 K |
| Quelle | [15] | [16] | [17] | [18] |
| KritischeGrößen[19] | ||||
|---|---|---|---|---|
| Name | But-1-en | (Z)-But-2-en | (E)-But-2-en | 2-Methylprop-1-en |
| Kritische Temperatur Tc | 146,35 °C / 419,5 K | 162,35 °C / 435,5 K | 155,45 °C / 428,6 K | 144,75 °C / 417,9 K |
| Kritischer Druck pc | 40,2 bar | 42,1 bar | 41,0 bar | 40,0 bar |
| KritischesMolvolumenVm,c | 0,2408 l·mol−1 | 0,2338 l·mol−1 | 0,2377 l·mol−1 | 0,2388 l·mol−1 |
| Kritische Dichte ρc | 4,15 mol·l−1 | 4,28 mol·l−1 | 4,21 mol·l−1 | 4,19 mol·l−1 |
Synthese
[Bearbeiten|Quelltext bearbeiten]Michael Faradayfand Butene 1825 als gasförmigen Bestandteil bei derDestillationvonErdöl(siehe auch:Flüssiggas). Butene können durchCrackenvon Erdöl als Isomerengemisch gewonnen werden. Sie werden auch durch katalytischeDehydrierungvonButanbzw.Isobutangewonnen. Die Trennung der Isomeren kann mit Hilfe vonZeolithenerfolgen.[10]
Verwendung
[Bearbeiten|Quelltext bearbeiten]Durch die C–C-Doppelbindungsind sie interessante und wichtige Ausgangsstoffe für chemischeSynthesen.Sie werden zur Herstellung von Verbindungen wie2-Butanol,2-Butanon(Ethylmethylketon) und1,3-Butadienverwendet und sind Ausgangsstoff zur Herstellung von Kunststoffen (z. B.ButylkautschukundPolyisobuten).[10]AlsAlkylierungsmitteldienen sie z. B. zur Synthese von Zusätzen für klopffeste Treibstoffe (2,2,4-Trimethylpentan(Isooctan)). Isobuten wird zur Synthese vonMethyl-tert-butylether(MTBE) bzw.Ethyl-tert-butylether(ETBE) benötigt. Auchtert-Butylester lassen sich über die Reaktion von Isobuten und (Carbon)säuren herstellen. Diese Syntheseroute bietet sich speziell dann an, wenn bei derVeresterungmittert-ButanolalsKonkurrenzreaktiondessenDehydratisierungdominiert.
Literatur
[Bearbeiten|Quelltext bearbeiten]- F.M.A. Geilen; G. Stochniol; S. Peitz; E. Schulte-Koerne:Butene,in:Ullmanns Enzyklopädie der Technischen Chemie,Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 2013;doi:10.1002/14356007.a04_483.pub3.
Einzelnachweise
[Bearbeiten|Quelltext bearbeiten]- ↑Eintrag zuBUTENEin derCosIng-Datenbankder EU-Kommission, abgerufen am 26. März 2022.
- ↑Eintrag zuButen, Isomerengemischin derGESTIS-StoffdatenbankdesIFA,abgerufen am 23. Oktober 2013.(JavaScript erforderlich)
- ↑abcdefEintrag zu1-Butenin derGESTIS-StoffdatenbankdesIFA,abgerufen am 11. August 2016.(JavaScript erforderlich)
- ↑abcdefEintrag zucis-2-Butenin derGESTIS-StoffdatenbankdesIFA,abgerufen am 11. August 2016.(JavaScript erforderlich)
- ↑abcdefEintrag zutrans-2-Butenin derGESTIS-StoffdatenbankdesIFA,abgerufen am 11. August 2016.(JavaScript erforderlich)
- ↑abcdefEintrag zu2-Methylpropenin derGESTIS-StoffdatenbankdesIFA,abgerufen am 11. August 2016.(JavaScript erforderlich)
- ↑abcV. Majer, V. Svoboda:Enthalpies of Vaporization of Organic Compounds: A Critical Review and Data Compilation.Blackwell Scientific Publications, Oxford 1985, S. 300.
- ↑R. C. Weast (Hrsg.):CRC Handbook of Chemistry and Physics.66. Auflage. CRC Press, 1985,ISBN 0-8493-0466-0.
- ↑abcE. Brandes, W. Möller:Sicherheitstechnische Kenngrößen.Band 1:Brennbare Flüssigkeiten und Gase.Wirtschaftsverlag NW – Verlag für neue Wissenschaft, Bremerhaven 2003.
- ↑abcdEintrag zuButene.In:Römpp Online.Georg Thieme Verlag, abgerufen am 25. Juni 2019.
- ↑Eintrag zuBut-1-eneimClassification and Labelling InventoryderEuropäischen Chemikalienagentur(ECHA), abgerufen am 11. August 2016. Hersteller bzw.Inverkehrbringerkönnen die harmonisierte Einstufung und Kennzeichnungerweitern.
- ↑Eintrag zu(Z)-but-2-eneimClassification and Labelling InventoryderEuropäischen Chemikalienagentur(ECHA), abgerufen am 11. August 2016. Hersteller bzw.Inverkehrbringerkönnen die harmonisierte Einstufung und Kennzeichnungerweitern.
- ↑Eintrag zu(E)-but-2-eneimClassification and Labelling InventoryderEuropäischen Chemikalienagentur(ECHA), abgerufen am 11. August 2016. Hersteller bzw.Inverkehrbringerkönnen die harmonisierte Einstufung und Kennzeichnungerweitern.
- ↑Eintrag zu2-methylpropeneimClassification and Labelling InventoryderEuropäischen Chemikalienagentur(ECHA), abgerufen am 11. August 2016. Hersteller bzw.Inverkehrbringerkönnen die harmonisierte Einstufung und Kennzeichnungerweitern.
- ↑C. C. Coffin, O. Maass:The Preparation and Physical Properties of «alpha», «beta»- and «gamma»-Butylene and Normal and Isobutane.In:J. Am. Chem. Soc.50, 1928, S. 1427–1437.
- ↑R. B. Scott, W. J. Ferguson, F. G. Brickwedde:Thermodynamic properties of cis-2-butene from 15° to 1,500 K.In:J. Res. NBS.33, 1944, S. 1–20.
- ↑L. Guttman, K. S. Pitzer:trans-2-Butene. The heat capacity, heats of fusion and vaporization, and vapor pressure. The entropy and barrier to internal rotation.In:J. Am. Chem. Soc.67, 1945, S. 324–327.
- ↑A. B. Lamb, E. W. Roper:The Vapor Pressures of Certain Unsaturated Hydrocarbons.In:J. Am. Chem. Soc.62, 1940, S. 806–814.
- ↑C. Tsonopoulos, D. Ambrose:Vapor-Liquid Critical Properties of Elements and Compounds. 6. Unsaturated Aliphatic Hydrocarbons.In:J. Chem. Eng. Data.41, 1996, S. 645–656.

