Photochemie
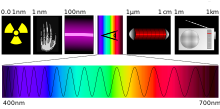
Unter dem BegriffPhotochemieversteht manchemische Reaktionen,die durch Einwirkung vonLichtinitiiert werden. Die Grundvoraussetzung hierfür ist eineAbsorptiondes Lichtes durch dasMolekül,das reagieren soll. Das heißt, dieWellenlängedes verwendeten Lichts muss zum Absorptionsverhalten des Moleküls passen. Neben der direkten Anregung gibt es auch Photoreaktionen, bei denen zunächst einPhotosensibilisatorangeregt wird und dieser dann Energie auf die zur Reaktion zu bringenden Moleküle überträgt.
Die Absorption einesLichtquantsführt zu energetisch (elektronisch) angeregten Zuständen, die dank der Anregungsenergie chemische Reaktionen eingehen können. Chemische Umwandlungen konkurrieren dabei mit photophysikalischen Deaktivierungsprozessen wie derPhotoemissionaus dem angeregtenSingulett-Zustand(Fluoreszenz) oder aus demTriplett-Zustand(Phosphoreszenz) sowie der strahlungslosenDeaktivierung.Das relative Ausmaß, mit dem die einzelnen Prozesse durchlaufen werden, wird durch dieQuantenausbeutenausgedrückt. Die Summe der Quantenausbeuten beträgt maximal 1 – außer beiKettenreaktionen.
Da die Absorption eines Lichtquants zu einer elektronischen Anregung führt, können im angeregten Zustand Reaktionen beobachtet werden, die im elektronischen Grundzustand des Moleküls nicht erlaubt sind (vgl.Woodward-Hoffmann-Regeln,perizyklische Reaktionen). Photochemische Reaktionen sind häufig eine gute Methode, um komplexe und hoch gespannte Moleküle aufzubauen.
Neben der Einwirkung von Licht lässt sich die Photochemie auch mit energiereicherenQuantenbetreiben. Mit solchen photoinduzierten Prozessen beschäftigt sich unter anderem die Röntgenphotochemie bzw. die Hochenergiephotochemie. Hierbei findet dieSynchrotronstrahlungin der Chemie eine Anwendung.[1]

Beispiele für photochemische Reaktionstypen
[Bearbeiten|Quelltext bearbeiten]- Spaltungen (Bindungshomolysen), wie sie beiPhotoinitiatorenbeobachtet werden – u. U. gefolgt von weiterer Fragmentierung der entstehenden Radikale, vgl. die Abspaltung vonKohlenmonoxidaus Carbonylverbindungen.
- Photoisomerisierungen, wie die Bildung von Fulven und Benzvalen aus Benzol über den ersten angeregten Singulettzustand oder die Bildung von Dewarbenzol aus dem zweiten angeregten Singulettzustand von Benzol.[2]
- Elektrocyclische Reaktionen, etwa die Umwandlung vonErgosterinzu Prävitamin D, dieCyclisierungvon Butadienen zu Cyclobutenen, die Cyclisierung voncis-Stilben zu Dihydrophenanthren oder von Diphenylamin zu Dihydrocarbazol.
- Umlagerungen, wie die Isomerisierung vonCycloheptatrienzuToluol.
- LichtinduzierteKettenreaktionen:
- Reaktion vonChlorundWasserstoff(Chlorknallgas) zuChlorwasserstoff,derenReaktionsmechanismusinsbesondere vonWalther NernstundMax Bodensteinaufgeklärt wurde.
- PhotochlorierungvonAlkanen,z. B.Methan.
- Regioselektive Seitenketten-Halogenierung von alkyliertenAromaten(einfachstes Beispiel: Chlorierung vonToluolan der Methylgruppe) gemäß der „SSS “-Regel (Sonne,Siedehitze,Seitenkette).[3]
- Sulfochlorierung von Alkanen mitSchwefeldioxidund Chlor.[4]
- Photo-Fries-Verschiebungvon Phenylestern unter Bildung vonKetonenmit einer Hydroxy-Funktion inortho- oderpara-Stellung am Phenylring.[5]
- [2+2]-Cycloadditionenvon Alkenen im Zuge einerPhotodimerisierungbzw.Photocyclisierung,die zuCyclobutanen(Vierring) führen, vgl. die Bildung vonQuadricyclandurch Belichtung vonNorbornadienoder die Photodimerisierung vonCyclopenten.
- [2+2]-Cycloaddition von Alkenen und Ketonen in derPaternò-Büchi-Reaktion.
- α-Spaltung von Thiolestern zu Aldehyden und Disulfiden.[6]
- Bildung vonThioxanthonendurch Umlagerungsreaktionen.[7]
- Isomerisierungen, wiecis-trans-Isomerisierungen (Standardbeispiele:cis-/trans-Stilben,cis-/trans-Azobenzol,Malein-/Fumarsäure). Zum Beispiel entsteht bei der Bestrahlung von Maleinsäure beziehungsweise Fumarsäure in beiden Fällen die gleiche Mischung aus 75 % Maleinsäure und 25 % Fumarsäure.[8]Die Lage des Photogleichgewichts kann durch die Anregungswellenlänge gesteuert werden.
- Photosensibilisierte Reaktionen, d. h. Photoisomerisierungen, Photocycloadditionen, unter Zusatz einesPhotosensibilisators,die zum Teil enantioselektiv verlaufen.[9][10]
- Photoreaktionen in der Biologie:
- Ein bekanntes Beispiel für eine chemische Reaktion mit photochemischen Reaktionsschritten ist diePhotosynthese.
- Ein weiteres Beispiel ist das Sehen mit dem menschlichen Auge. Dabei findet in den Stäbchen der Netzhaut des Auges eine Photoisomerisierung des für das Hell-Dunkel-Sehen verantwortlichen Rhodopsins statt, genauer gesagt, eine lichtgesteuertecis-trans-Isomerisierung des 11-cis-Retinals,das ein Bestandteil des Chromophors Rhodopsin ist.
Die ersten photochemischen Experimente gehen aufGiacomo Luigi Ciamicianzurück. Die ersten zusammenfassenden Bücher über die präparative organische Photochemie hatAlexander Schönberg[11]verfasst.
- Einphotophysikalischer Prozessin der Biologie:
Durchführung photochemischer Experimente
[Bearbeiten|Quelltext bearbeiten]Die Durchführung photochemischer Experimente erfordert eine Reihe von Voraussetzungen, die sich aus der Startbedingung – Absorption von Licht durch die Reaktanden – ergeben. Es muss bekannt sein, bei welcher Wellenlänge die photochemische Anregung erfolgen soll. Entsprechende Informationen zu den Reaktanden lassen sich Tabellenwerken entnehmen oder können durch Messung derUV-VIS-Spektrenerhalten werden. Im nächsten Schritt ist sicherzustellen, dass eine geeignete Lichtquelle zur Verfügung steht. Hierbei muss gewährleistet sein, dass die Lichtquelle ausreichende Leistung im relevanten Wellenlängenbereich liefert, unter Umständen muss ferner ausgeschlossen werden, dass Wellenlängen, die zu photochemischen Nebenreaktionen führen, ausgeschlossen werden. Die verwendeten Lösungsmittel müssen im relevanten Wellenlängenbereich transparent sein (außer sie fungieren als Sensibilisatoren für die Photoreaktion). Ferner dürfen die Lösungsmittel nicht als „Quencher “wirken (Singulett- oder Triplett-Anregungsenergie der Reaktanden übernehmen und somit die reaktiven Species deaktivieren) und müssen gegenüber den auftretenden Species inert sein. Sauerstoff führt in der Regel zu Nebenreaktionen, weshalb die Reaktionen meist unter Schutzgas (Stickstoff, Argon) durchgeführt werden (Ausnahme: Reaktionen vonSingulett-Sauerstoff,bei denen gezielt Sauerstoff durch die Reaktionsmischung geleitet wird). Da dieEindringtiefedes Lichts in der Regel nur wenige Millimeter beträgt (vgl.Lambert-Beer’sches Gesetz), ist für gute Durchmischung zu sorgen. Dies kann in Laborversuchen oftmals durch das sowieso notwendige Durchleiten von Inertgas erreicht werden. Sicherheitstechnisch relevant ist der Schutz vorUV-Strahlung(Augenschäden, „Sonnenbrand “) oder auch das Ableiten der z. B. durch Hochdrucklampen erzeugten hohen Wärmemengen.
Apparaturen für photochemische Experimente
[Bearbeiten|Quelltext bearbeiten]
Präparative photochemische Experimente werden im Labor bevorzugt in Tauchapparaturen durchgeführt. Hierzu wird ein unten abgeschlossenes Glasrohr in die zu belichtende Lösung getaucht. In das Glasrohr kann dann z. B. eineQuecksilber-Dampflampeeingestellt werden. Idealerweise wird das Tauchrohr doppelwandig ausgeführt, damit zu Kühlzwecken Wasser durchgeleitet werden kann. In guten Apparaturen ist das Außenrohr aus Quarz gefertigt, das Innenrohr lässt sich über eine Schraubverbindung austauschen. In solchen Aufbauten können dann verschiedene Innenrohre im Sinne eines Filters verwendet werden, um UV-Strahlung unterhalb einer gewissen Wellenlänge abzuschneiden (300 nm beiPyrexoderSolidex,ca. 350 nm bei Standardgläsern). Als Filter kann in doppelwandigen Einsätzen auch die Kühlflüssigkeit dienen, wenn entsprechende (stabile) Farbstoffe oder Metallsalze zugesetzt werden.
Einfachste Versuche mit kleinen Substanzmengen lassen sich ausführen, in dem Substanzen z. B. in NMR-Röhrchen oder Küvetten bestrahlt werden. Die Bestrahlung in Küvetten ist üblich bei photophysikalischen Untersuchungen und kann in geeigneten Aufbauten auch bei sehr tiefen Temperaturen (flüssiger Stickstoff) erfolgen.
Lichtquellen
[Bearbeiten|Quelltext bearbeiten]Lichtquellen für photochemische Arbeiten lassen sich prinzipiell in kontinuierliche und diskontinuierliche Strahler unterteilen. Bei der Auswahl ist ferner zu überlegen, welche Leistung für die Arbeiten benötigt wird. Kontinuierliche Strahler liefern Licht in einem weiten Wellenlängenbereich. Typische Beispiele sind schwarze Strahler (Sonne, Glühlampen). Ihre Spektren zeichnen sich durch eine sehr weite spektrale Verteilung aus, die vom Infraroten (Wärmestrahlung) über das Sichtbare bis hin in den (nahen) UV-Bereich reichen. Die UV-Anteile dieser Strahler sind jedoch gering, so dass für photochemische Arbeiten andere Lichtquellen benötigt werden. Als kontinuierliche Strahler im UV-Bereich eignen sich Gasentladungslampen auf Basis von Wasserstoff/Deuteriumoder von Edelgasen.[13]
| Gas | Emissionsbereich / nm |
|---|---|
| H2 | 170–350 |
| He | 58–100 |
| Ne | 74–79 |
| Ar | 107–160 |
| Kr | 124–150 |
| Xe | 147–170 |
Diese Lampen finden vornehmlich Anwendung in UV-Spektrometern (Wasserstoff/Deuteriumlampen) oder z. B. in Photoelektronen-Spektrometern.

Diskontinuierliche Stahler liefern Licht in Form diskreter Linien. Typische Vertreter sind Laser und Metalldampflampen. Bei den Metalldampflampen sind – mit steigendem Betriebsdruck zunehmend – die einzelnen Linien verbreitert oder sogar von einem Kontinuum überlagert. Für die präparative Photochemie sind dieQuecksilberdampflampenvon überragenderer Bedeutung, Laser haben einen breiten Einzug bei den mechanistischen Untersuchungen gefundn. Quecksilber-Niederdrucklampen (0,01–1 mbar) zeichnen sich durch ganz überwiegende Strahlung bei 254 nm aus (ca. 95 %). Beschichtung der Lampen mit geeigneten Phosphoren (analog zu Leuchtstoffröhren) erlaubt die Bereitstellung von Lichtquellen mit Emission um 300 nm bzw. 350 nm herum. Dies ist im Rayonet[14]umgesetzt, bei dem sich die Bestrahlungswellenlänge durch Austausch der Lampentypen realisieren lässt. Bei höheren Betriebsdrücken der Quecksilberlampen (0,1–100 bar) überwiegen zunehmend Emissionen bei 297 nm, 334 nm, 365 nm, 404 nm, 436 nm sowie bei 546 nm und 577 nm. Werden Metallsalze zugemischt (Eisen, Cadmium, Thallium, Indium), können weitere Hauptemissionslinien erzeugt werden. Vorteil der Hoch- und Höchstdrucklampen ist ihre hohe Leistungsabgabe. Bei industriellen Anwendungen kommen Lampen mit einer Leistung von mehreren 10 kW zum Einsatz.
Lösungsmittel, Sensibilisatoren und Quencher
[Bearbeiten|Quelltext bearbeiten]Eine Zusammenfassung von Lösungsmitteln für photochemische Arbeiten zeigt die nachfolgende Tabelle. Bei den angegebenen Wellenlängen wird die Lichtintensität durch die Eigenabsorption des Lösungsmittels über eine Strecke von 1 cm um rund 90 % reduziert.[15]
| Lösungsmittel | Wellenlänge / nm | Lösungsmittel | Wellenlänge / nm | |
|---|---|---|---|---|
| Wasser | 185 | Acetonitril | 190 | |
| n-Hexan | 195 | Ethanol | 204 | |
| Methanol | 205 | Cyclohexan | 215 | |
| Diethylether | 215 | 1,4-Dioxan | 230 | |
| Dichlormethan | 230 | Chloroform | 245 | |
| Tetrahydrofuran | 245 | Essigsäure | 250 | |
| Ethylacetat | 255 | Kohlenstofftetrachlorid | 265 | |
| Dimethylsulfoxid | 277 | Benzol | 280 | |
| Toluol | 285 | Pyridin | 305 | |
| Aceton | 330 |
Die Lichtabsorption und -emission finden überwiegend unter Erhaltung der Multiplizität statt, d. h., ein im Singulett-Zustand vorliegendes Molekül wird in einen angeregten Singulett-Zustand überführt bzw. zeigt schnelleFluoreszenzemission.Die direkte Anregung aus einem Singulett-Grundzustand in einen Triplett-Zustand ist quantenchemisch „verboten “und wird damit nur untergeordnet beobachtet. (Zum Vergleich: der strahlende Übergang eines Tripletts in den Grundzustand (Phosphoreszenz) ist entsprechend verboten und somit gegenüber der Fluoreszenz langsamer Vorgang.) Sollen daher photochemische Reaktionen über Triplett-Zustände verlaufen, werdenSensibilisatoreneingesetzt. Bei diesen findet im angeregten Zustand ein Singulett-Triplett-Übergang (Intersystem Crossing,ISC) in nennenswertem Ausmaß statt. Anschließend kann der Sensibilisator seine Triplett-Anregung auf einen Reaktanden übertragen, der dann chemische Reaktionen im Triplett-Zustand eingeht. Das Phänomen der Energieübertragung kann auch genutzt werden, um Einblick in den Mechanismus von Photoreaktionen zu erhalten. Hier werden Moleküle mit bekannten Singulett- oder Triplett-Energien eingesetzt, um bei Reaktionen auftretende angeregte Zustände zu „löschen “(„quenchen “). Liegt die Energie des Quenchers unterhalb der Energie des zu löschenden Zustands, so kommt es zur Energieübertragung und damit zur Unterbrechung der ursprünglichen Photoreaktion. Das Prinzip kann auf Reaktionen im Singulett- wie auch im Triplett-Zustand angewandt werden. Nachfolgend sind einige typische Sensibilisatoren und Quencher aufgeführt (Energien der ersten angeregten Singulett- und Triplett-Zustände, Quantenausbeuten für dasSingulett-Triplett Intersystem Crossing(ΦISC)):[15]
| Verbindung | ET/ (kJ·mol−1) | ES/ (kJ·mol−1) | Δ(ES− ET) / (kJ·mol−1) | ΦISC |
|---|---|---|---|---|
| Benzol | 353 | 459 | 106 | 0,25 |
| Toluol | 346 | 445 | 99 | 0,53 |
| Methylbenzoat | 326 | 428 | 102 | — |
| Aceton | 332 | 372 | 40 | 0,9–1,00 |
| Acetophenon | 310 | 330 | 20 | 1,00 |
| Xanthon | 310 | 324 | 14 | — |
| Benzaldehyd | 301 | 323 | 22 | 1,00 |
| Triphenylamin | 291 | 362 | 71 | 0,88 |
| Benzophenon | 287 | 316 | 29 | 1,00 |
| Fluoren | 282 | 397 | 115 | 0,22 |
| Triphenylen | 280 | 349 | 69 | 0,86 |
| Biphenyl | 274 | 418 | 144 | 0,84 |
| Phenanthren | 260 | 346 | 86 | 0,73 |
| Styrol | 258 | 415 | 157 | 0,40 |
| Naphthalin | 253 | 385 | 132 | 0,75 |
| 2-Acetylnaphthalin | 249 | 325 | 76 | 0,84 |
| Biacetyl | 236 | 267 | 31 | 1,00 |
| Benzil | 223 | 247 | 24 | 0,92 |
| Anthracen | 178 | 318 | 140 | 0,71 |
| Eosin | 177 | 209 | 32 | 0,33 |
| Bengalrosa | 164 | 213 | 49 | 0,61 |
| Methylenblau | 138 | 180 | 42 | 0,52 |
Siehe auch
[Bearbeiten|Quelltext bearbeiten]- Photochemische Verfahren(nach DIN 8580)
- Kasha-Regel
Quellen
[Bearbeiten|Quelltext bearbeiten]- ↑H. Baumgärtel:Synchrotronstrahlung in der Chemie.In:Chemie in unserer Zeit.28. Jahrg., Nr. 1, 1994,ISSN0009-2851,S. 6–17.
- ↑Jens Dreyer:Theoretische Untersuchungen zur photochemischen Reaktivität von Benzol und seinen Isomeren.Dissertation.WWU, Münster 1995.
- ↑Siegfried Hauptmann:Organische Chemie.2. Auflage. VEB Deutscher Verlag für Grundstoffindustrie, Leipzig 1985, S. 297.
- ↑Siegfried Hauptmann:Organische Chemie.2. Auflage. VEB Deutscher Verlag für Grundstoffindustrie, Leipzig 1985, S. 207.
- ↑Jürgen Martens,Klaus Praefcke,Ursula Schulze:Intramolekulare Photo-Friedel-Crafts-Reaktionen; ein neues Synthese-Prinzip für Heterocyclen1.In:Synthesis.Band1976,Nr.08,1976,S.532–533,doi:10.1055/s-1976-24110.
- ↑Jürgen Martens, Klaus Praefcke:Organische Schwefelverbindungen, VII. Photochemische α-Spaltung von Thiobenzoesäure-S-p-tolylestern in Lösung.In:Chemische Berichte.Band107,Nr.7,1. Juli 1974,S.2319–2325,doi:10.1002/cber.19741070716.
- ↑Gerd Buchholz,Jürgen Martens,Klaus Praefcke:Photochemische Thiaxanthon-Synthese aus 2-Halogen-thiobenzoesäure-S-arylestern1.In:Synthesis.Band1974,Nr.09,1974,S.666–667,doi:10.1055/s-1974-23399.;Gerd Buchholz, Jürgen Martens, Klaus Praefcke:2- und 4-Azathioxanthone durch Photoumlagerung von Thionicotinsäure-S-arylestern.In:Angewandte Chemie.Band86,Nr.15,1. August 1974,S.562–563,doi:10.1002/ange.19740861513.Gerd Buchholz, Jürgen Martens, Klaus Praefcke:2- and 4-Azathioxanthones by Photorearrangement of S-Aryl Thionicotinates.In:Angewandte Chemie International Edition in English.Band13,Nr.8,1. August 1974,S.550–551,doi:10.1002/anie.197405501.
- ↑Siegfried Hauptmann:Organische Chemie.2. Auflage. VEB Deutscher Verlag für Grundstoffindustrie, Leipzig 1985, S. 774.
- ↑A. Gilbert, J. Baggott:Essentials of Molecular Photochemistry.Blackwell, 1991, S. 168.
- ↑Martin Vondenhof,Jochen Mattay:Radical ions and photochemical charge transfer phenomena, 28. 1,1′-Binaphthalene-2,2′-dicarbonitrile in photochemically sensitized enantiodifferentiating isomerizations.In:Chemische Berichte.123, 1990, S. 2457–2459,doi:10.1002/cber.19901231232.
- ↑Alexander Schönberg:Präparative Organische Photochemie.mit einem Beitrag von G. O. Schenk, Springer-Verlag, Berlin/ Göttingen/ Heidelberg 1958; Alexander Schönberg:Preparative Organic Photochemistry.in cooperation with G. O. Schenk, O.-A. Neumüller. 2., kompl. überarb. Auflage vonPräparative Organische Photochemie.Springer-Verlag, Berlin/ Heidelberg/ New York 1968.
- ↑Wilhelm Nultsch:Allgemeine Botanik: kurzes Lehrbuch für Mediziner und Naturwissenschaftler.8. Auflage. Thieme Verlag, Stuttgart/New York 1986,ISBN 3-13-383308-1,S. 257.
- ↑G. von Bünau, T. Wolff:Photochemie: Grundlagen, Methoden, Anwendungen.VCH Verlagsgesellschaft, Weinheim/New York 1987,ISBN 3-527-26506-6.
- ↑rayonet.org
- ↑abJ. Mattay, A. Giesbeck (Hrsg.):Photochemical Key Steps in Organic Synthesis.VCH, Weinheim/New York/Basel/Cambridge/Tokyo 1994,ISBN 3-527-29214-4.