Nitrila klorido
| Nitrila klorido | |||||
 | |||||
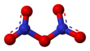
| Plata kemia strukturo de la Nitrila klorido | |||||
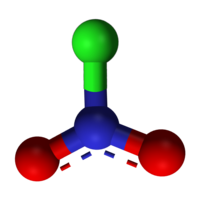 | |||||
| Tridimensia kemia strukturo de la Nitrila klorido | |||||
| Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | |||||
| CAS-numero-kodo | 13444-90-1 | ||||
| ChemSpider kodo | 10446393 | ||||
| PubChem-kodo | 11984615 | ||||
| Merck Index | 15,6744 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | senkolora aŭ palflava, koroda, toksa gaso, forte irita kun klorsimila odoro | ||||
| Molmaso | 81,459 g·mol-1 | ||||
| Denseco | 1,5g cm−3 | ||||
| Fandpunkto | -145°C[1] | ||||
| Bolpunkto | -14,3°C | ||||
| Solvebleco | Akvo:reakcias | ||||
| Mortiga dozo (LD50) | 58 mg/kg (buŝe) | ||||
| Sekurecaj Indikoj | |||||
| Riskoj | R14R34R37R50R45R53 | ||||
| Sekureco | S26S45S61 | ||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS Damaĝo Piktogramo |
| ||||
| GHS Signalvorto | Damaĝa substanco | ||||
| GHS Deklaroj pri damaĝoj | H270,H280,H314,H330,H400 | ||||
| GHS Deklaroj pri antaŭgardoj | P210,P260,P264,P271,P273,P280,P284,P301+330+331,P303+361+353,P304+340,P305+351+338,P310,P320,P321,P363,P377,P381,P391,P403,P403+233,P405,P410+403,P501 | ||||
(25 °C kaj 100 kPa) | |||||
Nitrila kloridoaŭNO2Clestas neorganika klora kombinaĵo denitrogenokajoksigeno,senkolora aŭ palflava, koroda, toksa gaso, forte irita kun klorsimila odoro, uzata en kemiaj sintezoj, kaj organikaj, kaj neorganikaj, kiel malkompona produkto el interagado denitrata acidokajklorida acido,kun forte potencaj oksidigaj, klorigaj kaj nitrogenigaj proprecoj.
Ĝia analogaĵo, lanitrozila kloridoestas ankaŭ konata kiel reakciaĵo de Tilden, omaĝe al ĝia kreinto, William Augustus Tilden (1842-1926).[2] Oni devas konstati ke du reakcioj eblas per interagado denitrata acidokajklorida acido.Kiam la reakciantoj estas egalmolumaj, tiam nitrila klorido estiĝas. Tamen, kiam oni uzas eksceson daklorida acido,tiam nitrozila klorido estiĝas, laŭ la jenaj reakcioj:
Sintezoj
[redakti|redakti fonton]Sintezo 1
[redakti|redakti fonton]- Preparado per interagado denitrita acidokajhipoklorita acidoen ĉeesto desulfata acido:
Sintezo 2
[redakti|redakti fonton]- Nitrila klorido estis preparata en jaro 1929 per oksidado de nitrozila klorido kun ozono:[3]
Sintezo 3
[redakti|redakti fonton]- Nitrila klorido sinteziĝas per agado deklorosulfonata acidosurnitrata acido:
Sintezo 4
[redakti|redakti fonton]- Nitrila klorido prepariĝas per traktado desulfurila kloridokunnitrita acido:
Sintezo 5
[redakti|redakti fonton]|
2 |
Sintezo 6
[redakti|redakti fonton]- Nitrila klorido estiĝas per interagado denatria nitritokajklorida acidoen akva medio:
Sintezo 7
[redakti|redakti fonton]- Per traktado denitrogena duoksidokajklorgasoprepareblas nitrilan kloridon:
Sintezo 8
[redakti|redakti fonton]- Preparado per interagado dearĝenta nitratokunklorida acido.[6]Zorgu: Se oni aldonas plian molekulon da arĝenta nitrato, ĝi reakcias kun la nitrila klorido formita por doni dunitrogenan kvinoksidon (vidu reakcion 7):
Sintezo 9
[redakti|redakti fonton]- Kvarfluoroborato de nitrogeniumo reakcias kunklorgasopor forminitrilan kloridon:
Sintezo 10
[redakti|redakti fonton]- Duklorido karbonoreakcias kunnitrita acidopor forminitrilan kloridonkajtrikloro-etilenono:[7]
|
2 |
Sintezo 11
[redakti|redakti fonton]- Preparado per interagado denitrogeiuma kvarfluoroboratokajkloro:
Sintezo 12
[redakti|redakti fonton]- Sintezo per interagado dedunitrogena kvaroksidokunkloro:
Sintezo 13
[redakti|redakti fonton]- Preparado per interagado dekalia klorokromiatokundunitrogena kvaroksido:[9]
Reakcioj
[redakti|redakti fonton]Reakcio 1
[redakti|redakti fonton]- Nitrila klorido malkomponiĝas per fotolizo ennitrogena duoksidokajkloro:
Reakcio 2
[redakti|redakti fonton]- Nitrila klorido reakcias kun akvo por forminitratan acidonkajkloridan acidon:
Reakcio 3
[redakti|redakti fonton]- Nitrila klorido reakcias kuntoluenopor formibenzilan kloridonkajnitritan acidon:
Reakcio 4
[redakti|redakti fonton]- Preparado denitrobenzenoper traktado de nitrila klorido kunbenzeno:[10]
|
|
Reakcio 5
[redakti|redakti fonton]- Preparado debenzila kloridoper interagado denitrila klorido,benzenokajkvarfluoroborato de arĝento:
Reakcio 6
[redakti|redakti fonton]- Preparado dearĝenta kloridoper interagado denitrila kloridokajarĝenta kvarfluoroborato:[12]
Reakcio 7
[redakti|redakti fonton]- Preparado dedunitrogena kvinoksidoper traktado denitrila kloridokunarĝenta nitrato:
Reakcio 8
[redakti|redakti fonton]- Preparado dekloro-piridino(CAS-numero109-09-1) per traktado denitrila fluoridokunpiridino(CAS-numero110-86-1):[13]
Reakcio 9
[redakti|redakti fonton]- Preparado detrikloro-etilenoper reakcio internitrila kloridokajetileno:
Reakcio 10
[redakti|redakti fonton]- Estante fluoro pli elektronegativa elemento ol kloro,nitrila fluoridoestiĝas per agado denitrila kloridosurfluorida acido:
Reakcio 11
[redakti|redakti fonton]- Nitrila klorido iĝas en nitrozilan kloridon per agado surnatria nitrito:
Literaturo
[redakti|redakti fonton]- Aromatic Nitration
- Inorganic Syntheses
- The Chemistry of Nonaqueous Solvents VB: Acid and Aprotic Solvents
- Journal of the Chemical Society
- The Chemistry of the Non-Metals
- History of Chemistry[rompita ligilo]
Referencoj
[redakti|redakti fonton]- ↑Chemical Book
- ↑History of Chemistry[rompita ligilo]
- ↑ACS Publications
- ↑Science Direct
- ↑Science Direct
- ↑A Manual of Inorganic Chemistry
- ↑A Dictionary of Chemistry and the Allied Branches of Other Sciences
- ↑A Dictionary of Chemistry and the Allied Branches of Other Sciences
- ↑Journal of the Chemical Society
- ↑ACS Publications
- ↑ACS Publications
- ↑Across Conventional Lines
- ↑Science Direct







![{\displaystyle {\mathsf {HNO_{3}+HCl{\xrightarrow[{}]{}}\,NO_{2}Cl+H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2e21908e140f95e3f77dd47834b82310fe7b2348)
![{\displaystyle {\mathsf {HNO_{3}+3\,HCl{\xrightarrow[{}]{}}\,NOCl+Cl_{2}+2\,H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4a9940d560c0cea0807aca8919802dfa6ba5df11)
![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{H2SO_{4}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0bce7868f02010bfe85771e719ff6e747f8435a8)
![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)