Piperidina
| Piperidina | ||
|---|---|---|
 | ||
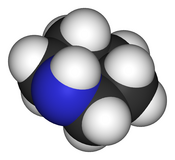 | ||
| Nombre IUPAC | ||
| Piperidina | ||
| General | ||
| Otros nombres |
Hexahidropiridina Azaciclohexano Ciclopentimina Hexazano Azinano | |
| Fórmula semidesarrollada | CH2(CH2)4NH | |
| Fórmula molecular | C5H11N | |
| Identificadores | ||
| Número CAS | 110-89-4[1] | |
| Número RTECS | TM3500000 | |
| ChEBI | 18049 | |
| ChEMBL | CHEMBL15487 | |
| ChemSpider | 7791 | |
| PubChem | 8082 | |
| UNII | 67I85E138Y | |
| KEGG | C01746 | |
|
C1CCNCC1
| ||
| Propiedades físicas | ||
| Apariencia | Líquidoincoloro o amarillo pálido. | |
| Olor | Amoniacal, a pimienta o pescado. | |
| Densidad | 862kg/m³;0,862g/cm³ | |
| Masa molar | 8515g/mol | |
| Punto de fusión | −11 °C (262 K) | |
| Punto de ebullición | 105 °C (378 K) | |
| Presión de vapor | 28,3 ± 0,2mmHg | |
| Índice de refracción(nD) | 1,4525 | |
| Propiedades químicas | ||
| Acidez | 11,28 pKa | |
| Solubilidadenagua | 250 g/L | |
| log P | 0,84 | |
| Familia | Amina | |
| Peligrosidad | ||
| Punto de inflamabilidad | 275,15 K (2 °C) | |
| NFPA 704 |
3
3
3
| |
| Compuestos relacionados | ||
| aminas heterocíclicas |
Pirrolidina Piperazina Nanofina Azepano Azocano Azecano | |
| piperidinas | 4-(1-pirrolidinil)-piperidina | |
| heterociclos con azufre |
Tiazolidina Tiomorfolina | |
| Valores en elSIy encondiciones estándar (25℃y 1atm), salvo que se indique lo contrario. | ||
Lapiperidinaes uncompuesto orgánicodefórmula molecularC5H11N,cuya estructura química corresponde a unaamina heterocíclicasaturadade seis miembros. Fue descrita por vez primera en 1850 por el químicoescocésThomas Andersony luego, de forma independiente, por elfrancésAuguste Cahoursen 1852, quien le dio nombre.[2] El término «piperidina» proviene de la palabraPiper,génerodeplantasmagnoliopsidasque incluye a lapimienta.[3][4]
Características físicas y químicas
[editar]A temperatura ambiente, la piperidina es unlíquidofumante incoloro o de color amarillo pálido. Desprende un característico olor aamoníaco,pimienta o pescado, definido también como nauseabundo.[5] Su sabor ha sido descrito como «a pimienta ardiente».[6] Tiene supunto de ebullicióna 105°Cy supunto de fusióna -11 °C. Menos denso que el agua (ρ= 0,862 g/cm³), essolubleenetanol,éter,acetona,bencenoycloroformo. Su solubilidad en agua —cifra estimada— es de 250 g/L.El valor dellogaritmode sucoeficiente de reparto,logP= 0,84, indica unasolubilidadmayor en disolventesapolaresque en disolventespolares.Su vapor es tres veces más denso que el aire.[6][7]
La piperidina es unabasedébil (pKa= 11,28).[6] Por ello,neutralizaácidosenreacciones exotérmicasformando sales y agua. Al combinarse conagentes reductoresfuertes comohidruros,puede generarhidrógenogaseoso.[8]
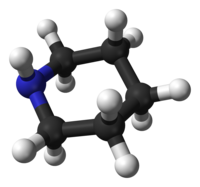
Conformación
[editar]La piperidina adopta diversasconformaciones espaciales,en concreto unaconformación de sillasimilar a la que presenta elciclohexano.Pero a diferencia de este, la piperidina tiene dos conformaciones de silla distinguibles: una con el enlace N–H en posición axial, y la otra en posición ecuatorial. Tras cierta controversia a mediados del sigloXX,se concluyó que la conformación ecuatorial es más estable (por 0,72kcal/mol) en fase gaseosa.[9] Dicha conformación parece también ser la más estable endisolucionesde piperidina en solventesapolares,si bien en solventes polares la conformación preferida puede ser la contraria.[10]
Los dosconfórmerosse interconvierten rápidamente a través de la denominadainversión del nitrógeno(oscilación del átomo denitrógenode uno al otro lado del plano formado por los grupos a los que está unido); laenergía libreestimada para este proceso es de 6,1 kcal/mol, sustancialmente más baja que los 10,4 kcal/mol necesarios para lainversión del anillo(oscilación más global que si bien conserva la forma del anillo, hace cambiar las posiciones espaciales entre átomos).[11] En el caso de la1-metilpiperidina,la conformación ecuatorial es la preferida por 3,16 kcal/mol,[9] energía mucho mayor que en el caso delmetilciclohexano(1,74 kcal/mol).
 |
 |
Fuentes de piperidina y de sus derivados
[editar]La piperidina ha sido obtenida a partir de lapimienta negra,[12] de las variedades naturalesPsilocaulon absimileN.E.Br (Aizoaceae)[13] yPetrosimonia monandra.[14]
Asimismo, la estructura de la piperidina está presente en numerososalcaloidesnaturales como lapiperina—que da a lapimienta negrasu sabor picante—, la toxina de las hormigas coloradasSolenopsis invicta,[15] el análogo de lanicotinaconocido comoanabasina—delarbustoNicotiana glauca—, lalobelinadeLobelia inflatao el alcaloide tóxicocicutinaprocedente del género de plantasConium.
Síntesis
[editar]A nivel industrial, la piperidina es producida porhidrogenaciónde lapiridina,normalmente catalizada pordisulfuro de molibdeno:[16]
- C5H5N + 3 H2→ C5H10NH
La piridina también puede ser reducida a piperidina porsodioenetanolen unareducción de Birchmodificada,[17] o utilizando como catalizadornanopartículasderuteniosobreóxido de magnesio.[18]
Otra vía de síntesis consiste en unadeshidrogenaciónde5-amino-1-pentanolutilizando complejos deosmioy rutenio como catalizadores.[19] También se puede obtener piperidina a partir de laciclacióndecadaverinaa 180 °C en presencia de un catalizador de rutenio endifenil éter.[20]
Usos
[editar]La piperidina se emplea como disolvente y como base. Lo mismo sucede con algunos de sus derivados, como laN-formilpiperidina,disolvente apróticocon mayor solubilidad parahidrocarburosque otros disolventes del grupo de lasamidas,y la2,2,6,6-tetrametilpiperidina,base muy útil debido a su bajanucleofiliay alta solubilidad en disolventes orgánicos.
Otra importante aplicación industrial de la piperidina es en la producción de dipiperidinil ditiuram tetrasulfuro, utilizado como acelerador en lavulcanizacióndelcaucho.[16]
La piperidina y sus derivados son muy empleados en la síntesis de productos farmacéuticos. La estructura de la piperidina se encuentra en compuestos comoparoxetina,risperidona,metilfenidato,raloxifeno,minoxidil,tioridazina,haloperidol,droperidol,mesoridazina,petidina,melperona,los agentes psicoquímicosDitran-B (JB-329),N-metil-3-piperidil benzilato(JB-336) y muchos otros.
La piperidina, como amina secundaria, se emplea para convertircetonasenenaminas,o como base en lacondensación de Knoevenagel.[21] Las enaminas así elaboradas pueden usarse en reacciones dealquilación de enaminas de Stork.[22] Asimismo, la piperidina es ampliamente utilizada en reacciones químicas de degradación, como la secuenciación deADNy la posterior escisión de algunosnucleótidosespecíficamente modificados.
Por otra parte, esta cicloamina aparece, como sustancia precursora, en la Tabla II de laConvención de las Naciones Unidas Contra el Tráfico Ilícito de Drogas Narcóticas y Sustancias Psicotrópicas,debido a su uso en los años 70 en la industria clandestina de lafenciclidina(compuesto también conocido como «polvo de ángel»).[23]
Precauciones
[editar]La piperidina es un compuestoinflamableque al arder desprendeóxidos de nitrógenotóxicos. Supunto de inflamabilidades 3 °C. Las mezclas del vapor de esta amina con el aire son explosivas a temperatura ambiente. Es un fuerte irritante que puede provocar daños permanentes después de una exposición corta incluso en pequeñas cantidades. Su ingestión puede implicar cambios tanto reversibles e irreversibles. Dosis de 30-60 mg/kg pueden ocasionar síntomas en el organismo humano.[6]
Véase también
[editar]Referencias
[editar]- ↑Número CAS
- ↑Véase:
- Edgar W. Warnhoff (1998) "When piperidine was a structural problem,"Bulletin of the History of Chemistry,22:29-34.University of Illinois
- Thomas Anderson (1850)"Vorläufiger Bericht über die Wirkung der Salpetersäure auf organische Alkalien",Annalen der Chemie und Pharmacie,75:80-83 (p. 82).
- Auguste Cahours (1852)"Recherches sur un nouvel alcali dérivé de la pipérine",Comptes rendus,34:481-484. Cahours la denominó piperidina (p. 483):"L'alcali nouveau dérivé de la piperine, que je désignerai sous le nom depiperidine... "
- (Nota: Ambos obtuvieron la piperidina haciendo reaccionar piperina conácido nítrico.)
- ↑Alexander Senning (2006).Elsevier's Dictionary of Chemoetymology.Amsterdam: Elsevier.ISBN0444522395.
- ↑Piperidine (ChEBI)
- ↑Frank Johnson Welcher (1947).Organic Analytical Reagents.D. Van Nostrand. pp.149.
- ↑abcdPiperidina(PubChem)
- ↑Piperidine(ChemSpider)
- ↑1-Oxa-4-azacyclohexane (Chemical Book)
- ↑abLuis Carballeira, Ignacio Pérez-Juste (1998).«Influence of calculation level and effect of methylation on axial/equatorial equilibria in piperidines».Journal of Computational Chemistry19(8): 961-976.doi:10.1002/(SICI)1096-987X(199806)19:8<961::AID-JCC14>3.0.CO;2-A.
- ↑Ian D. Blackburne, Alan R. Katritzky, Yoshito Takeuchi (1975). «Conformation of piperidine and of derivatives with additional ring hetero atoms».Acc. Chem. Res.8(9): 300-306.doi:10.1021/ar50093a003.
- ↑F.A.L. Anet, Issa Yavari (1977). «Nitrogen inversion in piperidine».J. Am. Chem. Soc.99(8): 2794-2796.doi:10.1021/ja00450a064.
- ↑Spaeth and Englaender, Ber.1935,68, 2218; cf. Pictet and Pictet, Helv. Chim. Acta, 1927, 10, 593
- ↑Rimington, S. Afr. J. Sci, 1934, 31, 184
- ↑Juraschewski and Stepanov, J. Gen. Chem., U.R.S.S., 1939, 9, 1687
- ↑Arbiser JL, Kau T, Konar M et al. (2007). «Solenopsin, the alkaloidal component of the fire ant (Solenopsis invicta), is a naturally occurring inhibitor of phosphatidylinositol-3-kinase signaling and angiogenesis».Blood109(2): 560-5.PMID16990598.doi:10.1182/blood-2006-06-029934.
- ↑abKarsten Eller, Erhard Henkes, Roland Rossbacher, Hartmut Höke “Amines, Aliphatic” Ullmann's Encyclopedia of Industrial Chemistry 2002 Wiley-VCH.doi10.1002/14356007.a02_001
- ↑C. S. Marvel and W. A. Lazier (1941). "Benzoyl Piperidine".Org. Synth.;Coll. Vol.1:99.
- ↑Minfeng Fang, Roberto A. Sánchez-Delgado (2014).«Ruthenium nanoparticles supported on magnesium oxide: A versatile and recyclable dual-site catalyst for hydrogenation of mono- and poly-cyclic arenes, N-heteroaromatics, and S-heteroaromatics».Journal of Catalysis311:357-368.Consultado el 12 de junio de 2016.
- ↑Marcello Bertoli; Aldjia Choualeb; Alan J. Lough; Brandon Moore; Denis Spasyuk; Dmitry G. Gusev (2011).«Osmium and Ruthenium Catalysts for Dehydrogenation of Alcohols».Organometallics30(13): 357-368.Consultado el 12 de junio de 2016.
- ↑Bui-The-Khai; Concilio, Carlo; Porzi, Gianni (1981).«Cyclization of. Alpha.,. Omega. aliphatic diamines and conversion of primary amines to symmetrical tertiary amines by a homogeneous ruthenium catalyst».The Journal of Organic Chemistry46(8): 1759-1760.Consultado el 12 de junio de 2016.
- ↑Vinayak V. Kane and Maitland Jones Jr (1990). "Spiro[5.7]trideca-1,4-dien-3-one".Org. Synth.;Coll. Vol.7:473.
- ↑Michael B. Smith; Jerry March (2001).March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure(5th edición). Wiley-Interscience.ISBN0-471-58589-0.
- ↑List of Precursors and Chemicals Frequently Used in the Illicit Manufacture of Narcotic Drugs and Psychotropic Substances Under International Control,International Narcotics Control Board

