Tuberculosis
| Tuberculosis | ||
|---|---|---|
 Radiografíade tórax proveniente de un paciente con tuberculosis muy avanzada | ||
| Especialidad |
infectología neumología | |
| Síntomas | Toscrónica,fiebre,tos con mucosidad sanguinolenta, pérdida de peso | |
| Causas | Mycobacterium tuberculosis | |
| Factores de riesgo | Tabaquismo,VIH/SIDA | |
| Diagnóstico | Rx de tórax, cultivo,prueba cutánea de tuberculina | |
| Prevención | Detección de personas con alto riesgo, tratamiento de las personas infectadas,vacunación con bacilo de Calmette-Guérin(BCG) | |
| Sinónimos | ||
| Tisis, tisis pulmonalis, tisis, gran peste blanca, héctico | ||
Latuberculosis(abreviadaTBCoTB), llamada alternativa e históricamentepeste blancaotisis[1] (delgriegoφθίσις,a través dellatínphthisis), es una infecciónbacterianacontagiosa que afecta a lospulmones,pero puede propagarse a otros órganos. La especie de bacteria más importante y representativa causante de la tuberculosis esMycobacterium tuberculosisobacilo de Koch,perteneciente alcomplejo Mycobacterium tuberculosis.[2] Existe una vacuna (BCG) para poder prevenir esta enfermedad.
Es, tal vez, laenfermedad infecciosamásprevalentedel mundo. Considerando su forma latente, en la cual no presenta síntomas, se estima que afecta al 33 % de la población mundial.[3] Es la segunda causa global de muerte, y la primera entre las enfermedades infecciosas.[4][5][6][7]
Otrasmicobacterias,comoMycobacterium bovis,Mycobacterium africanum,Mycobacterium canettiyMycobacterium microtipueden causar tuberculosis, pero todas esas especies no suelen hacerlo en un individuo sano.
Los síntomas de tuberculosis son:tos crónicaconesputo sanguinolento,fiebre,sudores nocturnosypérdida de peso.La infección de otros órganos causa una amplia variedad de síntomas.
El diagnóstico se basa en laradiología(radiografías torácicas), unaprueba de la tuberculina cutáneay un análisis de sangre. También se complementa con un examen microscópico y uncultivo microbiológicode los fluidos corporales, como las expectoraciones. El tratamiento es complicado y requiere largos periodos de exposición con antibióticos. Los familiares del enfermo también son analizados.
Durante los últimos años, la tuberculosis ha presentado una creciente resistencia a los múltiples antibióticos y para ello se ha optado, como medida de prevención, por campañas de vacunación, en general con la vacunaBacillus Calmette-Guérin(BCG)[8].[cita requerida]
Se contagia por vía aérea, cuando las personas infectadas tosen, estornudan o escupen. Además, un número creciente de personas del mundo la contrae debido a que su sistema inmunitario se debilita pormedicamentos inmunosupresoreso elsida.La distribución de la tuberculosis no es uniforme en el mundo; el 80 % de la población de países asiáticos y africanos da positivo, porcentaje que baja a 5-10 % de la población enEstados Unidos.
Según datos de laOrganización Mundial de la Salud(OMS), en 2022, 10,6 millones de personas enfermaron de tuberculosis en todo el mundo: 5,8 millones de hombres (55%), 3,5 millones de mujeres (33%) y 1,3 millones de niños (12%) de entre 0 y 14 años de edad. 1,3 millones de personas murieron por tuberculosis en 2022, de los cuales 167 000 teníaninfección por VIH.Las actividades desarrolladas en todo el mundo desde el año 2000 para combatir la tuberculosis han salvado la vida a 75 millones de personas, pero la OMS considera «todavía inaceptablemente alta» la cantidad de estas muertes prevenibles.[9]
Signos y síntomas[editar]


La tuberculosis se puede manifestar por signos clínicos y síntomas pulmonares o extrapulmonares.
Tuberculosis pulmonar[editar]
- Neumonía tuberculosa: puede deberse a primoinfección o a reactivación, aunque la infección primaria suele causar pocos síntomas (paucisintomática). La primoinfección se caracteriza por la formación del complejo primario de Ghon (adenitisregional parahiliar,linfangitisyneumonitis). La clínica en la reactivación suele ser insidiosa, confebrículay malestar general. Es frecuente la sudoración nocturna y la pérdida de peso. En cuanto a semiología pulmonar, suele haber tos persistente que puede estar acompañada deesputos hemoptoicos(sanguinolentos). La neumonía tuberculosa es muy contagiosa, sus pacientes deben estar aislados durante dos semanas desde el inicio del tratamiento.
- Pleuritis tuberculosa: aparece en personas jóvenes y suele hacerlo de forma aguda y unilateral. El signo principal es unexudado en el espacio pleural.Característica de este exudado es que se detecta la enzima adenosin-desaminasa (ADA) elevada. El tipo celular predominante en el exudado son loslinfocitosy las células mesoteliales son escasas.
Tuberculosis extrapulmonar[editar]
Latuberculosis extrapulmonar,puede aparecer en el contexto de unatuberculosis miliar,la reactivación de un foco pulmonar o en ausencia de enfermedad clínica pulmonar. Incluye:
- Tuberculosis meníngea:forma demeningitisbacterianacausada porMycobacterium tuberculosiso más raramenteMycobacterium bovis.El organismo se asienta en las meninges, predominante en la base encefálica, y forma microgranulomas con posterior rotura. El curso clínico tiende a ser subagudo, que progresa en días. Los síntomas pueden ser: dolor de cabeza, rigidez de nuca, déficits neurológicos.
- Tuberculosis ocular:infección tuberculosa deliris,cuerpos ciliares ycoroides.
- Tuberculosis cardiovascular: tuberculosis que afecta acorazón humano,pericardioovasos sanguíneos.Lapericarditis tuberculosapuede evolucionar a pericarditis constrictiva, hecho que lleva al uso de corticoesteroides en su tratamiento.
- Tuberculosis del sistema nervioso central: tuberculosis delcerebro,médula espinalomeninges.Causada porMycobacterium tuberculosiso, más raro, porMycobacterium bovis.
- Tuberculosis genitourinaria:causa habitual de piuria estéril (leucocitos en orina sin germen visible). El acceso de la infección al aparato genitourinario suele ser por vía sanguínea. Puede ser causa de esterilidad por afectación de los epidídimos en los hombres y de la trompas de Falopio en las mujeres.
- Tuberculosis ganglionar:compromete las cadenas ganglionares cervicales y supraclaviculares. Produce hinchazón de losganglios linfáticos.Puede presentar escrofulodermia: hinchazón de extensión local del tejido subcutáneo por una reactivación del bacilo tuberculoso en dichos tejidos. En este caso, se producen fístulas o úlceras drenantes, que presentan fibrosis e induración además de color rojizo oscuro. Es común en jóvenes y niños. En infantes es muy común que la infección se presentase en ganglios superficiales acompañados de fístulas. El 50 % de los casos, tanto en jóvenes como en niños, la enfermedad se manifiesta con grave hinchazón de los ganglios cervicales. El ganglio hinchado se presenta en exploración física como una gran masa dolorosa y con probable fistulación (escrófula). Dicha fistulación (escrofulodermia) suele ser de color rojo oscuro. En todos los casos hayfiebre.
- Tuberculosis osteoarticular:tras una infección pulmonar el bacilo puede circular por el torrente sanguíneo hasta alojarse en algún hueso o articulación, se trataría así de una osteoartritis tuberculosa o tuberculosis osteoarticular. También puede aparecer osteomielitis tuberculosa sin afectación articular, aunque su frecuencia es baja. La infección puede originarse por una herida producida por un objeto contaminado con el bacilo, si bien no está documentada ninguna por esta vía. En la década de 1930 se realizaban tratamientos conluz de arco de carbóncon resultados dispares.[11][12]
-Diseminados(TBC miliar)
- Tuberculosis miliar:forma de tuberculosis debida a la diseminación sanguínea del bacilo, afectando a distintos órganos. Suele ocurrir en personas con grave alteración del sistema inmune. Es más frecuente en ancianos. Puede cursar con inicio agudo o insidioso. La sintomatología es dominada por fiebre y otros síntomas constitucionales. Para su diagnóstico deben practicarse alguno o todos los siguientes cultivos: esputo, orina, jugo gástrico o médula ósea.
Transmisión[editar]
La transmisión de la tuberculosis solo puede realizarse por personas que tengan activa la enfermedad. La TBC se transmite a través de partículas expelidas por el pacientebacilífero(con TBC activa) con la tos, estornudo, hablando, escupida, etc., por lo que se recomienda no tener contacto con terceros. Las gotas infecciosas (flügge's o droplets) son de un diámetro entre 0,5 a 5µm,pueden producirse alrededor de 400 000 con un solo estornudo.[13] Cada una de esas gotitas proveniente de un enfermo activo puede transmitir el microorganismo, en especial sabiendo que la dosis infectante de la tuberculosis es considerada baja, de modo que la inhalación de una sola bacteria puede infectar.[14] La probabilidad de una transmisión eficaz aumenta con el número de partículas contaminadas expelidas por el enfermo, en lo buena que sea la ventilación del área, la duración de la exposición y en lavirulenciade lacepadelM. tuberculosis.Las personas con contactos frecuentes, prolongados, o intensos tienen un riesgo de alrededor del 25 % de ser infectados. Para un fumador las posibilidades de enfermar se multiplican por 2,5.[15] Un paciente con TBC activa sin tratamiento puede infectar entre 10-15 personas por año. Otros riesgos incluyen aquellas áreas donde la TBC es frecuente, en pacientes inmunodeprimidos con condiciones comomalnutriciónysida,poblaciones étnicas en alto riesgo y trabajadores de la salud sirviendo en regiones de alto riesgo.[16] En los pacientes con sida, la TBC actúa como enfermedad oportunista (coinfección) con fuerte asociación. También puede transmitirse por vía digestiva, sobre todo al ingerir leche no higienizada procedente de vacas tuberculosas infectadas conMycobacterium bovis.
La cadena de transmisión puede romperse si se aísla al enfermo con tuberculosis activa y comenzando de inmediato una terapia antituberculosis efectiva. Después de dos semanas con dicho tratamiento, aquellos pacientes con TBC activa y no-resistente dejan de ser contagiosos. Si una persona llegase a quedar infectada, le tomará menos de 20 a 60 días antes que pueda comenzar a transmitir la enfermedad a otros.[17]
Cuadro clínico de la tuberculosis[editar]

En elcomienzo de la enfermedad,las personas con tuberculosis pueden tener síntomas comunes a otras enfermedades, como sonfiebre,cansancio,falta deapetito,pérdida de peso,depresión,sudornocturno ydisneaen casos avanzados; más cuando se agregan las aflicciones de tos yexpectoraciónpurulenta por más de quince días debe estudiarse, pues se considera un síntoma respiratorio.
En un 25 por ciento de los casos activos, la infección se traslada de los pulmones, causando otras formas de tuberculosis. Ello ocurre con más frecuencia en aquellos pacientes inmunosuprimidos y en niños. Las infecciones extrapulmonares incluyen lapleura,elsistema nervioso centralcausandomeningitis,el sistema linfático causandoescrófuladel cuello, elsistema genitourinariocausando tuberculosis urogenital y los huesos o articulaciones en el caso de laenfermedad de Pott.Una forma muy seria de diseminada es latuberculosis miliar.A pesar de que la extrapulmonar no es contagiosa, puede coexistir con la contagiosa tuberculosis pulmonar.[18]
Historia[editar]
La tuberculosis es una de las enfermedades humanas más antiguas. Aunque se estima entre 15 000 a 22 000 años, se acepta más que esta especie evolucionó de otros microorganismos más primitivos dentro del géneroMycobacterium.Puede pensarse que en un momento, alguna especie de microbacterias traspasara labarrera biológica,por presión selectiva, y pasara a tener unreservorioenanimales.Es posible que esto haya dado lugar a un anciano progenitor delMycobacterium bovis,aceptada por muchos como la más antigua de las especies del complejoMycobacterium tuberculosis,que incluyeM. tuberculosis,M. bovis,M. africanumyM. microti.El "escalón" siguiente sería el paso delM. bovisa la especie humana, coincide con la domesticación de los animales. Así pudo surgir como patógeno para el perro.
Patogenia de la tuberculosis[editar]
La tuberculosis constituye un paradigma de la interacción de un agente exógeno y la respuesta inmunitaria del huésped. La Organización Mundial de la Salud estima 2000 millones de infectados por elM. tuberculosisy ocho millones de nuevos infectados cada año, venciendo la batalla en la mayoría de las ocasiones. Sin embargo, mueren casi dos millones de personas al año por causa de esta enfermedad.
- Infección tuberculosa latente:la infección porM. tuberculosissuele realizarse por vía aérea. De esta manera, el bacilo es fagocitado por losmacrófagosalveolares. En un 30 % de los casos, estos macrófagos son incapaces de destruirlo. Entonces se genera la infección, que se caracteriza por el crecimiento en el interior delfagosomade los macrófagos infectados. Ello se debe a que el bacilo es capaz de frenar la unión fago-lisosoma. Desde lo histopatológico, en elfoco de infecciónse genera ungranuloma,caracterizado por la presencia de tejido necrótico intragranulomatoso y que por fin se estructura con la adquisición de la inmunidad. Con la inmunidad, los macrófagos infectados pueden activarse y destruir el bacilo, de manera que se controla su concentración.
Entonces empieza la infección latente, caracterizada por la presencia de respuesta inmune específica, control de la concentración bacilar, pero con la presencia de bacilos latentes (en estado estacionario) en el tejido necrótico. A medida que los macrófagos van drenando este tejido, los bacilos latentes se confunden con esta necrosis y son drenados hacia el espacio alveolar, donde pueden reactivar su crecimiento de nuevo. De esta manera se mantiene la infección durante años.
Desde lo clínico, la infección tuberculosa latente no genera síntomas. Su diagnóstico se basa en eltest cutáneo de Mantoux.Los individuos con esta infección no pueden infectar a nadie. Sin embargo, en un 10 % de los casos, el control de la concentración bacilar se pierde, se reanuda el crecimiento y se puede generar una tuberculosis activa, o enfermedad tuberculosa propia. Por ello debe tratarse, sobre todo los pacientes recién infectados. El tratamiento representa la administración de isoniazida durante 9 meses, hecho que dificulta su seguimiento.
Progresión[editar]
Progresa de infección tuberculosa a enfermedad tuberculosa. Puede ocurrir de forma temprana (tuberculosis primaria, alrededor del 1-5 %) o varios años después de la infección (tuberculosis postprimaria, secundaria, reactivación tuberculosa en alrededor del 5 al 9 %). El riesgo de reactivación se ve incrementado con alteraciones en el sistema inmunitario, tales como las causadas por elVIH.En pacientes coinfectados de VIH y TBC, el riesgo de reactivación se incrementa un 10 % por año, mientras que en una persona inmunocompetente el riesgo es del 5 al 10 % durante toda la vida.
Algunos fármacos, incluyendo tratamientos usados en laartritis reumatoideque bloquean elfactor de necrosis tumoral,aumentan el riesgo de activación de una TBC latente debido a la importante acción de estacitoquinaen la respuesta inmune contra la TBC.
Diagnóstico[editar]
La TBC activa se diagnostica por la detección deMycobacterium tuberculosisen cualquier muestra del tracto respiratorio (TBC pulmonar) o fuera de él (TBC extrapulmonar). Aunque algunos métodos más modernos (diagnóstico molecular) han sido desarrollados, la visión microscópica debacilos ácido-alcohol resistentes(BAAR) y el cultivo enmedio de Löwenstein-Jensensiguen siendo elgold standarddel diagnóstico de la TBC, en especial en países con bajos recursos sanitarios, aunque el métodoMODSviene siendo validado dando resultados con una sensibilidad y especificidad superiores al cultivo. La microsocopía de BAAR es rápida y barata y un método muy eficiente para detectar pacientes contagiosos. El uso de cultivo en la TBC se realiza cuando hay poca carga bacteriana (mayor sensibilidad), para la identificación de la cepa y para el estudio de sensibilidades a los distintos tratamientos.Tanto la microscopia como el cultivo pueden usarse para monitorizar el tratamiento.[19]
Autofluorescencia[editar]
LaUniversidad Autónoma de Madridpublicó en elJournal of Clinical Microbiologyun trabajo donde se describe por primera vez que las micobacterias son capaces de emitir fluorescencia, lo que permite verlas en un microscopio de fluorescencia sin necesidad de una tinción previa. Esta característica presenta interés para el diagnóstico de la tuberculosis, ya que antes era necesario recurrir a las tinciones específicas para poder observar la mayoría de las bacterias, ya que muy pocas presentan autofluorescencia. Sin embargo, la autofluorescencia emitida por las micobacterias de color azul celeste es tan intensa y brillante como cuando son teñidas de verde con el método antiguo. Además se ha constatado que el fenómeno es permanente, no disminuyendo la autofluorescencia con el paso del tiempo por lo que no es necesaria una conservación especial de las muestras para su mantenimiento.[20]
Radiografía de tórax[editar]

La radiografía es esencial en el diagnóstico de la enfermedad. Las lesiones típicas radiológicas son apicales, en hemitórax derecho, en segmentos posteriores y en general forman cavidades.
La herramienta para el diagnóstico de caso de tuberculosis es la bacteriología (baciloscopía y cultivo) por su altaespecificidad,sensibilidadyvalor predictivo.En aquellas situaciones donde los estudios bacteriológicos no sean concluyentes será necesario realizar el seguimiento diagnóstico de acuerdo con la organización de la red de servicios de salud, utilizando otros criterios: clínico, epidemiológico, diagnóstico por imágenes, inmunológico, anatomopatológico.
Toda persona con diagnóstico de tuberculosis previa consejería y aceptación se deberá realizar la prueba de diagnóstico paraVIH.
Baciloscopiade esputo[editar]

Consiste en una prueba seriada (tres días consecutivos), donde se toma una muestra deesputopara ver qué bacteria se encuentra. Con un costo bajo y de rápida ejecución, la baciloscopia es una técnica que permite identificar al 70-80 % de los casos pulmonares positivos.[21] La bacteriaMycobacterium tuberculosisposee una estructura de pared diferente de aquellas que son capaces de ser tipificables por la tinción Gram, al presentar una cantidad de lípidos muy abundante. Se le denomina ácido-alcohol resistente y esta característica es la que permite su observación por latinción de Ziehl Neelsen.
Cultivo de muestra biológica[editar]
El cultivo puede hacerse en elmedio de Löwenstein-Jensen,que está constituido por:
- huevo (albúmina,lípidos) (coagula y le da solidez)
- verde de malaquita(inhibe otras bacterias)
- glicerol(fuente de carbono)
- asparaginas(fuente de nitrógeno)
Crece muy lento (30 a 90 días) a 37 °C en atmósfera con dióxido de carbono (en cultivo crecen mejor a pesar de ser aerobio estricto), dando colonias con aspecto de migas de pan (o huevos de araña), secas amarillentas y rugosas.
Prueba de la tuberculina mediante la técnica de Mantoux[editar]

Es una prueba cutánea (intradermoreacción) para detectar infección tuberculosa. Se utiliza como reactivo elPPD(Derivado Proteico Purificado). La prueba de la tuberculina Mantoux solo implica contacto, no infección.
MODS (Microscopic observation drug susceptibility)[editar]
Lasusceptibilidad a drogas de Mycobacterium tuberculosis mediante observación microscópica(MODS) es un método de desarrollo reciente que posee una sensibilidad y especificidad muy elevadas, como también una gran reducción del tiempo para el diagnóstico de infección por elMycobacterium tuberculosis,a la vez que evalúa la resistencia a antibióticos de primera línea, como laisoniaciday larifampicinapara los pacientes TB-MDR (multidrogorresistentes).[22]
Tratamiento[editar]
El tratamiento de la tuberculosis se realiza con combinaciones de fármacos antituberculosos, haciendo eficaces las pautas de seis meses de tratamiento, dos en la primera fase de tratamiento y cuatro meses en la segunda fase.[23]
La tuberculosis es curable, pero es necesario un diagnóstico temprano (acudir de inmediato al médico), ya que es una enfermedad grave si no se sigue el tratamiento. Además, es indispensable no abandonar el tratamiento dado por el médico porque, al suspenderlo, la enfermedad empeora rápido y favorece la proliferación debacilosresistentes a los medicamentos.
Tratamiento sanatorial de la tuberculosis[editar]

Se inicia a mediados del siglo XIX y primera mitad del XX, se generaliza como base del tratamiento, sobre todo en los países desarrollados, llega a ser uno de los índices que determinan el nivel sanitario de un país.
Los sanatorios se construían a gran altura, basándose en la teoríafisiológicade aumentar el flujo sanguíneo pulmonar, por lataquicardiainducida por la altura. Sin embargo, la evidencia de su eficacia resultó dudosa.
Tratamiento quirúrgico de la tuberculosis[editar]
Se realizaron diversas técnicas, todas ellas basadas en lacolapsoterapia,que consistía en hacer colapsar el pulmón para que permanecieraen reposoy así ayudar a una cicatrización de las lesiones.
- Procedimientos:
- Condrotomía de primera costilla
- Toracoplastias (amputación de un número decostillaspara conseguir el colapso)
- Resecciones pulmonares
- Frenicectomía(sección delnervio frénicopara paralizar eldiafragma)
- Escalenotomía (sección de losmúsculosescalenos)
- Pneumolisis extrapleural
- Neumotóraxterapéutico: quizá el procedimiento quirúrgico más frecuentemente realizado
Tratamiento farmacológico de la tuberculosis[editar]
La historia de la tuberculosis cambia después de la introducción de los agentes antibióticos. El tratamiento de la tuberculosis es fundamental para su control, dado que con él se rompe la cadena de trasmisión cuando el tratamiento es correcto y se sigue completo.
El tratamiento farmacológico comenzó en 1944 con laestreptomicina(SM) y el ácido paraaminosalicílico (PAS).[24] En 1950, se realizó el primer ensayo clínico comparando la eficacia de la SM y el PAS en conjunto o en monoterapia. El estudio demostró que la terapia combinada era más efectiva. En 1952, un tercer fármaco, laisoniacida(INH), se añadió a la combinación, mejorando en forma espectacular la eficacia del tratamiento, aunque todavía con una duración de 18-24 meses. Eletambutolse introdujo en 1960, sustituyendo al PAS en los esquemas de tratamiento y reduce la duración a 18 meses. En la década de 1970, con la introducción de larifampicina(RAM) en la combinación, el tratamiento se acorta a nueve meses. En 1980, lapirazinamida(PZA) se introduce en el esquema terapéutico, que puede reducirlo a seis meses.[25]
Dos hechos biológicos explican por qué la terapia combinada es más efectiva en el tratamiento de la TBC que la monoterapia. El primero es que el tratamiento con un solo fármaco induce la selección de bacilos resistentes y en consecuencia el fallo en eliminar la enfermedad. El segundo es que las diferentes poblaciones bacilares pueden coexistir en un paciente.
Los antituberculostáticos se clasifican en dos grupos en función de su eficacia, potencia y efectos secundarios:
- Fármacos de primera línea: isoniacida, rifampicina, pirazinamida, etambutol o estreptomicina[26]
- Fármacos de segunda línea: cicloserina, etionamida,ciprofloxacino,etc. Se utilizan en los casos de tuberculosis resistentes o cuando los de primera línea producen efectos secundarios.[26]
Un problema que se extiende en los últimos años es la aparición deM. tuberculosisresistentes a antibióticos.[27] Teniendo en cuenta las resistencias a antibióticos que presentan distintas cepas, es posible distinguir entre cepas multirresistentes (MDR), que son bacterias que desarrollan resistencia frente a rifampicina (RMP) e isoniacida (INH), y cepas ultrarresistentes (XDR), resistentes a drogas de primera línea y a cualquier miembro de la familia de las fluoroquinolonas y al menos frente a uno de segunda línea.[28]
Prevención[editar]

Se previene mediante una vida sana e higiénica, con identificación temprana de los enfermos y asegurando su curación para no contagiar a otras personas, por medio de la vacunaBCG.
La vacunación sistemática con la BCG en los recién nacidos se abandonó en España en 1980.[29][30][31]
Medidas preventivas[editar]
- La persona infectada debe protegerse siempre que tosa con pañuelos desechables.
- Lavado de manos después de toser.
- Ventilación adecuada de la residencia.
- Limpiar el domicilio con paños húmedos.
- Utilizar mascarilla en zonas comunes.
- Restringir visitas a personas no expuestas a la enfermedad.
- Garantizar adherencia al tratamiento.
- No fumar. Elcigarrillono causa tuberculosis, pero sí favorece el desarrollo de la enfermedad.
Vacunas[editar]
BCG[editar]
La vacuna BCG (Bacillus Calmette-Guérin), usada desde 1921, se sigue usando en muchos países como parte de los programas de control de la tuberculosis, en especial en niños. Esta vacuna fue desarrollada en elInstituto Pasteur,Francia,entre 1905 y 1921.[32] Sin embargo, las vacunaciones masivas no comenzaron hasta después de laSegunda Guerra Mundial.[33] La eficacia en la protección de la BCG en formas graves de tuberculosis (p. ej.:meningitis) en niños menores de 4 años es grande (BCG protege contralainfección porM. tuberculosis,así como contra la progresión de la infección a la enfermedad. Larevisión sistemáticaymetaanálisisse realizó en niños menores de 16 vacunados y no vacunados con exposición reciente a infección tuberculosa),[34] y está alrededor del 80 %; su eficacia en adolescentes y adultos es más variable, estando entre el 0 y el 80 %.[35]
RUTI[editar]
RUTI es una vacuna terapéutica que se desarrolla en la Unidad de Tuberculosis Experimental de Badalona (España) para disminuir el tratamiento de la infección tuberculosa latente[36][37] de 9 a 1 mes de administración de isoniacida. Responsables son Archivel Farma y elHospital Germans Trias i PujoldeBadalona,conocido como Can Ruti, lo que ha dado nombre a la vacuna.
Vacuna MTBVAC[editar]
LaMTBVACes la primera vacuna con el bacilo atenuado de tuberculosis humano. La actual BCG, es debos taurus.[38] El grupo de launiversidad de Zaragoza,dirigido por el investigadorCarlos Martín Montañés,en colaboración con la farmacéutica gallegaBiofabri,del grupoZendal,ha demostrado que su vacuna desarrollada da mayor protección contra el patógeno que la vacuna actual.[39]Biofabrirealizó en el años 2019 con éxito los primeros ensayos clínicos en humanos y tiene prevista su producción industrial.[40]
Día Mundial de la Lucha contra la Tuberculosis[editar]
LaOMSestipuló que el 24 de marzo sería elDía Mundial de la Lucha contra la Tuberculosis.Se conmemora que el 24 de marzo de 1882 el doctorRobert Kochanunció el descubrimiento delbacilode la tuberculosis.
En 1982 se realizó el primer Día Mundial de la Lucha contra la Tuberculosis, con el patrocinio de la Organización Mundial de la Salud (OMS) y la Unión Internacional Contra la Tuberculosis y las Enfermedades Respiratorias (UICTER). Este evento buscaba educar al público sobre las devastadoras consecuencias económicas y de salud causadas por la tuberculosis, su efecto en los países en desarrollo y su impacto continuo y trágico en la salud global.
Epidemiología en todo el mundo[editar]
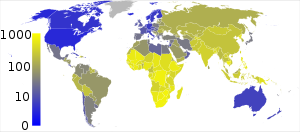

Según la Organización Mundial de la Salud (OMS), un cuarto de la población del mundo, han estado expuestas al patógeno de la tuberculosis. Sin embargo, no todas las infecciones porM. tuberculosiscausa la tuberculosis y muchas infecciones son asintomáticas. Cada año, ocho millones de personas se enferman con la tuberculosis, y dos millones de personas mueren de la enfermedad a escala mundial. En 2004, alrededor de 14,6 millones de personas tenían la enfermedad activa con 9 millones de nuevos casos. La tasa de incidencia anual varía de 356 por 100 000 en África y 41 por 100 000 en América. Provoca enfermedades infecciosas en las mujeres en edad reproductiva y es la principal causa de muerte entre las personas con sida.
En 2005, el país con la mayor incidencia estimada de tuberculosis fue deSuazilandia,con 1262 casos por cada 100 000 personas. La India tiene el mayor número de infecciones, con más de 1,8 millones de casos. En los países desarrollados, la tuberculosis es menos común y es una enfermedad urbana. En el Reino Unido, la incidencia de tuberculosis va desde 40 por 100 000 en Londres, a menos de 5 por 100 000 en zonas rurales del sur oeste de Inglaterra, de la media nacional es de 13 por 100 000. Las tasas más altas de Europa occidental se sitúan en Portugal (31,1 por 100 000 en 2005) y España (20 por 100 000). Estos rangos comparan con 113 por 100 000 en China y 64 por 100 000 en Brasil. En los Estados Unidos, la tasa general de casos de tuberculosis fue de 4,9 por 100 000 personas en 2004. En España la tuberculosis sigue siendo endémica en algunas zonas rurales. La incidencia de la tuberculosis varía con la edad. En África, la tuberculosis afecta a adolescentes y adultos jóvenes. Sin embargo, en países donde la tuberculosis ha pasado de alta a baja incidencia, como los Estados Unidos es una enfermedad de personas mayores o de los inmunocomprometidos.
Las infecciones, el aumento del VIH y el descuido de control de la tuberculosis por programas han permitido su resurgimiento. La aparición de resistencia en unas cepas también ha contribuido a una nueva epidemia, de 2000 a 2004, el 20 % de los casos de tratamientos estándar eran resistentes a de medicamentos de segunda línea. El ritmo de los nuevos casos varía con amplitud, incluso en los países vecinos, debido a las filas en los sistemas de atención sanitaria.
Un problema que se está extendiendo en los últimos años es la aparición deM. tuberculosisresistentes a antibióticos. La tuberculosis multirresistente se ha encontrado en casi todos los países estudiados. En 2012, entre los casos notificados de tuberculosis pulmonar hubo unos 450 000 casos de tuberculosis multirresistente. Casi el 50 % de ellos correspondían a la India, China y la Federación Rusa. Se cree que un 9,6 % de los casos de tuberculosis multirresistente presentaban tuberculosis ultrarresistente.[9]
Hay una serie de factores que hacen que las personas sean más susceptibles a la infección; el más importante de ellos es el VIH. La coinfección con el VIH es un problema particular en elÁfrica subsahariana,debido a la alta incidencia de VIH en estos países. Los fumadores que consumen más de 20 cigarrillos al día también aumentan el riesgo de la tuberculosis de dos a cuatro veces. Ladiabetes mellituses un factor de riesgo que está creciendo en importancia en los países en desarrollo.
Otros estados de enfermedad que aumentan el riesgo de desarrollar tuberculosis son ellinfoma de Hodgkin,el final de la enfermedad renal,enfermedad pulmonar crónica,ladesnutricióny elalcoholismo.
La dieta también puede modular el riesgo. Por ejemplo, entre los inmigrantes enLondresdesde el subcontinente indio, los vegetarianos hindúes tenían un 8,5 veces más riesgo de tuberculosis, en comparación con losmusulmanesque comían carne y pescado todos los días. A pesar de una relación de causalidad no se prueba por estos datos este aumento del riesgo que podría ser causado por las deficiencias demicronutrientes,es posible que de hierro,vitamina B12ovitamina D.
Otros estudios han proporcionado más evidencias de una relación entre la deficiencia de vitamina D y un mayor riesgo de contraer tuberculosis. La malnutrición grave común en algunas partes del mundo en desarrollo provoca un gran aumento en el riesgo de desarrollar tuberculosis activa, debido a sus efectos nocivos sobre el sistema inmunitario. Junto con elhacinamiento,la mala alimentación puede contribuir al fuerte vínculo entre la tuberculosis y la pobreza.
Véase también[editar]
- Bacilo de Koch
- Historia de la tuberculosis
- Fundación Bill y Melinda Gates
- Tuberculosis en Guipúzcoa
- Tuberculosis de los mamíferos
Referencias[editar]
- ↑Real Academia Española.«tisis».Diccionario de la lengua española(23.ª edición).Consultado el 14 de abril de 2019.
- ↑Delogu, Giovanni; Sali, Michela; Fadda, Giovanni (noviembre de 2013).«The Biology of Mycobacterium Tuberculosis Infection» [La biología de la infección por Mycobacterium Tuberculosis].Mediterr J Hematol Infect Dis(en inglés)(Roma: Catholic University in Rome)5(1): e2013070.PMID24363885.doi:10.4084/MJHID.2013.070.Consultado el 17 de noviembre de 2017.
- ↑«10 datos sobre la tuberculosis»(html).Organización Mundial de la Salud.31 de marzo de 2017. Archivado desdeel originalel 31 de enero de 2018.Consultado el 24 de septiembre de 2018.«Aproximadamente un tercio de la población mundial está infectada por el bacilo de la tuberculosis. Solo una pequeña proporción de los infectados enfermará de tuberculosis.»
- ↑Churchyard, Gavin; Kim, Peter; Shah, N. Sarita; Rustomjee, Roxana; Gandhi, Neel; Mathema, Barun;et al(noviembre de 2017).«What We Know About Tuberculosis Transmission: An Overview» [Lo que sabemos acerca de la transmisión de la tuberculosis: una perspectiva general].The Journal of Infectious Diseases(en inglés)(Infectious Diseases Society of America)216(Supl 6): S629-S635.ISSN1537-6613.doi:10.1093/infdis/jix362.Consultado el 18 de noviembre de 2017.
- ↑Al-Humadi, Hussam W.; Al-Saigh, Rafal J.; Al-Humadi, Ahmed W. (septiembre de 2017).«Addressing the Challenges of Tuberculosis: A Brief Historical Account» [Encarando los desafíos de la tuberculosis: un recuento histórico breve].Front Pharmacol(en inglés)(Frontiers Media SA)8:689.PMID29033842.doi:10.3389/fphar.2017.00689.Consultado el 18 de noviembre de 2017.
- ↑Sulis, Giorgia; Centis, Rosella; Sotgiu, Giovanni; D’Ambrosio, Lia; Pontali, Emanuele; Spanevello, Antonio;et al.(noviembre de 2016).«Recent developments in the diagnosis and management of tuberculosis» [Avances recientes en el diagnóstico y tratamiento de la tuberculosis].NPJ Prim Care Respir Med(en inglés)(Primary Care Respiratory Society UK/Macmillan Publishers Limited)26:16078.PMID27808163.doi:10.1038/npjpcrm.2016.78.Consultado el 18 de noviembre de 2017.
- ↑Houben, Rein M. G. J.; Dodd, Peter J. (octubre de 2016).«The Global Burden of Latent Tuberculosis Infection: A Re-estimation Using Mathematical Modelling» [La carga global de la infección latente de tuberculosis: una re-estimacvión usando modelado matemático].PLoS Med(en inglés)(Public Library of Science)13(10): e1002152.PMID27780211.doi:10.1371/journal.pmed.1002152.Consultado el 18 de noviembre de 2017.
- ↑«Bacillus Calmette-Guerin (BCG, TICE®, TheraCys®) | OncoLink».es.oncolink.org.Consultado el 6 de junio de 2023.
- ↑abWHO.«Global tuberculosis report 2024»(en inglés).WHO.Consultado el 23 de abril de 2024.
- ↑Schiffman, George (11 de junio de 2014).«Tuberculosis Causes, Symptoms, Treatment - Tuberculosis Symptoms and Signs - eMedicineHealth».eMedicineHealth(en inglés).Consultado el 18 de enero de 2016.
- ↑«Niños tratados con luz de arco de carbón (1938)».Archivado desdeel originalel 26 de septiembre de 2009.Consultado el 24 de septiembre de 2009.
- ↑«TUBERCULOSIS OSTEOARTICULAR».Archivado desdeel originalel 14 de abril de 2009.Consultado el 24 de septiembre de 2009.
- ↑Cole, E., Cook, C. (1998).«Characterization of infectious aerosols in health care facilities: an aid to effective engineering controls and preventive strategies».Am J Infect Control26(4): 453-64.PMID9721404.doi:10.1016/S0196-6553(98)70046-X.
- ↑Nicas, M., Nazaroff, W. W., Hubbard, A. (2005). «Toward understanding the risk of secondary airborne infection: emission of respirable pathogens».J Occup Environ Hyg2(3): 143-54.PMID15764538.doi:10.1080/15459620590918466.
- ↑OMS (noviembre de 2009).«La tuberculosis y el tabaco».Consultado el 12 de abril de 2015.
- ↑Griffith D, Kerr C (1996). «Tuberculosis: disease of the past, disease of the present».J Perianesth Nurs11(4): 240-5.PMID8964016.doi:10.1016/S1089-9472(96)80023-2.
- ↑«Causes of Tuberculosis»(en inglés).Mayo Clinic.21 de diciembre de 2006.Consultado el 19 de octubre de 2007.
- ↑Centers for Disease Control and Prevention(CDC), Division of Tuberculosis Elimination.Core Curriculum on Tuberculosis: What the Clinician Should Know.4.ª edición (2000). Actualizado en agosto de 2003. En inglés.
- ↑«CDC».Consultado el 8 de junio de 2007.
- ↑Universidad Autónoma de Madrid (24 de noviembre de 2008).«Autofluorescencia, comunicación de la Universidad Autónoma de Madrid».http:// uam.es.Archivado desdeel originalel 22 de septiembre de 2017.Consultado el 22 de septiembre de 2017.
- ↑«Manual de procedimientos para el diagnóstico bacteriológico de la tuberculosis por microscopía directa 2008.».Archivado desdeel originalel 31 de diciembre de 2022.Consultado el 29 de octubre de 2015.
- ↑Susceptibilidad a drogas de Mycobacterium tuberculosis mediante observación microscópica(MODS).Instituto Nacional de la Salud, Perú, 2011.
- ↑«Overview | Tuberculosis | Guidance | NICE».nice.org.uk.Consultado el 15 de septiembre de 2021.
- ↑Group, British Medical Journal Publishing (31 de octubre de 1998).«Streptomycin Treatment of Pulmonary Tuberculosis».BMJ(en inglés)317(7167): 1248.ISSN0959-8138.doi:10.1136/bmj.317.7167.1248b.Consultado el 15 de septiembre de 2021.
- ↑«Tuberculois 2007»(en inglés).Archivado desdeel originalel 3 de julio de 2007.Consultado el 10 de julio de 2007.
- ↑abGómez Ayala, Adela-Emilia (1 de noviembre de 2007).«Tuberculosis. Abordaje farmacoterapéutico».Offarm26(10): 88-94.ISSN0212-047X.Consultado el 31 de diciembre de 2021.
- ↑«Catálogo de la OMS_2021: Mutaciones genéticas asociadas a la resistencia a antimicrobianos».
- ↑Salazar-Austin, Nicole; Ordonez, Alvaro A.; Hsu, Alice Jenhet al.(2015). «Extensively drug-resistant tuberculosis in a young child after travel to India».The Lancet Infectious Diseases15(12): 1485-1491.PMID26607130.doi:10.1016/S1473-3099(15)00356-4.
- ↑«Información general | Vacunas / Asociación Española de Vacunología».Consultado el 19 de noviembre de 2021.
- ↑«Coberturas de Vacunación. DATOS ESTADÍSTICOS».
- ↑«Calendario de vacunaciones de la AEP 2011».Archivado desdeel originalel 2 de septiembre de 2011.
- ↑Bonah C. "The 'experimental stable' of the BCG vaccine: safety, efficacy, proof, and standards, 1921-1933."Stud Hist Philos Biol Biomed Sci.2005 Dec;36(4):696-721.PMID 16337557.
- ↑Comstock, G. W. The International Tuberculosis Campaign: a pioneering venture in mass vaccination and research.Clin Infect Dis.1994 Sep;19(3):528-40.PMID 7811874.
- ↑Roy A, Eisenhut M, Harris RJ, Rodrigues LC, Sridhar S, Habermann S, Snell L, Mangtani P, Adetifa I, Lalvani A, Abubakar I (August 2014).«Effect of BCG vaccination against Mycobacterium tuberculosis infection in children: systematic review and meta-analysis».BMJ349:g4643.PMC4122754.PMID25097193.doi:10.1136/bmj.g4643.
- ↑Bannon, M. J. «BCG and tuberculosis.»Arch Dis Child.1999 Jan;80(1):80-3.PMID 10325767.
- ↑«Unitat de Tuberculosi Experimental (UTE) de l’Institut per a la Investigació en Ciències de la Salut Germans Trias i Pujol».Archivado desdeel originalel 25 de septiembre de 2008.
- ↑Cardona, P. J.; Amat, I. (1 de enero de 2006).«Origen y desarrollo de RUTI, una nueva vacuna terapéutica contra la infección por Mycobacterium tuberculosis».Archivos de Bronconeumología42(1): 25-32.ISSN0300-2896.doi:10.1157/13083277.Consultado el 15 de septiembre de 2021.
- ↑Nacho Aguilo; Santiago Uranga; Dessislava Marinova; Marta Monzon; Juan Badiola; Carlos Martin (2016). «MTBVAC vaccine is safe, immunogenic and confers protective efficacy against Mycobacterium tuberculosis in newborn mice».Tuberculosis96:71-74.doi:10.1016/j.tube.2015.10.010.
- ↑Raquel Tarancón, Jorge Domínguez-Andrés, Santiago Uranga, Anaísa V. Ferreira, Laszlo A. Groh, Mirian Domenech, Fernando González-Camacho, Niels P. Riksen, Nacho Aguilo, José Yuste, Carlos Martín, Mihai G. Netea (2020). «New live attenuated tuberculosis vaccine MTBVAC induces trained immunity and confers protection against experimental lethal pneumonia».PLoS Pathog16(4).doi:10.1371/journal.ppat.1008404.
- ↑Press, Europa (13 de agosto de 2019).«El ensayo de la vacuna contra la tuberculosis MTBVAC en bebés de Sudáfrica ofrece resultados esperanzadores».europapress.es.Consultado el 15 de septiembre de 2021.
Bibliografía[editar]
- Kumar, Vinay; Abbas, Abul K.; Fausto, Nelson; & Mitchell, Richard N. (2007).Robbins Basic Pathology(8th ed.). Saunders Elsevier. pp. 516-522ISBN 978-1-4160-2973-1
- Raviglione M. C., O'Brien R. J. Tuberculosis deHarrison's Principles of Internal Medicine(16th ed.); Kasper D. L., Braunwald E., Fauci A.S., Hauser S. L., Longo D. L., Jameson J. L., Isselbacher K. J., eds. McGraw-Hill Professional, 2004; páginas = 953–66. doi =10.1036/0071402357 ISBN = 0071402357
Enlaces externos[editar]
- Día Mundial de la Tuberculosis OMS
- Documento de Consenso de la Sociedad Andaluza de Enfermedades Infecciosas sobre tuberculosis
- Página CDC sobre la tuberculosis
- Tuberculosis en MedLineplus
- Tuberculosis en el portal de enfermedades infecciosas la enciclopedia médica Infodoctor
- Días Mundiales De - recursos de información sobre la Tuberculosis
