Metal

Kimikan,metalak(grezieraz:Metallon)elektroiakgaldu etaioipositiboak (katioiak) erraz sortzen dituzten elementu kimikoak dira,atomoenarteanlotura metalikoakdituztenak. Metalakmoldakorrakizaten dira normalean (xaflafinetan mailakatuak izan daitezke), baitaharikorrakere (alanbreetanluza daitezke). Metalakelementu kimikoakizan daitezke,burdinaadibidez,aleazioak,esate baterako,altzairu herdoilgaitza,edokonposatu molekularrak,hala nolasufre-nitruro polimerikoa.Taula periodikoko118 elementuetatik 95 inguru metalak dira, edo izan daitezke. Kopurua zehaztugabea da; izan ere, metalen, ez-metalen eta metaloideen arteko mugak zertxobait aldatzen dira, inplikatutako kategorien definizio unibertsalik ez baitago.
Definizioak
[aldatu|aldatu iturburu kodea]Fisikan,metal esaten zaio, oro har,elektrizitateazero absolutukotenperaturaneroateko gai den edozein substantziari.[1]Normalean metal gisa sailkatzen ez diren elementu eta konposatu asko metaliko bihurtzen dira presio handien pean. Adibidez,iodoa,metala ez bada ere,presio atmosferikoabaino 40 eta 170 mila aldiz presio handiagoaren pean metal bihurtzen da pixkanaka. Era berean, metaltzat hartzen diren material batzukez-metalbihur daitezke.Sodioa,adibidez, ez-metal bihurtzen da presio atmosferikoa baino bi milioi aldiz presio txikiagoan.
Astrofisikan,"metal" terminoa era zabalagoan erabiltzen dahelioabaino pisutsuagoak direnizarretakobaten elementu kimiko guztiei erreferentzia egiteko, eta ez soilik metal tradizionalei. Ildo horretatik,nukleosintesiarenondorioz izarren nukleoetan metatzen diren lehen lau "metalak"karbonoa,nitrogenoa,oxigenoaetaneoiadira, guztiak ere elementu kimikoen sailkapenetan metaltzat hartzen ez direnak. Izarrek atomo arinak fusionatzen dituzte bere bizitzan zehar, batez ere,hidrogenoaeta helioa. Hortaz, objektu astronomikoenmetalikotasunaelementu kimiko astunenek osatzen duten materiaren proportzioa da.[2][3]
Metalak, elementu kimiko gisa, lurrazalaren % 25 dira, eta bizitza modernoaren arlo askotan erabiltzen dira. Metal batzuei, haien indar eta erresistentziagatik, askotariko erabilerak ematen zaizkie, adibidez, altuera handiko eraikinak eta zubiak eraikitzeko, edota ibilgailuak,etxetresnaelektrikoak,hodiaketatrenbideakfabrikatzeko.Metal preziatuaktxanpongisa erabiltzen ziren historikoki, baina aro modernoan, metal preziatuak ez ezik, beste 23 elementu kimiko erabiltzen dira gutxienez objektuak fabrikatzeko.
Badirudi metal finduen historiakobrearenerabilerarekin hasi zela duela 11.000 urte inguru.Urrea,zilarra,burdina,berunaetaletoiaere Kristoren aurreko bosgarren milurtekoan erabiltzen ziren, brontzearen lehen agerpen ezaguna baino lehen. Ondorengo garapenen artean, hauek dira aipagarrienak: altzairuzko lehen formen ekoizpena,sodioarenaurkikuntza (lehen metal arina) 1809an, aleazio-altzairu modernoen sorrera eta,Bigarren Mundu Gerrarenamaieratik, forma sofistikatuagoen garapena.
Ezaugarriak
[aldatu|aldatu iturburu kodea]Forma eta egitura
[aldatu|aldatu iturburu kodea]

Metalakdistiratsuakdira prestatu, leundu edo hautsi berriak direnean, behintzat.Mikrometrolodi gutxi batzuk baino gehiagoko metalezko xaflekopakodirudite, bainaurrezko ogiakargiberdeatransmititzen du.
Metalen egoera solidoak edo likidoak, neurri handi batean, osatzen dituzten atomo metalikoek berenelektroiakkanpoko geruzatik erraz galtzeko duten gaitasunaren ondorio da. Oro har, atomo baten kanpoko geruzako elektroiak atxikitzen dituzten indarrak ahulagoak izaten dira metal solidoaren edo likidoaren atomoen arteko interakzioetatik sortzen diren elektroi berekiko erakarpen-indarrak baino. Inplikatutako elektroiak deslokalizatu egiten dira, eta metalen elektroi-egitura elektroi-laino mugikor samarretan txertatutako atomo-bilduma gisa ikus daiteke. Interakzio mota horrilotura metalikoesaten zaio.[1]Oinarrizko metalen lotura metalikoen indarra maximora iristen datrantsizioko metalenseriearen erdigunearen inguruan, elementu horiek deslokalizatutako elektroi kopuru handia baitute.
Oinarrizko metal gehienek ez-metal gehienek bainodentsitatehandiagoak dituzten arren, dentsitateen artean aldakortasun handia dago.Litioada dentsitate txikiena duena (0,534 g/cm3) eta,osmioa,aldiz, dentsitate handiena duena (22,59 g/cm3).Magnesioa,aluminioaetatitanioagarrantzi komertzial handiko metal arinak dira. Euren 1,7, 2,7 eta 4,5 g/cm3-ko dentsitateak egiturazko metal zaharrenenekin aldera daitezke, hala nolaburdinarenakin(7,9 g/cm3) etakobrearenakin(8,9 g/cm3). Beraz, burdinazko bola batek bolumen bereko hiru aluminio-bolaren pisua edukiko luke.
Metalak malguak eta harikorrak izan ohi dira, eta bereizi gabe deformatzen diratentsiopean.[4]Lotura metalikoen izaera ez-norabidezkoak nabarmen laguntzen du solido metaliko gehienen moldakortasunerako. Aitzitik,konposatu ionikoetan,hala nolamahaiko gatzean,lotura ioniko baten planoak elkarren ondoan lerratzen direnean, kokapen-aldaketak gertatzen dira, eta karga bereko ioiak hurbildu egiten direlarik, kristala apurtu egiten da. Desplazamendu hori ez da ikustenlotura kobalenteaduten kristaletan,diamanteanadibidez, kristala hautsi eta zatitu egiten baita.[2]Metalen deformazio elastiko itzulgarria leheneratze-indarrentzakoHookeren legearenbidez deskriba daiteke, deskriba daiteke: tentsioa deformazioarekiko linealki proportzionala da.
Beroakedo metal batenmuga elastikoakbaino indar handiagoek deformazio iraunkorra (atzeraezina) eragin dezakete,deformazio plastiko edo plastikotasun esaten zaiona. Aplikatutako indarratrakziokoak,konpresiokoak,zizailatzekoak,tolestekoak edo bihurdurakoak izan daitezke. Tenperatura-aldaketek batek metalaren egitura-akatsen mugimenduan edo desplazamenduan eragin dezakete, besteak beste, ale-mugetan,huts puntualetan,lerro- eta torloju-dislokazioetan,pilaketa-failetanetamakletan,hala metalkristalinoetannolaez-kristalinoetan.Metalaren barne-lerradurak, jarioa etametal-nekeagerta daitezke.
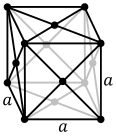
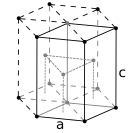
Substantzia metalikoen atomoak hiru egitura kristalino ohikoenetako bat eduki ohi dute, hau da, gorputzean zentratutako egitura kubikoa (gzk), aurpegian zentratutako egitura kubikoa (azk) edo egitura hexagonal itxia (hi). Gzk-an, atomo bakoitza beste zortzi atomoz inguratutako kubo baten erdian dago. Azk eta hi motetan, atomo bakoitza beste hamabi atomoz inguratuta dago, baina geruzen pilaketa desberdina da. Metal batzuek egitura desberdinak hartzen dituzte tenperaturaren arabera.[5]
-
Gorputzean zentratutako egitura kubikoa, adibidez kromoa, burdina edo wolframioa.
-
Aurpegian zentratutako egitura kubikoa, adibidez aluminioa, kobrea edo urrea.
-
Paketatze trinkoa hexagonoetan, 6 atomoko gelaxka unitatea, adibidez, titanioa, kobaltoa eta zinka
Kristal-egiturabakoitzarengexkala unitateakristalaren simetria globala duen atomo multzorik txikiena da, eta horretatik abiatuta kristal-sare osoa eraiki daiteke hiru dimentsiotan errepikatuz. Aurrez erakutsitako gorputzean zentratutako kristal-egitura kubikoaren kasuan, gelaxka unitatea erdiko atomoak eta izkinetako zortzi atomoetako bat-zortzik osatzen dute.
Elektrikoak eta termikoak
[aldatu|aldatu iturburu kodea]Metalen egitura elektronikoak aztertuta,elektrizitate-eroalenahiko onak direla ondoriozta daiteke. Materiako elektroiek energia-maila finkoak izan ditzakete aldagaien ordez, eta metal batean elektroien energia-mailak, maila jakin bateraino gutxienez, eroapen elektrikoak izan ditzakeen energia-mailei dagozkie. Silizioa edo sufre ez-metalikoa bezalako erdieroaleetan, energia-eten bat dago substantziaren elektroien eta eroapen elektrikoa gerta daitekeen energia-mailaren artean. Ondorioz, erdieroaleak eta ez-metalak nahiko eroale eskasak dira.
Oinarrizko metalek 6,9 × 103S/cm-ko elektrizitate-eroaletasunaren balioak dituztemanganesorako,eta 6,3 × 105S/cm-koazilarrerako.Aitzitik,boroabezalako metaloideerdieroaleekbatek eroankortasun elektrikoa du, 1,5 × 10−6S/cm. Nolanahi ere, elementu metalikoek eroankortasun elektrikoa murrizten dute berotzen direnean.Plutonioakelektrizitate-eroapena handitzen du, −175 eta 125 °C bitarteko tenperatura-tartean berotzen denean.
Metalak nahikobero-eroaleonak dira. Metalen elektroi-hodeiko elektroiak oso mugikorrak dira, eta erraz transmiti dezakete beroak eragindako bibrazio-energia.
Metalen elektroiek haren ahalmen termikoari eta bero-eroaletasunari egiten dioten ekarpena eta metalaren eroankortasun elektrikoaelektroi askeen ereduarenbidez kalkula daitezke. Hala ere, horrek ez du kontuan hartzen metalaren ioi-egitura zehatza egitura zehatza. Nukleo ionikoen kokapenak eragindako potentzial positiboa kontuan hartuta, metalenbanda elektronikoaren egituraetaenergia lotesleadeskriba daitezke. Zenbait eredu matematiko aplika daitezke, sinpleenaelektroi-eredua ia askeaizanik.
Ezaugarri kimikoak
[aldatu|aldatu iturburu kodea]Elektroiak galdu etakatioiaksortzeko joera izaten dute metalek.[6]Gehienek airekooxigenoarekinerreakzionatu eta oxidoak epe desberdinetan (potasio-erredurak segundotan, burdina urteetan zehar oxidatzen den bitartean). Beste batzuek, hala nolapaladioak,platinoaketaurreak,ez dute batere erreakzionatzen atmosferareko oxigenoarekin. Metal-oxidoak,oro har,basikoakdira,ez-metalakez bezala,azidoakedo neutroak izaten direnak. Salbuespenak,oxidazio-egoeraoso handiko oxidoak dira, hala nola CrO3,Mn2O7eta OsO4,guztiz azidoak baitira.
Pintura,anodizazioaedoestaldurametalenkorrosioasaihesteko modu onak dira. Hala ere,serie elektrokimikoanmetal erreaktiboagoa aukeratu behar da estaldurarako, batez ere estaldura irristatzea espero denean.
Taula periodikoaren distribuzioa
[aldatu|aldatu iturburu kodea]Kimikan, baldintza normaletan metaltzat jotzen diren elementuak gorriz, laranjaz eta morez nabarmenduta ageri dira taula periodikoan. Gainerako elementuak metaloideak (B, Si, Ge, As, Sb eta Te, eskuarki halakotzat hartzen direnak) edo ez-metalak dira. Astatina (At), normalean, ez-metal edo metaloide gisa sailkatzen da, baina ikerketa batzuek metal bat izatea espero dute. Propietate ezezagunak dituzten gainerako elementuak metalak dira seguruenik, baina zalantzaren bat badago kopernioaren (Cn), flerobioaren (Fl) eta oganessonaren (Og) kasuetan.
| Taldea→ ↓Periodoa |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |
| 1 | 1 H |
2 He | |||||||||||||||||
| 2 | 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne | |||||||||||
| 3 | 11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar | |||||||||||
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr | |
| 5 | 37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 Mo |
43 Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe | |
| 6 | 55 Cs |
56 Ba |
* | 71 Lu |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 At |
86 Rn |
| 7 | 87 Fr |
88 Ra |
** | 103 Lr |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Lv |
117 Ts |
118 Og |
| *Lantanoideak | 57 La |
58 Ce |
59 Pr |
60 Nd |
61 Pm |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb | |||||
| **Aktinidoak | 89 Ac |
90 Th |
91 Pa |
92 U |
93 Np |
94 Pu |
95 Am |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 No | |||||
Elementu metalikoak
[aldatu|aldatu iturburu kodea]- Banadioa(V)
- Boroa(Bh)
- Burdina(Fe)
- Darmstadtioa(Ds)
- Dubnioa(Db)
- Eskandioa(Sc)
- Hafnioa(Hf)
- Hasioa(Hs)
- Iridioa(Ir)
- Kadmioa(Cd)
- Kromoa(Cr)
- Kobaltoa(Co)
- Kobrea(Cu)
- Manganesoa(Mn)
- Meitnerioa(Mt)
- Merkurioa(Hg)
- Molibdenoa(Mo)
- Nikela(Ni)
- Niobioa(Nb)
- Osmioa(Os)
- Paladioa(Pd)
- Platinoa(Pt)
- Renioa(Re)
- Rodioa(Rh)
- Roentgenioa(Rg)
- Rutenioa(Ru)
- Rutherfordioa(Rf)
- Seaborgioa(Sg)
- Tantaloa(Ta)
- Teknezioa(Tc)
- Titanioa(Ti)
- Tungstenoa(W)
- Ununbioa(Uub)
- Urrea(Au)
- Itrioa(Y)
- Zilarra(Ag)
- Zinka(Zn)
- Zirkonioa(Zr)
Nahasturak
[aldatu|aldatu iturburu kodea]Metalen nahasturekaleazioakeratzen dituzte, hala nola,altzairua(karbono-burdina), kobre nahasturak (brontzea,letoia), amalgamak (zilarbizinahasturak)..
Aleazioak
[aldatu|aldatu iturburu kodea]Aleazioak propietate metalikoak dituzten substantziak dira, bielementuzedo gehiagoz osatuta daudenak; elementu horietako bat metala da. Aleazioek osaera aldakorra edo finkoa izan dezakete. Adibidez, urrez eta zilarrez osatutako aleazioetan, urre- eta zilar-proportzioak nahieran doi daitezke; titanioz eta silizioz osatutako Ti2Si aleazioan, bi osagaien proportzioa finkatzen da (konposatu intermetalikogisa ere ezagutzen dena).

Metal puru gehienak bigunegiak, hauskorregiak edo kimikoki erreaktiboegiak dira, erabilera praktikorako. Metalen proportzio desberdinen konbinazioen bidez, hala nola aleazioen bidez, metal puruen propietateak aldatzen dira, nahi diren ezaugarriak sortzeko. Aleazioak egiteko, normalean, ez dira oso hauskorrak, gogorragoak, korrosioarekiko erresistenteak, edo kolore eta distira desiragarriagokoak izan behar. Gaur egun erabiltzen diren aleazio metaliko guztietatik,burdinaleazioak (altzairua,altzairu herdoilgaitza,burdina urtua,erremintetarako altzairua,aleazio-altzairua) dira proportzio handiena dutenak, bai kantitateari dagokionez, bai balio komertzialari dagokionez ere. Karbono-proportzio desberdinak dituen burdina aleatuak karbono gutxiko, ertaineko eta altuko altzairuak sortzen ditu, zenbat eta karbono maila altuagoa eduki, orduan eta mugatuagoak/ txikiagoak dira harikortasuna eta zailtasuna.Silizioagehituz burdina urtuzko xaflak sortzen dira, karbono-altzairueikromoa,nikela etamolibdenoagehituz (% 10 baino gehiago), berriz, altzairu herdoilgaitzak lortzen dira.
Beste aleazio metaliko garrantzitsu batzuk diraaluminiozkoak,titaniozkoak,kobrezkoaketamagnesiozkoak.Kobre-aleazioak historiaurretik dira ezagunak —brontzeakBrontze Aroarieman zion izena—, eta gaur egun aplikazio asko dituzte, garrantzitsuena kableatu elektrikoan. Beste hiru metalen aleazioak nahiko berriki garatu dira, erreaktibotasun kimikoa dutenez, erauzketaelektrolitikokoprozesuak behar baitituzte. Aluminio-, titanio- eta magnesio-aleazioak preziatuak dira duten indar/pisu erlazio handiagatik; magnesioakeremu elektromagnetikoaere sor dezake. Material horiek idealak dira indar/pisu erlazio handia kostu materiala baino garrantzitsuagoa den egoeretan, hala nola espazio aeroespazialean eta bere indarrez dabiltzan aplikazio batzuetan.
Aplikazio oso zorrotzetarako bereziki diseinatutako aleazioek, hala nolaerreakzio-motorrek,hamar elementu baino gehiago izan ditzakete.
Kategoriak
[aldatu|aldatu iturburu kodea]Metalak beren propietate fisiko edo kimikoen arabera sailka daitezke. Hauek dira bereizi ohi diren kategoria batzuk:metal ferrosoaketaez-ferrosoak;metal hauskorrak etametal erregogorrak;metal zuriak;metal astunaketaarinak;etaoinarrizko metalak,nobleaketapreziatuak.Atal honetako elementu metalikoen taulan oinarrizko metalak sailkatzen dira, beren propietate kimikoetan oinarrituta:metal alkalinoaketalurralkalinoak;trantsiziozkoetatrantsizio ondokometalak; etalantanidaketaaktinidoak.Beste kategoriabatzuk ere badaude, sartzeko irizpideen arabera. Adibidez, metalferromagnetikoak—giro-tenperaturan magnetikoak direnak— burdina, kobaltoa eta nikela dira.
Metal ferrosoak eta ez-ferrosoak
[aldatu|aldatu iturburu kodea]Artikulu nagusiak:burdinazko metalurgiaetaburdinazkoa ezden metala
"Ferroso" terminoa "burdindun" esan nahi duenlatinezkohitzetik dator. Alde batetik, burdinapurua,burdinaforjatumoduan aurki daiteke. Bestetik, burdina dutenaltzairuzkoaleazioak ere aurki daitezke. Metal ferrosoakmagnetikoakizaten dira askotan, baina ez dute bakarrik ezaugarri hori. Metal ez-ferrosoek eta aleazioek ez dute burdin kantitate handirik.
Metal hauskorrak
[aldatu|aldatu iturburu kodea]Ia metal guztiak xaflakorrak edo harikorrak diren arren, batzuk —berilioa, kromoa, manganesoa, galioa eta bismutoa— hauskorrak dira.[7]Metaltzat har daitezkeen artsenikoa eta antimonioa ere hauskorrak dira.
Metal erregogorrak
[aldatu|aldatu iturburu kodea]Artikulu nagusia:Metal erregogorrak
Materialen zientzietan, metalurgian eta ingeniaritzan, metal erregogor esaten zaie beroaren aurreko erresistentzia handia dutenei. Metal erregogorren artean, niobioa, molibdenoa, tantaloa, tungstenoa eta renioa daude. Guztiek 2.000 °C-tik gorako urtze-puntuak dituzte, etagogortasunhandia erakusten dute giro-tenperaturan.
-
Niobiozko kristalak eta 1 cm3-ko niobioanodizatutakokubo bat.
-
Molibdeno-kristalak eta 1 cm3-ko molibdeno-kubo bat.
-
Tantalozko kristala, kristal-zati batzuk eta 1 cm3-ko tantalozko kubo bat.
-
Renio kristala, barra urtu bat eta 1 cm3-ko renio kubo bat.
Metal zuriak
[aldatu|aldatu iturburu kodea]Metal zuriakmetal zurien (edo haien aleazioen) sorta bat dira, eta urtze-puntu nahiko txikiak dituzte. Metal horien artean, zinka, kadmioa, eztainua, antimonioa (metala), beruna eta bismutoa daude, eta horietako batzuk nahiko toxikoak dira.
Metal gogor eta bigunak
[aldatu|aldatu iturburu kodea]Artikulu nagusiak:Metal astunaketametal arinak
Metal astunak deritze nahiko trinkoak diren metal edometaloideei.[8]Definizio zehatzagoak proposatu dira, baina inork ez du definizio orokorra lortu. Metal astun batzuek erabilera espezifikoak dituzte, edo oso toxikoak dira; beste batzuk, aldiz, funtsezkoak dira elementu aztarna modura. Gainerako metal guztiak metal arinak dira.
Metal preziatuak
[aldatu|aldatu iturburu kodea]Artikulu nagusiak:Metal arruntak,metal nobleaketametal preziatuak
Kimikan,oinarrizko metal terminoa modu informalean erabiltzen da errazoxidatzenedokorrosionatzendiren metalei erreferentzia egiteko. Hala nola,azido klorhidrikodiluituarekin (HCl) erraz erreakzionatzen duten eta metal-kloruroa eta hidrogenoa sortzen duten metalak izendatzeko. Adibide batzuk dira, burdina,nikela,berunaeta zinka. Kobrea oinarrizko metaltzat hartzen da, nahiko erraz oxidatzen baita, nahiz eta ez duen HCl-arekin erreakzionatzen.
Metal nobleterminoa normaleanoinarrizko metalarenkontrakoa adierazteko erabiltzen da. Metal nobleek korrosioarekiko edooxidazioarekikoerresistenteak dira,[9]oinarrizko metal gehienek ez bezala. Metal preziatuak izan ohi dira metal nobleak, hautemandako bitxitasunengatik. Metal nobleen adibideak dira urrea, platinoa, zilarra, rodioa, iridioa eta paladioa.
Portaera kimikoari dagokionez, metal preziatuak (metal nobleak bezala) ez dira elementu gehienak bezainerreaktiboak,distirahandia dute eta bai elektrizitate-eroaletasun handia ere. Historikoki, metal preziatuak garrantzitsuak zirenmonetagisa, baina orain inbertsio eta produktu industrialtzat hartzen dira nagusiki. Metal preziatu ezagunenakurreaetazilarradira. Biek industria-erabilera badute ere, ezagunagoak dira arteanbitxigintzaneta txanpongintzan dituzten erabilerengatik. Beste metal preziatu batzuk platinozko taldeko metalak dira: rutenioa, rodioa, paladioa, osmioa, iridioa eta platinoa. Horietatik platinoa da komertzializatuena.
Metal preziatuen eskari handia dago, erabilera praktikoagatik ez ezik, inbertsio gisa etabalio-biltegigisa duten eginkizunagatik ere.
Metalak kulturan
[aldatu|aldatu iturburu kodea]
Metalaren langintza, historikoki, kulturalki inportantea eta are, oinarri sakratuko langintza kontsideratu izan da. Zenbaitmitologiatan,metala lantzeko gaitasuna jainkoek erremintariei edo lehen erremintari mitiko bati transmititutako gaitasuna da. Metalaren emaile edo maisu gisako jainkoak izan diraThoreskandinaviarren arteam,Vulkanoerromatarren jainkoa,Hefestogreziarrena,Svarogeslaviarrenjainkoa...
Horrez gain, erremintariek gaitasunxamanikoakizan dituzte historikoki hainbat kulturatan. Langintza berezitu eta esklusibo gisa definitu daitekeen historiako lehen ofizioetako bat izan daiteke, non eta beste antzinako zeregin batzuk (zurgintza, ehiza, nekazaritza) pertsona baten egiteko desberdinetan osagarriak izan daitezkeen.[10]
Patxi Errementariarenelezahar euskaldunak ere badu langintzaren alde misteriotsu eta magikoarekin loturarik.[11]
Metalak aro historikoak izendatzeko
[aldatu|aldatu iturburu kodea]
Metal langintzaren agerpen historikoa gizateriaren eboluzioan hain da inportantea nonneolitoaedo harriaren aroa harria erabili zeneko azken fase historiko gisa izendatzea konbentzio ezagun bat den. Ondoren datoz metalaren aroak,brontzearoaetaburdinaroabereziki, ordena horretan.
Kulturaren eboluzioaren izendapen hauek, metal horietan oinarrituek, badute logika eta hurrenkera historiko egiazko bati dagozkie, baina nolabait zorizkoa da nola finkatu diren: Danimarkak, XIX. mendean Norvegia galdu zuelarik (erresuma independente gisa sezesionatu zen), Danimarkako museo bateko arduradunak,Christian Jürgensen Thomsenek(1788–1865), jaso zuen enkargua museoko artefaktu zaharrak antolatzekoa: metodo zientifiko argirik gabe, ezaugarri bertsuak zeuzkaten elementu multzoak sailkatu zituen, "hemen brontzezkoak beraiekin batera aurkitutako elementuekin", eta "hemen burdinazkoak"... Objektu sailkatuek garai historiko zehatzak definitzen zituztela ikusi zuen Thomsenek, eta are gehiago, ezaugarri kultural komunen araberako artefaktu sailkapenak ere egin zitezkeela jabetu zen.[12]
Fikziozko metalak
[aldatu|aldatu iturburu kodea]Metala material miragarri bezala kontsideratzea antzinako kontua izateaz gain, kultura adierazpide modernoetan ere agertzen da tarteka. Botere edo gaitasun ikusgarriak dituzten metalak agertzen dira fikzio moderno askotan. Eta aurrekaririk ez zaie falta, antzina ere metal fantastikoak deskribatu izan baitziren, hala nolaPlatonekaipaturikoorikalkoa,Atlantidakometala.[13]
Esate baterako:mithrilelfoen metalaEraztunen Jaunarenmunduan,vibranioetaadamantioelementu fikzionalMarvelkomiki eta istorioetan,beskarizeneko supermetalaStar Wars-eko abenturetan edovaliriar altzairuaGame of Thrones-eko unibertsoan, batzuk aipatzearren.[14]
Erreferentziak
[aldatu|aldatu iturburu kodea]- ↑abMortimer, Charles E.. (1983).Chemistry.(5th ed. argitaraldia) Wadsworth Pub. CoISBN0-534-01184-5.PMC8552913.(Noiz kontsultatua: 2022-06-08).
- ↑ab«Ductility Review - Strength Mechanics of Materials»engineersedge(Noiz kontsultatua: 2022-06-08).
- ↑(Ingelesez)Martin, John C.; Morrison, Heather L.. (1998-10).«A New Analysis of RR Lyrae Kinematics in the Solar Neighborhood»The Astronomical Journal116 (4): 1724–1735.doi:.ISSN0004-6256.(Noiz kontsultatua: 2022-06-08).
- ↑«Hogg, John C., Alley, Otis E., and Rickel, Charles L. Chemistry. New York: D. Van Nostrand Company, 1953. 772 p»Science Education37 (5): 341–341. 1953-12doi:.ISSN0036-8326.(Noiz kontsultatua: 2022-10-25).
- ↑Wiberg, Egon. (2001).Inorganic chemistry.(1st English ed.. argitaraldia) Academic PressISBN0-12-352651-5.PMC48056955.(Noiz kontsultatua: 2022-10-25).
- ↑«Hogg, John C., Alley, Otis E., and Rickel, Charles L. Chemistry. New York: D. Van Nostrand Company, 1953. 772 p»Science Education37 (5): 341–341. 1953-12doi:.ISSN0036-8326.(Noiz kontsultatua: 2022-10-21).
- ↑Russell, Alan M.. (2005).Structure-property relations in nonferrous metals.John WileyISBN0-471-70853-4.PMC607802504.(Noiz kontsultatua: 2022-10-25).
- ↑Metal contamination.IFREMER 2007ISBN2-84433-028-2.PMC470693456.(Noiz kontsultatua: 2022-10-25).
- ↑Chemical oxidation applications for industrial wastewaters.2010ISBN978-1-78040-141-6.PMC874148114.(Noiz kontsultatua: 2022-10-25).
- ↑(Ingelesez)journal, SCIENCE First Hand.«A Blacksmith and a Shaman»SCIENCE First Hand(Noiz kontsultatua: 2023-05-24).
- ↑(Ingelesez)boneandsickle. (2022-01-24).«Myth and Magic of the Smith»Bone and Sickle(Noiz kontsultatua: 2023-05-24).
- ↑Anthony, David W.. (2007).The Horse, the wheel and language: how bronze-age riders from the eurasian steppes shaped the modern world.Princeton University PressISBN978-0-691-05887-0.(Noiz kontsultatua: 2023-05-24).
- ↑(Ingelesez)Coggan, Devan. (2022).«Shiny fictional metals ranked, from vibranium to Valyrian steel»EW(Noiz kontsultatua: 2023-05-24).
- ↑Preston, Douglas; Preston, Douglas. (1999).Riptide.Warner BooksISBN978-0-446-60717-9.(Noiz kontsultatua: 2023-05-24).