Catalyse

En chimie, lacatalyse(du nomgrec:κατάλυσις/katálusis,« dissolution[1]») se réfère à l'accélération ou la réorientation de lacinétiquede réaction au moyen d'un catalyseur, et dans certains cas à la sélectivité pour diriger la réaction dans un sens privilégié (réaction concurrente, production d'un produit plutôt qu'un autre)[2]. Le catalyseur est utilisé en quantité beaucoup plus faible que les produits réactifs. Il n'apparaît pas en général dans le bilan de réaction, donc pas dans son équation globale. Cependant les molécules du catalyseur participent à la réaction dans une étape, ce qui explique leur influence sur la vitesse de réaction, et ensuite elles sont régénérées dans une étape subséquente[3].Le catalyseur reste parfois intimement mélangé au produit final.
La catalyse joue un rôle dans de très nombreux domaines. Depuis plus de cent ans, elle a des applications dans le domaine duchauffage(exemple: poêle à gaz catalytique): descombustionscomplètes, à température plus basse (moins dangereuses), quasiment sans flamme, et avec beaucoup moins de résidus de combustion dangereux (monoxyde de carbone,oxyde d'azote). Plus de 80 % des réactions chimiques industrielles sont réalisées à l'aide de procédés catalytiques en réduisant considérablement leur coût. Par exemple en 2007, les ventes mondiales de catalyseurs du domaine de dépollution des gaz de moteurs s'élevaient à environ seize milliards de dollars.
La vision populaire de ce domaine des catalyses est négative: pollution, dispersions de poussières de métaux rares et dangereux, vols de catalyseurs automobiles. Ces domaines de la science sont mal connus.[réf.souhaitée]
Enbiologie,dans lescellules,lesenzymes,très nombreuses, jouent ces rôles d'accélérateur, de catalyseurs, dans les processus biochimiques:métabolisme digestif,de lareproduction,de latranscriptionde l'information génétique,les sciences dugénome,leyaourt,lapâte à pain,etc.
Typologie
[modifier|modifier le code]Différents types de catalyse peuvent être distingués selon la nature du catalyseur:
- catalyse homogène,si le catalyseur et les réactifs ne forment qu'une seulephase(souvent liquide);
- catalyse hétérogène,si le catalyseur et les réactifs forment plusieurs phases (généralement un catalyseur solide pour des réactifs en phase gazeuse ou liquide);
- catalyse enzymatique,si le catalyseur est uneenzyme,c'est-à-dire une protéine; de nombreux caractères de la catalyse enzymatique (influence de la concentration du catalyseur, types de succession d'étapes,etc.) sont les mêmes que ceux de la catalyse homogène.
La catalyse peut être aussi classée en fonction du mécanisme mis en jeu:
- catalyse acido-basique (générale ou spécifique);
- catalyse d'oxydoréduction;
- catalyse nucléophile;
- catalyse par transfert de phase.
Un catalyseur ne modifie ni le sens d'évolution d'une transformation ni la composition du système à l'état final. Tout catalyseur d'une réaction dans le sens direct catalyse aussi la réaction en sens inverse. De ce fait, un catalyseur ne permet pas à des réactions thermodynamiquement peu déplacées de modifier leurtaux d'avancementfinal.
Par exemple, la réaction
ne se produit pas en l'absence de catalyseur (à température ordinaire) et aucun catalyseur ne peut la faire se produire avec un rendement satisfaisant.
Cependant, comme un catalyseur peut modifier fortement la vitesse d'une réaction parmi un grand nombre de réactions concurrentes possibles, il peut favoriser une réaction qui parait ne pas exister en son absence. C'est le cas de l'oxydation de l'ammoniacpar ledioxygène:
- en l'absence de catalyseur, la réaction (non intéressante d'un point de vue industriel) est essentiellement: 2NH3+O2→ N2+ 3H2O
- en présence deplatinecomme catalyseur, il se forme surtout dumonoxyde d'azote(précieux intermédiaire dans la production d'acide nitrique): 2NH3+O2→ 2NO + 3H2O
Le monoxyde d'azote n'apparaît pas de façon mesurable en l'absence de platine.
Ne sont pas des catalyseurs…
[modifier|modifier le code]- La température, bien qu'elle augmente la vitesse de réaction. Le catalyseur est uneespèce chimique,ce que n'est pas la température.
- La lumière peut initier certainesréactions photochimiques,mais ce n'est pas un catalyseur pour autant car la lumière n'est pas une espèce chimique. De plus, la lumière ne ressort pas indemne, puisqu'une part de son énergie seraabsorbée,et salongueur d'ondesera donc modifiée.
- Unamorceur,bien que ce soit une espèce chimique, qu'il augmente la vitesse, et qu'il n'apparaisse pas dans le bilan. En effet, l'amorceur est consommé en début de réaction. Par exemple, unamorceur radicalairepermet de produire les premiersradicauxqui permettent à unepolymérisation radicalairede se produire.
Histoire
[modifier|modifier le code]Étapes de la découverte
[modifier|modifier le code]
Quelques étapes notables sur la découverte et la compréhension de la notion de catalyse sont listées ici par ordre chronologique. Les premières découvertes sont liées au domaine de labiocatalyse:
- 6 000 ansav. J.-C.,procédés techniques de lafermentation alcooliquedes sucres, utilisés par lesSumériensenMésopotamie:production d'acide acétiquede l'alcool au moyen d'enzymes.
- Accélération et orientation des fermentations du lait pour les fromages: les découvertes liées permettaient très rapidement de diminuer les risques de colonisation par les agents pathogènes et augmentaient nettement la durée de consommation des produits laitiers (à l'échelle du temps du produit de base, c'était une technique de toute première importance).
- Les processus depanificationdes farines permettant la réalisation en épaisseur de cuisson au four et une modification de la digestibilité du composant de base.
Après ces débuts, la découverte de toute une série de nouvelles réactions catalytiques a eu lieu dans lesXVIIIeet début duXIXesiècle.
- Au milieu duXVIIIesiècle, le physicien britanniqueJohn Roebuckélabore un procédé permettant la formation d'acide sulfuriquepar oxydation dudioxyde de soufrepar l'air; la réaction est effectuée en présence d'un catalyseur, l'acide nitrosylsulfurique,dans une cuve en plomb[4].
- Vers 1780, multiples découvertesAntoine-Augustin Parmentier,pharmacien militaire, agronome, nutritionniste et hygiéniste français: catalyse acide du sucre.
- 1782, découverte deCarl Wilhelm Scheele,sur l'estérification catalysée par unacidedes alcools.
- 1783,Joseph Priestley,transformation de l'éthanol à partir d'éthylène.
- 1794,Elizabeth Fulhame,décrit dans sonEssay on Combustionl'importance de l'eau dans certaines réactions d’oxydation[5].
- Dès 1814,Constantin Kirchhoffrapporte l'hydrolysede l'amidon catalysée par les acides.
- En 1817,Humphry Davydécouvre que l'introduction deplatinechaud dans un mélange d'air et de gaz issus du charbon conduit à chauffer à blanc lemétal.
- En 1824,William Henryrapporte l'empoisonnement d'un catalyseur: l'éthylèneinhibe la réaction entre l'hydrogène et l'oxygène sur du platine. Il remarque par ailleurs l'oxydation sélective dans la réaction entre l'oxygène et un mélange gazeux composé d'hydrogène, demonoxyde de carboneet deméthane.
- Le terme catalyse est introduit parBerzeliusen1835(du nomgrec:κατάλυσις/katálusis,« dissolution[1]») pour nommer lacaused'un groupe de réactions[6].Cette idée n'eut pas que des adeptes et Liebig, par exemple, s'opposa, dans le cas de lafermentation,à la théorie de la catalyse avancée par Berzelius. Pour Liebig, la cause de la fermentation était due à la transmission de vibrations des particules de ferment[7].
- En 1845,William Grovemontre qu'un filament de platine est également un catalyseur pour la décomposition de l'eau en hydrogène et oxygène.
- Dans les années 1850,Kekulécomprit que laloi d'action de masseet les forces catalytiques avaient de l'importance sur les réactions chimiques, et que les forces qui favorisaient l'association des moléculesAneinanderlagerungcausaient également leur décomposition, et que des produits intermédiaires pouvaient être isolés[8].Voir la représentation ci-contre.

- En 1871, leprocédé Deacon(en),utilisé pour l'oxydation de l'acide chlorhydriqueen chlore, est développé: il utilise un catalyseur à base de brique en argile imprégnée de sels de cuivre.
- Peu de temps après, en 1877,Clément Georges Lemoinedémontre que la décomposition de l'iodure d'hydrogèneen dihydrogène etdiiodeatteint le même point d'équilibre à350°Cque la réaction soit menée avec ou sans catalyseur (platine).
- Cette propriété est confirmée deux ans plus tard parClaude Louis Bertholletavec l'estérificationdesacides organiqueset l'hydrolyse desestersdont l'équilibre de réactionreste identique avec ou sans catalyseur.
- Vers 1901, Georg Bredig mettait en avant l'importance de l'empoisonnement d'un catalyseur[9].
La catalyse au développement de la chimie
[modifier|modifier le code]Le début duXXesiècle marque une découverte qui continue d'avoir des répercussions de nos jours[10].Wilhelm Normann réalise l'hydrogénationde l'acide oléique(acidecis-9-octadécènoïque C17H33COOH), liquide, enacide stéarique(acide octadécanoïqueC17H35COOH), solide, sur dunickelfinement divisé. Cette hydrogénation est encore largement utilisée auXXIesiècle dans de nombreux domaines (alimentation, pharmacie, savonnerie, parfumerie, peinture,etc.) et le nickel reste le catalyseur phare.
Lasynthèse de l'ammoniac(NH3) à partir du diazote et du dihydrogène est mise au point parFritz Habersous haute pression, à température moyenne et catalysée par le fer (Fe3O4réduit). Cet ammoniac peut être oxydé enmonoxyde d'azotepar oxydation, catalysé cette fois par le platine, pour servir de base à la fabrication d'acide nitrique(HNO3). En 1923,BASFcommande une usine de fabrication duméthanolà partir demonoxyde de carboneet d'hydrogène sur un catalyseur à base d'oxyde de zincet d'oxyde de chrome.Durant la même période, leprocédé Fischer-Tropschpermet d'obtenir desalcanes,desalcèneset desalcoolsà partir de monoxyde de carbone et d'hydrogène à l'aide de catalyseur à base de fer et de cobalt. L'oxydation catalytique dudioxyde de soufreentrioxyde de soufresur l'oxyde de vanadium(V)(V2O5) permet la synthèse à grande échelle d'acide sulfurique.
À la fin des années 1930, lecraquage catalytiqueapparaît, offrant la possibilité de rompre lesliaisons C-C.Ceprocédé Houdry,utilise un catalyseur à base d'argile de typemontmorillonitetraitée à l'acide, et permet de scinder les grosses molécules du pétrole, typiquement contenues dans lesgasoils,en plus petites, constituant les essences. Durant la même décennie, l'oxydation sélective de l'éthylèneenoxyde d'éthylènesur un catalyseur à base d'argent est mise au point, développée et commercialisée parUnion Carbide.Tous ces procédés permettent d'avoir accès, à une échelle industrielle, à des produits de base de la chimie, ouvrant ainsi la voie au développement de la chimie de base etde spécialité.
Juste après la Seconde Guerre mondiale, lesTrente Glorieusesprofiteront largement à la chimie avec un grand développement des procédés en tout genre pour des productions de plus en plus diversifiées. La catalyse sera un acteur important de ce développement. Lapolymérisationse développe grandement en profitant des molécules de base produites. Dans lesannées 1950,lepolyéthylène,lepolypropylèneet lepolybutadièneapparaissent grâce notamment au procédé depolymérisation coordinativeZiegler-Nattautilisant des catalyseurs à base decomplexesorganométalliques de titane et aluminium. Le traitement du pétrole s'affirme avec l'hydrodésulfurationsur des catalyseurs à base de sulfure de cobalt et de molybdène, l'hydrotraitementdesnaphtassur des catalyseurs cobalt-molybdène déposés suralumine.
Les années 1960 marquent l'apparition deszéolithesde synthèse actives et sélectives pour l'isomérisationdes alcanes et le craquage catalytique. Dès lors, ces matériaux vont faire l'objet d'intenses études pour leurs propriétés catalytiques et les chercheurs mettent au point de nombreuses zéolithes aux propriétés adaptées selon les réactions à catalyser, mais aussi à la forme des molécules par le contrôle de la taille des canaux. Les réactions mises en jeu conduisent à des molécules de plus en plus diverses: l'ammoxydationdupropylènesur des catalyseurs à base d'oxydesde bismuth et de molybdène conduit à la fabrication d'acrylonitrile,alors que l'oxychlorationde l'éthylènesur des catalyseurs à base dechlorure de cuivre(II)conduit auchlorure de vinyle.
Ladécennie 1970voit apparaître lepot catalytiqueà base de platine, rhodium et palladium, alors qu'ailleurs se développe industriellement la catalyse enzymatique avec l'immobilisation d'enzymes, permettant de produire despénicillinessemi-synthétiques ou l'isomérisation duglucoseenfructose.La découverte des zéolithes synthétiques aboutit industriellement dans lesannées 1980,le procédé MTG (methanol to gasoline:« méthanol vers essence ») permet de fabriquer de l'essence à partir duméthanolgrâce au zéolithe H-ZSM5, production de diesel à partir CO et H2grâce à des catalyseurs à base de cobalt. Lachimie finen'est pas en reste avec la synthèse de lavitamine K4à l'aide d'un catalyseur membranaire à base de platine.
La liste est encore très longue et les molécules de plus en plus élaborées et de nouvelles perspectives s'ouvrent dans lesannées 2010[11],[12],[13],[14],[15],[16],[17],[18]avec l'utilisation de catalyseurs à un seul atome, qui devraient encore améliorer lacatalyse hétérogène,dont dans les domaines de la chimie et de l'énergie[19].
Considérations générales
[modifier|modifier le code]Catalyseur
[modifier|modifier le code]En chimie, un catalyseur est une substance qui augmente la vitesse d'uneréaction chimique;il participe à la réaction dans une étape, mais est régénéré dans une étape subséquente. Il ne fait donc pas partie des réactifs. S'il fait partie des produits, la réaction est dite autocatalysée. C'est le cas par exemple de la réaction d'équation
- 2 MnO4−+ 5 H2C2O4+ 6 H+→ 2 Mn2++ 10 CO2+ 8 H2O
pour laquelle les ions Mn2+ont un rôle catalytique.
Lorsqu’un catalyseur est utilisé pour accélérer une transformation, on dit que celle-ci est catalysée. Les catalyseurs agissent seulement sur des produits prédéterminés. Si un catalyseur accélère la réaction, il est dit positif. S'il la ralentit, il est dit négatif[20].
Les catalyseurs sont largement utilisés dans l'industrie et enlaboratoireparce qu'ils augmentent considérablement la production des produits tout en minimisant les coûts de production. Dans la nature et en biochimie, certainesprotéinespossèdent une activité catalytique. Il s'agit desenzymes.
Le catalyseur augmente lavitesse de réactionen introduisant de nouveaux chemins de réaction (mécanisme), et en abaissant sonénergie d'activation,ouénergie librede Gibbs d'activation. Ce faisant il permet d'augmenter la vitesse, ou d'abaisser la température de la réaction. Le catalyseur ne modifie pas l'énergie libre de Gibbstotale de la réaction qui est une fonction d'état du système et n'a donc aucun effet sur laconstante d'équilibre.
En plus de modifier la vitesse de réaction, le choix d'un catalyseur peut reposer sur d'autres paramètres:
- la sélectivité: un catalyseur sélectif favorise la formation du produit désiré par rapport aux produits secondaires. Par exemple, quand on utilise l'argentmétallique pour catalyser la réaction de formation de l'oxyde d'éthylène,à partir d'oxygèneet d'éthylène,cette réaction est accompagnée par la formation plus favorable thermodynamiquement de CO2et H2O;
- la durée de vie: le catalyseur doit pouvoir demeurer intact après plusieurs cycles de réaction.

La succession des étapes conduisant à la formation d'un produit n'est pas la même en présence et en l'absence d'un catalyseur.
- En l'absence de catalyseur, l'énergie potentielle du système chimique prend une valeur importante rendant la réaction lente (ou par analogie la promenade épuisante).
- En revanche, la présence d'un catalyseur permet d'atteindre le même état final mais par une succession d'étapes dont aucune ne possède une énergie potentielle élevée.
Le chemin réactionnel est donc différent en présence et en absence du catalyseur; le nombre d'étapes est généralement plus élevé avec catalyse que sans, mais toutes les étapes sont rapides.
Mécanisme type
[modifier|modifier le code]Le catalyseur réagit généralement avec un ou plusieursréactifspour donner unintermédiaire,qui donne leproduit de la réactiontout en régénérant le catalyseur. Par exemple, le bilan d'uneréaction R → P,en présence d'un catalyseur (C) peut s'écrire:
- R + C → RC (1)
- RC → P + C (2)
- Ces deux étapes peuvent ou non être deséquilibres chimiques.
Bien que le catalyseur soit consommé dans l'étape (1), il est régénéré par l'étape (2). La somme des deux étapes est donc identique au bilan annoncé:
- R → P
Cependant, le catalyseur parait généralement dans laloi de vitesse.Si l'étape cinétiquement déterminanteau schéma ci-dessus est la premièreétape R + C → RC,la réaction catalysée sera dusecond ordreavec l'équation de vitessev=kcat[R][C]. Mais le mécanisme catalysé a lieu en parallèle avec la réaction non catalysée. Si cette dernière estélémentaire,son équation de vitesse serav=k0[R] et l'équation de vitesse globale serav=k0[R] +kcat[R][C], que l'on peut écrire
- v=k[R], oùk=k0+kcat[C].
Ici le coefficient de vitesse (k) est la somme de deux termes. Le premier terme, normalement faible, représente laconstante de vitessede la réaction sans catalyseur. Le deuxième terme est proportionnel à la concentration du catalyseur, qui elle demeure constante lors de l'évolution d'une réaction dans le temps.
Catalyse et énergie de réaction
[modifier|modifier le code]Un catalyseur fonctionne en permettant un mécanisme alternatif mettant en jeu différents états de transition et des énergies d'activation plus basses. Ainsi, dans le cas d'une réactionbimoléculairesimple detype A + B,l'état de transition est remplacé par un intermédiaire réactionnel de plus basse énergie, accompagné par deux états de transition, eux-mêmes de plus basse énergie. L'effet de ce changement est que plus de collisions moléculaires ont l'énergie nécessaire pour atteindre l'état de transition. Ainsi, un catalyseur permet d'effectuer des réactions qui, bien que thermodynamiquement faisables, étaient cinétiquement impossibles, ou nettement plus lentes. Un catalyseur abaisse donc l'énergie d'activation d'une réaction.
Un catalyseur ne peut pas rendre possible une réaction énergétiquement défavorable, pas plus qu'il ne peut déplacer l'équilibre final. La réaction et la réaction inverse sont également catalysées (principe demicroréversibilité). L'enthalpie libre de la réaction est inchangée.
Classement selon la nature du catalyseur
[modifier|modifier le code]Catalyse hétérogène
[modifier|modifier le code]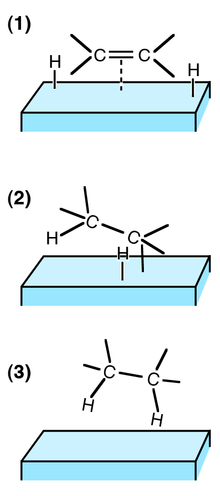
(1) Les réactifs sontadsorbéssur la surface du catalyseur et H2est dissocié;
(2) Un atome H se lie à l'un des atomes C. L'autre atome C est attaché à la surface;
(3) Un2eatome C se lie à un atome H. La molécule s'éloigne de la surface.
La catalyse esthétérogènequand le catalyseur et les réactifs ne sont pas dans la même phase. L'immense majorité des cas de catalyse hétérogène fait intervenir un catalyseur sous forme solide, les réactifs étant alors gazeux et/ou liquides. Les principales étapes du mécanisme sont décrites par la figure ci-contre.
Catalyse homogène
[modifier|modifier le code]En catalysehomogène,les réactifs et le catalyseur sont présents dans la même phase. On retrouve beaucoup ce type de catalyse en chimie organique où de nombreuses réactions se déroulent avec des réactifs en solution, en présence d'ions H+,d'acides de Lewis,de complexes,etc.,tous étant également solubles.
Catalyse enzymatique
[modifier|modifier le code]Dans la biologie, lesenzymessont des catalyseurs des réactionsmétaboliques.Elles ont des structures basées sur desprotéines.Les enzymes solubles peuvent être considérées comme intermédiaires entre les catalyseurs homogènes et hétérogènes; elles sont homogènes au niveau macroscopique mais au niveau moléculaire les réactions catalysées ont lieu sur la surface de l'enzyme comme pour la catalyse hétérogène. Les enzymes liés auxmembranes biologiquespar contre sont hétérogènes.
Classement selon le type de réaction activée
[modifier|modifier le code]Catalyse acido-basique
[modifier|modifier le code]Dans ces réactions, le catalyseur agit en tant qu'acideoubase.Cet acide ou cette base sont généralement des ions H+,HO−,des acides ou des bases de Lewis, ou encore desoxydes métalliques(Al2O3,V2O5,etc.). On distingue deux cas, selon que la réaction est accélérée par tous les acides (respectivement toutes les bases), ce qui s'appelle la catalyse générale, ou s'il faut un acide (ou une base) en particulier, ce qui s'appelle la catalyse spécifique.
Catalyse spécifique
[modifier|modifier le code]Dans certains cas, un acide particulier sert de catalyseur. Le mécanisme passe alors par un mécanisme qui lui est propre, et qui serait différent pour un autre acide. C'est le cas de la réaction d'halogénation de lapropanone[21]:
- CH3-CO-CH3+ X2→ CH3-CO-CH2X+ HX
- X = I ou Br
Cette réaction est accélérée par H3O+(ou par HO−). Laconstante de vitesseest de la forme
- k=k0+k1[H3O+] +k2[HO−].
- aveck0,constante de vitesse de la réaction non catalysée. La valeur dek0est très faible devantk1etk2(d'où l'effet notable de l'augmentation de la vitesse par les catalyseurs H3O+et HO−).
L'ajout d'unacide faiblene modifie la vitesse que par la variation de la concentration [H3O+] qu'il permet, et non par la variation de sa propre concentration. Cela indique que c'est spécifiquement H3O+le catalyseur, et non n'importe quel acide.
L'inversion du saccharoseest également de type catalyse spécifique. Son équation est:
- Saccharose + eau → glucose + fructose
- soit C12H22O11+ H2O→ C6H12O6+ C6H12O6
L'halogénation des nitroalcanes est un exemple de catalyse basique spécifique.
Catalyse générale
[modifier|modifier le code]Pour qu'une catalyse soit acido-basique générale, il faut que des acides (ou des bases) faibles catalysent également la réaction. Cette catalyse doit dépendre de la concentration enacide faible,et pas seulement du fait que cet acide peut libérer des ions H+.
Laconstante de vitesse,en catalyse acide spécifique est donc de la forme:
- k=k0+k1[H3O+] +k2[AH].
- où [AH] est la concentration en acide faible.
Pour montrer cette propriété de catalyse acide générale, il faut par exemple déterminer la dépendance de la vitesse (donc dek) en fonction de la quantité de AH ajouté, mais celadans un milieu tamponné,afin que le termek1[H3O+] soit maintenu constant[22].
Catalyse d'oxydoréduction
[modifier|modifier le code]Desréactions d'oxydoréductionpeuvent aussi être catalysées. Par exemple, ladismutationde l'eau oxygénéeest catalysée par les ions Fe2+ou Fe3+,l'hydrogénationdesalcènespar lenickel de Raney,ou par ou métaux nobles supportés[23].L'hydrogénation et l'hydrodésoxygénation sont largement étudiées en raison de leur pertinence pour la valorisation des composés biosourcés[24].Les procédés oxydatifs sont utilisés pour la synthèse de produits chimiques tels que le formaldéhyde[25],acétaldéhyde[26],l'acide acrylique[27],[28],l'acide benzoïque[29].Une telle catalyse met généralement en jeu uncouple redoxdont lepotentielsera compris entre le potentiel de l'oxydantet celui duréducteur.
- Catalyse nucléophile[réf. nécessaire]
Des réactions de substitutions nucléophiles peuvent être fortement accélérées en présence de traces d'autres nucléophiles. L'exemple classique est l'iodure de lithium. Dans ce sel, l'ion iodure est très peu lié au lithium, et est un nucléophile assez efficace. L'ion iodure est aussi un nucléofuge très efficace. Il sera donc déplacé par le nucléophile principal plus rapidement que ne se serait déroulée la réaction en absence de catalyseur.
- Catalyse par transfert de phase
Ici, l'idée est d'amener en contact des espèces se trouvant dans deux phases différentes. Ainsi, des substitutions nucléophiles, par exemple
- RCl + HO−→ ROH + Cl−
seraient réalisables si la base HO−qui est en phase aqueuse et le substrat RCl qui en phase organique pouvaient se rencontrer. Uneespèce chimiquequi transporterait l'ionhydroxydede la phase aqueuse à la phase organique, puis retransporterait lenucléofugeCl−de la phase organique à la phase aqueuse sans se transformer lui-même serait un catalyseur, et dans ce cas, un catalyseur par transfert de phase. Une règle essentielle est que chaque phase doit respecter l'électroneutralité, si bien que si un cation change de phase, un anion doit changer en même temps (ou un cation doit passer en même temps dans l'autre direction).
Les cations ammonium substitués par des chaînes alkyle, par exemple (C4H9)N+,peuvent jouer un tel rôle catalytique. De par leur charge positive, ils peuvent être solvatés en phase aqueuse, et par leurs chaînes alkyle, ils peuvent l'être en phase organique. La première étape est dans ce cas, le transfert de (C4H9)N++ HO−(espèce globalement neutre). La réaction de substitution peut avoir lieu en phase organique, et produire l'anion Cl−.L'espèce (C4H9)N++ Cl−(toujours globalement neutre) peut passer en phase aqueuse. Le cation ammonium est alors à nouveau disponible pour un nouveau transfert d'ion HO−.
Les substitutions nucléophiles ne sont pas les seules à pouvoir mettre en jeu une catalyse à transfert de phase, par exemple l'oxydation dustyrènepar les ions permanganate[30],en présence de (C4H9)N++ HSO4−.
- Autocatalyse
Dans certains cas, le catalyseur apparaît dans le bilan de la réaction, du côté des produits: la réaction est alorsautocatalysée.L'effet d'une autocatalyse se traduit par une augmentation de la vitesse de réaction (alors que la vitesse diminue toujours lorsque la réaction avance) avant de diminuer. L'augmentation de la vitesse est due à l'augmentation de la concentration en catalyseur, et sa diminution à la disparition importante de ses réactifs.
Quelques exemples de réactions et de procédés
[modifier|modifier le code]
Un grand nombre deprocédés chimiquescomportent au moins une étape catalysée, que ce soit pour la fabrication de fibres synthétiques, de médicaments ou d'additifs alimentaires, sans compter toutes les réactions biologiques catalysées par les enzymes. Par ailleurs, en favorisant des réactions peu polluantes, la catalyse est un des piliers de lachimie verte.La suite de cette section fournit des exemples de réactions catalysées suivant les secteurs d'applications.
Catalyse dans la vie quotidienne
[modifier|modifier le code]
- Le chauffage individuel au gaz par catalyse n'est pas dangereux car il n'émet pratiquement pas de CO[31].
- Lepot catalytiqueest sans doute l'exemple le plus connu de catalyses.
- L'utilisation de lalevure de boulangerpour la fabrication du pain.
Catalyse dans les grands procédés industriels
[modifier|modifier le code]
D'après[32].
Lesprocédés industrielsqui utilisent des catalyseurs permettent d'économiser des produits chimiques (meilleurs rendements, synthèse en moins d'étapes), du temps (donc de l'argent) et de l'énergie en mettant en jeu des procédés à plus basse température. Quelques exemples de grands procédés industriels sont:
- synthèse de l'ammoniac NH3à partir de ses éléments H2et N2,catalysée par le fer (procédé Haber);
- synthèse de l'acide sulfurique par leprocédé de contact(oxydation de SO2en SO3catalysé par V2O5);
- reformageenpétrochimie(conversion par le platine et l'alumine demolécules naphténiquesenmolécules aromatiques);
- craquageen pétrochimie pour transformer les coupes lourdes en petites molécules, grâce auxzéolithes.
Expériences utilisées pour l'enseignement de la catalyse
[modifier|modifier le code]- Expérience de la lampe sans flamme (oxydation de l'éthanol par l'air en présence de cuivre)[33].
- Diverses décomposition de l'eau oxygénéepar des ions fer, du platine, du dioxyde de manganèse, du sang, une rondelle de radis,etc.
- Réactions enchimie organique(estérification,hydrolyse,etc.) catalysées par unacide fort.
Catalyse amusante
[modifier|modifier le code]- Lacendrepeut servir de catalyseur lors de la combustion dusucre.Ce dernier, chauffé au briquet, ne produit aucune flamme. Recouvert de cendre, il peut s'enflammer et brûle d'une flamme bleue.
- Lalampe Bergerélimine les mauvaises odeurs en diffusant une substance active dans l'air, par combustion catalytique de son substrat.[réf.souhaitée].
Notes et références
[modifier|modifier le code]- Anatole Bailly; 2020: Hugo Chávez, Gérard Gréco, André Charbonnet, Mark De Wilde, Bernard Maréchal & contributeurs, «Le Bailly», surbailly.app,(consulté le).
- L. Schuffenecker, G. Scacchi G., B. Proust, J.-F. Foucaut, L. Martel et M. Bouchy,Thermodynamique et cinétique chimiques,Éd. Tec & doc,coll.« info chimie », 1991,p.351.
- (en)Laidler Keith J. et Meiser John H.,Physical Chemistry(Benjamin/Cummings 1982),p.424(ISBN0-8053-5682-7).
- (en)Benoît Join, «La catalyse», surLa Recherche,(consulté le).
- AdelineCrépieuxet NataliePigeard-Micault,Petit dictionnaire illustré des femmes scientifiques: 110 noms, d'Hypatie aux récentes nobélisées,Ellipses,(ISBN978-2-340-07966-3)
- J. R. Partington(en)(1989),A Short History of Chemistry,Éd. Dover,p.196, 213.
- Ibid.,p.230.
- Ibid.,p.289.
- Ibid.,p.341.
- «Catalyse», surphysique-et-matiere.com(consulté le).
- SharonMitchellet JavierPérez-Ramírez,«Single atom catalysis: a decade of stunning progress and the promise for a bright future»,Nature Communications,vol.11,no1,(ISSN2041-1723,DOI10.1038/s41467-020-18182-5,lire en ligne,consulté le)
- Abhaya K.Datyeet HuaGuo,«Single atom catalysis poised to transition from an academic curiosity to an industrially relevant technology»,Nature Communications,vol.12,no1,(ISSN2041-1723,DOI10.1038/s41467-021-21152-0,lire en ligne,consulté le)
- HongzhouYang,LuShang,QinghuaZhanget RunShi,«A universal ligand mediated method for large scale synthesis of transition metal single atom catalysts»,Nature Communications,vol.10,no1,(ISSN2041-1723,DOI10.1038/s41467-019-12510-0,lire en ligne,consulté le)
- HuishanShang,XiangyiZhou,JuncaiDonget AngLi,«Engineering unsymmetrically coordinated Cu-S1N3 single atom sites with enhanced oxygen reduction activity»,Nature Communications,vol.11,no1,(ISSN2041-1723,DOI10.1038/s41467-020-16848-8,lire en ligne,consulté le)
- ShiFang,XiaorongZhu,XiaokangLiuet JianGu,«Uncovering near-free platinum single-atom dynamics during electrochemical hydrogen evolution reaction»,Nature Communications,vol.11,no1,(ISSN2041-1723,DOI10.1038/s41467-020-14848-2,lire en ligne,consulté le)
- MengyaoOuyang,Konstantinos G.Papanikolaou,AlexeyBoubnovet Adam S.Hoffman,«Directing reaction pathways via in situ control of active site geometries in PdAu single-atom alloy catalysts»,Nature Communications,vol.12,no1,(ISSN2041-1723,DOI10.1038/s41467-021-21555-z,lire en ligne,consulté le)
- HengpanYang,QingLin,ChaoZhanget XinyaoYu,«Carbon dioxide electroreduction on single-atom nickel decorated carbon membranes with industry compatible current densities»,Nature Communications,vol.11,no1,(ISSN2041-1723,DOI10.1038/s41467-020-14402-0,lire en ligne,consulté le)
- GuodongSun,Zhi-JianZhao,RentaoMuet ShenjunZha,«Breaking the scaling relationship via thermally stable Pt/Cu single atom alloys for catalytic dehydrogenation»,Nature Communications,vol.9,no1,(ISSN2041-1723,DOI10.1038/s41467-018-06967-8,lire en ligne,consulté le)
- (en)«Single atom catalysts push the boundaries of heterogeneous catalysis»,Nature Communications,vol.12,no1,,p.5884, s41467–021–26130-0(ISSN2041-1723,PMID34635653,PMCIDPMC8505485,DOI10.1038/s41467-021-26130-0,lire en ligne,consulté le)
- Association québécoise des utilisateurs de l'ordinateur au primaire-secondaire, «Facteurs qui influencent la vitesse d'une réaction», Association québécoise des utilisateurs de l'ordinateur au primaire-secondaire,(consulté le).
- Schuffenecker L., Scacchi G., Proust B. Foucaut J.-F., Martel L. et Bouchy M. (1991),Thermodynamique et cinétique chimiques,Éd. Tec & doc,coll.« info chimie »,p.354.
- Schuffenecker L., Scacchi G., Proust B. Foucaut J.-F., Martel L. et Bouchy M. (1991),Thermodynamique et cinétique chimiques,Éd. Tec & doc,coll.« info chimie »,p.356.
- (en)EmőkeSikora,AdriennKiss,ZsuzsaH. Göndöret PéterPekker,«Fine-tuning the catalytic activity by applying nitrogen-doped carbon nanotubes as catalyst supports for the hydrogenation of olefins»,Reaction Kinetics, Mechanisms and Catalysis,(ISSN1878-5204,DOI10.1007/s11144-019-01705-7,lire en ligne,consulté le).
- (en)FerasAlshehri,ClementFeral,KathleenKirkwoodet S. DavidJackson,«Low temperature hydrogenation and hydrodeoxygenation of oxygen-substituted aromatics over Rh/silica: part 1: phenol, anisole and 4-methoxyphenol»,Reaction Kinetics, Mechanisms and Catalysis,vol.128,no1,,p.23–40(ISSN1878-5204,DOI10.1007/s11144-019-01630-9,lire en ligne,consulté le).
- (en)DanChen,JingShi,YanbinYaoet ShiwenWang,«Enhanced catalytic activity towards formaldehyde oxidation over Ag catalysts supported on carbon nanotubes»,Reaction Kinetics, Mechanisms and Catalysis,vol.127,no1,,p.315–329(ISSN1878-5204,DOI10.1007/s11144-019-01549-1,lire en ligne,consulté le).
- (en)Mikhail V.Parfenovet Larisa V.Pirutko,«Oxidation of ethylene to acetaldehyde by N2O on Na-modified FeZSM-5 zeolite»,Reaction Kinetics, Mechanisms and Catalysis,vol.127,no2,,p.1025–1038(ISSN1878-5204,DOI10.1007/s11144-019-01610-z,lire en ligne,consulté le).
- (en)«Surface chemistry of phase-pure M1 MoVTeNb oxide during operation in selective oxidation of propane to acrylic acid»,J. Catal.,vol.285,,p.48-60(lire en ligne).
- (en)«The reaction network in propane oxidation over phase-pure MoVTeNb M1 oxide catalysts»,J. Catal.,,p.369-385(lire en ligne).
- (en)«Multifunctionality of Crystalline MoV(TeNb) M1 Oxide Catalysts in Selective Oxidation of Propane and Benzyl Alcohol»,ACS Catal.,vol.3,no6,,p.1103-1113(lire en ligne).
- R. Barbe et J.-F. Le Maréchal (2007),La chimie expérimentale,t.2,Dunod, Sciences sup,p.39.
- Patrick Gélin,La combustion catalytique[PDF],IRCELyon(consulté le 27 novembre 2020).
- «3 – Grands procédés industriels en catalyse hétérogène»[PDF],surcours.espci.fr(consulté le).
- « La lampe sans flamme »,surscienceamusante.net.
Voir aussi
[modifier|modifier le code]Bibliographie
[modifier|modifier le code]- Jacques Angenault,La Chimie - dictionnaire encyclopédique,Dunod, 1995(ISBN2-10-002497-3)
Articles connexes
[modifier|modifier le code]- Réaction autocatalytique
- Pot catalytique
- Inhibiteur (chimie)•Poison de catalyseur
- Cycle carbone-azote-oxygène(phénomène nucléaire analogue à la catalyse et actif dans les étoiles)
- Sonocatalyse
Liens externes
[modifier|modifier le code]
- Ressource relative à la santé:
- Notices dans des dictionnaires ou encyclopédies généralistes:
- Patrick Gélin,La combustion catalytique[PDF],IRCELyon
- La catalyse,conférence filmée de Christian Minot,Universités de tous les savoirs
- Évolution de catalyseurs solides,SFRS/CERIMES (film pédagogique ancien, 1970)


