Bifluorure
Apparence
| Bifluorure | |
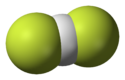 Structure de l'ion bifluorure. |
|
| Identification | |
|---|---|
| NoCAS | |
| PubChem | 85305403 |
| ChEBI | 30480 |
| Propriétés chimiques | |
| Formule | HF2 |
| Masse molaire[1] | 39,004 75 ± 7,0E−5g/mol H 2,58 %, F 97,42 %, |
| Unités duSIetCNTP,sauf indication contraire. | |
| modifier |
|
L'ionbifluorure(ou hydrogénodifluorure) désigne l'aniondeformuleHF2−.
Cetionprésente la plus forteliaison hydrogèneconnue, avec une longueur de liaisonH-Fde 114pm[2]et uneénergie de liaisonsupérieure à155kJ mol−1[3].Lediagramme d'orbitales moléculairesde l'anionmontre que lesatomessont liés entre eux par uneliaison à 3 centres et 4 électrons[4].
Certains sels de HF2sont courants, notamment lebifluorure de potassiumKHF2et lebifluorure d'ammonium(NH4)HF2.
L'ion bifluorure participe à l'autoprotolysede l'acide fluorhydriqueHFlors de laquelle les ions H+et F−issus de son ionisation sont solvatés par HF:
- 3HFH2F+(HF)+ HF2−(HF)
Notes et références[modifier|modifier le code]
- Masse molaire calculée d’après«Atomic weights of the elements 2007», surwww.chem.qmul.ac.uk.
- Greenwood, Norman N.; Earnshaw, A. (1997),Chemistry of the Elements (2nd ed.),Oxford: Butterworth-Heinemann,(ISBN0-7506-3365-4)
- Emsley, J.,Very Strong Hydrogen Bonds,Chemical Society Reviews, 1980, 9, 91-124.
- Pimentel, G. C. The Bonding of Trihalide and Bifluoride Ions by the Molecular Orbital Method.J. Chem. Phys.1951,19,446-448,DOI10.1063/1.1748245.

