Molécule hypervalente
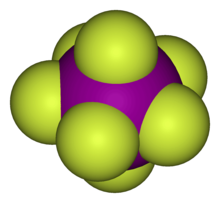
Unemolécule hypervalenteest uneespèce chimiqueconsidérée comme comportant unatomequi, en ayant plus de huitélectronsdans sacouche de valence,ne respecte pas larègle de l'octet.L'iontriiodureI3−,letrifluorure de chloreClF3,l'ionphosphatePO43−,lepentachlorure de phosphorePCl5,l'hexafluorure de soufreSF6ou encore l'heptafluorure d'iodeIF7sont des exemples de molécules hypervalentes. Ce concept a été introduit en 1969 par Jeremy I. Musher pour les molécules formées par les éléments des colonnes 15 à 18 dans tous leursétats d'oxydationautres que l'état le plus bas[1].
Afin de rendre compte de ces structures, des théories ont été proposées visant à aménager larègle de l'octet.Le concept deliaison à trois centres et quatre électronsa été proposé dans ce but en 1951: il est fondé sur uneorbitaleliante occupée, uneorbitale haute occupéenon liante et uneorbitale basse vacanteantiliante.Ce modèle a reçu le soutien de J.I. Musher[2].
La nomenclature N-X-L, introduite en 1980[3],est souvent utilisée pour classer les composés hypervalents:
- N = nombre d'électrons de valence impliqués dans les liaisons
- X = symbole chimique de l'atome central
- L = nombre deligandssur l'atome central
Quelques exemples:
Le termehypervalenta été contesté par le chimiste canadienRonald Gillespie,qui estime que « puisqu'il n'y a pas de différence fondamentale entre les liaisons de molécules hypervalentes et non hypervalentes, il n'y a pas de raison pour continuer à utiliser le termehypervalent»[4].Le Prof.Paul von Ragué Schleyera suggéré de désigner ces molécules commehypercoordonnées,afin de ne pas présupposer du type des liaisons impliquées dans leur structure.
Il a été montré que, dans les molécules hypercoordonnées avec des ligandsélectronégatifstelles quePF5,cesligandstendent à dépouiller l'atome central de ses électrons de sorte que celui-ci retrouve huit électrons dans sacouche de valence,voire moins. De plus, de telles molécules àfluoruren'ont pas d'équivalent àhydrure;ainsi, lephosphoranePH5est une molécule instable, contrairement aupentafluorure de phosphorePF5.
Notes et références
[modifier|modifier le code]- Musher, J.L. The Chemistry of Hypervalent MoleculesAngew. Chem. Int. Ed. Engl.1969,8,54-68.[1]
- The Origin of the Term "Hypervalent"Jensen, William B.J. Chem. Educ.200683 1751.Link
- Perkins,C. W.; Martin, J. C.; Arduengo, A. J.; Lau, W.; Alegria, A,; Kochi, J. K.; An Electrically Neutral a-Sulfuranyl Radical from the Homolysis of a Perester with Neighboring Sulfenyl Sulfur: 9-S-3 speciesJ.Am. Chem. Soc.1980,102, 7753-7759DOI10.1021/ja00546a019
- Gillespie, R. J.; Silvi, B. The octet rule and hypervalence: two misunderstood concepts.Coord. Chem. Rev.2002,233-234,53-62.[2]
