Pectine
Lespectines(dugrec ancienπηκτός/pêktós,« épaissi,caillé»), ou plus largement les substances pectiques, sont despolyosides,rattachées auxglucides.Ce sont des composés exclusivement d’originevégétale.Les pectines sont présentes en grande quantité dans lesparois primairesdesdicotylédones,et en particulier dans les parois végétales de nombreuxfruitsetlégumes[1].Elles sont extraites industriellement des coproduits de l'industrie desjus de fruits,principalement desagrumeset en moins grande quantité des marcs depomme[2].
Lapectolyseest lalysede pectines par des enzymes pectolytiques.
Composition chimique
[modifier|modifier le code]
Ce sont despolysaccharidescaractérisés par un squelette d’acide α-D-galacturoniqueet de faibles quantités deα-L-rhamnoseplus ou moins ramifiés. Le modèle généralement accepté décrit les pectines comme un enchaînement de deux structures majoritaires: une chaîne principale homogalacturonique (ou "zone lisse", dénommée HG) et une chaîne rhamnogalacturonique (ou "zone hérissée", dénommée RG)[3],[4].
Les homogalacturonanes sont la principale chaîne qui compose les pectines (représentant en règle générale plus de 60 % des pectines)[3].Ce sont des polymères d’acide α-D-galacturoniqueliés en (1→4). La longueur de ces chaînes peut aller de 70 à 100 résidus d’acide galacturonique dans lecitron,labetterave sucrièreou dans lapomme[5],c’est-à-dire présentant desmasses molairesde l’ordre 12 à 20 kDa. La fonction carboxylique des acides α-D-galacturoniques peut être sous formeacide,ou ionisés par différentscationsdont lecalcium,ouestérifiéepar duméthanol.Par ailleurs les acides galacturoniques peuvent êtreacétylésen O-2 et /ou O-3[3].En fonction de ces estérifications, les pectines sont caractérisées par un degré deméthylation(DM) et un degré d’acétylation(DA) qui correspond au rapport des acides galacturoniques estérifiés (méthylés ou acétylés) sur les acides galacturoniques totaux. D’un point de vue fonctionnel, on distingue trois catégories de pectines:
- si un degré de méthylation est inférieur à 5 % (DM<5) il s'agit d'acides pectiques;
- si le degré de méthylation est inférieur à 50 % (DM<50), il s'agit de pectines faiblement méthylées (LM);
- si le degré de méthylation est supérieur à 50 % (DM>50), il s'agit de pectines hautement méthylées (HM).
Le degré d’estérification des pectines a un impact sur la flexibilité de lamolécule:plus le degré d’estérification est faible, plus la pectine est rigide[6],[7].Il a également un fort impact sur leurs propriétés degélification.Les pectines sont synthétisées sous forme fortementméthylée[4]et c'est donc sous cette forme (DM d'environ 70 à 80) qu'elles sont en général présentes dans lesparois végétales.
Le squelette de la zone rhamnogalacturonique est construit par la répétition d'undimèred'acide galacturoniqueetrhamnose,avec la structure suivante...α-D-GalA-(1→2)-α-L-Rha-(1→4)- α-D-GalA-(1→2)-α-L-Rha-(1→4)[8].Ces zones rhamnogalacturoniques présentent de plus des ramifications composées essentiellement degalactoseet d'arabinose,portées par la fonctionalcoolen C3 ou C4 du rhamnose[3].
Deux structures présentes en quantité moindre présentent desramificationssur la chaîne homogalacturonique.Les homogalacturonanes peuvent êtresubstituéspar des unités simples deβ-D-xyloselié sur le C3 des acides galacturoniques. Ces zones sont appelées xylogalacturonanes[3].
Les rhamnogalacturonanes de type II ont été isolés d'hydrolysatsenzymatiquesde parois[9]et ainsi nommés car le rhamnose et l'acide galacturonique sont leurs principaux constituants; cependant cette dénomination est trompeuse, car ils sont caractérisés par un squelette homogalacturonique portant des ramifications complexes. Les rhamnogalacturonanes de type II sont constitués d’un enchaînement de huitrésidusd’acide galacturoniques liés en α-(1→4), substitués par quatrechaînes latéralesd’oligosaccharides(A, B, C et D). La chaîne latérale B est liée au cinquième résidu d’acide galacturonique par lecarbone2, en partant de l’extrémitéréductricedu squelette, tandis que la chaîne D est principalement liée par le carbone 3 du sixième résidu d’acide galacturonique[10]. Ces rhamnogalacturonanes comportent 12osesdifférents dont certains sont rares tels que l’apiose,le 2-O-méthyl- L-fucose,le 2-O-méthyl-D-xylose,l’acide acérique (3-C-carboxy-5-deoxy-L-xylose), le Kdo (acide 3-deoxy-D-manno-octolosonique) et le Dha (acide 3-deoxyD-lyxo-heptulosarique)[9].Leur structure est très conservée dans l'ensemble desplantes terrestres,et ils jouent un rôle majeur dans l'intégrité et la cohésion desparois végétales,où ils permettent laréticulationdes chaînes pectiques par l'intermédiaire de ponts borates[4],[11].
Propriétés chimiques
[modifier|modifier le code]Les molécules d’acide uroniquepossèdent desfonctions carboxyles.Cette fonction confère aux pectines la capacité d’échanger desions.Dans le cas des parois végétales, ces ions sont surtout lecalciumprovenant de lacirculation apoplasmique.Ces ions bivalents ont la capacité de former desponts calciquesentre deux groupements carboxyles de deux molécules de pectine différentes. La cellule contrôle la proportion de fonction carboxyle. En effet, elle peut estérifier de manière réversible ses fonctions en les méthylant par une pectine-méthylestérase. Selon la proportion de monomères méthylés ou non, la chaîne est plus ou moins acide. Cette acidité est également contrôlée par despompes à protonsrégulé notamment par l’auxine.La concentration forte enprotonsprovoque alors le remplacement du calcium.
Une forte proportion de fonction carboxyle dans un pH alcaline favorise la cohésion des molécules de pectines entre elles. Des chaînes peuvent ainsi se lier et les pectines forment alors un gel. De même qu’une augmentation de la méthylation couplé à une forte acidité favorise le relâchement de la pectine. Expérimentalement, les chercheurs peuvent interrompre cette gélification en enlevant artificiellement le calcium. Ceci est réalisé lors de l’extraction par l’EDTA,qui est unchélateurpuissant du calcium. Cela peut également être réalisé aussi si on diminue lepH.
Rôles physiologiques
[modifier|modifier le code]Les pectines sont un des constituants de laparoi végétale.Elles sont également le composé prédominant au sein de lalamelle moyenne.Elles maintiennent ensemble les cellules destissus végétaux. Les pectines jouent un rôle structural dépendant des conditions ioniques du milieu (rapport H+/Ca2+). Les chaînes formées sont reliées entre elles pour constituer un réseau ou gel. Cet ensemble permet d’emmagasiner une grande quantité d’eau.L’hydrolysedes pectines est remarquable lors de la maturation desfruitslorsque les fibres decellulosedeviennent plus lâches.
Applications industrielles
[modifier|modifier le code]L’hydrolyse des pectines est nécessaire pour permettre la clarification spontanée des jus de fruits ou desmoûtsavantfermentation alcooliquecomme dans le cas de l’élaboration duvin rosé.Elle est alors réalisée parenzymage.
Intérêt culinaire
[modifier|modifier le code]
La pectine du commerce, dont celle souvent utilisée pour épaissir lesconfitureset lesgelées,est extraite du marc depommesdesséchées. Elle est vendue sous forme liquide ou de cristaux. On trouve aussi dusucre gélifiant,préadditionné de pectine. L’union européenneautorise l’utilisation de la pectine commetexturant alimentaire,sous le numéro E440. La réussite des confitures et des gelées dépend de la proportion de sucre, de pectine et d’acides contenus dans les fruits utilisés.
Une étude[12]publiée en 2002 n’a pas trouvé d’interaction moléculaire spécifique entre composés odorants et pectine, mais confirme que la pectine, même à faible dose (0,1 %) ne modifie pas les composés odorants; elle les bloque ou en freine l’extraction spontanée dans les confitures ou gelées lorsqu’ils sont volatils et/ouhydrophobes.Ces molécules odorantes sont encagées dans le maillage tridimensionnel des molécules de pectines, mais elles sont pour partie relâchées et reconnues par les récepteurs olfactifs lorsque la confiture ou la gelée est mangée.
Modification génétique
[modifier|modifier le code]Des chercheurs américains ont modifié legénomede latomate.Cette modification porte sur les gènes qui codent la formation des pectines. Ceci se traduit par un pourcentage de pectines moindre dans les tomatestransgéniques.Cette déficience en pectine permet d’obtenir des tomates plus fermes plus longtemps. Ces tomates sont les premiers végétaux transgéniques comestibles mis sur le marché américain.
Intérêt médical
[modifier|modifier le code]La pectine a des propriétésentérosorbantes,c’est-à-dire qu’elle peut absorber certainsmétaux lourdset radionucléides lors de son passage dans le tube digestif. Cette propriété pourrait être liée à sa capacité à échanger desions.Elle semble aussi pouvoir limiter l'entérocolite induite par certains toxiques absorbés avec l'alimentation, dont des médicaments tels que leméthotrexate[13]
La pectine est, selon des scientifiques biélorusses ayant travaillé sur les conséquences de lacatastrophe de Tchernobyl,capable d’aider l’organisme à ne pas absorber certainsradionucléides,dont lecésium 137radioactif,et ceci, sans les effets secondaires deschélateurschimiques, mais avec d’autres effets. Elle semble aussi pouvoir aider l’organisme à mieux ou plus rapidement se débarrasser du Césium qu’il contient.
Son efficacité est controversée voire douteuse[14],mais la pectine est par exemple utilisée en complément alimentaire chez les enfants vivant dans les zones exposées aux retombées de Tchernobyl, qui sont victimes de pathologies liées à l’accumulation ducésium 137ingéré avec la boisson ou la nourriture.Vassili Nesterenko[15]cite[16]une expérience ayant porté sur 64 enfants du districtbélarusdeGomel,très contaminé par les retombées deTchernobyl.Ces enfants ont passé un mois dans unsanatoriumoù ils n’ont consommé que de la nourriture non contaminée. Un groupe-témoin a pris de la pectine matin et soir; l’autre, unplacebo.Après un mois, les enfants du groupe pectine ont vu leur taux decésium 137diminuer de 62,6 %. Dans l’autre groupe, le césium n’a baissé que de 13,9 %[17].
Nesterenko a comparé les comprimés effervescents ukrainiens de pectine depommeà des algues connues (spiruline) pour leur capacité de fixer leradiocésium,ainsi qu’à une préparation développée à Minsk, tirée des résidus séchés de pomme, obtenus après l’extraction du jus. Les experts du Centre de Recherche de la Commission Européenne à Ispra ont analysé cette préparation et noté qu’elle contient 15 à 16 % de pectine. Mélangée à de l’eau ou du lait, cetteforme galéniqueest mieux acceptée et tolérée par les enfants et au moins aussi efficace que les tablettes effervescentes d’Ukraine,et beaucoup plus efficaces que laspiruline.Ces résultats ont justifié le développement par l'Institut BELRADde cette poudre enrichie de vitamines et d’oligoéléments, sous le nom de Vitapect. Vitapect a été enregistré en Biélorussie et donné aux enfants de villages fortement contaminés, pour des cures de trois à quatre semaines. Environ 200 000 enfants de Biélorussie ont reçu cette préparation, avec un contrôle radiométrique duCs137incorporé, avant et après la cure.
Nesterenko a aussi démontré que 3 à 4 cures de 4 semaines de pectine par an, distribué aux enfants dans les écoles de villages hautement contaminés, parvenaient à maintenir la charge enCs137au-dessous du seuil de 50 becquerels par kilogramme de poids (Bq/kg), seuil à partir duquel Bandajevsky observe des lésions irréversibles au niveau du cœur, de l’œil, dusystème immunitaireet endocrinien, ou d’autres organes[18],[19].
L’Association pour le contrôle de la radioactivité dans l’Ouesta également trouvé que des enfants ayant reçu de la pectine lors de leur séjour en France ont vu leur contamination aucésium 137baisser de 31 % en moyenne contre seulement 15 % chez ceux qui n’en ont pas reçu hors la part naturellement présente dans l’alimentation. Toujours selon l’ACRO, la pectine augmente et accélère l'élimination du césium, mais moins rapidement que le disent ceux qui l’ont promue[20].
DesONGaident les familles à se fournir en «Vitapect», pour que leurs enfants puissent en faire des cures régulières (trois par an idéalement, selon les promoteurs de la pectine).
Digestion
[modifier|modifier le code]L'être humain ne sécrète pas lui-même d'enzymes dégradant la pectine (l'une des molécules les plus difficiles à dégrader de notre alimentation); c'est lemicrobiote intestinalqui permet sa digestion, et il est en partie sélectionné par la présence des pectines[21].Les microbessymbiotiques[22]et processus responsables de cette digestion ont été récemment (publication 2017) identifiés, en particulier le rôle d'une bactérie intestinale dénomméeBacteroides thetaiotaomicrona été mis en évidence[23],[24].
Dégradation
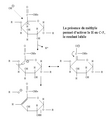
[modifier|modifier le code]La pectine est un polysaccharides fragile[25],et est en particulier dépolymérisée par des chauffages même modérés en milieu légèrement acide à neutre. Cette dépolymérisation joue un rôle important dans l'attendrissement de la texture des légumes lors de leur cuisson[26].Cette dépolymérisaton est due au phénomène dit de "béta-élimination" qui nécessite la présence d'acides galacturoniques méthylés. En effet, la présence du méthyle rend plus labile l'hydrogène porté par le C-5, et en présence d'ions hydroxydes (OH-) ceci conduit à une trans-élimination avec perte d'un électron et formation d'une double liaison en C4-C5, et rupture de la liaison glycosidique.
-
Mécanisme chimique de la béta-élimination des pectines
-
Schéma de la bétaélimination
De nombreuses espèces phytopathogènes (ex[27]:Erwinia carotovora,bactérie phytopathogène résistante au froid) sécrètent probablement de tels enzymes, nécessaires pour attaquer les cellules végétales. L’utilisation de ces enzymes est à la base de la clarification des jus de fruits comme lors de l’opération dedébourbagedans la vinification des vins blancs et desvins rosés.
Notes et références
[modifier|modifier le code]- (en)Voragen AG.J., Pilnik W., Thibault J.-F., Axelos M.A.V. et Renard C.M.G.C.,Pectins,in: Food Polysaccharides and Their Applications,New-York,Marcel Dekker,,287-339p.
- (en)May C.D., «Industrial pectins: sources, production and applications»,Carbohydrate Polymers,vol.12,,p.79-99
- (en)Voragen A.G.J., Coenen G.J., Verhoef R.P. et Schols H.A., «Pectin, a versatile polysaccharide present in plant cell walls»,Structural Biochemistry,vol.20,,p.263‑275
- (en)Caffall K.H. et Mohnen D., «The structure, function, and biosynthesis of plant cell wall pectic polysaccharides»,Carbohydrate Research,vol.344,,p.1879-1900
- (en)Thibault J.-F., Renard C.M.G.C., Axelos M.A.V., Roger P. et Crépeau M.-J., «Studies of the Length of Homogalacturonic Regions in Pectins by Acid-Hydrolysis»,Carbohydrate Research,vol.20,,p.271‑286.
- (en)Morris G.A., Foster T.J. et Harding S.E., «The effect of the degree of esterification on the hydrodynamic properties of citrus pectin»,Food Hydrocolloids,vol.14,,p.227-235
- (en)Axelos M.A.V. et Thibault J.-F., «Influence of the substituents of carboxyl groups and of the rhamnose content on the solution properties and flexibility of pectins»,International Journal of Biological Macromolecules,vol.13,,p.77-82
- (en)Renard C.M.G.C., Lahaye M., Mutter M., Voragen F.G.J. et Thibault J.-F., «solation and characterisation of rhamnogalacturonan oligomers generated by controlled acid hydrolysis of sugar-beet pulp.»,Carbohydrate Research,vol.305,,p.271-280
- (en)Darvill A.G., McNeil M. et Albersheim P., «Structure of Plant Cell Walls VIII. A New Pectic Polysaccharide.»,Plant Physiology,vol.62,,p.418-422
- (en)Vidal S., Doco T., Williams P., Pellerin P., York W.S., O'Neill M.A. et Albersheim P., «Structural characterization of the pectic polysaccharide rhamnogalacturonan II: evidence for the backbone location of the aceric acid-containing oligoglycosyl side chain.»,Carbohydrate Research,vol.326,,p.277-294
- (en)Ishii T., Matsugana T., Pellerin P., O'Neill M.A., Darvill A. et Albersheim P., «The Plant Cell Wall Polysaccharide Rhamnogalacturonan II Self-assembles into a Covalently Cross-linked Dimer»,Journal of Biological Chemistry,vol.274,,p.13098‑13104
- Flavour release from pectin gels: Effects of texture, molecular interactions and aroma compounds diffusion(REGA Barbara; GUICHARD Elisabeth; VOILLEY Andrée, inSciences des aliments,2002,vol.22,no3,p.235-248, 14p.ISSN 0240-8813,(anglais) Fiche Inist.
- (en)Mao Y, Kastrari B, Nabaeks, Wang LR, Adari D, Roos G. Stenram U, Molin G, Bengmark S et B. Jeppson, « Pectin supplemented external dietreduces the severity of methotrexate induced enterocolitis in rat »J Gastroenterol.1996;31(6):558-67.
- Jean-René Jourdain, «Evaluation de l’emploi de la pectine chez les enfants vivant sur les territoires contaminés par le césium - Etat de l’art et analyse critique des publications»
 [PDF],surirsn.fr,(consulté le)
[PDF],surirsn.fr,(consulté le)
- Directeur de l’institut indépendant de Radioprotection Belrad.
- Laure Noualhat,«La pomme contre l'atome: Et si la pectine était un remède pour les enfants vivant dans les zones contaminées par Tchernobyl? Reportage en Biélorussie»,Libération,(lire en ligne)
- (en)Nesterenko VB, Nesterenko AV, Babenko VI, Yerkovich TV, Babenko IV, «Reducing the 137Cs-load in the organism of "Chernobyl" children with apple-pectin»,Swiss Med Wkly,vol.134,nos1-2,,p.24-7.(PMID14745664,lire en ligne[PDF])
- (en)YIBandazhevsky,«Chronic Cs-137 incorporation in children's organs»,Swiss Med Wkly,vol.133,nos35-36,,p.488-90.(PMID14652805,lire en ligne[PDF])
- Bandajevsky Y.I. & Bandajevskaya G.« Myopathies au Césium 137 »Cardinale2003;15(8):40-3.
- Page de l’ACRO consacrée à la pectine(décembre 2004).
- Koropatkin, N. M., Cameron, E. A. & Martens, E. C. (2012)How glycan metabolism shapes the human gut microbiota.Nat. Rev. Microbiol. 10, 323–335
- Martens, E. C. et al.Recognition and degradation of plant cell wall polysaccharides by two human gut symbionts.PLoS Biol. 9, e1001221 (2011)
- Didier Ndeh & al. (2017)Complex pectin metabolism by gut bacteria reveals novel catalytic functions(résumé)
- Mirjam Czjzek (2017)Biochemistry: A wine-induced breakdown;Nature 22 Mars 2017; doi:10.1038/nature21901
- (en)Albersheim P., «Instability of pectin in neutral solutions»,Biochemical and Biophysical Research Communications,vol.1,,p.253-256
- Sila D.N.et al.,«Pectins in Processed Fruit and Vegetables: Part II - Structure-Function Relationships»,Comprehensive Reviews in Food Science and Food Safety,vol.8,,p.86-104(DOIDOI: 10.1111/j.1541-4337.2009.00070.x)
- Fiche Inist concernant une étude de l’université de Rouen.