Pyrophosphate

Lespyrophosphates(appelés aussi « diphosphates ») sont l'anion (base conjuguée), lesselset lesestersde l'acide pyrophosphorique.
Les pyrophosphates sont constitués de deux molécules dephosphatecondensées. Ils sont constitués autour d'une liaison P-O-P de typeanhydride d'acide(formule semi-développée(O3P)–O–(PO3)4−). Les esters sont constitués autour d'une liaison de type C–O–P (formule semi-développée R–O–(PO2)–O–(PO3)3−).
Synthèse
[modifier|modifier le code]Les pyrophosphates sont formés en chauffant des phosphates (hydrogénophosphates); ils tirent ainsi leur nom de cette origine (le préfixepyroen grec signifiant feu).
Exemples
[modifier|modifier le code]| Nom | Formule | Numéro E |
|---|---|---|
| Dihydrogénopyrophosphate de disodium | Na2H2P2O7 | E450i |
| Hydrogénopyrophosphate de trisodium | Na3HP2O7 | E450ii |
| Pyrophosphate de tétrasodium (pyrophosphate de sodium) | Na4P2O7 | E450iii |
| Nom | Formule |
|---|---|
| Pyrophosphate de diméthylallyle | 
|
| Adénosine diphosphate | 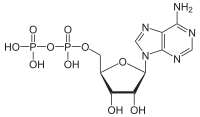
|
Rôle biochimique
[modifier|modifier le code]Les pyrophosphates ont un rôle majeur dans les processus de transfert d'énergie dans les cellules vivantes. Les anionspyrophosphates inorganiquesHP2O3−
7,abrégés enPPià l'instar desphosphates inorganiques,sont par exemple formés par l'hydrolysede l'ATPenAMP:
- ATP + H2O→ AMP + PPi+ H+ΔrG°=−45,6kJ/mol.
Utilisation
[modifier|modifier le code]Les pyrophosphates sont parfois utilisés comme arômes dans l'industrie de la nourriture pour chats, dans la mesure où ces derniers sont instinctivement très attirés par ces substances.

