Disulfure
Enchimie,disulfuredésigne généralement legroupe fonctionnelconstitué de deuxatomesdesoufreliés par uneliaison covalentesimple.
Pont disulfure
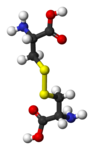
[modifier|modifier le code]On appellepont disulfuretout groupe disulfure dont les atomes de soufre sont chacun liés par covalence à un atome decarboned'uncomposé organique.Cela peut s'écrire de façon génériqueR1–S–S–R2,R1etR2étant desrésidusorganiques. C'est par exemple le cas dudisulfure de diphényleC6H5–S–S–C6H5,de lacystineHOOC–HCNH2–CH2–S–S–CH2–HCNH2–COOH—dimèredecystéinesliées par leur atome de soufre — ou encore de l'acide lipoïqueHOOC–CH2–CH2–CH2–CH2–C3H5S2,dans lequel le disulfure ferme unhétérocycle.
Anion disulfure
[modifier|modifier le code]L'aniondisulfure a pour formule S22−,également écrit−S–S−.Contrairement à l'anionsulfureS2−,denombre d'oxydation–2avec laconfiguration électroniquede l'argon(ungaz noble), l'anion disulfure S22−est constitué de deux anions de soufre S−dont le nombre d'oxydation est–1et la configuration électronique est celle duchlore,unhalogène:ces anions S−tendent ainsi à se lier avec d'autres anions S−pour former l'anion disulfure S22−.On trouve ce dernier par exemple dans ledisulfure de ferFeS2
Par extension
[modifier|modifier le code]On parle également de disulfures pour désigner des composés qui contiennent deux anions sulfure S2−.Contrairement aux cas précédents, cesespèces chimiquesne contiennent pas deliaison covalentesimpleS–S.C'est typiquement le cas dudisulfure de carboneCS2,dont laformule développées'écritS=C=S;ledisulfure de molybdèneMoS2ne pos sắc de pas non plus de liaisonS–S.