Histona
| Histona | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||
| Identificadores | |||||||||||
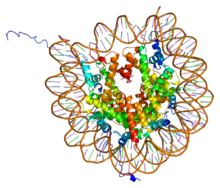
| Símbolo | Core histone | ||||||||||
| Pfam | PF00125 | ||||||||||
| Pfamclan | CL0012 | ||||||||||
| InterPro | IPR007125 | ||||||||||
| SCOPe | 1hio/SUPFAM | ||||||||||
| |||||||||||
| Histona | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||
| Identificadores | |||||||||||
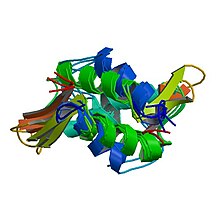
| Símbolo | Linker histone | ||||||||||
| Pfam | PF00538 | ||||||||||
| InterPro | IPR005818 | ||||||||||
| SMART | SM00526 | ||||||||||
| SCOPe | 1hst/SUPFAM | ||||||||||
| |||||||||||
Ashistonassonproteínascon moitos residuos alcalinos ou básicos presentes nonúcleo celulardoseucariotasque empaquetan e ordenan oADNen unidades estruturais chamadasnucleosomas.[1][2]Son os principais compoñentes proteicos dacromatina,actúan como unha especie de carretes aredor dos cales se enrola o ADN, e xogan un papel importante naregulación xénica.Sen histonas o ADN estaría desenrolado nos cromosomas e sería moi longo (a razón lonxitude/largura sería de máis de 10 millóns a 1 no ADN humano). Por exemplo, cada célula humana ten uns 1,8 metros de ADN, pero se están enrolados sobre as histonas formando cromatina ten só uns 90 milímetros (0,09 m), e, máis tarde, cando se duplica e condensa acromosomasdurante amitose,ocupa unha lonxitude de só 120micrómetros.[3]
Clases de histonas
[editar|editar a fonte]A secuencia de aminoácidos das histonas está moiconservadaevolutivamente e poden ser agrupadas en cinco clases principais:H1/H5,H2A,H2B,H3,eH4.[2][4][5]Estes 5 tipos están agrupados nas dúas superclases seguintes:
- Histonas do octámero ou histonascore– H2A, H2B, H3 e H4.
- Histonas de unión ou enlace ou histonaslinker– H1 e H5.
Cada unha das histonascoreensámblase con outra igual, e despois ensámblanse todas xuntas para formar os octámeros dosnucleosomas,orixinando unha especie de carrete no que se enrolan 147pares de basesde ADN formando unha superhélice que se enrola á esquerda e dá 1,65 voltas ao carrete.[6]As histonas de unión H1 únense ao nucleosoma e aos puntos de entrada e saída do ADN do octámero, de maneira que fixan o ADN no seu lugar[7]o que permite a formación dunha estrutura de orde superior. A máis básica de tales estruturas é a fibra de 10 nm da cromatina ou conformación encolar de doas.Isto implica o enrolamento do ADN arredor dosnucleosomasdeixando un tramo de ADN de aproximadamente 50 pares de bases que separa cada dous nucleosomas, chamado ADN espazador. O conxunto das histonas ensambladas e o ADN chámasecromatina.As estruturas de orde superior que pode formar a cromatina son a fibra cromatínica de 30 nm (que forma un zigzag irregular) e a fibra de 100 nm, que se poden atopar en células interfásicas. Durante amitosee ameiose,unha maior condensación da cromatina orixina oscromosomas,formados polas interaccións entre os nucleosomas e outras proteínas reguladoras.
A seguinte é unha lista das proteínas histonas humanas:
| Superfamilia | Familia | Subfamilia | Membros |
|---|---|---|---|
| Histonas de unión ou enlace (linker) | |||
| H1 | |||
| H1F | H1F0,H1FNT,H1FOO,H1FX | ||
| H1H1 | HIST1H1A,HIST1H1B,HIST1H1C,HIST1H1D,HIST1H1E,HIST1H1T | ||
| Histonas do octámero (core) | |||
| H2A | |||
| H2AF | H2AFB1,H2AFB2,H2AFB3,H2AFJ,H2AFV,H2AFX,H2AFY,H2AFY2,H2AFZ | ||
| H2A1 | HIST1H2AA,HIST1H2AB,HIST1H2AC,HIST1H2AD,HIST1H2AE,HIST1H2AG,HIST1H2AI,HIST1H2AJ,HIST1H2AK,HIST1H2AL,HIST1H2AM | ||
| H2A2 | HIST2H2AA3,HIST2H2AC | ||
| H2B | |||
| H2BF | H2BFM,H2BFO,H2BFS,H2BFWT | ||
| H2B1 | HIST1H2BA,HIST1H2BB,HIST1H2BC,HIST1H2BD,HIST1H2BE,HIST1H2BF,HIST1H2BG,HIST1H2BH,HIST1H2BI,HIST1H2BJ,HIST1H2BK,HIST1H2BL,HIST1H2BM,HIST1H2BN,HIST1H2BO | ||
| H2B2 | HIST2H2BE | ||
| H3 | |||
| H3A1 | HIST1H3A,HIST1H3B,HIST1H3C,HIST1H3D,HIST1H3E,HIST1H3F,HIST1H3G,HIST1H3H,HIST1H3I,HIST1H3J | ||
| H3A2 | HIST2H3C | ||
| H3A3 | HIST3H3 | ||
| H4 | |||
| H41 | HIST1H4A,HIST1H4B,HIST1H4C,HIST1H4D,HIST1H4E,HIST1H4F,HIST1H4G,HIST1H4H,HIST1H4I,HIST1H4J,HIST1H4K,HIST1H4L | ||
| H44 | HIST4H4 |
Estrutura
[editar|editar a fonte]
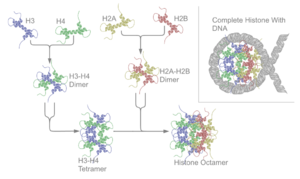
O octámero oucoredonucleosomaestá formado por dousdímerosdas proteínas H2A-H2B e untetrámeroH3-H4, que forman dúas metades case simétricas naestrutura terciaria(simetríaC2;unhamacromoléculaé a imaxe especular da outra).[6]Os dímeros H2A-H2B e o tetrámero H3-H4 tamén mostran unha simetría pseudodíada. As 4 histonascore(H2A, H2B, H3 e H4) son relativamente semellantes en estrutura e a súa secuencia está moi conservada na evolución, e todas presentan un motivo estrutural "hélice xiro hélice xiro hélice" (que permite unha fácil formación do dímero). Tamén comparten a característica de teren longas "colas" nun extremo da súa cadea deaminoácidos,que é a parte na que se producen asmodificacións postraducionais(véxase máis adiante).
Tense proposto que as proteínas histonas están relacionadas evolutivamente coa parte helicoidal do dominio AAA+ATPaseestendido, co dominio C, e co dominio de recoñecemento de substrato N-terminal das proteínas Clp/Hsp100. Malia as diferenzas na súa topoloxía, estes tres pregamentos comparten un motivo homólogo hélice-cadea-hélice.[8]
A distancia entre nucleosomas foi medida por investigadores británicos usando a técnica daresonancia magnéticade electróns, e variaba de 59 a 70Å.[9]
As histonas poden establecer cinco tipos deinteraccións co ADN:
- Dipolos de hélice formados nashélices αnas histonas H2B, H3, e H4 orixinan que se acumule unha carga neta positiva no punto de interacción cos gruposfosfatocargados negativamente do ADN.
- Enlaces de hidróxenoentre o ADN e o grupoamidada cadea principal das proteínas histonas.
- Interaccións non polares entre a histona e os azucresdesoxirribosado ADN.
- Pontes salinas(atraccións electrostáticas) eenlaces de hidróxenoentre ascadeas lateraisdos aminoácidos básicos (especialmentelisinaearxinina) e os osíxenos do fosfato do ADN.
- Insercións non específicas do suco menor das colas N-terminais de H3 e H2B en dous sucos menores da molécula de ADN.
A natureza moi básica das histonas, ademais de facilitar as interaccións ADN-histonas, contribúe á súa solubilidade en auga.
As histonas están suxeitas amodificacións postraducionaisrealizadas porencimas,fundamentalmente nas colas N-terminais, mais tamén nos dominios globulares.[10]Estas modificacións afectan á súa función de regulación xénica (verfuncións). Tales modificacións inclúen:
- metilación,unión encimática de gruposmetilo(-CH3).
- citrulinación,conversión dearxininaencitrulina.
- acetilación,unión dun grupoacetilo(-CH3-CO).
- fosforilación,unión dunfosfato.
- SUMOilación,unión das pequenas proteínas reguladorasSUMO(parecidas áubiquitina,pero con outra función).
- ubiquitinación,unión da pequena proteína reguladora ubiquitina, que marca a proteína para a degradación.
- ADP-ribosilación,adición de restos deADP-ribosa.
Función
[editar|editar a fonte]Compactación das cadeas do ADN
[editar|editar a fonte]As histonas actúan como carretes arredor dos cales se enrola o ADN. Isto permite a compactación necesaria para acomodar os grandesxenomaseucarióticos dentro donúcleo celular.A molécula compactada é 40.000 veces máis curta ca a molécula sen compactar.
Regulación da cromatina
[editar|editar a fonte]As histonas sofrenmodificacións postraducionaisque alteran a súa interacción coADNe as proteínas nucleares. As histonas H3 e H4 teñen longas colas que saen do nucleosoma, que poden ser modificadascovalentementeen varios puntos. Estas modificacións inclúen metilación, acetilación, fosforilación, ubiquitinación, SUMOilación, citrulinación, e ADP-ribosilación. Ademais das colas, a parte central das the histonas H2A, H2B, e H3 pode tamén modificarse. Pénsase que certas combinacións de modificacións constitúen un código, o chamado "código de histonas".[11][12]A modificación de histonas intervén en diversos procesos bioloxicos como aregulación xénica,areparación do ADNe a condensación cromosómica (mitose) eespermatoxénese(meiose).[13]
A nomenclatura normal para indicar as modificacións nas histonas consta de varias parte, e é:
- Ponse primeiro o nome da histona (por exemplo, H3)
- Despois a abreviación dunha letra do nome doaminoácidoafectado (por exemplo, K paralisina) e a posición do aminoácido na proteína.
- Finalmente o tipo de modificación (Me:metil,P:fosfato,Ac:acetil,Ub:ubiquitín)
Así H3K4me1 significa monometilación do 4º residuo (unha lisina) empezando polo principio (extremoN-terminal) da proteína H3.
Exemplos de modificacións de histonas na regulación da transcrición son:
| Tipo de modificación |
Histona | ||||||
|---|---|---|---|---|---|---|---|
| H3K4 | H3K9 | H3K14 | H3K27 | H3K79 | H4K20 | H2BK5 | |
| mono-metilación | activación[14] | activación[15] | activación[15] | activación[15][16] | activación[15] | activación[15] | |
| di-metilación | represión[17] | represión[17] | activación[16] | ||||
| tri-metilación | activación[18] | represión[15] | represión[15] | activación,[16] represión[15] |
represión[17] | ||
| acetilación | activación[18] | activación[18] | |||||
Historia
[editar|editar a fonte]As histonas foron descubertas en 1884 porAlbrecht Kossel.O nomehistonadata de finais do século XIX e procede do alemánHiston,de orixe incerta: quizais vén do gregohistanaiou dehistos.Ata principios da década de 1990, as histonas eran consideradas por moitos investigadores como un material de recheo para o ADN nuclear eucariótico, baseándose en parte nos modelos da "bóla e pau" deMark Ptashnee outros que crían que a transcrición estaba activada por interaccións proteína-ADN eproteína-proteínasobre moldes de ADN basicamente espidos, como é o caso dasbacterias.Durante a década de 1980s, os traballos deMichael Grunstein[19]demostraron que as histonas eucarióticas reprimían a transcrición xénica, e que a función dos activadores transcricionais é superar esta represión. Sabemos agora que as histonas xogan un papel tanto positivo coma negativo na regulación daexpresión dos xenes,o que constitúe as bases docódigo de histonas.
O descubrimento dahistona H5parece datar da década de 1970,[20][21]e na clasificación foi agrupada coahistona H1.[2][4][5]
Conservación entre especies
[editar|editar a fonte]As histonas atopáronse no núcleo dascélulas eucariotase en certasArchaea,concretamente aseuriarqueas,pero non enbacterias.As histonas das arqueas poden ser parecidas aos precursores das histonas eucarióticas. As histonas están entre as proteínas coa secuencia máis conservada entre os eucariotas, o que indica o seu importante papel na bioloxía do núcleo.[2]Polo contrario, as células espermáticas maduras usan en gran medidaprotaminaspara empaquetar o seu ADN xenómico (en vez de histonas), moi probablemente porque isto lles permite acadar un grao de empaquetamento aínda maior.[22]
As histonas do octámero (core) están tan conservadas, que presentan moi poucas diferenzas entre as súas secuencias de aminoácidos en diferentes especies. As histonas de unión (linker) xeralmente presentan máis dunha forma dentro dunha especie e están menos conservadas ca as outras.[23]
Hai algunhas formasvariantesnalgunhas das principais clases. Estas variante compartenhomoloxíana secuencia de aminoácidos e semellanza estrutural na parte central con algunha clase específica das histonas principais, pero tamén teñen as súas propias características que as distinguen das histonas principais. Estashistonas secundariasnormalmente levan a cabo funcións específicas no metabolismo da cromatina. Por exemplo, a histonaCenpA(similar á H3) é unha histona que está asociada exclusivamente coa rexión docentrómerodo cromosoma. A variante H2A.Z da histona H2 está asociada cos promotores dos xenes que están en activa transcrición e tamén está implicada na prevención da propagación daheterocromatinasilenciosa. Outra variante da H2, a H2A.X únese ao ADN que ten roturas na dobre cadea e marca a zona do ADN que está sometida a reparación. A histona H3.3 está asociada con xenes transcritos activamente.[24]
Notas
[editar|editar a fonte]- ↑Youngson, Robert M. (2006).Collins Dictionary of Human Biology.Glasgow: HarperCollins.ISBN0-00-722134-7.
- ↑2,02,12,22,3Cox, Michael; Nelson, David R.; Lehninger, Albert L (2005).Lehninger Principles of Biochemistry.San Francisco: W.H. Freeman.ISBN0-7167-4339-6.
- ↑Redon C, Pilch D, Rogakou E, Sedelnikova O, Newrock K, Bonner W (2002). "Histone H2A variants H2AX and H2AZ".Curr. Opin. Genet. Dev.12(2): 162–9.PMID11893489.doi:10.1016/S0959-437X(02)00282-4.
- ↑4,04,1Bhasin M, Reinherz EL, Reche PA (2006). "Recognition and classification of histones using support vector machine".J. Comput. Biol.13(1): 102–12.PMID16472024.doi:10.1089/cmb.2006.13.102.
- ↑5,05,1Hartl, Daniel L., Freifelder, David Snyder, Leon A. (1988). Jones and Bartlett Publishers - Boston, ed.Basic Genetics.ISBN0-86720-090-1.
- ↑6,06,1Luger K, Mäder AW, Richmond RK, Sargent DF, Richmond TJ (1997). "Crystal structure of the nucleosome core particle at 2.8 A resolution".Nature389(6648): 251–60.PMID9305837.doi:10.1038/38444.PDB1AOI
- ↑Farkas, Daniel (1996).DNA simplified: the hitchhiker's guide to DNA.Washington, D.C: AACC Press.ISBN0-915274-84-1.
- ↑Alva V, Ammelburg M, Lupas AN (2007)."On the origin of the histone fold".BMC Struct Biol7.PMID17391511.doi:10.1186/1472-6807-7-17.
- ↑Ward R, Bowman A, El-Mkami H, Owen-Hughes T, Norman DG (2009). "Long distance PELDOR measurements on the histone core particle".J. Am. Chem. Soc.131(4): 1348–9.PMID19138067.doi:10.1021/ja807918f.
- ↑Strahl, Brian D.; Allis, C. David (2000-01)."The language of covalent histone modifications".Nature(eninglés)403(6765): 41–45.ISSN0028-0836.doi:10.1038/47412.
- ↑Strahl BD, Allis CD (Jan 2000). "The language of covalent histone modifications".Nature403(6765): 41–5.PMID10638745.doi:10.1038/47412.
- ↑Jenuwein T, Allis CD (Aug 2001). "Translating the histone code".Science293(5532): 1074–80.PMID11498575.doi:10.1126/science.1063127.
- ↑Ning Song, Jie Liu, Shucai An, Tomoya Nishino, Yoshitaka Hishikawa and Takehiko Koji (2011). "Immunohistochemical Analysis of Histone H3 Modifications in Germ Cells during Mouse Spermatogenesis". Acta Histochemica et Cytochemica 44 (4): 183–90. doi:10.1267/ahc.11027. PMC 3168764.PMID 21927517.
- ↑Benevolenskaya EV (2007)."Histone H3K4 demethylases are essential in development and differentiation".Biochem. Cell Biol.85(4): 435–43.PMID17713579.doi:10.1139/o07-057.
- ↑15,015,115,215,315,415,515,615,7Barski A, Cuddapah S, Cui K, Roh TY, Schones DE, Wang Z, Wei G, Chepelev I, Zhao K (2007). "High-resolution profiling of histone methylations in the human genome".Cell129(4): 823–37.PMID17512414.doi:10.1016/j.cell.2007.05.009.
- ↑16,016,116,2Steger DJ, Lefterova MI, Ying L, Stonestrom AJ, Schupp M, Zhuo D, Vakoc AL, Kim JE, Chen J, Lazar MA, Blobel GA, Vakoc CR (2008)."DOT1L/KMT4 recruitment and H3K79 methylation are ubiquitously coupled with gene transcription in mammalian cells".Mol. Cell. Biol.28(8): 2825–39.PMC2293113.PMID18285465.doi:10.1128/MCB.02076-07.
- ↑17,017,117,2Rosenfeld JA, Wang Z, Schones DE, Zhao K, DeSalle R, Zhang MQ (2009)."Determination of enriched histone modifications in non-genic portions of the human genome".BMC Genomics10:143.PMC2667539.PMID19335899.doi:10.1186/1471-2164-10-143.
- ↑18,018,118,2Koch CM, Andrews RM, Flicek P, Dillon SC, Karaöz U, Clelland GK, Wilcox S, Beare DM, Fowler JC, Couttet P, James KD, Lefebvre GC, Bruce AW, Dovey OM, Ellis PD, Dhami P, Langford CF, Weng Z, Birney E, Carter NP, Vetrie D, Dunham I (2007)."The landscape of histone modifications across 1% of the human genome in five human cell lines".Genome Res.17(6): 691–707.PMC1891331.PMID17567990.doi:10.1101/gr.5704207.
- ↑Kayne PS, Kim UJ, Han M, Mullen JR, Yoshizaki F, Grunstein M. Extremely conserved histone H4 N terminus is dispensable for growth but essential for repressing the silent mating loci in yeast. Cell. 1988 Oct 7;55(1):27-39.PMID 3048701
- ↑Crane-Robinson C, Dancy SE, Bradbury EM, Garel A, Kovacs AM, Champagne M, Daune M (1976). "Structural studies of chicken erythrocyte histone H5".Eur. J. Biochem.67(2): 379–88.PMID964248.doi:10.1111/j.1432-1033.1976.tb10702.x.
- ↑Aviles FJ, Chapman GE, Kneale GG, Crane-Robinson C, Bradbury EM (1978). "The conformation of histone H5. Isolation and characterisation of the globular segment".Eur. J. Biochem.(2 ed.)88:363–71.PMID689022.doi:10.1111/j.1432-1033.1978.tb12457.x.
- ↑Clarke HJ (1992). "Nuclear and chromatin composition of mammalian gametes and early embryos".Biochem. Cell Biol.70(10-11): 856–66.PMID1297351.doi:10.1139/o92-134.
- ↑Mónica Sancho, Erika Diani, Miguel Beato, Albert Jordan. Depletion of Human Histone H1 Variants Uncovers Specific Roles in Gene Expression and Cell Growth. PLOS Genetics.[1]Cita: Histone H1 in vertebrates is a family of closely related, single-gene encoded proteins, showing much less evolutionary conservation than core histones.
- ↑Ahmad K, Henikoff S (2002). "The histone variant H3.3 marks active chromatin by replication-independent nucleosome assembly".Mol. Cell9(6): 1191–200.PMID12086617.doi:10.1016/S1097-2765(02)00542-7.
Véxase tamén
[editar|editar a fonte]Outros artigos
[editar|editar a fonte]Ligazóns externas
[editar|editar a fonte]- Animación sobre cromatina, histonas e catepsina
- NextbioArquivado02 de marzo de 2009 enWayback Machine.
