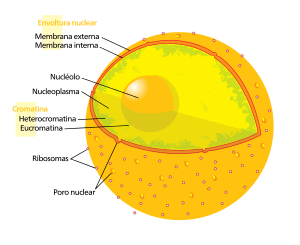
Núcleo celular

(1)Membrana nuclear(2)Ribosomas(3) Complexo doporo nuclear(4)Nucléolo(5)Cromatina(6) Núcleo (7)Retículo endoplasmático(8)Nucleoplasma
Toda a estrutura está rodeada polo citoplasma.
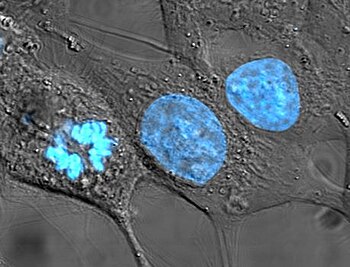
Enbioloxía celular,onúcleo(dolatínnucleusounuculeus) é unha parte das células que se atopa en todas ascélulas eucariotase contén a maioría do materialxenético.O núcleo, en xeral, controla as actividades da célula, e ten dúas funcións primarias: controla as reaccións químicas celulares, na súa maioríacitoplasmáticas,e garda ainformaciónque se precisa para adivisión celular.[1]
Á parte de conter o xenoma da célula, o núcleo contén certas proteínas que regulan a expresión dos xenes. Aexpresión xenéticaao nivel nuclear envolve complexos procesos detranscrición,oprocesamentodopre-ARNme a exportación do mesmo cara ao citoplasma.[1]
O núcleo ten un tamaño medio de 6micrómetrosnos mamíferos[2];os máis grandes son as de células vexetais, que poden chegar a 25 micrómetros ou máis. Está rodeado por unha dobre membrana chamadamembrana nuclear.A membrana exterior e a interior fúndense nuns determinados intervalos, formandoporos nucleares.Amembrana nuclearregula e facilita o transporte entre o núcleo e o citoplasma, e tamén separa as reaccións químicas producidas no citoplasma das do núcleo.[3]A membrana exterior está asociada coretículo endoplasmáticoe ás veces pode conterribosomas.O espazo entre as dúas membranas é continuo co espazo interno do retículo endoplasmático. A cara nuclear da membrana está rodeada duns filamentos que forman alámina nuclear.[4]O interior do núcleo está cheo dun líquido que constitúe onucleoplasma.Dentro do núcleo encóntrase onucléolo,onde se fabrican as subunidades ribosómicas. Atópanse tamén outras formacións menores chamadas corpos subnucleares, que son diversas agrupacións de ARN e proteínas.[5]
Historia
[editar|editar a fonte]

O núcleo foi o primeiroorgánuloen ser descuberto. Probablemente, o debuxo máis antigo que se conserva deste orgánulo remóntase a un dos primeiros microscopistas,Antoni van Leeuwenhoek(1632-1723). Este investigador observou un oco ou"lume",o núcleo, eneritrocitosdesalmón.[6]A diferenza dos eritrocitos demamífero,os do resto devertebradosson nucleados. O núcleo tamén foi descrito en1804porFranz Bauer,e posteriormente con máis detalle polobotánicoescocésRobert Brownnunha charla ditada perante aSociedade linneana de Londresen1831.[7]Brown estaba estudando a estrutura microscópica dasorquídeascando observou unha área opaca, que chamou aréola ou núcleo, nas células da capa externa daflor,aínda que non suxeriu unha función potencial para tal estrutura.[8]En 1838Matthias Schleidenpropuxo que o núcleo desempeñaba un papel na xeración de células, denominándoo "citoblasto" (construtor de células). Pensaba que observara células novas arredor destes "citoblastos".Franz Meyenfoi un forte opositor desta opinión, xa que describira previamente células que se multiplicaban por división e cría que moitas células carecerían de núcleo. A idea de que as células se podían xerarde novo,ben polo "citoblasto" ou ben doutro modo, contradicía os traballos deRobert Remak(1852) eRudolf Virchow(1855), os cales propagaron decisivamente o novoparadigmade que as células só se xeraban por outras células ( "Omnis cellula ex cellula" ). A función do núcleo permanecía sen aclarar.[9]
Entre 1876 e 1878Oscar Hertwigpublicou varios estudos sobre afecundaciónde ovos deourizo de mar,mostrando que o núcleo doespermatozoideentraba nooocitofusionándose co seu núcleo. Esta foi a primeira vez que se suxeriu que un individuo se desenvolvía a partir dunha soa célula nucleada. Isto estaba en contradición coa teoría deErnst Haeckel,que enunciaba que se repetía a filoxenia completa dunha especie durante odesenvolvemento embrionario,incluíndo a xeración da primeira célula nucleada a partir dunha "monerula", unha masa desestruturada democoprimordial ( "Urschleim", enalemán). Polo tanto, a necesidade do núcleo espermático para a fecundación estivo en discusión por un tempo. Porén, Hertwig confirmou a súa observación noutros grupos animais, como por exemplo enanfibiosemoluscos.Eduard Strasburgerobtivo os mesmos resultados enplantas(1884). Isto abriu o camiño para a asignación dun papel importante ao núcleo naherdanza xenética.En 1873August Weismannpostulou a equivalencia das células xerminais paternas e maternas na herdanza. A función do núcleo como portador de información xenética non se fixo evidente ata máis tarde, tras o descubrimento damitosee o redescubrimento dasleis de Mendela principios doséculo XX.Isto supuxo o desenvolvemento dateoría cromosómica da herdanza.[9]
Estruturas
[editar|editar a fonte]O núcleo é oorgánulode maior tamaño das células animais.[10]Nas células demamífero,o diámetro de media do núcleo é de aproximadamente 6micrómetros(μm), e ocupa aproximadamente o 10% do total do volume celular.[2]Nos vexetais, o núcleo xeralmente mide de 5 a 25 µm e é visible conmicroscopioóptico. Nosfungosobserváronse casos de especies con núcleos moi pequenos, de arrededor de 0,5 µm, os cales son visibles soamente con microscopio electrónico. NasoosferasdeCycase deconíferasacada un tamaño de 0,6mm,é dicir, é visible a simple vista.[11]
O líquido viscoso do seu interior denomínasenucleoplasma,e a súa composición é similar á que se encontra nocitosoldocitoplasma.[12]Ten o aspecto xeral dun orgánulo denso e esférico.
Envoltura e poros nucleares
[editar|editar a fonte]- Artigos principais:Envoltura nuclearePoro nuclear.
Aenvoltura nuclear,tamén coñecida como membrana nuclear, componse de dúas membranas, unha interna e outra externa, dispostas en paralelo unha sobre a outra cunha separación de 10 a 50nanómetros(nm). A envoltura nuclear rodea completamente o núcleo e separa o material xenético celular do citoplasma circundante, servindo como barreira que evita que asmacromoléculasdifundan libremente entre o nucleoplasma e o citoplasma.[13]A membrana nuclear externa é continua coa membrana doretículo endoplásmicorugoso (RER), e está igualmente inzada deribosomas.O espazo entre as membranas coñécese como espazo perinuclear e é continuo coa luz do RER.
Osporos nucleares,que forman canais acuosos que atravesan a envoltura, están compostos por múltiplesproteínasque colectivamente se coñecen comonucleoporinas.Os poros teñen un peso molecular de 125 millóns dedaltonse compóñense de 50 (enlévedos) a 100proteínas(envertebrados) aproximadamente.[10]Os poros teñen un diámetro total de 100 nm; non obstante, o oco polo que difunden libremente as moléculas é de 9 nm de largo debido á presenza de sistemas de regulación no centro do poro. Este tamaño permite o libre paso de pequenas moléculas hidrosolubles mentres que evita que moléculas de maior tamaño entren ou saian de maneira inadecuada, comoácidos nucleicose proteínas grandes. Estas moléculas grandes deben ser transportadas ao núcleo de forma activa. O núcleo típico dunha célula de mamífero dispón de entre 3000 e 4000 poros ao longo da súa envoltura,[14]cada un dos cales contén unha estrutura en anel con simetría octal na posición na que as membranas interna e externa se fusionan.[15]Ancorada ao anel encóntrase a estrutura denominadacesta nuclear,que se estende cara ao nucleoplasma, e unha serie de extensións filamentosas que se proxectan no citoplasma. Ambas as estruturas median a unión a proteínas de transporte nucleares.[10]
A maioría das proteínas, subunidades do ribosoma e algúns ARN transpórtanse a través dos complexos de poro nun proceso mediado por unha familia de factores de transporte coñecidos comocarioferinas.Entre estas se encontran asimportinas,que interveñen no transporte en dirección ao núcleo, e as que realizan o transporte en sentido contrario, que se coñecen comoexportinas.A maioría das carioferinas interactúan directamente coa súa carga, aínda que algunhas utilizan proteínas adaptadoras.[16]Ashormonasesteroides como ocortisole aaldosterona,xunto con outras moléculas pequenas hidrosolubles implicadas nasinalización celularpoden difundir a través da membrana celular e no citoplasma, onde se unen a proteínas que actúan comoreceptores nuclearese son levadas ao núcleo. Serven comofactores de transcricióncando se unen ao seuligando.En ausencia de ligando moitos destes receptores funcionan como unhahistona desacetilaseque reprime aexpresión xénica.[10]
Lámina nuclear
[editar|editar a fonte]- Artigo principal:Lámina nuclear.
Nas células animais existen dúas redes defilamentos intermediosque dan soporte mecánico ao núcleo: alámina nuclearforma unha trama organizada na cara interna da envoltura, mentres que na cara externa este soporte está menos organizado. Ambas as redes de filamentos intermedios tamén serven de lugar de ancoraxe para os cromosomas e os poros nucleares.[2]
A lámina nuclear está composta por proteínas que se denominanproteínas laminaresoulaminas.Como todas as proteínas, estas son sintetizadas no citoplasma e máis tarde transpórtanse ao interior do núcleo, onde se ensamblan antes de incorporarse á rede preexistente.[4][17]As proteínas laminas tamén se encontran no interior do nucleoplasma, onde forman outra estrutura regular coñecida comoveo nucleoplásmico,[18]que é visible usandomicroscopio de fluorescencia.A función do veo non se coñece, pero está excluído da zona donucléoloe está presente na interfase.[19]As estruturas de proteínas laminas que forman o veo únense ácromatina,e por medio da quebra da súa estrutura inhiben a transcrición dexenesque codifican proteínas.[20]
Como acontece cos compoñentes doutrosfilamentos intermedios,osmonómerosde proteínas laminas conteñen un dominio enhélice alfautilizado por dous monómeros para enroscarse un co outro, formando undímerocun motivo enhélice superenrolada.Dúas desas estruturas diméricas únense posteriormente lado con lado dispostas de xeitoantiparalelopara formar untetrámerodenominadoprotofilamento.Oito deses protofilamentos dispóñense lateralmente para formar unfilamento.Eses filamentos pódense ensamblar ou desensamblar de modo dinámico, o que significa que os cambios na lonxitude do filamento dependen do balance entre as taxas de adición e desensamblaxe.[2]
Asmutaciónsnos xenes das proteínas laminas orixinan defectos na ensamblaxe dos filamentos coñecidas comolaminopatías.Destas, a máis destacable é a familia de enfermidades coñecidas comoproxerias,que dan aos doentes a aparencia de teren unenvellecementoprematuro. Descoñécese o mecanismo exacto polo que os cambios bioquímicos asociados dan lugar aofenotipoavellentado.[21]
Cromosomas
[editar|editar a fonte]- Artigo principal:Cromosoma.
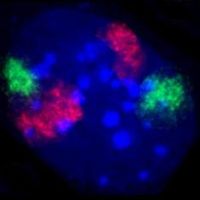
O núcleo celular contén a maior parte do material xenético celular en forma de múltiples moléculas lineais deADNcoñecidas comocromatina,e durante a división celular esta aparece na forma ben definida que se coñece comocromosoma.Unha pequena fracción dos xenes sitúase noutros orgánulos, como asmitocondriasou oscloroplastosdas células vexetais.
Existen dous tipos de cromatina: aeucromatinaé a forma de ADN menos compacta, e contén xenes que son expresados frecuentemente pola célula.[22]O outro tipo, coñecido comoheterocromatina,é a forma máis compacta, e contén ADN que se transcribe de forma infrecuente. Esta estrutura clasifícase á súa vez en heterocromatinafacultativa,que consiste en xenes que están organizados como heterocromatina só en certos tipos celulares ou en certos estadios do desenvolvemento, e heterocromatinaconstitutiva,que consiste en compoñentes estruturais do cromosoma como ostelómerose oscentrómeros.[23]Durante a interfase a cromatina organízase en territorios individuais discretos, osterritorios cromosómicos.[24][25]Os xenes activos, que se encontran xeralmente na rexión eucromática do cromosoma, tenden a localizarse nas fronteiras dos territorios cromosómicos.[26]
Determinadosanticorpospara certos tipos de organización cromatínica, en particular osnucleosomas,foron asociados con variasenfermidades autoinmunescomo olupus eritematoso sistémico.[27]Estes anticorpos son coñecidos comoanticorpos antinucleares(ANA) e tamén se observaron en casos deesclerose múltipleno contexto dunha disfunción inmune xeneralizada.[28]Como o caso antes mencionado da proxeria, o papel que desempeñan os anticorpos na indución dos síntomas da enfermidade autoinmune non foi aínda aclarado.
Nucléolo
[editar|editar a fonte]- Artigo principal:Nucléolo.

Onucléoloé unha estrutura discreta que se tingue densamente e se encontra no núcleo. Non está rodeado por unha membrana, polo que en ocasións se di que é unsuborgánulo.Fórmase arredor de repeticións en tándem deADNr,que é o ADN que codifica oARN ribosómico(ARNr). Estas rexións chámanseorganizadores nucleolares.O principal papel do nucléolo é sintetizar o ARNr e ensamblar os ribosomas. A cohesión estrutural do nucléolo depende da súa actividade, dado que a ensamblaxe ribosómica no nucléolo orixina unha asociación transitoria dos compoñentes nucleolares, facilitando a posterior ensamblaxe doutros ribosomas. Este modelo está apoiado pola observación de que a inactivación do ADNr dá como resultado a mestura das estruturas nucleolares.[29]
O primeiro paso da ensamblaxe ribosómica é atranscricióndo ADNr polaARN polimerase I,formando un longo pre-ARNr precursor. Este é escindido nas subunidades deARNr 5,8S,18S,e28S.[30]A transcrición,procesamentopostranscricional e ensamblaxe do ARNr ten lugar no nucléolo, axudado por moléculas deARN nucleolar pequeno,algunhas das cales se derivan deintrónsdeARN mensaxeirosque sufrironsplicing(empalme) relacionados coa función ribosomal. Estas subunidades ribosómicas ensambladas son as estruturas máis grandes que pasan a través dos poros nucleares.[10]
Cando se observa comicroscopio electrónico,pode verse que o nucléolo se compón de tres rexións distinguibles: os centros fibrilares, rodeados polo compoñente fibrilar denso, que á súa vez está beireado polo compoñente granular. A transcrición do ADNr ten lugar tanto nos centros fibrilares coma na zona de transición entre os centros fibrilares e o compoñente fibrilar denso, e iso explica que cando a transcrición do ADNr aumenta, se observan máis centros fibrilares. A maior parte da escisión e modificación dos ARNr ten lugar no compoñente fibrilar denso, mentres que os últimos pasos que implican a ensamblaxe de proteínas nas subunidades ribosómicas teñen lugar no compoñente granular.[30]
Outros corpos subnucleares
[editar|editar a fonte]| Nome da estrutura | Diámetro da estrutura |
|---|---|
| Corpos de Cajal | 0,2–2,0 µm[31] |
| PIKA | 5 µm[32] |
| Corpos PML | 0,2–1,0 µm[5] |
| Paraspeckles | 0,2–1,0 µm[33] |
| Speckles | 20–25 nm[32] |
Ademais do nucléolo, o núcleo contén unha certa cantidade de corpos non delimitados por membranas. Entre estes están oscorpos de Cajal,os chamados Xémini dos corpos enrolados, a denominada Asociación Cariosómica Interfásica Polimórfica (PIKA), os Corpos da Leucemia Promielocítica (corpos PML), os "paraspeckles"e os" speckles de splicing ". Aínda que se sabe pouco sobre o número destes dominios subnucleares, son significativos porque mostran que o nucleoplasma non é unha mestura uniforme, senón que máis ben contén subdominios funcionais organizados.[5]
Outras estruturas subnucleares aparecen como parte de procesos patolóxicos. Por exemplo, viuse a presenza de pequenas formacións intranucleares con aspecto de bastón nalgúns casos demiopatía nemalínica.Esta doenza prodúcese tipicamente por mutacións noxenedaactina,e os propios bastóns están constituídos pola actina producida a partir de tales xenes mutantes, xunto con outras proteínas docitoesqueleto.[34]
Corpos de Cajal e GEMs
[editar|editar a fonte]O núcleo típico posúe de 1 a 10 estruturas compactas denominadascorpos de Cajalou corpos enrolados (CB, porCoiled Bodyen inglés), cuxo diámetro mide entre 0,2 µm e 2,0 µm dependendo do tipo celular e especie.[31]Cando se ollan comicroscopio electrónico,asemellan nobelos de fíos enguedellados,[32]e son focos densos de distribución da proteínacoilina.[35]Os corpos de Cajal están implicados en varios tipos distintos de funcións relacionadas coprocesamento do ARN,especificamente na maduración doARN nucleolar pequeno(snoRNA) e oARN nuclear pequeno(snRNA), e modificación doARNmdehistonas.[31]
Semellantes aos corpos de Cajal son os Xémini de corpos enrolados ou GEMs (do inglésGemini of Coiled Bodies), cuxo nome se deriva da constelación deXéminipola súa relación case como de xemelgos cos corpos de Cajal. Os GEMs son similares en forma e tamaño a estes últimos, e de feito son virtualmente indistinguibles aomicroscopio.[35]A diferenza dos corpos de Cajal, non conteñensnRNP(ribonucleoproteínas pequenas nucleares dosespliceosomas), pero conteñen unha proteína que se denominasupervivencia de motoneurona(SMN, en ingléssurvival of motor neuron), cuxa función se relaciona coa bioxénese das snRNP. Crese que os GEMs axudan aos corpos de Cajal na bioxénese dassnRNP,[36]aínda que tamén se suxeriu a partir de evidencias de microscopía que os corpos de Cajal e os GEMs son diferentes manifestacións da mesma estrutura.[35]
Dominios PIKA e PTF
[editar|editar a fonte]Os dominios PIKA, ou Asociacións Cariosómicas de Interfase Polimórficas, foron descritos por primeira vez en estudos de microscopía en 1991. A súa función era e permanece pouco clara, aínda que non se pensa que estean asociados coa replicación activa de ADN, transcrición ou procesamento de ARN.[37]Viuse que frecuentemente se asocian con dominios discretos definidos por localizacións densas dofactor de transcriciónPTF, que promove a transcrición doARN nuclear pequeno.[38]
Corpos PML
[editar|editar a fonte]Oscorpos PMLou daproteína da leucemia promielocítica(PML, polo inglésPromyelocytic leukaemia) son corpos esféricos que se atopan espallados polo nucleoplasma, e que miden arredor de 0,2–1,0 µm. Coñécense por outros nomes, como dominio «nuclear 10» (ND10), «corpos de Kremer» e «dominiosoncoxénicosPML». A miúdo poden verse no núcleo asociados cos corpos de Cajal. Tense suxerido que desempeñan un papel na regulación da transcrición.[5]
Paraspeckles
[editar|editar a fonte]Descubertos en 2002, osparaspecklesson compartimentos de forma irregular do espazo intercromatínico do núcleo.[39]Foron documentados por primeira vez encélulas HeLa(cancerosas), onde polo xeral se encontran de 10 a 30 por núcleo,[40]e sábese que osparaspecklestamén existen en todas as células primarias humanas, liñas de células transformadas e en seccións de tecidos.[41]O seu nome deriva da súa distribución no núcleo e consta do prefixo para (paralelo) e despeckles,facendo referencia a que se encontran na proximidade dossplicing specklesou "manchas desplicing".[40]
Osparaspecklesson estruturas dinámicas que se alteran en resposta a cambios na actividade celular metabólica. Son dependentes da transcrición,[39]e en ausencia de transcrición daARN pol II,osparaspecklesdesaparecen, e todas as proteínas asociadas que o compoñen (PSP1, p54nrb, PSP2, CFI(m)68 e PSF) forman un casquete perinucleolar en forma de cuarto crecente no nucléolo. Este fenómeno maniféstase durante ociclo celular,no cal osparaspecklesestán presentes eninterfasee durante toda a mitose, agás entelofase.Durante a telofase, cando se forman os dous núcleos fillos, non hai transcrición por parte daARN polimerase II,de modo que os compoñentes proteicos forman o mencionado casquete perinucleolar.[41]
Specklesdesplicing
[editar|editar a fonte]Osspeckles('manchas') son estruturas subnucleares que están enriquecidas en factores para osplicingdopre-ARNme están localizados nas rexións intercromatínicas do nucleoplasma de células de mamíferos. Con microscopio de fluorescencia aparecen como estruturas punteadas irregulares, que varían en forma e tamaño, e con microscopio electrónico vense como agrupacións de gránulos de intercromatina. Osspecklesson estruturas dinámicas, e tanto as súas proteínas coma os seus compoñentes ARN-proteína poden circular continuamente entre osspecklese outras localizacións nucleares, incluíndo sitios activos de transcrición. Os estudos da composición, estrutura e comportamento dosspecklesproporcionaron un modelo para comprender a compartimentalización funcional do núcleo e a organización da maquinaria deexpresión xénica.[42]
En ocasións denominadosagrupacións de gránulos intercromatínicosoucompartimentos de factores de splicing,osspecklesson ricos ensnRNP(ribonucleoproteínas nucleares pequenas) dosplicinge outras proteínas dosplicingque se necesitan no procesamento do pre-ARNm.[42]Debido aos requirimentos variables da célula, a composición e localización destes corpos cambia de acordo coa transcrición de ARNm e a regulación porfosforilaciónde proteínas específicas.[43]
Funcións
[editar|editar a fonte]A principal función do núcleo celular é controlar a expresión xenética e mediar na replicación do ADN durante ociclo celular.O núcleo proporciona un lugar para atranscrición,permitindo niveis de regulación que non están dispoñibles enprocariotas.
Compartimentalización celular
[editar|editar a fonte]A envoltura nuclear permite ao núcleo controlar o seu contido e separalo do resto do citoplasma cando sexa necesario. Isto é importante para controlar procesos en calquera dos lados da membrana nuclear. Nalgúns casos, cando se precisa restrinxir un proceso citoplasmático, un participante chave retírase ao núcleo, onde interacciona con factores de transcrición para reprimir a produción de certos encimas da vía metabólica. Este mecanismo regulador ten lugar no caso daglicólise,unha ruta celular na que se utiliza aglicosapara producir enerxía. Ahexoquinaseé o encima responsable do primeiro paso da glicólise, producindoglicosa-6-fosfatoa partir da glicosa. A altas concentracións defrutosa-6-fosfato,unha molécula que se forma posteriormente a partir da glicosa-6-fosfato, unha proteína reguladora retira a hexoquinase ao núcleo,[44]onde forma un complexo con outras proteínas nucleares que reprime a transcrición dos xenes implicados na glicólise.[45]
Para controlar que xenes se deben transcribir, a célula impide o acceso físico dalgúnsfactores de transcriciónresponsables de regular a expresión xénica ata que son activados por outras vías de sinalización. Isto impide que se dean mesmo pequenos niveis de expresión xénica desaxeitada. Por exemplo, no caso dos xenes controlados porNF-κB,que están implicados na maior parte das respostasinflamatorias,a transcrición indúcese en resposta a unha fervenza de sinalización celular como a que se inicia coa molécula sinalizadoraTNF-αuníndose a un receptor da membrana celular, o que produce o recrutamento de proteínas sinalizadoras e finalmente a activación do factor de transcrición NF-κB. Unsinal de localización nuclearque posúe a proteína NF-κB permítelle ser transportada a través doporo nuclearao núcleo, onde estimula atranscricióndos xenes diana.[2]
A compartimentalización permite á célula impedir a tradución de ARNm inmaturo.[46]OARNmconténintrónsque se deben retirar antes de ser traducidos para producir proteínas funcionais. Amaduración(modificación dos extremos esplicing) do ARNm efectúase no interior do núcleo antes de que o ARNm poida acceder aos ribosomas para a súa tradución. Sen o núcleo, os ribosomas traducirían ARNm ao ser transcrito sen procesar, o que produciría proteínas cunpregamentoincorrecto e deformadas.
Expresión xénica
[editar|editar a fonte]
Aexpresión xénicaimplica en primeiro lugar atranscrición,na que o ADN se utiliza como molde para producir ARN. No caso dos xenes que codifican proteínas, o ARN xerado por este proceso éARN mensaxeiro(ARNm), que posteriormente precisa sertraducidopolosribosomaspara formar unha proteína. Posto que os ribosomas se localizan fóra do núcleo, o ARNm sintetizado debe ser exportado.[47]
Dado que o núcleo é o lugar onde se produce a transcrición, está dotado dun conxunto de proteínas que, ou ben están implicadas directamente neste proceso, ou na súa regulación. Entre estas encontramos ashelicases,que desenrolan a molécula de ADN de dobre cadea para facilitar o acceso da maquinaria de síntese, aARN polimerase,que sintetiza o ARN a partir do molde de ADN, atopoisomerase,que varía o grao desuperenrolamentodo ADN, así como unha ampla variedade defactores de transcriciónque regulan a expresión xénica.[48]
Procesamento do pre-ARNm
[editar|editar a fonte]As moléculas de ARNm recentemente sintetizadas coñécense como transcritos primarios oupre-ARNm.Posteriormente débense someter amodificación postranscricionalno núcleo antes de ser exportados ao citoplasma. O ARNm que aparece no núcleo sen estas modificacións acaba degradado en vez de utilizarse para a tradución nos ribosomas. As tres modificacións principais son: A doextremo 5'(ou5' caping),apoliadenilacióndoextremo 3'e o empalme (splicing) do ARN. Mentres permanece no núcleo, o pre-ARNm asóciase con varias proteínas en complexos coñecidos comoribonucleoproteínas heteroxéneas nuclearesou hnRNPs. A adición das modificacións do extremo 5' ten lugar no momento da transcrición e é o primeiro paso nasmodificacións postranscricionais.A cola de poliadenina 3' só se engade unha vez que a transcrición está completa.
O procesamento por corte e empalme (splicing) do ARN, levado a cabo por un complexo denominadoespliceosomaé o proceso polo que osintrónsson eliminados do pre-ARNm, permanecendo unicamente osexónsconectados entre si para formar unha soa molécula continua. Este proceso normalmente finaliza tras os dous anteriores, mais pode comezar antes de que a síntese estea completa en transcritos con moitos exóns.[10]Moitos pre-ARNm, incluíndo os que codificananticorpos,pódense cortar e empalmar de múltiples formas para producir diferentes ARNm maduros, que codifican diferentes secuencias de proteínas. Este proceso coñécese comosplicingalternativo,e permite a produción dunha gran variedade de proteínas a partir dunha cantidade limitada de ADN.
Dinámica e regulación
[editar|editar a fonte]Transporte nuclear
[editar|editar a fonte]
A entrada e saída de grandes moléculas do núcleo está estritamente controlada polos complexos deporos nucleares.Aínda que as pequenas moléculas poden entrar no núcleo sen regulación,[49]as macromoléculas como o ARN e as proteínas requiren asociarse acarioferinaschamadasimportinaspara entraren no núcleo, e aexportinaspara saíren. As proteínas cargadas que deben ser translocadas desde o citoplasma ao núcleo conteñen curtas secuencias de aminoácidos coñecidas comosinais de localización nuclearque están unidas ás importinas, mentres que as transportadas desde o núcleo ao citoplasma posúensinais de exportación nuclearunidas ás exportinas. A capacidade das importinas e as exportinas para transportar a súa carga está regulada porGTPases,encimas que hidrolizanGTPliberando enerxía. A GTPase chave no transporte nuclear é a proteínaRan,que pode unir ou ben GTP ou benGDP(guanosín difosfato), dependendo de se está localizada no núcleo ou no citoplasma. Mientres que as importinas dependen deRan-GTPpara disociarse da súa carga, as exportinas necesitan Ran-GTP para unirse á súa carga.[16]
A importación nuclear depende de que a importina se una á súa carga no citoplasma e a trasporte a través doporo nuclearao núcleo. Dentro do núcleo, a Ran-GTP actúa separando a carga da importina, permitindo a esta saír do núcleo e ser empregada de novo. A exportación nuclear é similar, xa que a exportina se une á carga dentro do núcleo nun proceso facilitado por RanGTP, e sae a través do poro nuclear, separándose da súa carga no citoplasma.
As proteínas especializadas de exportación serven para a translocación deARNmmaduro eARNtao citoplasma despois de que a modificación postranscripcional se completa. Este mecanismo de control de calidade é importante debido ao papel central desas moléculas na tradución de proteínas. A expresión inadecuada dunha proteína debido a unha escisión de exóns incompleta ou á incorporación impropia de aminoácidos podería ter consecuencias negativas para a célula. Por iso, o ARN non modificado por completo que acada o citoplasma é degradado en vez de ser utilizado na tradución.[10]
Ensamblaxe e desensamblaxe
[editar|editar a fonte]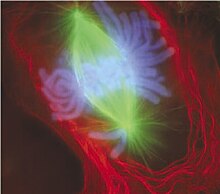
Durante o seu período de vida un núcleo pode desensamblarse, o que se pode producir no decurso dadivisión celular,ou ben como consecuencia daapoptose,unha forma regulada de morte celular. Durante estes acontecementos, os compoñentes estruturais do núcleo (aenvolturae alámina) son sistematicamente degradados.
Durante ociclo celulara célula divídese para formar dúas células. Para que este proceso sexa posible, cada unha das novas células fillas debe adquirir un xogo completo de xenes, un proceso que require a replicación doscromosomas,e a súa segregación en xogos separados. Isto prodúcese cando os cromosomas xa replicados, ascromátidesfillas, se unen aosmicrotúbulos,os cales á súa vez se unen a diferentescentrosomas.As cromátides fillas poden ser fraccionadas cara a localizacións separadas na célula. Non obstante, en moitas células o centrosoma localízase no citoplasma, fóra do núcleo, polo que os microtúbulos non poderían unirse ás cromátides en presenza da envoltura nuclear.[50]Polo tanto, nos estadios iniciais do ciclo celular, comezando naprofasee ata case aprometafase,desmantélase a membrana nuclear.[18]De forma semellante, durante o mesmo período desensámblase a lámina nuclear, un proceso que está regulado pola fosforilación das proteínaslaminas.[51]Cara ao final do ciclo celular refórmase a membrana nuclear, e aproximadamente ao mesmo tempo, alámina nuclearreensámblasedesfosforilandoasproteínas laminares.[51]
Aapoptoseé un proceso controlado no que os compoñentes estruturais da célula son destruídos, o que produce a morte da célula. Os cambios asociados coa apoptose afectan directamente ao núcleo e aos seus contidos, por exemplo na condensación da cromatina e a desintegración da envoltura nuclear e a lámina nuclear. A destrución das redes da lámina nuclear está controlada porproteasesapoptóticas especializadas denominadascaspases,que desintegran alámina nucleare dese modo degradan a integridade estrutural do núcleo. A desintegración da lámina nuclear utilízase en ocasións nos laboratorios como indicador da actividade da caspase enensaiosde actividade apoptótica temperá.[18]As células que expresan láminas resistentes ás caspases son deficientes nos cambios nucleares relacionados coa apoptose, o que suxire que as láminas desempeñan un papel importante no inicio dos eventos que levan á degradación apoptótica do núcleo.[18]A inhibición da propia ensamblaxe da lámina nuclear é de seu un indutor da apoptose.[52]
A envoltura nuclear actúa como unha barreira que evita que virus de ADN ou ARN penetren no núcleo. Algúns virus precisan acceder a proteínas dentro do núcleo para se replicar ou ensamblar. Os virus de ADN, como osherpesvirusreplícanse e ensámblanse no núcleo celular, e saen a través da membrana nuclear interna. Este proceso vai acompañado da desensamblaxe da lámina nuclear na cara nuclear da membrana interna.[18]
Células anucleadas e polinucleadas
[editar|editar a fonte]
Aínda que a maior parte das células teñen un único núcleo, algúns tipos celulares carecen del, mentres que outros posúen múltiples núcleos. Isto pode ser un proceso normal, como é no caso da maduración doseritrocitos,ou ben o resultado dunha división celular defectuosa.
As células anucleadas carecen de núcleo, e polo mesmo son incapaces de dividirse para producir células fillas. O caso mellor coñecido de célula anucleada é o eritrocito de mamífero, que tamén carece doutrosorgánuloscomomitocondrias,e serven en principio como vehículos de transporte deosíxenodesde ospulmónsaos tecidos. Os eritrocitos maduran grazas áeritropoesenamedula ósea,onde perden o seu núcleo, orgánulos e ribosomas. O núcleo é expulsado durante o proceso dediferenciacióndeeritroblastoareticulocito,o cal é o precursor inmediato do eritrocito maduro.[53]Os axentesmutáxenospoden inducir a liberación dalgúns eritrocitos inmaturos "micronucleados" á circulación sanguínea.[54][55]Tamén poden aparecer células anucleadas a partir dunha división celular defectuosa na que unha célula filla carece de núcleo, mentres que a outra posúe dous.
As células polinucleadas conteñen múltiples núcleos. A maior parte dosprotozoosda claseAcantharea,[56]e algúnsfungosque formanmicorrizas,[57]teñen células polinucleadas de forma natural. Outros exemplos serían osparasitosintestinais do xéneroGiardia,que posúen dous núcleos en cada célula.[58]Nos seres humanos, omúsculo esqueléticoposúe células, chamadasmiocitos,que se converten en polinucleadas durante o seu desenvolvemento. A disposición resultante dos núcleos na rexión periférica da célula permite un espazo intracelular máximo para asmiofibrilas[10].As células multinucleadas tamén poden ser anormais en humanos. Por exemplo, as que xorden da fusión demonocitosemacrófagos,coñecidas como células multinucleadas xigantes, poden ser observadas en ocasións acompañando áinflamación,[59]e tamén están implicadas na formación detumores.[60]
Evolución
[editar|editar a fonte]- Artigo principal:Eucarioxénese.
Ao ser a mellor característica que define a célula eucariota, a orixe evolutiva do núcleo foi obxecto de moita especulación. Entre as teorías propostas, pódense considerar catro como as principais, aínda que ningunha delas encontrou un amplo apoio.[61]
A teoría coñecida como "modelo sintrófico" propón que unha relaciónsimbióticaentrearqueasebacteriascreou a primeira célula eucariota nucleada (vereucarioxénese). Suponse que a simbiose tivo lugar cando unha arquea antiga similar aos actuaismetanóxenosfoi invadida e parasitada por bacterias similares ás actuaismixobacterias,formando finalmente o núcleo primitivo. Esta teoría é análoga á teoría aceptada da orixe dasmitocondriasecloroplastoseucariotas, dos que se pensa que se orixinaron por unha relación endosimbionte similar entre protoeucariotas e bacterias aerobias.[62]A orixe arqueana do núcleo está apoiada pola circunstancia de que tanto arqueas coma eucariotas teñen xenes similares en certas proteínas, incluíndo ashistonas.Ao observarmos que as mixobacterias son móbiles, poden formar complexos multicelulares e posúenproteínas Gsimilares ás de eucariotas, tamén podemos aceptar unha orixe bacteriana da célula eucariota.[63]
Un segundo modelo propón que as células protoeucariotas evolucionaron a partir de bacterias sen que se dera un estadio simbionte. Este modelo baséase na existencia dunha bacteria moderna pertencente ao filoPlanctomycetesque posúen unha estrutura nuclear con poros primitivos e outras estruturas compartimentalizadas por membrana.[64]Unha proposta similar establece que unha célula similar á eucariota, ocronocito,apareceu en primeiro lugar, e posteriormentefagocitouarqueas e bacterias para dar lugar ao núcleo e á célula eucariota.[65]
O modelo máis controvertido, coñecido comoeucarioxénese viralafirma que moitas características da célula eucariota, como a presenza dun núcleo que se continúa coa membrana, xurdiron pola infección dun devanceiro procariota por un virus. Isto está suxerido baseándose en similitudes entre eucariotas e virus como as cadeas lineais de ADN, o procesamento "caping" do extremo 5' do ARNm e a forte unión a proteínas do ADN (facendo ás histonas análogas daenvoltura vírica). Unha versión desta proposta suxire que o núcleo evolucionou concertadamente coa fagocitose para dar lugar a undepredadorcelular primitivo.[66]Outra variante propón que os eucariotas se orixinaron de arqueas primitivas infectadas porpoxvirus,baseándose na semellanza das modernasADN polimerasesentre estes e os eucariotas.[67][68]Tense suxerido tamén que a cuestión non resolta da evolución da sexualidade puido estar relacionada coa hipótese da eucarioxénese viral.[69]
Finalmente, unha proposta moi recente suxire que as variantes tradicionais da teoríaendosimbionteson insuficientes para explicar a orixe do núcleo eucariota. Este modelo, denominado ahipótese da exomembrana,propón que o núcleo se orixinou en vez de por endosimbiose a partir dunha célula primitiva orixinal que desenvolveu unha segunda membrana celular exterior. A membrana interior que encerraba a célula orixinal converteuse entón na membrana nuclear evolucionando para desenvolver estruturas de poro cada vez máis elaboradas para o paso de compoñentes celulares sintetizados internamente, como as subunidades ribosómicas.[70]
Notas
[editar|editar a fonte]- ↑1,01,1Tripathi, Vidisha; Prasanth, Kannanganattu V (2011). "Cell Nucleus".eLS(eninglés)(Chichester: John Wiley & Sons Ltd).doi:10.1002/9780470015902.a0001337.pub2.
- ↑2,02,12,22,32,4Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, Peter Walter, ed. (2002).Molecular Biology of the Cell, Capítulo 4(4ª ed.). Garland Science. pp. 191–234.
- ↑"Cell Nucleus and Nuclear Envelope".HyperPhysics Concepts(eninglés).Georgia State University.Consultado o 10 de xullo de 2015.
- ↑4,04,1Goldman A, Moir R, Montag-Lowy M, Stewart M, Goldman R (1992). "Pathway of incorporation of microinjected lamin A into the nuclear envelope".J Cell Biol119(4): 725–735.PMID1429833.doi:10.1083/jcb.119.4.725.
- ↑5,05,15,25,3Dundr, Miroslav; Misteli, Tom (2001). "Functional architecture in the cell nucleus".Biochem. J.(356): 297–310.PMID11368755.doi:10.1146/annurev.cellbio.20.010403.103738.
- ↑Leeuwenhoek, A. van:Opera Omnia, seu Arcana Naturae ope exactissimorum Microscopiorum detecta, experimentis variis comprobata, Epistolis ad varios illustres viros.J. Arnold et Delphis, A. Beman, Lugdinum Batavorum 1719–1730. Citado por: Dieter Gerlach, Geschichte der Mikroskopie. Verlag Harry Deutsch, Frankfurt am Main, Germany, 2009.ISBN 978-3-8171-1781-9.
- ↑Harris, H. (1999).The Birth of the Cell.New Haven: Yale University Press.
- ↑Brown, Robert (1866). "On the Organs and Mode of Fecundation of Orchidex and Asclepiadea".Miscellaneous Botanical WorksI:511–514.
- ↑9,09,1Cremer, Thomas (1985).Von der Zellenlehre zur Chromosomentheorie.Berlin, Heidelberg, New York, Tokyo: Springer Verlag.ISBN3-540-13987-7.Online Versionhere
- ↑10,010,110,210,310,410,510,610,7Lodish, H; Berk, A; Matsudaira, P; Kaiser, CA; et al. (2004). WH Freeman, ed.Molecular Cell Biology(5th ed.). New York.
- ↑González, A.M.Núcleo celularArquivado02 de xullo de 2011 enWayback Machine.. Morfología de Plantas Vasculares. Facultad de Ciencias Agrarias, Universidad Nacional del Nordeste. Consultado o30 de outubro de 2009.
- ↑Clegg JS (1984)."Properties and metabolism of the aqueous cytoplasm and its boundaries".Am. J. Physiol.246(2 Pt 2): R133–51.PMID6364846.
- ↑Paine P, Moore L, Horowitz S (1975). "Nuclear envelope permeability".Nature254(5496): 109–114.PMID1117994.doi:10.1038/254109a0.
- ↑Rodney Rhoades; Richard Pflanzer, eds. (1996). "Ch3".Human Physiology(3rd ed.). Saunders College Publishing.
- ↑Shulga N, Mosammaparast N, Wozniak R, Goldfarb D (2000). "Yeast nucleoporins involved in passive nuclear envelope permeability".J Cell Biol149(5): 1027–1038.PMID10831607.doi:10.1083/jcb.149.5.1027.
- ↑16,016,1Pemberton L, Paschal B (2005). "Mechanisms of receptor-mediated nuclear import and nuclear export".Traffic6(3): 187–198.PMID15702987.doi:10.1111/j.1600-0854.2005.00270.x.
- ↑Stuurman N, Heins S, Aebi U (1998). "Nuclear lamins: their structure, assembly, and interactions".J Struct Biol122(1–2): 42–66.PMID9724605.doi:10.1006/jsbi.1998.3987.
- ↑18,018,118,218,318,4(Goldman et al. 2002)
- ↑Moir RD, Yoona M, Khuona S, Goldman RD. (2000). "Nuclear Lamins A and B1: Different Pathways of Assembly during Nuclear Envelope Formation in Living Cells".Journal of Cell Biology151(6): 1155–1168.PMID11121432.doi:10.1083/jcb.151.6.1155.
- ↑Spann TP, Goldman AE, Wang C, Huang S, Goldman RD. (2002). "Alteration of nuclear lamin organization inhibits RNA polymerase II–dependent transcription".Journal of Cell Biology156(4): 603–608.PMID11854306.doi:10.1083/jcb.200112047.
- ↑Mounkes LC, Stewart CL (2004). "Aging and nuclear organization: lamins and progeria".Current Opinion in Cell Biology16:322–327.PMID15145358.doi:10.1016/j.ceb.2004.03.009.
- ↑Ehrenhofer-Murray A (2004). "Chromatin dynamics at DNA replication, transcription and repair".Eur J Biochem271(12): 2335–2349.PMID15182349.doi:10.1111/j.1432-1033.2004.04162.x.
- ↑Grigoryev S, Bulynko Y, Popova E (2006). "The end adjusts the means: heterochromatin remodelling during terminal cell differentiation".Chromosome Res14(1): 53–69.PMID16506096.doi:10.1007/s10577-005-1021-6.
- ↑M. Schardin, T. Cremer, H. D. Hager, M. Lang (1985)."Specific staining of human chromosomes in Chinese hamster x man hybrid cell lines demonstrates interphase chromosome territories".Human Genetics(Springer Berlin / Heidelberg)71(4): 281–287.PMID2416668.doi:10.1007/BF00388452.Arquivado dendeo orixinalo 13 de setembro de 2019.Consultado o 07 de xuño de 2011.
- ↑(Lamond & Earnshaw 1998)
- ↑A. Kurz, S Lampel, JE Nickolenko, J Bradl, A Benner, RM Zirbel, T Cremer and P Lichter (1996)."Active and inactive genes localize preferentially in the periphery of chromosome territories".The Journal of Cell Biology(The Rockefeller University Press)135:1195–1205.PMID8947544.doi:10.1083/jcb.135.5.1195.Arquivado dendeo orixinalo 29 de setembro de 2007.Consultado o 07 de xuño de 2011.
- ↑NF Rothfield, BD Stollar (1967). "The Relation of Immunoglobulin Class, Pattern of Antinuclear Antibody, and Complement-Fixing Antibodies to DNA in Sera from Patients with Systemic Lupus Erythematosus".J Clin Invest46(11): 1785–1794.PMID4168731.
- ↑S Barned, AD Goodman, DH Mattson (1995). "Frequency of anti-nuclear antibodies in multiple sclerosis".Neurology45(2): 384–385.PMID7854544.
- ↑D. Hernandez-Verdun (2006). "Nucleolus: from structure to dynamic".Histochem. Cell. Biol125(125): 127–137.doi:10.1007/s00418-005-0046-4.
- ↑30,030,1Lamond, A.I.; Sleeman, Judith E. "Nuclear substructure and dynamics".Current Biology13(21): R825–828.PMID14588256.doi:10.1016/j.cub.2003.10.012.
- ↑31,031,131,2Cioce M, Lamond A. "Cajal bodies: a long history of discovery".Annu Rev Cell Dev Biol21:105–131.PMID16212489.doi:10.1146/annurev.cellbio.20.010403.103738.
- ↑32,032,132,2(Pollard & Earnshaw 2004)
- ↑Archa Fox. Entrevistador: R. Sundby. Paraspeckle Size. E-mail Correspondence. 7 de marzo de 2007
- ↑Goebel, H.H.; Warlow, I. (1997). "Nemaline myopathy with intranuclear rods—intranuclear rod myopathy".Neuromuscular Disorders7(1): 13–19.PMID9132135.doi:10.1016/S0960-8966(96)00404-X.
- ↑35,035,135,2Matera AG, Frey MA. (1998). "Coiled Bodies and Gems: Janus or Gemini?".American Journal of Human Genetics63(2): 317–321.PMID9683623.doi:10.1086/301992.
- ↑A. Gregory Matera (1998). "Of Coiled Bodies, Gems, and Salmon".Journal of Cellular Biochemistry(70): 181–192.PMID9671224.doi:10.1086/301992.
- ↑Saunders WS, Cooke CA, Earnshaw WC (1991). "Compartmentalization within the nucleus: discovery of a novel subnuclear region.".Journal of Cellular Biology115(4): 919–931.doi:10.1083/jcb.115.4.919.PMID 1955462
- ↑Pombo A, Cuello P, Schul W, Yoon J, Roeder R, Cook P, Murphy S (1998). "Regional and temporal specialization in the nucleus: a transcriptionally active nuclear domain rich in PTF, Oct1 and PIKA antigens associates with specific chromosomes early in the cell cycle".EMBO J17(6): 1768–1778.PMID9501098.doi:10.1093/emboj/17.6.1768.
- ↑39,039,1Fox, Archa; et al. (2002)."Paraspeckles:A Novel Nuclear Domain"(PDF).Current Biology12:13–25.doi:10.1016/S0960-9822(01)00632-7.
- ↑40,040,1Fox, Archa; Bickmore, Wendy (2004)."Nuclear Compartments: Paraspeckles".Nuclear Protein Database. Arquivado dendeo orixinalo 02 de maio de 2006.Consultado o 6 de marzo de 2007.
- ↑41,041,1Fox, A.; et al. (2005)."P54nrb Forms a Heterodimer with PSP1 That Localizes to Paraspeckles in an RNA-dependent Manner".Molecular Biology of the Cell16:5304–5315.PMID16148043.doi:10.1091/mbc.E05-06-0587.PMID 16148043
- ↑42,042,1(Lamond & Spector 2003)
- ↑Handwerger, K.E.; Gall, Joseph G. (2006). "Subnuclear organelles: new insights into form and function".TRENDS in Cell Biology16(1): 19–26.PMID16325406.doi:10.1016/j.tcb.2005.11.005.
- ↑Lehninger, Albert L.; Nelson, David L.; Cox., Michael M. (2000).Lehninger principles of biochemistry(3rd ed.). New York: Worth Publishers.ISBN1-57259-931-6.
- ↑Moreno F, Ahuatzi D, Riera A, Palomino CA, Herrero P. (2005). "Glucose sensing through the Hxk2-dependent signalling pathway.".Biochem Soc Trans33(1): 265–268.PMID15667322.doi:10.1042/BST0330265.
- ↑Görlich, Dirk; Kutay, Ulrike (1999). "Transport between the cell nucleus and the cytoplasm".Ann. Rev. Cell Dev. Biol.(15): 607–660.PMID10611974.doi:10.1042/BST0330265.
- ↑Nierhaus, Knud H.; Wilson, Daniel N. (2004).Protein Synthesis and Ribosome Structure: Translating the Genome.Wiley-VCH.ISBN3527306382.
- ↑Nicolini, Claudio A. (1997).Genome Structure and Function: From Chromosomes Characterization to Genes Technology.Springer.ISBN0792345657.
- ↑Watson JD, Baker TA, Bell SP, Gann A, Levine M, Losick R. (2004). "Ch9–10".Molecular Biology of the Gene(5th ed.). Peason Benjamin Cummings; CSHL Press.
- ↑Jennifer Lippincott-Schwartz (7 de marzo de 2002). "Cell biology: Ripping up the nuclear envelope".Nature416(6876): 31–32.PMID11882878.doi:10.1038/416031a.
- ↑51,051,1Boulikas T (1995). "Phosphorylation of transcription factors and control of the cell cycle".Crit Rev Eukaryot Gene Expr5(1): 1–77.PMID7549180.
- ↑Steen R, Collas P (2001). "Mistargeting of B-type lamins at the end of mitosis: implications on cell survival and regulation of lamins A/C expression".J Cell Biol153(3): 621–626.PMID11331311.doi:10.1083/jcb.153.3.621.
- ↑Skutelsky, E.; Danon, D. (1970). "Comparative study of nuclear expulsion from the late erythroblast and cytokinesis".J Cell Biol(60(3)): 625–635.PMID5422968.doi:10.1083/jcb.153.3.621.
- ↑D.K. Torous, =Dertinger SD, Hall NE, Tometsko CR. (2000). "Enumeration of micronucleated reticulocytes in rat peripheral blood: a flow cytometric study".Mutat Res(465(1–2)): 91–99.PMID10708974.doi:10.1083/jcb.153.3.621.
- ↑Hutter, K.J.; Stohr, M. (1982). "Rapid detection of mutagen induced micronucleated erythrocytes by flow cytometry".Histochemistry(75(3)): 353–362.PMID7141888.doi:10.1083/jcb.153.3.621.
- ↑L.A. Zettler, Sogin ML, Caron DA (1997). "Phylogenetic relationships between the Acantharea and the Polycystinea: A molecular perspective on Haeckel's Radiolaria".Proc Natl Acad Sci USA(94): 11411–11416.PMID9326623.doi:10.1083/jcb.153.3.621.
- ↑T.R. Horton (2006). "The number of nuclei in basidiospores of 63 species of ectomycorrhizal Homobasidiomycetes".Mycologia(98(2)): 233–238.PMID16894968.doi:10.1083/jcb.153.3.621.
- ↑Adam RD (1991)."The biology of Giardia spp".Microbiol. Rev.55(4): 706–32.PMC372844.PMID1779932.
- ↑A. McInnes, Rennick DM (1988). "Interleukin 4 induces cultured monocytes/macrophages to form giant multinucleated cells".J Exp Med(167): 598–611.PMID3258008.doi:10.1083/jcb.153.3.621.
- ↑S.R. Goldring, Roelke MS, Petrison KK, Bhan AK (1987). "Human giant cell tumors of bone identification and characterization of cell types".J Clin Invest(79(2)): 483–491.PMID3027126.doi:10.1083/jcb.153.3.621.
- ↑Pennisi E. (2004). "Evolutionary biology. The birth of the nucleus".Science305(5685): 766–768.PMID15297641.doi:10.1126/science.305.5685.766.
- ↑Margulis, Lynn (1981).Symbiosis in Cell Evolution.San Francisco: W. H. Freeman and Company. pp.206–227.ISBN0-7167-1256-3.
- ↑Lopez-Garcia P, Moreira D. (2006). "Selective forces for the origin of the eukaryotic nucleus".Bioessays28(5): 525–533.PMID16615090.doi:10.1002/bies.20413.
- ↑Fuerst JA. (2005). "Intracellular compartmentation in planctomycetes".Annu Rev Microbiol.59:299–328.PMID15910279.doi:10.1146/annurev.micro.59.030804.121258.
- ↑Hartman H, Fedorov A. (2002). "The origin of the eukaryotic cell: a genomic investigation".Proc Natl Acad Sci U S A.99(3): 1420–1425.PMID11805300.doi:10.1073/pnas.032658599.
- ↑Bell PJ. (2001). "Viral eukaryogenesis: was the ancestor of the nucleus a complex DNA virus?"J Mol BiolSep;53(3):251–256.PMID 11523012
- ↑Takemura M. (2001). Poxviruses and the origin of the eukaryotic nucleus.J Mol Evol52(5):419–425.PMID 11443345
- ↑Villarreal L, DeFilippis V (2000). "A hypothesis for DNA viruses as the origin of eukaryotic replication proteins".J Virol74(15): 7079–7084.PMID10888648.doi:10.1128/JVI.74.15.7079-7084.2000.
- ↑Bell PJ (7 de novembro de 2006). "Sex and the eukaryotic cell cycle is consistent with a viral ancestry for the eukaryotic nucleus".J Theor Biol243(1): 54–63.PMID16846615.
- ↑de Roos AD (2006). "The origin of the eukaryotic cell based on conservation of existing interfaces".Artif Life12(4): 513–523.PMID16953783.doi:10.1162/artl.2006.12.4.513.
Véxase tamén
[editar|editar a fonte]| Wikimedia Commonsten máis contidos multimedia na categoría: Núcleo celular |

Bibliografía
[editar|editar a fonte]- Goldman, R; Gruenbaum, Y; Moir, R; Shumaker, D; Spann, T (2002)."Nuclear lamins: building blocks of nuclear architecture".Genes Dev16(5): 533–547.PMID11877373.doi:10.1101/gad.960502.
- Lamond, Angus I.; Earnshaw, WC (24 de abril de 1998). "Structure and Function in the Nucleus".Science(eninglés)280(5363): 547–553.PMID9554838.doi:10.1126/science.280.5363.547.
- Lamond, Angus I.; Spector, D.L. (2003). "Nuclear speckles: a model for nuclear organelles".Nat. Rev. Mol. Cell Biol.(eninglés)4(8): 605–12.PMID12923522.doi:10.1038/nrm1172.
- Pennisi E. (2004). "Evolutionary biology. The birth of the nucleus".Science(eninglés)305(5685): 766–768.PMID15297641.doi:10.1126/science.305.5685.766.
- Pollard, Thomas D.; Earnshaw, William C. (2004).Cell Biology(eninglés).Philadelphia: Saunders.ISBN0-7216-3360-9.
Outros artigos
[editar|editar a fonte]Ligazóns externas
[editar|editar a fonte]- "The Cell Nucleus".Molecular Expressions(eninglés).
- "The Nucleus".Kimball's Biology Pages(eninglés).Arquivado dendeo orixinalo 23 de xuño de 2015.Consultado o 10 de xullo de 2015.