Virus da rabia
- Para a enfermidade causada por este virus verrabia.
| Rabia | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
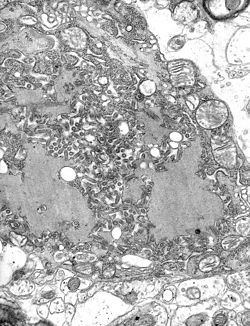 Micrografía electrónicadeviriónsdo virus da rabia (partículas con forma de bastón grises escuras) e corpos de Negri (as grandes inclusións celulares características da infección da rabia.) | |||||||||||
| Clasificación científica | |||||||||||
| |||||||||||
Ovirus da rabiaé unvirus neurotrópicodo xéneroLyssavirusque causa a enfermidade fatal darabiaen animais e humanos. A transmisión do virus da rabia adoita ocorrer a través da saliva de animais.
O virus da rabia ten unha morfoloxía cilíndrica e é aespecie tipodo xéneroLyssavirusda familiaRhabdoviridae.Estes virus teñenenvolturae unxenomadeARNmonocatenario de sentido negativo. A información xenética está empaquetada en forma dun complexoribonucleoproteicono cal o ARN está estreitamente unido ásnucleoproteínasvirais. O xenoma de ARN do virus codifica cinco xenes cuxo orde está moi conservado. Estes xenes codifican unha nucleoproteína (N),fosfoproteína(P), proteína da matriz (M), glicoproteína (G) e aARN polimerase(L).[1]A secuencia xenómica completa vai desde 11.615 a 11.966nucleótidosde lonxitude.[2]
Todos os eventos detranscricióne replicación teñen lugar no citoplasma dentro dunha "fábrica de virus" especializada chamadacorpo de Negri(chamada así en honor deAdelchi Negri[3]). Estes corpos teñen de 2 a 10µmde diámetro e son característicos (patognomónicos) da infección darabiae considéranse unha proba histolóxica definitiva desta infección.[4]
Estrutura
[editar|editar a fonte]O virus da rabia ten unha simetría helicoidal, o cal non é moi común entre os virus que afectan aos mamíferos. Un dos extremos do virus é arredondado ou cónico e o outro é plano ou cóncavo, o que lle dá unha característica forma de bala. Ten unha lonxitude duns 180nme un diámetro en sección duns 75 nm. A envolta lipoproteica ten espículas con forma de protuberancia compostas polaglicoproteínaG. As espículas non cobren o extremo plano dovirión(partícula vírica). Debaixo da envoltura está a membrana ou capa da proteína da matriz (M), que pode estarinvaxinadano extremo plano. O centro do virión está formado pola ribonucleoproteína disposta helicoidalmente.
Ciclo de replicación
[editar|editar a fonte]Despois da unión do virus ao seu receptor da superficie da célulahóspede,o virus entra na célula por medio da vía de transporteendosómica.Os valores baixos dopHinducen o proceso de fusión de membranas, que permite que o xenoma viral chegue aocitosol.Ambos os procesos, unión ao receptor e fusión de membranas, están catalizados pola glicoproteína G, que xoga un papel crítico na patoxénese (un virus mutante sen as proteínas G non pode propagarse).[1]
O seguinte paso despois da entrada é atranscrición xenéticado xenoma viral pola P-L polimerase (P é un cofactor esencial para a L polimerase) para fabricar as novas proteínas virais. A polimerase viral só pode recoñecer aribonucleoproteínae non pode utilizarse cun molde de ARN puro. A transcrición está regulada por unelemento cis reguladordo xenoma vírico e pola proteína M, que non só é esencial para a evaxinación do virus da célula senón que tamén regula a fracción da lonxitude doARNmpara a replicación. Posteriormente, cando está máis avanzada a infección, a actividade dapolimerasecambia á replicación para producir copias de ARN de sentido positivo e de lonxitude completa. Estes ARN complementarios utilízanse como moldes para facer novos xenomas do ARN vírico de sentido negativo. Estes son empaquetados xunto coa proteína N para formar ribonucleoproteínas, que despois poden formar novos virus.[4]
Infección
[editar|editar a fonte]En 1903Adelchi Negri,o médico italiano describiu por primeira vez oscorpos de Negri,que cría eran orixinados porprotozoos.En setembro de 1931, o Dr.Poupe Charles Jonesda illa caribeña deTrinidad,daquela nasIndias Occidentais,que era un bacteriólogo do goberno, encontrou oscorpos de Negrino cerebro dun morcego con comportamento infrecuente, e afirmou que un virus da rabia era esencial para explicar a lisofobia. En 1932, o Dr. Russ Pfister foi o primeiro que descubriu que os morcegosvampirosinfectados podían transmitir a rabia aos humanos e outros animais.[5][6]
Desde a ferida de entrada, o virus da rabia viaxa rapidamente ao longo das vías nerviosas dosistema nervioso periférico.Otransporte axonal retrógradodo virus da rabia ata osistema nervioso centralé un paso esencial para a patoxénese durante a infección natural. O mecanismo molecular exacto deste transporte non se coñece aínda que se sabe que se produce a unión da proteína P do virus da rabia á proteínaDYNL1da cadea lixeira dadineína.[7]A proteína P tamén actúa como antagonista dointerferón,polo que fai diminuír aresposta inmunitariado hóspede.
Desde o sistema nervioso central, o virus espállase a outros órganos. Asglándulas salivareslocalizadas na boca reciben grandes concentracións do virus, que deste xeito pode transmitirse por proxección da saliva sobre feridas e mucosas ou mordedelas do animal. Segundo os casos, pode producirse a morte desde dous días a cinco anos despois da infección inicial.[8]Porén, isto depende en grande medida da especie de animal que actúa como reservorio. A maioría dos mamíferos infectados morren en semanas, mentres que certas razas de especies como a mangosta africanaCynictis penicillatapoden sobrevivir asintomaticamente a unha infección durante anos.[9]
Antixenicidade
[editar|editar a fonte]Despois da entrrada do virus no corpo e tamén despois da vacinación contra este virus, o corpo produceanticorposneutralizadores do virus, que se unen e inactivan ao virus. Rexións específicas da proteína G son as máis antixénicas para orixinar a produción deanticorpos neutralizantesdo virus. Estes sitios antixénicos ouepitoposestán categorizados nas rexións I-IV e o sitio menor a. Traballos previos demostraran que os sitios antixénicos II e III son os máis comunmente usados para a unión dos anticorpos neutralizantes naturais.[10]Ademais, demostrouse que unanticorpo monoclonalcon funcionalidade neutralizante se une ao sitio I.[11]Outras proteínas, como a nucleoproteína, non poden orixinar a produción de anticorpos neutralizantes do virus.[12]Os epitopos aos que se unen os anticorpos neutralizantes son ambos os douslineareseconformacionais.[13]
Xenotipos
[editar|editar a fonte]Hai sete xenotipos de lisavirus da rabia. Os casos en Eurasia débense a tres deles (o xenotipo 1 ou rabia clásica, e en menor medida os xenotipos 5 e 6 ou lisavirus do morcego europeo tipos 1 e 2).[14]O xenotipo 1 evolucionou en Europa noséculo XVIIe espallouse por Asia, África e as Américas como resultado da exploración e colonización europea. O xenotipo 1, ou virus da rabia clásica, é prevalente na maior parte do mundo, pode ser transportado por calquera mamífero, e é a especie tipo do xénero.
Aplicación
[editar|editar a fonte]O virus da rabia utilízase en investigación para orastreo neuronal viralpara establecer as conexiónssinápticase a direccionalidade da transmisión sináptica.
Notas
[editar|editar a fonte]- ↑1,01,1Finke S, Conzelmann KK (2005). "Replication strategies of rabies virus".Virus Res.111(2): 120–131.PMID15885837.doi:10.1016/j.virusres.2005.04.004.
- ↑"Rabies complete genome".NCBINucleotide Database.Consultado o 29-May-2013.
- ↑WhoNamedIt - Negri bodies
- ↑4,04,1Albertini AA, Schoehn G, Weissenhorn W, Ruigrok RW (2008)."Structural aspects of rabies virus replication".Cell. Mol. Life Sci.65(2): 282–294.PMID17938861.doi:10.1007/s00018-007-7298-1.
- ↑Pawan J.L. (1936), pp. 137-156.
- ↑Pawan, J.L. (1936b). "Rabies in the Vampire Bat of Trinidad with Special Reference to the Clinical Course and the Latency of Infection."Annals of Tropical Medicine and Parisitology.Vol. 30, No. 4. December, 1936.
- ↑Raux H, Flamand A, Blondel D (2000)."Interaction of the rabies virus P protein with the LC8 dynein light chain".J. Virol.74(21): 10212–10216.PMC102061.PMID11024151.doi:10.1128/JVI.74.21.10212-10216.2000.
- ↑"Rabies".University of Northern British Columbia. Arquivado dendeo orixinalo 06 de setembro de 2008.Consultado o2008-10-10.
- ↑Taylor PJ (1993). "A systematic and population genetic approach to the rabies problem in the yellow mongoose (Cynictis penicillata)".Onderstepoort J. Vet. Res.60(4): 379–87.PMID7777324.
- ↑Benmansour A (1991)."Antigenicity of rabies virus glycoprotein".Journal of Virology65(8): 4198–4203.PMID1712859.
- ↑Marissen, WE.; Kramer, RA.; Rice, A.; Weldon, WC.; Niezgoda, M.; Faber, M.; Slootstra, JW.; Meloen, RH.; Clijsters-van der Horst, M. (2005)."Novel rabies virus-neutralizing epitope recognized by human monoclonal antibody: fine mapping and escape mutant analysis.".J Virol79(8): 4672–8.PMID15795253.doi:10.1128/JVI.79.8.4672-4678.2005.
- ↑Wiktor, TJ.; György, E.; Schlumberger, D.; Sokol, F.; Koprowski, H. (1973). "Antigenic properties of rabies virus components.".J Immunol110(1): 269–76.PMID4568184.
- ↑Bakker, AB.; Marissen, WE.; Kramer, RA.; Rice, AB.; Weldon, WC.; Niezgoda, M.; Hanlon, CA.; Thijsse, S.; Backus, HH. (2005)."Novel human monoclonal antibody combination effectively neutralizing natural rabies virus variants and individual in vitro escape mutants.".J Virol79(14): 9062–8.PMID15994800.doi:10.1128/JVI.79.14.9062-9068.2005.
- ↑McElhinney LM, Marston DA, Stankov S, Tu C, Black C, Johnson N, Jiang Y, Tordo N, Müller T, Fooks AR (2008) Molecular epidemiology of lyssaviruses in Eurasia. Dev Biol (Basel) 131:125-131
