ברזל
| קובלט-ברזל-מנגן | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| נתונים בסיסיים | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| מספר אטומי | 26 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| סמל כימי | Fe | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| סדרה כימית | מתכות מעבר | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| מראה | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| מתכת מבריקה בגווני אפרפר וכסף | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| תכונות אטומיות | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| משקל אטומי | 55.845u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| סידור אלקטרונים ברמות אנרגיה | 2, 8, 14, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| קונפיגורציה אלקטרונית |
[Ar] 3d⁶ 4s² | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| דרגות חמצון |
2, 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| תכונות פיזיקליות | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| צפיפות | 7,874 kg/m3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| מצב צבירהבטמפ' החדר | מוצק | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| נקודת רתיחה | 3,134.15K(2,861°C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| נקודת התכה | 1,811.15K(1,538°C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| לחץ אדים | 7.05Paב-1,808K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| מהירות הקול | 4,910 מטר לשנייה ב-293.15K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| מגנטיות |
פרומגנטיות | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| שונות | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| אלקטרושליליות | 1.83 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| קיבול חום סגולי | 440 J/(kg·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| מוליכות חשמלית | 9.93 106/m·Ω | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| מוליכות חום | 80.2 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| אנרגיית יינוןראשונה | 762.5 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| היסטוריה | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| תאריך גילוי |
האלף ה־5 לפנה״ס? | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ברזל(בלטינית:Ferrum) הואיסוד כימימתכתישסמלו הכימיFe ומספרו האטומי26.
ברזל הוא היסוד העיקרי בהרכבכדור הארץמבחינתמסה,והרביעי בהרכבקרום כדור הארץ.יש לו שימושים רבים בתרבות האנושית עוד מתקופותפרהיסטוריות.שיטות להפקת ברזל ועיבודו התפתחו בעיקר החל מהמאה ה-19והביאו לפיתוח התעשייההכבדה, בה הברזל הוא היסוד המופק בכמות הרבה ביותר. בתרבות המודרנית ברזל הוא מרכיב עיקרי בבנייהובייצורמכונות,כליםומוצרי צריכהרבים.
הברזל הוא החומר הפרומגנטיהראשון שזוהה, ותכונה זו קרויה על שמו. תכונה זו גורמת לברזל להימשך אל קוטבימגנטומאפשרת יצירת מגנטים מברזל.
בבעלי חיים,הברזל הואמינרל קורטהחיוני לבניית התרכובת האורגניתהם,אשר מאפשרת נשיאתחמצןעל ידיתאי דם אדומים.כמו כן הברזל משמש בשמירת החמצן בתוך רקמת תא בתוךמיוגלובין.
מחסור בברזל בתזונה יכול לגרום לאנמיהועייפות,[1]לפגיעה בחוש הטעם, וכן לפגיעה בבריאות המנטלית.[2]
בטבע
[עריכת קוד מקור|עריכה]הברזל מיוצר כחלק מתהליךנוקליאוסינתזה כוכבית–היתוך גרעיניבכוכביםבעלי מסה גבוהה, והוא היסוד היציב הכבד ביותר והאחרון המיוצר בתהליך זה. בליבה של כוכבים אלה נוצרות כמויות גדולות של ברזל, יחד עםניקלויסודות קלים יותר. כוכבים שעברו פיצוץסופרנובהפיזרו את הברזל שבליבתם ברחביהיקום,וזה מקורו של כל הברזל הקיים מחוץ לשמשות (בכוכבי לכת,אסטרואידיםוגופים קטנים יותר). ברזל הוא היסוד השישי הנפוץ ביותר ביקום.[3]
ברזל הוא היסוד המתכתי הנפוץ ביותר בכדור הארץ(כ-5% ממסת קרום כדור הארץ, כ-32% ממסת כדור הארץ הכוללת). בקרום כדור הארץ הוא נמצא כמעט תמיד בצורתתרכובותכמוהמטיט(Fe2O3),מגנטיט(Fe3O4) וטקוניט.ברזל במצב מתכתי נמצא על פני כדור הארץ בכמויות קטנות שמקורן במטאוריטים(בסגסוגת עםניקל). ההנחה המקובלת בגאופיזיקההיא כי ליבת כדור הארץ וכוכבי הלכת הדומים לו מורכבת מסגסוגת דומה.
ברזל מופיע בטבע בארבעהאיזוטופים:
- 54Fe (5.845%, אולירדיואקטיביעםמחצית חייםמעל 3.1×1022שנים)
- 56Fe (91.754%, יציב)
- 57Fe (2.119%, יציב)
- 58Fe (0.282%, יציב)
כמו כן ידועים 24 איזוטופים רדיואקטיביים, רובם בעלי זמן מחצית חיים קצר (חלקיקי שנייה עד שנים בודדות) ולכן אינם מצויים בטבע. רק לאיזוטופ60Fe זמן מחצית חיים ארוך יחסית, כ-2.6 מיליון שנה. איזוטופ זה נוצר בתהליך המתרחש רק במהלךסופרנובה,ומתפרק ל-60Ni, איזוטופ יציב של ניקל. קיומו של60Ni בשיעור גדול מהצפוי באסטרואידים מצביע על כך שההרכב הראשוני שלמערכת השמשכלל שיעור ניכר של60Fe, ומכך ניתן להסיק כי נוצרה מכוכבים קדומים יותר.
בתעשייה
[עריכת קוד מקור|עריכה]
הפקה
[עריכת קוד מקור|עריכה]ברזל ממוצה מעפרותיו (בעיקר המטיט ומגנטיט) כשהוא מחומם עם פחמן בכבשןלטמפרטורהשל 2,000מעלות צלזיוס.לכבשן מוכנס אוויר חם ברציפות ומתרחשת התגובה:
הפחמן החד-חמצנימגיב עם המטיט (או מקור ברזל אחר) כך:
בשנת2000הופקו כ-1,100 מיליון טון עפרות ברזל בשווי 25 מיליארדדולר.חמש המפיקות הגדולות ביותר של עפרות ברזל הןסין,ברזיל,אוסטרליה,רוסיהוהודו.
מוצרי תעשיית הברזל
[עריכת קוד מקור|עריכה]- ברזל גולמי(Pig Iron) מכיל בין 5%-4%פחמןוכמויות משתנות של זיהומים כגוןגופרית,צורןוזרחן.לברזל זה תכונות ביניים של מחצב ברזל, ברזל יציקה ופלדה.
- ברזל יציקה(יצקת) (Cast Iron) מכיל 3.5%-2% פחמן וכמויות קטנות שלמנגן.זיהומים כמו בברזל גולמי מסולקים ממנו על מנת למנוע פגיעה בתכונותיו. טמפרטורת ההיתוך שלו נעה בין 1,147–1,197מעלות צלזיוס.
- פלדה(Carbon Steel) שמכילה בין 0.5% ל-1.5% פחמן, עם כמויות קטנות של מנגן, גופרית, זרחן וצורן.
- ברזל חשיל(Wrought Iron) מכיל פחות מ-0.5% פחמן. סגסוגת זו רכה, ניתנת לריקוע ויוצרה במיוחד עבורנפחים.
סגסוגות ברזל מכילות לעיתים חומרים כמוכרום,ניקל,מוליבדן,ונדיוםטונגסטןועוד לקבלת תכונות רצויות.
שימושים
[עריכת קוד מקור|עריכה]ברזל הוא המתכת השימושית ביותר לאדם (95% מכלל המתכת שמופקת בעולם). המחיר הנמוך ורמת הקשיחות הגבוהה הופכים אותו לחומר מקובל מאוד בבנייתמכוניות,אוניות,בניינים וכדומה. שימושים נוספים של ברזל:
- מוטות ורשתות ברזל (פלדה) משולבים בתוך יציקותבטוןליצירתבטון מזוין,שלו עמידות גבוהה בפנימאמצים.בטון מזוין הוא חומר עיקרי בבניה של מבנים גדולים בכל העולם, ובישראלהוא משמש גם לבניית בתי מגורים. מחיר הברזל הוא מרכיב עיקרי בעלות הבניה של מבנים אלה.
- ברזל הוא מרכיב עיקרי בהתקנים חשמליים המשתמשים בשדות מגנטיים,כגוןמנועים,שנאים,גנרטוריםואלקטרומגנטים.
- צבעניםמבוססיתחמוצותברזל נפוצים מאוד בצבעים תעשייתיים, צבעי אמנות ואיפור מינרלי,ממקור סינתטי או טבעי. הצבעניםאינם רעילים ונוחים לשימוש, ועל כן נפוצים מאוד. לדוגמהאומברה שרופה,אושחור מאדים.
תכונות
[עריכת קוד מקור|עריכה]לברזלמבנה גבישיקובייתי ממורכז גוף או קובייתי ממורכז פאה. ברזל טהור שאינו מעורב בפחמן הוא חומר רך וקל לריקוע, אולם אפילו כמות קטנה של פחמן (אשר מעורב בברזל בתהליך הפקתו) גורמת עליה ניכרת בחוזקובקשיות.סגסוגת של ברזל ופחמן ביחסים שונים (הקרויותפלדה) מאפשרות קבלת שילובים שונים של חוזק, גמישות וקשיות.
ברזל בטמפרטורות נמוכות מ-770 מעלות צלזיוס הוא חומרפרומגנטי– הוא נמשך לקטבים של מגנט ויכול להתמגנט בעצמו. בנוכחותשדה מגנטיחיצוני, נוצר בתוך ברזל שדה מגנטי פנימי חזק יותר. תכונה זו שימושית לבנייתאלקטרומגנטיםושנאים,בהם השדה המגנטי מוכל ברובו בתוך ליבת ברזל המעוצבת בצורה הרצויה.
ברזל מגיב עםחמצן,בעיקר בנוכחותמים,בתהליךשיתוך(קורוזיה) היוצר תערובת של תרכובות ברזל המוכרת בשםחלודה.בניגוד למתכות אחרות שהתחמוצות שלהן יוצרות שכבת מגן (פסיבציה) העוצרת את תהליך השיתוך, חלודה היא רכה יותר ובעלת צפיפות נמוכה יותר מהברזל ממנו היא נוצרת. כתוצאה מכך החלודה נוטה לפרק את הברזל ולהתקלף ממנו, תוך חשיפת שכבה חדשה של ברזל לחמצן ולמים, כך שתהליך החלודה יכול להמשיך ואף להתגבר, עד להפיכת כל הברזל לתחמוצת. ניתן לעכב את התפשטות החלודה על ידי צביעה בצבע אטום למים, או ציפוי במתכת אחרת כגון אבץ (תהליך הקרויגלווןמאפשר יצירת שכבה אחידה של ציפוי). בסגסוגת של פלדה עםכרום(פלדת אל-חלדהמוכרת גם בשם המסחרינירוסטה) מתאפשרת פסיבציה המונעת החלדה של הברזל.
יוני ברזל
[עריכת קוד מקור|עריכה]קיימות ארבע צורות (מצביחמצון) שליוניברזל:
- Fe+2:מכונה כיוםברזל (II);באנגליתכונה בעברFerrous,ובעברית:קט-ברזל.
- Fe+3:מכונה כיוםברזל (III);באנגלית כונה בעברFerric,ובעברית:רב-ברזל.
- Fe+4:מכונה כיוםברזל (IV);באנגלית כונה בעברFerryl.צורה זו פחות שכיחה מהקודמות.
- Fe+6:מכונה כיוםברזל (VI);באנגלית כונה בעברFerrate.צורה זו נדירה מאוד.
על מנת להבין מדוע הצורות ברזל (II) ו-ברזל (III) הן הצורות היציבות יותר יש צורך להסתכל על קונפגורציית האלקטרונים באורביטלות היון. הברזל במצבו הנייטרלי הוא בעל 26 אלקטרונים הפרוסים על פני האורביטלות בקונפיגורציה של:.כאשר מייננים אטום, האלקטרונים נלקחים מהרמה הגבוהה ביותר.[4]במקרה זה מארוביטלת 4s. לכן קונפיגורציה בה אין בכלל רמה 4 היא יציבה יחסית. במצב של ברזל II בדיוק שני אלקטרונים נלקחים ומתירים את רמה 4 ריקה. במקרה של ברזל III האורביטלים לא רק שרמה 4 מבוטלת אלא גם יש בדיוק מילוי של חצי מאורביטלת d. דבר המקנה גם הוא יציבות יחסית.
הברזל נוטה ליצורקשרים יונייםעםאל-מתכותוקשרים מתכתייםעם מתכות ויכול ליצורקשר קוולנטיבצורתיון מורכב.
הברזל ביצורים חיים
[עריכת קוד מקור|עריכה]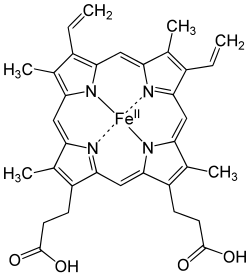
לברזל חשיבות עליונה בביולוגיה;הוא חומר חיוני לרוב היצורים החיים.הברזל נמצא בעיקר באתר הפעיל של כמהאנזימיםוחלבוניםחשובים כמרכיב בתרכובת האורגניתהם.
בבעלי חייםנמצא הברזל בהמוגלובין,החלבון נושא החמצןבכדוריות הדם האדומותאשר בדםובמיוגלוביןהנושא חמצן מהדם לשרירים.החמצן הנקלט בריאותנקשר באופן ישיר אלאטוםהברזל, ומועבר באמצעות הדם אל כלתאיהגוף.חוסר ברזל בגוף (עקב תזונה לקויה אומחלה) עלול לגרום לאנמיה.בכל היצורים האווירנייםמצוי הברזל במרכזו של החלבוןציטוכרום,חלבוןמרכזי בתהליך הנשימה התאית.לברזל חשיבות גם למחזור התא,להפיכה שלריבונוקלאוטידים(המרכיב את ה-RNA) לדאוקסיריבונוקלאוטיד (המרכיב את ה-DNA).[5]
בגוף האדםהבוגר יש בין ארבעה לחמישה גרם של ברזל. כ-65 אחוזים בהמוגלובין, 4–5 אחוזים במיוגלובין, כאחוז אחד במרכיבים שונים שלחמצון תוך-תאי,כעשירית האחוז מחובר לחלבוןטרנספריןוכ־15–30 אחוזים מאוכסנים בתאיכבדובמערכת הרטיקולואנדותלית.ברזל מאוחסן בתאים בפריטיןאו בהמוסידרין(Hemosiderin).
תזונה
[עריכת קוד מקור|עריכה]ברזל הוא מרכיב תזונה חשוב לגוף, כמות נמוכה מדי של ברזל גורמת לאנמיה– ירידה בכמות ההמוגלוביןבתאי הדם האדומים, כמו גם לירידה במספר תאי הדם האדומים. דבר זה מוביל לירידת כמות החמצןשמגיע לרקמות בגוף ולתפקוד פחות טוב של רקמות אלה. גם כמות גדולה מדי של ברזל עלולה להיות מסוכנת לבריאות.
בממוצע, הכמות היומית המומלצת לגבר בוגר היא 8.7 מיליגרם ולאישה בגיל הפוריות 14.8 מיליגרם. נשים בתקופת הפוריות צריכות כמות גדולה יותר של ברזל מגברים, משום שהן מאבדות דם בווסת.
הברזל מצוי במזונות צמחיים ובמזונות שמקורם בבעלי חיים.
במזונות מן הצומח מצוי הברזל בקטניות,כמושעועית,אפונה,פול,חמצה,עדשים;מוצריסויה(כמוטופו,חלב סויהועוד),אגוזים,טחינה,ברוקולי,אבוקדו,פירות יבשים;קינואה,דבשה,בורגולושמרי בירה;ומזון מדגנים מלאיםכמולחם מלא.
במזונות מן החי מצוי הברזל בבשר אדום,בדגים,ובבשר עוף.כבדהוא מקור עשיר לברזל.
קפהותהמכילים תרכובותפוליפנולשעלולות להקשות על ספיגת הברזל בגוף, לכן מומלץ למי שחושש ממחסור בברזל להימנע משתייתם בזמן הארוחה או עד חצי שעה לאחריה.ויטמין Cמסייע לגוף לספוג ברזל, ולכן אכילת ירקות כמוכרוב ניצנים,פטרוזיליה,ברוקולי,פלפלאוכרוב הקלחבזמן הארוחהאו אכילת פירות כמותפוז,תות שדהאופפאיהלקינוחעשויות לסייע לספיגת הברזל בגוף.
מחסור בברזל
[עריכת קוד מקור|עריכה] ערך מורחב –אנמיה מחוסר ברזל
ערך מורחב –אנמיה מחוסר ברזל
מחסור בברזל יכול לגרום לתופעות כגוןנשירת שיער,שבירת ציפורניים,עייפות,דיכאון,חרדהועוד.
מעת לעת במסגרת מעקב רפואי יישלח מטופל לביצועבדיקות דם,ובנוסף לרמות ההמוגלובין, ייבדקו גם רמות ה-iron (ברזל זמין),פריטיןוטראנספרין(Transferrin, מאגרי הברזל ויכולת ניודו).
תורמי דם נמצאים בסיכון מיוחד של רמות ברזל נמוכות בדם. לכן מתבצעת בדיקתהמוגלוביןלמבקשים לתרום דם. רמת ההמוגלובין צריכה להיות לפחות 12 גרם לדציליטר לאישה, ו-13 גרם לדציליטר לגבר. אם הרמה נמוכה יותר, לא לוקחיםתרומת דםמאותו אדם.
עודף ברזל
[עריכת קוד מקור|עריכה]קליטת ברזל בגוף מווסתת בדרך כלל בזמן העיכול.לגוף אין תהליך לפליטת ברזל ולכן הדרך לוויסות כמות הברזל בגוף היא בקרה על קליטתו.
עודף ברזל בגוף יכול לגרום למחלות כמוהמוכרומטוזיסשבה כמות רבה של ברזל נאגרת באיברים. תופעה זו עלולה להתרחש אצל אנשים שבקרת קליטת הברזל שלהם אינה תקינה, בדרך כלל כתוצאה מפגם גנטי תורשתי. מעריכים ששכיחות התופעה היא כ-0.3% עד 0.5% מהאוכלוסייה אצל אנשים לבנים. לכן עדיף להימנע מנטילת תוספי מזון המכילים ברזל ללא המלצת רופא.
היסטוריה
[עריכת קוד מקור|עריכה]תקופת הברזלהחלה לפני כשלושת אלפיםשנה,כשהאדםגילה את הברזל ותכונותיו. הוא השתמש בברזל לייצור כלים שונים (כמו חוד שלחנית) ומאוחר יותר למד להפיקפלדה,שהיאסגסוגתשל ברזל ופחמן(אחוז הפחמן 0.02%–2.06%) ולפעמים עם מתכות שונות נוספות, כגוןכרוםאוניקל.

בהודוהשתמשו בברזל כבר בשנת 2500 לפנה "ס. סדרת הפסליםהמפורסמת "אשוקה פילאר" לידדלהיעשויה מברזל נקי למדי (98%) שלא החליד או נשחק עד היום. בין השנים 3000–2000 לפנה "ס, גדלו מספר החפצים העשויים ברזל (המקור ככל הנראה בברזל ממטאור) במסופוטמיה,השימושים היו טקסיים וברזל היה מתכת יקרה מאוד, אפילו יותר מזהב.באיליאדה,מתואר שכלי נשק היו עשויים מארד,אבל השתמשו במטילי ברזל בסחר. מספר מקורות מציעים שברזל היה מופק באותו זמן כתוצר נלווה לזיקוקנחושת.
בין השנים 1600–1200 לפנה "ס, גבר השימוש בברזל במזרח התיכוןאבל הוא לא החליף את הארד. בין המאה ה-12 לפנה "ס למאה ה-10 לפנה" ס הייתה מגמה להחליף כלי ארד לכלי ברזל במזרח התיכון. באותו זמן התגלתה טכניקת הפחמון(או קרבוניזציה, שבה מעלים את אחוז הפחמן במתכת) שבעזרתה אנשי המזרח התיכון ייצרו ברזל חזק בהרבה ופחות שביר.
בתרבות
[עריכת קוד מקור|עריכה]הברזל משמשסמללכוח עקב שימושו הרב ככלי נשקובתעשייההכבדה.
טריאתלון איש הברזלהוא תחרותספורטהדורשתכושר גופניגבוה מאוד ונחשבת לתובענית במיוחד.
איירון מן( "איש הברזל" באנגלית) הוא דמות שלגיבור-עלשהואממציא,מהנדסותעשייןעשיר החמוש בחליפת שריון טכנולוגית מתקדמת.
בישראלידועהמערכת ההגנה האוויריתכיפת ברזל.מספרעוצבותשריוןמכילות "ברזל" או "פלדה" בשמן, הידועה שבהן היאעוצבת עקבות הברזל(חטיבה 401) שהייתה הראשונה להצטייד בטנקמרכבה סימן 4.
ראו גם
[עריכת קוד מקור|עריכה]קישורים חיצוניים
[עריכת קוד מקור|עריכה]- ברזל,באתראנציקלופדיה בריטניקה(באנגלית)
- אמיר רובין,על חשיבות הברזל בפעילות גופנית,באתראיירון סיינס,27 ביוני 2020
- ברזלב-Webelements(באנגלית)
- ברזלבספרייה הווירטואלית של מט "ח(בעברית)
- שי שמש,ברזל מכוכב אחר,באתרמדע גדול, בקטנה,18 בדצמבר 2017
 ברזל,דף שער בספרייה הלאומית
ברזל,דף שער בספרייה הלאומית
הערות שוליים
[עריכת קוד מקור|עריכה]- ^Iron-Deficiency Anemia
- ^Association between psychiatric disorders and iron deficiency anemia among children and adolescents: a nationwide population-based study,ncbi
- ^I. McDonald, G. C. Sloan, A. A. Zijlstra, N. Matsunaga, M. Matsuura, K. E. Kraemer, J. Bernard-Salas, A. J. Markwick,RUSTY OLD STARS: A SOURCE OF THE MISSING INTERSTELLAR IRON?,The Astrophysical Journal717, 2010-06-18, עמ' L92–L97doi:10.1088/2041-8205/717/2/l92
- ^Eric Scerri2013-11-07T00:00:00+00:00,The trouble with the aufbau principle,RSC Education(באנגלית)
- ^FM Torti and SV Torti,Regulation of ferritin genes and protein,Blood Journal, 2002
| הטבלה המחזורית | ||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | |||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||||||||
| ||||||||||||||||||||||||||||||||||||||||||



![{\displaystyle [1s^{2}2s^{2}2p^{6}3s^{2}3p^{6}]4s^{2}3d^{6}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/89d6c00b9edc34342fc7176d41d8184b30a134f6)