Kemija
| Kemija | |
 Antoine Laurent de Lavoisiersmatra se osnivačem moderne kemije. Godine 1789. objavio je svojuElementarnu raspravu o kemiji(Traité élémentaire de chimie). | |
| Znanstveno područje | Prirodne znanosti |
|---|---|
| Klasifikacija znanosti u Hrvatskoj | |
Kemija(grčki: χημείαchimeía;starofrancuski:alkemie;arapskial-kimia:umjetnost preobrazbe;nekad hr.lučba) jeznanostkoja proučava ustroj, osobine, sastav i pretvorbu tvari. Kemija se bavikemijskim elementimaispojevima,koji se sastoje odatomai molekula, kao i njihovim odnosima.
Prije više od stoljeća, ova se znanost nazivalalučbom.Danas se izrazludžba(usklađeno s modernim pravopisom) ne upotrebljava.
Pregled[uredi|uredi kôd]
Atomska teorijaje osnova kemije. Ta teorija kaže da se sve tvari sastoje od vrlo malih čestica,atoma.Jedan od prvih zakona koji je doveo do utemeljenja kemije kao znanosti bio jeZakon očuvanja mase.Taj zakon kaže da tijekomkemijske reakcijenema primjetne promjene u količini tvari. Jednostavno rečeno, ako na početku imate 10.000 atoma i napravite mnogo kemijskih reakcija, na kraju ćete opet imati 10.000 atoma.Masaje ostala ista ako uračunamo energiju koja se pritom izgubila ili stekla. Kemija proučava odnose među atomima: ponekad među pojedinačnim atomima, ali češće kad su atomi vezani uz druge atome i čineioneimolekule.Atomi stupaju u odnos s drugim atomima (npr. logorska vatra je kombinacija atomakisikaiz zraka s atomimaugljikaivodikaiz drveta), a mogu imati odnos i sasvjetlom(fotografija nastaje zbog promjena koje svjetlo izaziva na kemikalijama filmske vrpce) i drugim zračenjima.
Neobično se brzo otkrilo da se atomi gotovo uvijek slažu u određenim omjerima: silicijski pijesak je struktura gdje omjer atomasilicijai atoma kisika iznosi 1:2. Danas znamo da tajzakon određenih proporcijaima iznimke (npr. integrirani strujni krugovi). Iz toga vidimo da se tvari ponašaju po određenimkemijskim zakonitostima.
Drugo ključno otkriće: kad god se izvodi određena kemijska reakcija, količina stečene ili izgubljene energije uvijek je ista. To je dovelo do važnih pojmova kao što suravnoteža,termodinamikaikinetika.
Fizikalna kemijazasniva se na modernojfizici,jer jeu načelumoguće opisati sve kemijske sustave koristeći teorijukvantne mehanike.Ta je teorija matematički složena i nije razumno koristiti je za normalan rad u kemiji. U praksi se samo najjednostavniji kemijski sustavi mogu istraživati isključivo kroz kvantnu mehaniku, te se za praktičke svrhe moraju raditi aproksimacije. Zato u većem dijelu kemije nije potrebno detaljno znanje kvantne mehanike, jer se važne posljedice te teorije (prvenstveno orbitalna aproksimacija) mogu razumjeti i primijeniti na jednostavniji način.
Iako sekvantna mehanikačesto može zanemariti, njezin osnovni pojam -kvantizacija energije- mora se uzeti u obzir. Kemičari koriste kvantne efekte prilikom svihspektroskopskihtehnika (i raznih drugih stvari), iako mnogi kemičari nisu svjesni toga! Osim toga, često se i fizika može zanemariti, a konačni rezultat (npr.NMR spektar) svejedno može imati smisla.
Potpun fizikalni opis kemije mora također uzeti u obzirrelativnost,koja je druga glavna teorija moderne fizike, također matematički složena. Srećom, efekti relativiteta važni su samo u izuzetno preciznim izračunima atomske strukture, koji se uglavnom tiču težih elemenata, dok je u praksi relativnost nevažna za gotovo čitavu kemiju.
Kemija se obično dijeli ovako:analitička kemija,koja određuje sastav i dijelove tvari;organska kemija,koja proučava ugljikove spojeve;anorganska kemija,koja istražuje šire elemente koje organska kemija ne naglašava;biokemija,proučavanje kemije u biološkom sustavu; ifizikalna kemija,koja je osnova svih drugih grana jer obuhvaća fizikalne osobine tvari i teorije za njihovo istraživanje.
Neke druge multidisciplinarne i specijalizirane grane:znanost o materijalima,kemijapolimera,kemija okoliša,farmacija.
- znanstvena metoda
- osnovna jedinica SI
- značajni brojevi
- atom
- orbitale
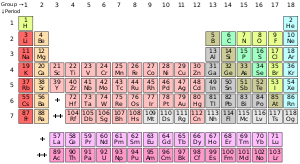
- periodni sustav elemenata
- izomeri
- alotropi
- izotopi
- ion
- elektronska konfiguracija
- Periodični trendovi
- elementarne skupine:S-blok,D-blok,F-blok,P-blok
Kemikalije i odnosi[uredi|uredi kôd]
- sustavna imena
- kemijska formula
- kemijska veza
- kemijski polaritet
- kemijska jednadžba
- kemijska reakcija
- boje kemikalija
Kvantitativna kemija[uredi|uredi kôd]
Stanja tvari[uredi|uredi kôd]
- kinetička teorija plinova
- idealni plin
- fizika čvrstog stanja
- otopine
- koncentracijaotopina
- koloidna svojstva
- kemijska ravnoteža
- Le Chatelierovo načelo
- topljivost
- ukapljivanje
- efekt zajedničkog iona
Kiseline i baze[uredi|uredi kôd]

- teorije reakcija kiselina i baza
- jake kiseline
- slabe kiseline
- pHi jačina kiselina
- sustavno imenovanjekiselina i baza
- samo-ionizacija vode
- titracijakiselina-lužina
- redoks-reakcije
- elektrokemija
Kinetika i termodinamika[uredi|uredi kôd]
- kemijska kinetika
- stope reakcije
- spontani procesi
- entalpija
- entropija
- Gibbsova slobodna energija
- nuklearna kemija
- biokemija
Povijest kemije[uredi|uredi kôd]
- podrijetlo kemije
- rani razvoj kemije
- alkemija
- flogistonska kemija
- otkriće kemijskih elemenata
- Nobelova nagrada za kemiju
Poznati kemičari[uredi|uredi kôd]

- Marie Curie
- Pierre Curie
- John Dalton
- Jöns Jakob Berzelius
- Dmitrij Ivanovič Mendeljejev
- Antoine Laurent de Lavoisier
- SirErnest Rutherford
- Louis Pasteur
- SirHumphry Davy
- Robert Boyle
- Michael Faraday
- Sima Lozanić
- Fran Bubanović
Vanjske poveznice[uredi|uredi kôd]
- Mrežna mjesta
- kemija,Hrvatska enciklopedija
- Razred za matematičke, fizičke i kemijske znanostiHAZU
- Hrvatsko kemijsko društvo
- Hrvatsko društvo kemijskih inženjera i tehnologa
- M. Sikirica, M. Vrbnjak Grđen, K. Holenda,e-Kemija,interaktivni udžbenik i pojmovnik
- www.periodni.com,portal o kemiji i pojmovnik
| |||||
