Karbamátok
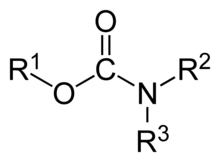
Akarbamátokszerves vegyületek,akarbamidsav(NH2COOH) származékai. A karbamátcsoport, a karbamát-észterek (például az etil-karbamát) és a karbamidsavak szerkezetileg összefüggőfunkciós csoportok,és kémiailag is gyakran átalakulnak egymásba. A karbamát-észtereketuretánoknak is nevezik.
Előállításuk
[szerkesztés]A karbamidsavakataminokbólnyerik:
- R2NH + CO2→ R2NCO2H
A karbamidsav körülbelül ugyanolyan erős sav, mint azecetsav[forrás?],belőle egy proton leadásával karbamát anion, a karbamidsav konjugált bázisa keletkezik:
- R2NCO2H → R2NCO2-+ H+
A kloroformamidok hidrolízise során is karbamátok keletkeznek:
- R2NC(O)Cl + H2O → R2NCO2H + HCl
Karbamátok keletkezhetnekCurtius-lebontássorán is, ha a létrejöttizocianátokalkohollalreagálnak:
- RNCO + R'OH → RNHCO2R'
Előfordulásuk és felhasználásuk
[szerkesztés]A cikkben többnyire a szerves karbamátokkal foglalkozunk, de megjegyzendő, hogy az egyik szervetlen sót, az ammónium-karbamátot nagy mennyiségben állítják elő köztitermékként akarbamidammóniábólésszén-dioxidbóltörténő gyártása során.
Karbamátok a biokémiában
[szerkesztés]A dezoxihemoglobin α- és β-láncaiban levő valin aminosav maradékának N-terminális aminocsoportjai karbamátok formájában találhatók. Ezek segítik a fehérje stabilizálását a dezoxihemoglobinná alakulás során és növelik a fehérjéhez kötött maradék oxigénmolekulák felszabadulásának valószínűségét. Ezen karbamátcsoportoknak a hemoglobin O2iránti affinitására kifejtett hatását Bohr-effektusnak nevezik.
Az ureázok és foszfotriészterázok lizin aminosav maradékának ε-aminocsoportjai is karbamát alakjában fordulnak elő. Az aminoimidazolból származó karbamát az inozin bioszintézisének köztiterméke. A karbamoil-foszfát inkább karboxifoszfátból, semmint CO2-ből keletkezik.[1]
CO2megkötése ribulóz-1,5-biszfoszfát-karboxilázzal
[szerkesztés]Talán a legfontosabb karbamát a növények CO2-megkötésében részt vevő vegyület, mivel ez a folyamat a globális felmelegedés szempontjából is érdekes. A ribulóz-1,5-biszfoszfát-karboxiláz/oxigenáz enzim a reduktív pentózfoszfát-ciklus (Calvin-ciklus) első lépéseként egy molekula szén-dioxidot köt meg karbamát formájában. Az enzim aktív centrumában egy Mg2+ion kötődik glutamát és aszpartát aminosav maradékához és egy lizin-karbamáthoz. A karbamát akkor keletkezik, amikor az ionhoz közeli töltés nélküli lizin oldallánc reagál a levegőből származó szén-dioxid molekulával (ésnema szubsztrát szén-dioxid molekulával). Ennek révén a lizin oldallánc töltötté válik, és így képessé válik a Mg2+ion megkötésére.
Karbamát vegyületek
[szerkesztés]Karbamát inszekticidek
[szerkesztés]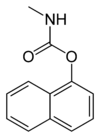
Az úgynevezett karbamát inszekticidekben karbamát észter funkciós csoport található. Ebbe a vegyületcsoportba tartozik az aldikarb, akarbofurán(Furadan), a karbaril (Sevin), az etienokarb, a fenobukarb, az oxamil és a metomil. Ezek az inszekticidek a rovarokat azacetilkolin-észterázreverzibilis inaktiválásával pusztítják el. A szerves foszfátvegyületek is ezt az enzimet gátolják, hatásuk azonban irreverzibilis, és így súlyosabb kolinerg mérgezést okozhatnak.[2]
A fenoxikarb ugyan tartalmaz karbamátcsoportot, de hatása inkább juvenilis hormonhatásán alapul, semmint az acetilkolin-észteráz gátlásán.[3]
Az ikaridin nevű rovarűzőszer szubsztituált karbamát.
Poliuretánok
[szerkesztés]A poliuretánok szerkezetében több karbamátcsoport is található. A „poliuretán” névben az „uretán” ezekre a karbamát csoportokra utal, a poliuretán nem tartalmaz és a gyártása során sem használnak etil-karbamátot (hétköznapi nevén „uretánt” ). A poliuretán polimerek változatos tulajdonságokkal rendelkeznek, kereskedelmileg mint habok, elasztomerek és szilárd anyagok kaphatók. A poliuretánokat jellemzően diizocianátok, például toluol-diizocianát és diolok reakciójával állítják elő, a karbamát csoportok az alkoholok és izocianátok reakciójában keletkeznek:
- RN=C=O + R'OH → RNHC(O)OR'
Konzerválószerek és kozmetikumok
[szerkesztés]A jódpropinil-butilkarbamát fa- és festékkonzerválószer, de kozmetikumokban is használják.[4]
Gyógyszerek
[szerkesztés]Az uretánt vagy etil-karbamátot az Egyesült Államokban korábban kereskedelmi léptékben gyártották, mint rákellenes és egyéb betegségek kezelésére használt gyógyszert, de kiderült, hogy többnyire nem hatásos, hanem mérgező.[5]Esetenként állatgyógyászati szerként alkalmazzák.
Néhány karbamátot alkalmaznak a humán farmakoterápiában, például aneosztigminésrivasztigminkolinészteráz-gátlókat, melyek kémiai szerkezete afizosztigmin,egy természetesalkaloidvázán alapul. További példák a meprobamát és származékai, például kariszoprodol, felbamát és tibamát, melyek az 1960-as években, abenzodiazepinekelterjedése előtt széles körben használt szorongásoldó és izomlazító gyógyszerek voltak, és egyes esetekben még ma is alkalmazzák őket.
Adarunavirban– a proteáz-inhibitorok közé tartozó HIV-ellenes gyógyszer – is található karbamát funkciós csoport.
Kénanalógok
[szerkesztés]Az (1) jelű ROC(=O)NR2karbamátban két oxigénatom található, melyek bármelyike vagy mindkettő kicserélhető kénatomra. A karbamátok azon megfelelőit, melyekben csak egy oxigént helyettesít kénatom, tiokarbamátoknak nevezzük (2és3). A mindkét helyen kénatommal helyettesített származékok (4) az RSC(=S)NR2általános képletűditiokarbamátok.
A tiokarbamátoknak két különböző típusú szerkezeti izomerje létezik:
- O-tiokarbamátok (2), ROC(=S)NR2,melyekben akarbonilcsoportot(C=O)tiokarbonilcsoport(C=S) helyettesíti
- S-tiokarbamátok (3), RSC(=O)NR2,melyekben az R–O– csoport helyett R–S– csoport található
AzO-tiokarbamátok izomerizációs reakcióban, például aNewman–Kwart-átrendeződéssorán átalakulhatnakS-tiokarbamáttá.

Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben aCarbamatecímű angol Wikipédia-szócikkezen változatánakfordításán alapul.Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Jegyzetek
[szerkesztés]- ↑Bartoschek, S.; Vorholt, J. A.; Thauer, R. K.; Geierstanger, B. H. and Griesinger, C., "N-Carboxymethanofuran (carbamate) formation from methanofuran and CO2 in methanogenic archaea: Thermodynamics and kinetics of the spontaneous reaction", Eur. J. Biochem., 2001, 267, 3130-3138.doi:10.1046/j.1432-1327.2000.01331.x
- ↑Robert L. Metcalf “Insect Control” in Ullmann’s Encyclopedia of Industrial Chemistry” Wiley-VCH, Weinheim, 2002.doi:10.1002/14356007.a14_263
- ↑Cornell University site on Fenoxycarb
- ↑Badreshia, S (2002). „Iodopropynyl butylcarbamate”.American Journal of Contact Dermatitis13(2), 77–79. o.DOI:10.1053/ajcd.2002.30728.ISSN1046199X.
- ↑Holland JR, Hosley H, Scharlau C, Carbone PP, Frei E 3rd, Brindley CO, Hall TC, Shnider BI, Gold GL, Lasagna L, Owens AH Jr, Miller SP (1966. március 1.). „A controlled trial of urethane treatment in multiple myeloma”(free fulltext).Blood27(3), 328–42. o. [2007. március 28-i dátummal azeredetibőlarchiválva].ISSN0006-4971.PMID5933438.(Hozzáférés: 2010. szeptember 11.)
