Sejtmag
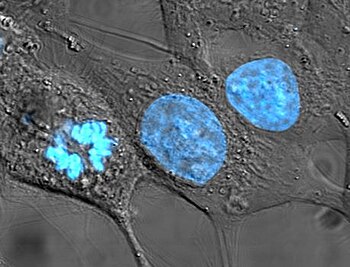
Asejtmag(latinulnucleus) kettős membránnal körülvettorganellumazeukariótasejtenbelül. Elsődleges funkciója a sejt genetikai anyagának, akromoszómáknaka tárolása és elkülönítése acitoplazmától,valamint agénekkifejeződésének szabályozása. Belső tartalmát a citoplazmától amaghártya– kettős lipidréteg – különíti el. Formáját a sejtmagváz, a nukleoszkeleton adja.
A fehérjék, nukleinsavak és egyéb molekulák maghártyán való átjutása a bonyolult szerkezetűmagpórusokonkeresztül történik, és gondosan szabályozott folyamat. A sejtmagon belül más, membránnal elkülönített organellumok nincsenek, de belseje nem egyenletes, több, fehérjéből ésRNS-ből álló szubnukleáris test is megfigyelhető; közülük legismertebb ariboszómákösszeállítását végzősejtmagvacska(nucleolus).
Felfedezése
[szerkesztés]

A sejtmag volt az első sejten belüli szervecske (organellum), amit felfedeztek. Az eddig ismert legrégebbi ábrázolása az első mikrobiológustól, a mikroszkóp tökéletesítőjétől, a 17. századiAnton van Leeuwenhoek-től származik, aki a lazac vörösvérsejtjeiben figyelt meg belső „űrt”[1](az emlősök vörösvértestjeitől eltérően a többi gerinces állat vérsejtjeinek van sejtmagjuk). 1804-benFranz Baueris leírta a sejtmagot,[2]majd részletesebben 1831-ben a skót botanikus,Robert Brownszámolt be róla aLondoni Linné Társaságegyik ülésén. Brown orchideák virágjának külső sejtrétegében figyelt meg áttetsző különálló részt, melyet ő areolának vagy nucleusnak nevezett el,[3]de nem kötötte azt valamilyen sejtfunkcióhoz. 1838-ban a németMatthias Schleidenfelvetette, hogy a sejtmag az új sejtek létrehozásában játszik szerepet, és a citoblaszt (sejtépítő) elnevezést javasolta, és azt állította, hogy sikerült megfigyelnie a „citoblasztok” körül csoportosuló kis sejteket.Franz Meyenhatározottan ellenezte ezt az elképzelést, mert korábban leírta a sejtosztódást, és nézete szerint sok sejtnek egyáltalán nem volt magja. Az újonnan, semmiből létrejövő sejtek elméleteRobert Remak(1852) ésRudolf Virchow(1855) eredményeinek is ellentmondott, akik szerint sejt csak sejtből jöhet létre(Omnis cellula e cellula).A sejtmag funkciója ekkor még ismeretlen maradt.[4]
1877–78-banOscar Hertwigtöbb közleményben publikálta megfigyeléseit atengeri sünökpetesejtjénekmegtermékenyüléséről. Kimutatta, hogy a spermium sejtmagja behatol a petesejtbe és ott egyesül annak sejtmagjával; emellett bebizonyította, hogy az élőlények egyetlen, nukleusszal rendelkező sejtből fejlődnek ki. Ezzel ellentmondottErnst Haeckelkorábbi elméletének, miszerint az egyedfejlődés teljes mértékben megismétli a törzsfejlődési utat, beleértve azt, hogy a kiindulási sejt egy strukturálatlan masszából („Urschleim” ) jön létre. Az elméletét ért támadások után Hertwig bebizonyította, hogy a sejtmagra apuhatestűekés akétéltűekmegtermékenyülésénél is feltétlenül szükség van.Eduard Strasburger1884-ben ugyanerre jutott a növények tanulmányozása során. Fokozatosan felismerték, hogy a sejtmag az öröklődésben játszik fontos szerepet. 1873-banAugust Weismannkimondta, hogy az öröklődés során az apai és anyai ivarsejtek egyenlő jelentőséggel bírnak. Miután megfigyelték amitózistés a 20. század elején újra felfedeztékMendeltörvényeit, egyértelművé vált, hogy a sejtmag a genetikai információk hordozója.[4]
Felépítés
[szerkesztés]A sejtmag az állati sejt legnagyobb organelluma.[5]Az emlőssejt nukleuszának átmérője kb. 6 mikrométer, és a sejt térfogatának 10%-át foglalja el.[6]Belsejét viszkózus folyadék, a magplazma (nukleoplazma vagy karioplazma) tölti ki, amelynek összetétele hasonló acitoszoléhoz.[7]Alakja többnyire gömbszerű, de számos szabálytalan sejtmagforma is ismert (korong, pálca, karéjozott stb.).
A maghártya és a magpórusok
[szerkesztés]Amaghártyakét, egymás mellett elhelyezkedősejtmembránból,a külső és belső membránból áll, amelyeket egy 10–50 nanométeres rés választ el egymástól. A maghártya feladata, hogy elválassza a sejt genetikai anyagát, a kromoszómákat az őt körülvevő citoplazmától, és megakadályozza a makromolekulák szabad átjárását a citoplazma és a nukleoplazma között.[8]A külső membrán közvetlenül kapcsolódik a durva felszínűendoplazmatikus retikulumhoz,és hozzá hasonlóanriboszómákkalvan teleszórva.[8]A két membrán közötti rés a perinukleáris űr, és közvetlenül folytonos az endoplazmatikus retikulum belső terével.
A maghártyán keresztül történő transzport amagpórusokonát zajlik. A pórusok bonyolult szerkezetű képződmények, amelyek 50 (élesztőben) vagy néhány száz (gerincesekben) fehérjéből tevődnek össze, és tömegük eléri a 125 millió daltont.[5]A pórus teljes átmérője 100 nm, de a tényleges tér, ahol a molekulák szabadon átdiffundálhatnak, alig 9 nm. Ezáltal a kis, vízoldékony vegyületek szabadon átjárnak, de a pórus meggátolja a nagy makromolekulák –fehérjék,nukleinsavak– irányítatlan közlekedését. A nagy molekulák aktív transzporttal kerülnek be a sejtmagba vagy ki a sejtmagból. Egy átlagos emlőssejtmag felületén mintegy 3–4 ezer pórus található.[9]A pórus egy nyolcszoros szimmetriájú, gyűrűszerű szerkezet, amely mellett a külső és belső membránok egybeolvadnak.[10]A gyűrűhöz belülről (a nukleoplazma felől) egy kosárnak nevezett szerkezet kapcsolódik, míg a másik oldalon szálszerű filamentumok nyúlnak a citoplazmába. Mindkét struktúra a transzportfehérjék kötődésére szolgál.[5]
A legtöbb fehérjét, riboszómaalegységet és egyes DNS-eket akarioferinneknevezett transzportproteinek viszik át a pórusokon. A sejtmagba befelé történő szállítást szabályozó karioferineketimportinnak,a kifelé történőtexportinnaknevezik. A legtöbb karioferin közvetlenül kapcsolódik a szállítmányához, bár bizonyos esetekben adaptor proteineket is használnak.[11]Az olyan lipidoldékony szteroidhormonok, mint ahidrokortizon,vagy azaldoszteronképesek átdiffundálni a sejthártyán, és a citoplazmában ún.nukleáris receptorokkötik meg őket, amelyek ezután aktív transzporttal a sejtmagba vándorolnak, ahol a génkifejeződést szabályozzák: a hormonnal kapcsolódva serkentik, anélkül gátolják az adott gén átírását.[5]
Nukleáris lamina
[szerkesztés]Az állati sejtekben két,intermedier filamentumokbólálló állványzat biztosítja a sejtmag alakjának megtartását. Anukleáris laminaa maghártya belső felén alkot jól szervezett hálózatot, míg a hártya külső, citoplazma felőli oldalát egy kevésbé sűrű filamentumegyüttes támasztja meg. Mindkét rendszer segít a maghártya alakjának megőrzésében, és kapcsolódási pontokat nyújt a kromoszómáknak és a pórusoknak.[6]
A nukleáris lamina főleg alaminfehérjéből áll. A többi proteinhez hasonlóan a lamin is a citoplazmában szintetizálódik, majd transzporttal bekerül a sejtmagba, ahol beépül a nukleáris lamina már meglévő hálózatába.[12][13]A maghártya külső oldalára irányított laminok (pl. azemerinés anesprin) a citoszkeletonhoz kapcsolódva rögzítik a sejtmagot. Laminokat a nukleoplazmában is találhatunk, ahol az ún. nukleoplazmatikus fátylat hozzák létre,[14]amelyfluoreszcenciamikroszkópbanjól megfigyelhető. A fátyol funkciója ismeretlen, de a sejtmagvacskában nincs jelen, és a két sejtosztódás közötti interfázisban lehet megfigyelni.[15]A fátyol a kromoszómákhoz kapcsolódik, és ha ezt a kötődést meggátoljuk, akkor a gének átírása megszűnik.[16]
A többi intermedier filamentumhoz hasonlóan a lamin alapegysége, fehérjemonomerjealfa-hélixszerkezetű. Két ilyen alegység egymás köré tekeredve alkot egy dimert, majd két dimer egymás mellett, fej-láb elhelyezkedéssel a protofilamentumnak nevezett tetramert hozza létre. Nyolc egymáshoz kapcsolódott protofilamentum alkotja a csavart, kötélszerű filamentumot, melynek hossza a kapcsolódó, illetve leváló alegységek miatt folyamatosan változhat.[6]
A lamin egyes mutációi elégtelen szálösszeálláshoz vezethetnek, és a ritka, laminopátia nevű öröklődő betegségcsoportot okozzák. A legismertebb ilyen betegség aprogeria,amely a betegek korai, akár kisgyerekkori testi öregedésével jár. Nem teljesen ismert, hogy a biokémiai változások hogyan vezetnek az öregedés külső szimptómáihoz.[17]
Kromoszómák
[szerkesztés]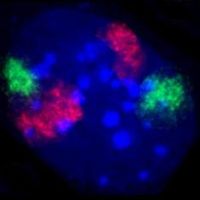
A sejtmag tartalmazza a sejt genetikai információjának döntő többségét (valamennyi amitokondriumokbanés a növényikloroplasztiszokbanis található). Az információ hosszú, lineárisDNS-molekulákban van kódolva, amelyek a kromoszómákat alkotják. Minden egyes kromoszóma egyetlen, hosszú DNS-szálat tartalmaz, illetve osztódáskor, amikor megduplázódik, akkor kettőt, ezek adják akariotípusbólismert X-formát. Minden emberi sejt kb. két méternyi DNS-t tartalmaz. A kromoszóma anyaga akromatin,a DNS és a hozzá kapcsolódó szabályozó és struktúrfehérjék (hisztonok) együttese.
A kromatinnak két fajtája ismert. Az eukromatin lazább szerkezetű, és azokat a géneket tartalmazza, amelyekre a sejtnek gyakran van szüksége, sokszor átír.[18]A heterokromatin viszont jóval kompaktabb, és a kevéssé használt DNS-szakaszok tartoznak hozzá. A heterokromatin további két részre osztható, a fakultatív heterokromatinra, amelynek génjeit időnként azért átírják (például a szervezet bizonyos fejlődési stádiumában), illetve az állandó heterokromatinra, amelyhez az olyan strukturális régiók tartoznak, mint atelomerekéscentromerek.[19]Azinterfázisalatt a fellazult, normál fénymikroszkópban nem látható kromoszómák adott „kromoszómaterületen” helyezkednek el.[20][21]Az aktív, eukromatikus gének ilyenkor többnyire a terület határán találhatók.[22]
Egyesautoimmun betegségekben,mint aszisztémás lupus erythematodesben,a kromatin alegységeihez, anukleoszómákhozkötődő ellenanyagok képződnek.[23]Hasonló nukleáris ellenanyagokatsclerosis multiplexbenis megfigyeltek, és kapcsolatba hozták az immunrendszer általános zavarával.[24]A progeriához hasonlóan nem világos, hogyan vezet az ellenanyagok termelődése a betegségek konkrét tüneteihez. Bár korábban úgy gondolták, hogy az autoimmun betegségekben azautoantitesteknem képesek behatolni a sejtmagokba, újabban bizonyíték van ennek ellenkezőjére.[25]
Sejtmagvacska
[szerkesztés]
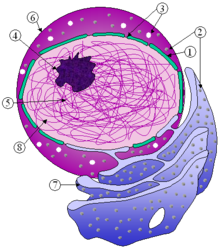
Asejtmagvacskavagy nukleólusz (nucleolus) egy különálló, sötéten festődő struktúra a sejtmagon belül. Nem veszi körül külön membrán, és néha szuborganellumként emlegetik. A sejtmagvacska a kromoszómákriboszomális RNS-t (rRNS) kódoló régiói körül formálódik; ezek a gének nagyon sok példányban vannak jelen egymás mellett. A nukleólusz fő funkciója a riboszomális RNS szintézise és ariboszómákösszeállítása. Struktúrájának tömörsége aktivitásától függ, a riboszóma-összeszerelés fokozza a sejtmagvacska komponenseinek ideiglenes összekapcsolódását, amely még hatékonyabb riboszómakészítéshez vezet. Megfigyelték, hogy ha inaktiválják az rRNS-t, a sejtmagvacska struktúrái összekuszálódnak.[26]
A riboszóma-összeszerelés első lépéseként azRNS-polimeráz Ia DNS-ről átírja az rRNS génjét, miáltal egy hosszú pre-rRNS keletkezik. Ennek feldarabolódásával jönnek létre az alegységek 5,8S, 18S és 28S rRNS-ei.[27]Az átírás (transzkripció), feldarabolás és a riboszóma-alegységek összeállítása a sejtmagvacskában történik a kis nukleoláris RNS (snoRNS) segítségével. Utóbbiak részben a riboszómák funkcióihoz kapcsolódó génekmRNS-einek kivágottintronjaibólszármaznak. Az összeállított riboszóma-alegységek a legnagyobb struktúrák, amelyek átférnek a maghártya pórusain.[5]
Elektronmikroszkópalatt a neukleóluszban három régió különböztethető meg. A legbelső fibrilláris centrumokat (FC) az elektrondenz fibrilláris komponens (dense fibrillar component,DFC) veszi körül, amelyet viszont a granuláris komponens (granular component,GC) határol. Az rRNS transzkripciója az FC régióban vagy az FC-DFC határon zajlik, így ha a sejt igénye megnő a riboszómákra, a sejtmagvacskában több FC-t lehet megfigyelni. A pre-rRNS szétvágása és utólagos módosítása a DFC-ben, a fehérjék hozzákapcsolása az alegységek elkészítéséhez pedig a GC-ben történik.[27]
További struktúrák
[szerkesztés]| Név | Átmérő | |
|---|---|---|
| Cajal-testek | 0,2–2,0 µm | [28] |
| PIKA | 5 µm | [29] |
| PML-testek | 0,2–1,0 µm | [30] |
| Parafoltok | 0,2–1,0 µm | [31] |
| Foltok | 20–25 nm | [29] |
A sejtmagvacskán kívül a mag több kisebb, membránnal nem határolt testet tartalmaz. Ilyenek aCajal-testek,az iker-spiráltestek, a polimorf interfázisbeli karioszomális halmaz (PIKA), a promielocitás leukémia (PML)-testek, a parafoltok és a splicing-foltok. Sokukról nagyon kevés információ áll rendelkezésre, de egyértelművé teszik, hogy a nukleoplazma egyáltalán nem homogén, hanem funkcionális kisebb terekre oszlik.[30]
Egyes szubnukleáris struktúrák bizonyos betegségekben tűnnek fel. Miopathia nemalinica esetén kis pálcikaszerű testek jelennek meg a sejtmagban, ami feltehetően egy mutáció miatt megváltozott szerkezetűaktinvagy acitoszkeletonmás fehérjéje.[32]
- Cajal-testek.Egy sejtmag átlagosan 1–10 Cajal-testnek vagy spiráltestnek nevezett kompakt struktúrát tartalmaz, melyek átmérője 0,2–2 µm között változik, fajtól és sejttípustól függően.[28]Elektronmikroszkóp alatt gubancos fonalgombolyagnak látszanak[29]és nagy mennyiségű coilin fehérjét tartalmaznak.[33]A feladatuk a különböző RNS-ek (kis nukleoláris RNS,kis nukleáris RNSés ahisztonmRNS) utólagos módosítása.[28]
A Cajal-testek mellett helyezkednek el az iker-spiráltestek (innen kapták a nevüket is), amelyeket mikroszkóp alatt nem is lehet megkülönböztetni tőlük.[33]A Cajal-testektől eltérően azonban nem tartalmaznak kis nukleáris ribonukleoproteint (snRP, a hírvivő RNS utólagos módosítását végzi); funkciójuk feltehetően az snRP szintézisének segítése a Cajal-testekben,[34]de olyan vélemény is létezik, hogy a Cajal-testek és az ikertestek ugyanazon struktúra különböző formái.[33]
- PIKA.A polimorf interfázisbeli karioszomális halmazokat (PIKA, vagy más néven RAFA-domén) először 1991-ben figyelték meg mikroszkóppal. Feladatuk ismeretlen, de valószínűleg nincs közük a DNS másolásához, átírásához vagy az RNS utólagos módosításához.[35]Többnyire a PTF transzkripciós faktor (amely a kis nukleáris RNS, snRNS transzkripcióját segíti) halmazai közelében találhatók.[36]
- PML-testek.A promielocitás leukémia-testek (PML-testek, más néven nukleáris domén 10 vagy Kremer-testek) a nukleoplazmában elszórtan található kerek, 0,1–1 µm átmérőjű szerkezetek. Nevüket fő komponensükről, apromielocitás leukémia proteinrőlkapták. Többnyire a Cajal-testek vagy spliceoszómák és egyéb hasonló struktúrák közelében láthatók.[30]A PML-testek feltehetően a sejtmag sok fontos funkciójában (DNS-másolás, transzkripció, génműködés-gátlás) van koordináló szerepe, melyet főleg SUMO-val (kis ubiquitin-szerű módosító protein) való összekapcsolással ér el. A PML-hiányos sejtek (amelyekben a génjüket mesterségesen kikapcsolták) nem fejlődnek és funkcionálnak normálisan, azaz feladatuk biztosan alapvető fontosságú.
- Splicing-foltok(splicing speckle,más néven magfolt –nuclear speckle–, interkromatin granulumhalmaz, B-sznörposzóma).[37]A splicing-foltok az emlőssejtek kromatinközi régiójában találhatók, és az mRNS utólagos módosítását,splicingját(ejtsd: szplájszing) végző molekulák halmozódnak fel bennük. Fluoreszcenciamikroszkóp alatt változó méretű és alakú, szabálytalan, pettyezett foltok; elektronmikroszkóppal szemcsés halmaznak látszanak. Szerkezetük és összetételük változó, RNS és fehérjekomponenseik gyakran más helyre vándorolnak, például aktívan átíródó génekhez. A foltok összetétele és elhelyezkedése a génexpresszió változásával összhangban változik.[38]
- Parafoltok(paraspeckle).A 2002-ben felfedezett parafoltok a kromatinközi térben található szabálytalan formájú alakzatok.[39]Először HeLa sejtekben mutatták ki őket, de azután észlelték valamennyi emberi sejttípusban, beleértve a laboratóriumban tenyésztett immortalizált sejtvonalakat.[40]Egy sejtmagban 10–30 van belőlük. Nevüket onnan kapták, hogy a splicing-foltok közelében, azokkal paralel módon helyezkednek el.[41]Nagyságuk és elhelyezkedésük a sejt génexpressziójának függvényében változik. Létük az aktív génátírástól függ, ha a fehérjekódoló géneket átíróRNS-polimeráz IIinaktív, akkor valamennyi parafolt eltűnik és fehérjekomponenseik a sejtmagvacskában tárolódnak. Ez a folyamat a sejtosztódás telofázisában is lezajlik, a génátírás ilyenkor is szünetel.[40]
Funkciója
[szerkesztés]A sejtmag elválasztja a génektranszkripciójánakhelyét a fehérjeszintézistől, atranszlációtól,és ezáltal a génszabályozásnak olyan lehetőségeit nyújtja, amire aprokariótasejtek nem képesek. A sejtmag fő feladata a génkifejeződés és a DNS-replikáció szabályozása a sejtciklus során.
Génkifejeződés
[szerkesztés]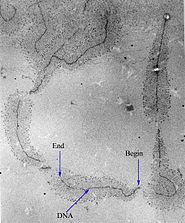
A gének kifejeződésemRNS-sé való átírásukkal indul, majd az mRNS sokféleképpen módosul, és végül a riboszómákhoz kapcsolódva a transzláció révén fehérjék képződnek róla. Az utóbbi folyamat kivételével a többi tevékenység a sejtmagban zajlik.[42]A sejtmagban találhatók a transzkripcióhoz közvetlenül és közvetve szükséges enzimek és az ezeket szabályzótranszkripciós faktorokis. Az enzimek közé tartoznak ahelikázok,amelyek szétcsavarják a kettős szálú DNS-t, az RNS-polimerázok, amelyek az mRNS szintézisét végzik és atopoizomerázok,amelyek a DNS széttekeredéséből származó fizikai feszültséget tüntetik el.[43]
Az átírt mRNS-t többféleképpen módosítani kell, mielőtt „érett”, transzlációra alkalmas lesz. Ezek közül a legfontosabbak az 5’cap („sapka” ) és az adenozinokból álló poli(A) farok elhelyezése rajta, valamint asplicing.Az 5’cap-et a transzkripciós komplexhez tartozó enzim köti az mRNS-hez, a poli(A) farkat pedig közvetlenül az átírás után kapja meg. A splicing aspliceoszómanevű komplexen belül zajlik, és hosszú, sokintronttartalmazó mRNS-ek esetében már azelőtt elkezdődhet, hogy a transzkripció befejeződött.[5]Sok esetben a pre-mRNS-t többféleképpen állítják össze érett mRNS-sé, ez az únalternatív splicing;így keletkeznek például a rendkívül változatos ellenanyagok is.
Kompartmentalizáció
[szerkesztés]A kompartmentalizáció a sejten belüli folyamatok fizikai elválasztását, különböző térrészekbe való elhelyezését jelenti. A maghártya elválasztja a genetikai anyagot a citoplazma többi részétől, és lehetővé teszi, hogy attól elkülönülve kontrollálja a gének átírását. Az egyik általánosan elterjedt módszer szerint a megállítandó folyamat egyik közbenső molekuláját a sejtmagba transzportálják, ahol az transzkripciós faktorokhoz kötődve gátolja az adott reakciót katalizáló enzim génexpresszióját. Ilyen például a sejt energia-háztartásában alapvetőglikolízis.Ennek első lépésében ahexokinázaglükózbólglukóz-6-foszfátotgenerál, amiből pedigfruktóz-6-foszfátlesz. Ha az utóbbi koncentrációja túl magas, egy regulátor fehérje a sejtmagba viszi a hexokinázt,[44]ahol az más proteinekkel olyan komplexumot formál, amely meggátolja a glikolízis enzimjeinek kifejeződését.[45]
A génkifejeződést szabályozó transzkripciós faktorokat a sejt sokszor fizikailag elszeparálja a kromoszómáktól, hogy a minimális génátírást is megakadályozza. Ezek a faktorok csak akkor fejthetik ki működésüket, ha a megfelelő szignál aktiválja őket. Például a gyulladási folyamatokban szerepet játszó géneket aktiválóNF-κBfaktor a citoplazmában található, amíg a sejt külső membránján lévő receptorokhoz nem csatlakozik valamilyen szignálmolekula (például aTNF-α), és a receptor aktiválja az NF-κB-t, amely ezután a rajta találhatónukleáris lokalizációs szignálrévén a sejtmagba vándorol és megindítja a megfelelő gének transzkripcióját.[6]
A kompartmentalizáció tudja megakadályozni, hogy a génekről frissen átírt, módosítatlan pre-mRNS transzlációja azonnal megkezdődjék.[46]Az eukarióták génjeiben közbeszúrt szakaszok, intronok vannak, amelyeket el kell távolítani, mielőtt fehérjévé fordítanák át. A baktériumoknál a transzláció sokszor már ezelőtt elkezdődik, hogy a hírvivő RNS transzkripciója teljesen befejeződne, eukarióták esetében ez az intronok miatt hibás, használhatatlan fehérjék termelődéséhez vezetne.
Nukleáris transzport
[szerkesztés]
A nagy molekulák mozgása a sejtmagba befelé és onnan kifelé szigorúan szabályozott, és a pórusokon keresztül történik. Míg a kis méretű molekulák szabadon átjárhatnak,[47]a fehérjék és nukleinsavak csak akarioferinneknevezett proteinhez kapcsolódva haladhatnak át a póruson. A befelé szállító karioferinek az importinok, a sejtmagból kifelé vivők az exportinok. A szállítandó fehérjén rövid aminosav-szekvencia, ún. nukleáris lokalizációs szignál jelzi, hogy végcélja a sejtmag; ugyanez igaz a sejtmagból kiszállítandó polipeptidekre is. A póruson való átszállítás energiájaguanozin-trifoszfát(GTP) hasításából származik, amit GTPázok végeznek. A nukleáris transzport legfontosabb GTPáza aRannevű protein. Az importinoknak a RanGTP komplexre ahhoz van szükségük, hogy elengedjék szállítmányukat, míg az exportinok esetében a kapcsolódás miatt elengedhetetlen a Ran jelenléte.[11]
Nukleáris import esetén a citoplazmában található fehérjeszállítmányhoz odakötődik az importin és átviszi a póruson keresztül a magba. Odabent az importin a RanGTP segítségével leválasztja magáról a szállítmányt és visszatér a citoplazmába. Az exportálandó fehérjéhez az exportin köt hozzá a RanGTP energiája felhasználásával, átszállítja a póruson, leválik róla és visszatér a sejtmagba.
Az érett mRNS éstranszfer RNS(tRNS) kiszállítására külön exportproteinek specializálódtak. Ezek a sejten belüli „minőségellenőrző” rendszer részei, amely megakadályozza hogy a nem vagy csak részben érett mRNS a riboszómákhoz jusson. A rendszer a citoplazmába kijutó, nem teljesen módosított mRNS-t még azelőtt lebontja, hogy elkezdődhetne rajta a transzláció.[5]
A sejtmag lebomlása és újjászerveződése
[szerkesztés]
A sejtéletciklusánakbizonyos szakaszaiban – a sejtosztódás és a programozott sejthalál, azapoptózissorán - a sejtmag megszűnik, és az elkülönülését biztosító struktúrák, a maghártya és a nukleáris lamina tervezetten lebomlik.
A legtöbb sejtben amitózisprofázisának végén a mag membránjai szétesnek. Vannak kivételek, például egyes egysejtű eukarióták (élesztő) ún. zárt mitózis révén osztódnak, amikor maghártyájuk épen marad. Ilyenkor a leánykromoszómák a sejtmag két ellenkező végére vándorolnak, majd a mag osztódik. A fejlettebb eukariótákra azonban a maghártya lebomlásával járó nyílt mitózis jellemző, ahol a leánykromoszómák a mitotikus orsó pólusaihoz mozognak, és új sejtmag jön létre körülöttük.
A sejtosztódás után mindkét leánysejtnek teljes kromoszómakészletre van szüksége, ezért a mitózis előtt a kromoszómák megkettőződnek, majd az osztódás során amitotikus orsófonalai (mikrotubulusai) hozzájuk kapcsolódnak, és a leánykromoszómákat a sejt ellentétes végeibe, az orsó pólusához, a centroszómához húzzák. A legtöbb sejtben a centroszómák a magon kívül, a citoplazmában helyezkednek el, így ép maghártya esetén a mikrotubulusok nem férnének hozzá a kromoszómákhoz.[48]Emiatt a mitózis korai szakaszában, a profázisban kezdve és a prometafázisban befejeződve, a sejtmagot körülvevő membránokat szétbontják.[14]Ugyanekkor szétesik a nukleáris lamina is; ez a folyamat a laminfehérjék foszforilálásával jár.[49]A sejtosztódás végén a maghártya újból összeáll, akárcsak az immár defoszforilált laminokból álló lamina.[49]
Adinoflagellátáknála centroszóma szintén a citoplazmában van, azonban a maghártya ép marad, és a kromoszómákcentromerjeibeépülnek a sejtmag membránjába, hogy a mikrotubulusok hozzájuk kapcsolódhassanak (ún. extranukleáris orsó). Sok más egysejtűnél (csillósok,sporozoák,egyes gombák) a centroszómák a magon belül találhatók, és a mag nem bomlik fel a sejtosztódáskor.
Azapoptózisa sejt ellenőrzött, előre programozott pusztulása. Ennek során mélyreható változások történnek, akromatinkondenzálódik, a maghártya és a lamina szétesik. A lamina hálózatának szétbontását akaszpáznevű proteázok (fehérjebontó enzimek) végzik, amelyek szétvágják a laminokat. A kaszpázaktikivitást laboratóriumi tesztekben a korai apoptózis kimutatására használják.[14]Léteznek mutáns sejtvonalak, melyek laminja ellenálló a kaszpázokkal szemben, ezekben nem zajlik le a sejtmag apoptotikus bomlása.[14]
A maghártya avírusokbehatolását is meggátolja. Egyes vírusok szaporodásához a sejtmagban található proteinekre van szükség. Egyes DNS-vírusok (például aherpeszvírusok) a sejtmagban szaporodnak és állítják össze új virionjaikat. Ezek úgy szabadulnak ki, hogy lebontják a belső laminát és a maghártyán át bimbózással távoznak, miközben annak egy darabját burokként magukkal viszik.[14]
Mag nélküli és többmagvú sejtek
[szerkesztés]
A sejteknek általában egy nukleuszuk van, de egyes esetekben több is lehet, esetleg egy sem. Ez lehet előre tervezett folyamat eredménye (például az emlősökvörösvértestjei) vagy hibás sejtosztódás következménye.
A sejtmag nélküli sejtek nem képesek osztódni. Legismertebb példájuk az emlősök vörösvértestje (eritrocitája), amelyből az egyéb organellumok (pl. mitokondriumok) is hiányoznak, és gyakorlatilag csak az oxigénszállítóhemoglobintartályául szolgálnak. Az eritrociták a vöröscsontvelőbenvaló érésük során veszítik el magjukat, riboszómáikat és organellumaikat. A sejtmag akkor tűnik el, amikor a kiindulási eritroblasztbólretikulocita(az érett vörösvértest prekurzora) lesz.[50]Egyes mutagének hatására éretlen, mikronukleusszal rendelkező eritrociták is kikerülhetnek a véráramba.[51][52]Mag nélküli sejtek hibás sejtosztódás során is keletkezhetnek, amikor az egyik leánysejtnek két sejtmagja lesz, a másiknak pedig egy sem.
Ezzel szemben asugárállatkákAcanthareacsoportjának tagjai[53]és egyes mikorrhizás gombák több sejtmaggal is rendelkeznek sejtenként,[54]de aGiardiaegysejtű bélparazitának is két magja van.[55]Az emberben aharántcsíkolt izomsejtjei, a miociták összeolvadnak ésszincíciumotalkotnak; eközben az eredeti sejtmagok megmaradnak.[5]Betegségek és kórképek kísérőjelensége is lehet a többmagvú sejtek megjelenése, például agyulladásesetén időnkéntmonocitákésmakrofágokösszeolvadásából származó óriás többmagvú sejtek figyelhetők meg,[56]és tumorképződésben is előfordulhatnak.[57]Bizonyos vírusok, például aHIVburokfehérjéi a sejtmembránba épülve a sejtek összeolvadását és sokmagvú szincíciumok kialakulását okozzák.[58]
Adinoflagellátákegyes fajainak két sejtmagva van,[59]azonban ezek genetikai anyaga különbözik: az egyik az eredeti sejtmag, a másik pedig a vele szimbiózisban élőkovamoszaté.
Evolúciója
[szerkesztés]A sejtmag megléte az egyik alapvető különbség a prokarióták és eukarióták között, és kialakulására négy jelentősebb elmélet is született, de általános elfogadottsággal egyik sem bír.[60]
Az első, az ún. szintropikus modell szerint egyarchea(ősbaktérium) és egy baktériumszimbiózisábóljött létre a magot tartalmazó eukarióta sejt.[61]Az elképzelés szerint a maimetánbaktériumokhozhasonló archea belsejében parazita vagy szimbionta prokarióta (pl.myxobaktérium) élt, és idővel teljes mértékben alkalmazkodtak egymáshoz. Ez az elmélet analóg amitokondriumokéskloroplasztiszokbakteriális eredetét hirdető, a szakértők által általánosan elismertendoszimbionta elmélettel.[62]Az ősbaktériumi eredetet támogatja, hogy az eukarióták és archeák génjei (pl. a hisztongének) sok tekintetben hasonlóak. Hasonlóan, a myxobaktériumok is sok olyan tulajdonsággal rendelkeznek (soksejtű komplexumokat alkotnak, mozgékonyak,G-proteinjeikés kinázaik az eukariótákéra hasonlítanak), ami az eukariótákra jellemző.[63]
A második elmélet endoszimbionta állapot nélküli evolúciós átmenetet tételez fel. Például aPlanctomycetesbaktériumcsoportot hozzák fel, amely membránnal és primitív pórusokkal ellátott sejtmagszerű organellummal rendelkezik.[64]Egy hasonló elképzelés szerint a proto-eukarióta sejtfagocitózissalkebelezte be az archeákat vagy baktériumokat és szerezte meg génjeiket.[65]
A leginkább vitatott modell, a virális eukariogenezis szerint az eukarióták megkülönböztető sajátosságai, közte a membránnal elkülönített sejtmag, vírusfertőzés következményei. Az elmélet alapja az eukarióták és egyes vírusok közötti hasonlóságok: a lineáris kromoszómák, azmRNS5’cap-ja (sapkája) és a DNS csomagolását végző hisztonok analógiája a vírusok nukleoproteinjeivel. Az elmélet egyik verziója szerint a sejtmag a fagocitózissal párhuzamosan fejlődött ki, és a korai eukarióták egysejtű ragadozók voltak.[66]Egy másik változat szerint az eukariótákhimlővírussalfertőzött ősbaktériumtól erednek, aminek az adja az alapját, hogy ezeknek a vírusoknak aDNS-polimerázahasonlít az eukariótákéra.[67][68]A víruseredettel megpróbálták az ivaros szaporodás tisztázatlan kezdeteit is magyarázni.[69]
A legújabb elmélet, az exomembrán-hipotézis szerint az eukarióták őse egy olyan archea volt, amely egy második membránt fejlesztett az eredeti köré, amelyikből a maghártya lett, és addigi membránkötött struktúráiból kialakultak a pórusok, hogy lehetővé tegyék a belül szintetizált termékei – pl. riboszómák – külső transzportját.[70]
Jegyzetek
[szerkesztés]- ↑Leeuwenhoek, A. van: Opera Omnia, seu Arcana Naturae ope exactissimorum Microscopiorum detecta, experimentis variis comprobata, Epistolis ad varios illustres viros. J. Arnold et Delphis, A. Beman, Lugdinum Batavorum 1719–1730. Cited after: Dieter Gerlach, Geschichte der Mikroskopie. Verlag Harry Deutsch, Frankfurt am Main, Germany, 2009.ISBN 978-3-8171-1781-9.
- ↑Harris, H.The Birth of the Cell.New Haven: Yale University Press (1999).ISBN 0-300-07384-4
- ↑Brown, Robert (1866). „On the Organs and Mode of Fecundation of Orchidex and Asclepiadea”.Miscellaneous Botanical Works I,511–514. o.
- ↑abCremer, Thomas.Von der Zellenlehre zur Chromosomentheorie.Berlin, Heidelberg, New York, Tokyo: Springer Verlag (1985).ISBN 3-540-13987-7Online Versionhere
- ↑abcdefghLodish, H.Molecular Cell Biology,5th, New York: WH Freeman (2004).ISBN 0-7167-2672-6
- ↑abcdszerk.: Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, Peter Walter:Molecular Biology of the Cell, Chapter 4, pages 191–234,4th, Garland Science (2002)
- ↑Clegg JS (1984. február 1.). „Properties and metabolism of the aqueous cytoplasm and its boundaries”.Am. J. Physiol.246(2 Pt 2), R133–51. o.PMID 6364846.
- ↑abPaine P, Moore L, Horowitz S (1975). „Nuclear envelope permeability”.Nature254(5496), 109–114. o.DOI:10.1038/254109a0.PMID 1117994.
- ↑szerk.: Rodney Rhoades, Richard Pflanzer: Ch3,Human Physiology,3rd, Saunders College Publishing (1996)
- ↑Shulga N, Mosammaparast N, Wozniak R, Goldfarb D (2000). „Yeast nucleoporins involved in passive nuclear envelope permeability”.J Cell Biol149(5), 1027–1038. o.DOI:10.1083/jcb.149.5.1027.PMID 10831607.
- ↑abPemberton L, Paschal B (2005). „Mechanisms of receptor-mediated nuclear import and nuclear export”.Traffic6(3), 187–198. o.DOI:10.1111/j.1600-0854.2005.00270.x.PMID 15702987.
- ↑Stuurman N, Heins S, Aebi U (1998). „Nuclear lamins: their structure, assembly, and interactions”.J Struct Biol122(1–2), 42–66. o.DOI:10.1006/jsbi.1998.3987.PMID 9724605.
- ↑Goldman A, Moir R, Montag-Lowy M, Stewart M, Goldman R (1992). „Pathway of incorporation of microinjected lamin A into the nuclear envelope”.J Cell Biol119(4), 725–735. o.DOI:10.1083/jcb.119.4.725.PMID 1429833.
- ↑abcdeGoldman R, Gruenbaum Y, Moir R, Shumaker D, Spann T (2002). „Nuclear lamins: building blocks of nuclear architecture”.Genes Dev16(5), 533–547. o.DOI:10.1101/gad.960502.PMID 11877373.
- ↑Moir RD, Yoona M, Khuona S, Goldman RD. (2000). „Nuclear Lamins A and B1: Different Pathways of Assembly during Nuclear Envelope Formation in Living Cells”.Journal of Cell Biology151(6), 1155–1168. o.DOI:10.1083/jcb.151.6.1155.PMID 11121432.
- ↑(2002) „Alteration of nuclear lamin organization inhibits RNA polymerase II–dependent transcription”.Journal of Cell Biology156(4), 603–608. o.DOI:10.1083/jcb.200112047.PMID 11854306.
- ↑Mounkes LC, Stewart CL (2004). „Aging and nuclear organization: lamins and progeria”.Current Opinion in Cell Biology16(3), 322–327. o.DOI:10.1016/j.ceb.2004.03.009.PMID 15145358.
- ↑Ehrenhofer-Murray A (2004). „Chromatin dynamics at DNA replication, transcription and repair”.Eur J Biochem271(12), 2335–2349. o.DOI:10.1111/j.1432-1033.2004.04162.x.PMID 15182349.
- ↑Grigoryev S, Bulynko Y, Popova E (2006). „The end adjusts the means: heterochromatin remodelling during terminal cell differentiation”.Chromosome Res14(1), 53–69. o.DOI:10.1007/s10577-005-1021-6.PMID 16506096.
- ↑Schardin, Margit (1985. december 1.). „Specific staining of human chromosomes in Chinese hamster x man hybrid cell lines demonstrates interphase chromosome territories”.Human Genetics71(4), 281–287. o, Kiadó: Springer Berlin / Heidelberg. [2019. szeptember 13-i dátummal azeredetibőlarchiválva].DOI:10.1007/BF00388452.PMID 2416668.(Hozzáférés: 2015. május 29.)
- ↑Lamond, Angus I. (1998. április 24.). „Structure and Function in the Nucleus”.Science280(5363), 547–553. o.DOI:10.1126/science.280.5363.547.PMID 9554838.
- ↑Kurz, A (1996). „Active and inactive genes localize preferentially in the periphery of chromosome territories”.The Journal of Cell Biology135(5), 1195–1205. o, Kiadó: The Rockefeller University Press. [2007. szeptember 29-i dátummal azeredetibőlarchiválva].DOI:10.1083/jcb.135.5.1195.PMID 8947544.(Hozzáférés: 2015. május 29.)
- ↑NF Rothfield, BD Stollar (1967). „The Relation of Immunoglobulin Class, Pattern of Antinuclear Antibody, and Complement-Fixing Antibodies to DNA in Sera from Patients with Systemic Lupus Erythematosus”.J Clin Invest46(11), 1785–1794. o.DOI:10.1172/JCI105669.PMID 4168731.
- ↑S Barned, AD Goodman, DH Mattson (1995). „Frequency of anti-nuclear antibodies in multiple sclerosis”.Neurology45(2), 384–385. o.DOI:10.1212/WNL.45.2.384.PMID 7854544.
- ↑Böhm I. IgG deposits can be detected in cell nuclei of patients with both lupus erythematosus and malignancy.Clin Rheumatol2007;26(11) 1877-1882
- ↑Hernandez-Verdun, Daniele (2006). „Nucleolus: from structure to dynamics”.Histochem. Cell. Biol125(1–2), 127–137. o.DOI:10.1007/s00418-005-0046-4.PMID 16328431.
- ↑abLamond, Angus I. (2003. október 1.). „Nuclear substructure and dynamics”.current biology13(21), R825–828. o.DOI:10.1016/j.cub.2003.10.012.PMID 14588256.
- ↑abcCioce M, Lamond A (2005). „Cajal bodies: a long history of discovery”.Annu Rev Cell Dev Biol21,105–131. o.DOI:10.1146/annurev.cellbio.20.010403.103738.PMID 16212489.
- ↑abcPollard, Thomas D..Cell Biology.Philadelphia: Saunders (2004).ISBN 0-7216-3360-9
- ↑abcDundr, Miroslav (2001). „Functional architecture in the cell nucleus”.Biochem. J.356(Pt 2), 297–310. o.DOI:10.1042/0264-6021:3560297.PMID 11368755.
- ↑Fox, Archa. R. Sundby interjúja..Paraspeckle Size.,E-mail Correspondence. 2007. március 7.
- ↑Goebel, H.H. (1997. január 1.). „Nemaline myopathy with intranuclear rods—intranuclear rod myopathy”.Neuromuscular Disorders7(1), 13–19. o.DOI:10.1016/S0960-8966(96)00404-X.PMID 9132135.
- ↑abcMatera AG, Frey MA. (1998). „Coiled Bodies and Gems: Janus or Gemini?”.American Journal of Human Genetics63(2), 317–321. o.DOI:10.1086/301992.PMID 9683623.
- ↑Matera, A. Gregory (1998). „Of Coiled Bodies, Gems, and Salmon”.Journal of Cellular Biochemistry70(2), 181–192. o.DOI:<181::aid-jcb4>3.0.co;2-k 10.1002/(sici)1097-4644(19980801)70:2<181::aid-jcb4>3.0.co;2-k.PMID 9671224.
- ↑Saunders WS, Cooke CA, Earnshaw WC (1991). „Compartmentalization within the nucleus: discovery of a novel subnuclear region.”.Journal of Cellular Biology115(4), 919–931. o.DOI:10.1083/jcb.115.4.919.PMID 1955462
- ↑Pombo A, Cuello P, Schul W, Yoon J, Roeder R, Cook P, Murphy S (1998). „Regional and temporal specialization in the nucleus: a transcriptionally active nuclear domain rich in PTF, Oct1 and PIKA antigens associates with specific chromosomes early in the cell cycle”.The EMBO Journal17(6), 1768–1778. o.DOI:10.1093/emboj/17.6.1768.PMID 9501098.
- ↑Cellular component Nucleus speckle.UniProt: UniProtKB. (Hozzáférés: 2013. augusztus 30.)
- ↑Handwerger, Korie E. (2006. január 1.). „Subnuclear organelles: new insights into form and function”.TRENDS in Cell Biology16(1), 19–26. o.DOI:10.1016/j.tcb.2005.11.005.PMID 16325406.
- ↑Fox, Archa (2002). „Paraspeckles:A Novel Nuclear Domain”.Current Biology12(1), 13–25. o. [2012. december 8-i dátummal azeredetibőlarchiválva].DOI:10.1016/S0960-9822(01)00632-7.PMID 11790299.(Hozzáférés: 2015. május 29.)
- ↑abFox, A. (2005). „P54nrb Forms a Heterodimer with PSP1 That Localizes to Paraspeckles in an RNA-dependent Manner”.Molecular Biology of the Cell16(11), 5304–5315. o.DOI:10.1091/mbc.E05-06-0587.PMID 16148043.
- ↑Fox, Archa:Nuclear Compartments: Paraspeckles.Nuclear Protein Database, 2004. [2006. május 2-i dátummal azeredetibőlarchiválva]. (Hozzáférés: 2007. március 6.)
- ↑Nierhaus, Knud H..Protein Synthesis and Ribosome Structure: Translating the Genome.Wiley-VCH (2004).ISBN 3-527-30638-2
- ↑Nicolini, Claudio A..Genome Structure and Function: From Chromosomes Characterization to Genes Technology.Springer (1997).ISBN 0-7923-4565-7
- ↑Lehninger, Albert L..Lehninger principles of biochemistry,3rd, New York: Worth Publishers (2000).ISBN 1-57259-931-6
- ↑Moreno F, Ahuatzi D, Riera A, Palomino CA, Herrero P. (2005). „Glucose sensing through the Hxk2-dependent signalling pathway.”.Biochem Soc Trans33(1), 265–268. o.DOI:10.1042/BST0330265.PMID 15667322.PMID 15667322
- ↑Görlich, Dirk (1999). „Transport between the cell nucleus and the cytoplasm”.Ann. Rev. Cell Dev. Biol.15(1), 607–660. o.DOI:10.1146/annurev.cellbio.15.1.607.PMID 10611974.
- ↑Watson, JD. Ch9–10,Molecular Biology of the Gene,5th, Peason Benjamin Cummings; CSHL Press. (2004).ISBN 0-8053-9603-9
- ↑Lippincott-Schwartz, Jennifer (2002. március 7.). „Cell biology: Ripping up the nuclear envelope”.Nature416(6876), 31–32. o.DOI:10.1038/416031a.PMID 11882878.
- ↑abBoulikas T (1995). „Phosphorylation of transcription factors and control of the cell cycle”.Crit Rev Eukaryot Gene Expr5(1), 1–77. o.PMID 7549180.
- ↑Skutelsky, E. (1970. június 1.). „Comparative study of nuclear expulsion from the late erythroblast and cytokinesis”.J Cell Biol60(60(3)), 625–635. o.DOI:10.1016/0014-4827(70)90536-7.PMID 5422968.
- ↑Torous, DK (2000). „Enumeration of micronucleated reticulocytes in rat peripheral blood: a flow cytometric study”.Mutat Res465(465(1–2)), 91–99. o.DOI:10.1016/S1383-5718(99)00216-8.PMID 10708974.
- ↑Hutter, KJ (1982). „Rapid detection of mutagen induced micronucleated erythrocytes by flow cytometry”.Histochemistry75(3), 353–362. o.DOI:10.1007/bf00496738.PMID 7141888.
- ↑Zettler, LA (1997). „Phylogenetic relationships between the Acantharea and the Polycystinea: A molecular perspective on Haeckel's Radiolaria”.Proc Natl Acad Sci USA94(21), 11411–11416. o.DOI:10.1073/pnas.94.21.11411.PMID 9326623.
- ↑Horton, TR (2006). „The number of nuclei in basidiospores of 63 species of ectomycorrhizal Homobasidiomycetes”.Mycologia98(2), 233–238. o.DOI:10.3852/mycologia.98.2.233.PMID 16894968.
- ↑Adam RD (1991. december 1.). „The biology of Giardia spp”.Microbiol. Rev.55(4), 706–32. o.PMID 1779932.
- ↑McInnes, A (1988). „Interleukin 4 induces cultured monocytes/macrophages to form giant multinucleated cells”.J Exp Med167(2), 598–611. o.DOI:10.1084/jem.167.2.598.PMID 3258008.
- ↑Goldring, SR (1987). „Human giant cell tumors of bone identification and characterization of cell types”.J Clin Invest79(2), 483–491. o.DOI:10.1172/JCI112838.PMID 3027126.
- ↑Watkins, Brynmor A, Alberta E. „Syncytium formation induced by human immunodeficiency virus type 1 isolates correlates with affinity for CD4.”.Journal of General Virology78(10), 2513–2522. o.DOI:10.1099/0022-1317-78-10-2513.ISSN1465-2099.
- ↑(2012) „Tertiary endosymbiosis in two dinotoms has generated little change in the mitochondrial genomes of their dinoflagellate hosts and diatom endosymbionts”.PLOS ONE7(8), e43763. o.DOI:10.1371/journal.pone.0043763.
- ↑Pennisi E. (2004). „Evolutionary biology. The birth of the nucleus”.Science305(5685), 766–768. o.DOI:10.1126/science.305.5685.766.PMID 15297641.
- ↑C.Michael Hogan. 2010.Archaea.eds. E.Monosson & C.Cleveland, Encyclopedia of Earth. National Council for Science and the Environment, Washington DC.
- ↑Margulis, Lynn.Symbiosis in Cell Evolution.San Francisco: W. H. Freeman and Company,206–227. o. (1981).ISBN 0-7167-1256-3
- ↑Lopez-Garcia P, Moreira D. (2006). „Selective forces for the origin of the eukaryotic nucleus”.BioEssays28(5), 525–533. o.DOI:10.1002/bies.20413.PMID 16615090.
- ↑Fuerst JA. (2005). „Intracellular compartmentation in planctomycetes”.Annu Rev Microbiol.59,299–328. o.DOI:10.1146/annurev.micro.59.030804.121258.PMID 15910279.
- ↑Hartman H, Fedorov A. (2002). „The origin of the eukaryotic cell: a genomic investigation”.Proc Natl Acad Sci U S A.99(3), 1420–1425. o.DOI:10.1073/pnas.032658599.PMID 11805300.
- ↑Bell PJ (2001. szeptember 1.). „Viral eukaryogenesis: was the ancestor of the nucleus a complex DNA virus?”.J. Mol. Evol.53(3), 251–6. o.DOI:10.1007/s002390010215.PMID 11523012.
- ↑Takemura M (2001). „Poxviruses and the origin of the eukaryotic nucleus”.J Mol Evol52(5), 419–425. o.DOI:10.1007/s002390010171.PMID 11443345.
- ↑Villarreal L, DeFilippis V (2000). „A hypothesis for DNA viruses as the origin of eukaryotic replication proteins”.J Virol74(15), 7079–7084. o.DOI:10.1128/JVI.74.15.7079-7084.2000.PMID 10888648.
- ↑Bell PJ (2006. november 1.). „Sex and the eukaryotic cell cycle is consistent with a viral ancestry for the eukaryotic nucleus”.J. Theor. Biol.243(1), 54–63. o.DOI:10.1016/j.jtbi.2006.05.015.PMID 16846615.
- ↑de Roos AD (2006). „The origin of the eukaryotic cell based on conservation of existing interfaces”.Artif Life12(4), 513–523.. o.DOI:10.1162/artl.2006.12.4.513.PMID 16953783.
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben aCell nucleuscímű angol Wikipédia-szócikkezen változatánakfordításán alapul.Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
További információk
[szerkesztés]- Goldman, Robert D. (2002). „Nuclear lamins: building blocks of nuclear architecture”.Genes & Dev.16(5), 533–547. o.DOI:10.1101/gad.960502.PMID 11877373.
- Görlich, Dirk (1999). „Transport between the cell nucleus and the cytoplasm”.Ann. Rev. Cell Dev. Biol.15,607–660. o.DOI:10.1146/annurev.cellbio.15.1.607.PMID 10611974.
- Lamond, Angus I. (1998. április 24.). „Structure and Function in the Nucleus”.Science280(5363), 547–553. o.DOI:10.1126/science.280.5363.547.PMID 9554838.
- Pennisi E. (2004). „Evolutionary biology. The birth of the nucleus”.Science305(5685), 766–768. o.DOI:10.1126/science.305.5685.766.PMID 15297641.
- Pollard, Thomas D..Cell Biology.Philadelphia: Saunders (2004).ISBN 0-7216-3360-9
- sejtmag(magyar nyelven). Sulinet - Sebőkné Orosz Katalin. [2013. szeptember 14-i dátummal azeredetibőlarchiválva]. (Hozzáférés: 2015. június 21.)




