Diolok


Adiolokvagyglikolokolyanszerves vegyületek,amelyekben kéthidroxilcsoport(−OH csoport) található.[1]A funkciós csoportok páros előfordulása meglehetősen gyakori, így számos alkategóriát különböztetnek meg. A természetben a leggyakoribb diolok acukrokés ezek polimerjei, acellulóz.Az ipar által leggyakrabban használt diol az etilénglikol. További példák diolokra, melyekben a két hidroxilcsoport egymástól távolabb helyezkedik el: 1,4-butándiol (HO–(CH2)4–OH ),biszfenol-A,propilén-1,3-diol vagy béta-propilén-glikol (HO–CH2–CH2–CH2–OH).
Csoportosításuk
[szerkesztés]Geminális diolok
[szerkesztés]Ageminális diolokbanugyanahhoz a szénatomhoz két hidroxilcsoport kapcsolódik. Ilyen például ametándiol(H2C(OH)2), mely a formaldehid hidratált formája. Másik példa a (F3C)2C(OH)2,ahexafluoracetonhidratált formája.
Vicinális diolok
[szerkesztés]A vicinális diolokban a két hidroxilcsoport vicinális helyzetű, azaz szomszédos atomokhoz kapcsolódnak. Glikoloknak is nevezik őket. Vicinális glikol például a fagyállókban gyakran használt 1,2-etándiol vagyetilénglikol(HO−(CH2)2−OH) és a propán-1,2-diol vagy alfa-propilénglikol(HO−CH2−CH(OH)−CH3), melyet az élelmiszer- és gyógyszeripar használ, de a kevésbé mérgező fagyállók komponenseként is alkalmazzák.
Diszjunkt diolok
[szerkesztés]A két hidroxilcsoportot egymástól messzebb tartalmazó diolokra példa az1,4-butándiol(HO−(CH2)4−OH) és abiszfenol-A.
Alifás diolok
[szerkesztés]| A diol lánca | Hidroxilcsoport a szomszédos szénen (vicinális diolok) | Hidroxilcsoport nem szomszédos szénatomokon |
|---|---|---|
| Egyenes | etilénglikol | 1,3-propándiol;1,4-butándiol;1,5-pentándiol;1,8-oktándiol |
| Elágazó | 1,2-propándiol;1,2-butándiol;2,3-butándiol | 1,3-butándiol;1,2-pentándiol;etohexadiol;p-mentán-3,8-diol;2-metil-2,4-pentándiol |
Előállításuk
[szerkesztés]Mivel a diolok gyakran előfordulófunkciós csoportok,számos módszert dolgoztak ki előállításukra.
- Vicinális diolok állíthatók előalkénekoxidációjával, rendszerint híg savaskálium-permanganátfelhasználásával. Lúgos kálium-permanganát alkalmazásakor a sötét ibolyaszín zöldre változik, míg a savas kálium-permanganát teljesen elszíntelenedik.
- Alkének hasonló módonozmium-tetroxiddalis vicinális diolokká oxidálhatók.
- Alkénekhidrogén-peroxiddalepoxidképződése közben reagálnak, melyből hidrolízissel diol keletkezik, mint például atransz-ciklohexándiolszakaszos[2]vagy folyamatos mikroreaktoros[3]szintézisében:
- A Sharpless aszimmetriás dihidroxilezéssel királis diolok állíthatók elő alkénekből ozmát reagens és királis katalizátor felhasználásával.
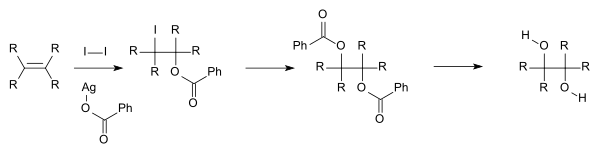
- Másik lehetőség a Woodward-féle cisz-hidroxilezés (cisz-diol) és az alább bemutatott, hasonló Prévost-reakció (anti-diol). Mindkét módszer jódot és ezüst karbonsavsót használ.
- APrins-reakcióban1,3-diolok állíthatók előformaldehidésalkénreagáltatásával.
- Geminális diolok képezhetők ketonok hidratálásával.
Reakcióik
[szerkesztés]Diolok általános reakciói
[szerkesztés]A diolok csakúgy, mint az alkoholok, észter- vagy éterképződési reakciókba lépnek.
A diolokat, például az etilénglikolt polimerizációs reakciókban komonomerként alkalmazzák egyes poliészterek és poliuretánok előállítása során. Ahhoz, hogy a polimerizáció ismételt észteresítési lépésekkel tovább folytatódjon, egy másik, két azonos funkciós csoportot tartalmazó monomer is szükséges. Ez lehet például dioil-diklorid vagy disav.
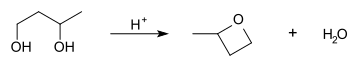
A diolok savkatalízis hatására gyűrűs éterré alakíthatók, ez a reakció a diol ciklizáció. Ekkor először a hidroxilcsoport protonálódik, majd a másik hidroxilcsoport intramolekuláris nukleofil szubsztitúciós reakcióban megtámadja az elektronhiányos szénatomot. Amennyiben a szénlánc elég hosszú ahhoz, hogy ne lépjen fel nagymértékű gyűrűfeszülés, gyűrűs éter keletkezik.
Vicinális diolok
[szerkesztés]A glikolhasítás során a vicinális diolokban a C–C kötés keton vagy aldehid funkciós csoport keletkezése közben felhasad.
Geminális diolok
[szerkesztés]A szerves geminális diolok általában könnyen dehidratálódnak, éskarbonilcsoporttáalakulnak. Aszénsav((HO)2C=O) például instabil,szén-dioxiddá(CO2) és vízzé (H2O) alakul át. Ritkán azonban akémiai egyensúlya geminális diol keletkezésének irányába van eltolódva. Például amikorformaldehid(H2C=O) oldódik vízben, a geminális diolmetándiol(H2C(OH)2) képződése a kedvezményezett. További példák adekahidroxiciklopentán(C5(OH)10) ésdodekahidroxiciklohexán(C6(OH)12), melyek stabil gyűrűs geminális diolok, míg a megfelelő oxovegyületek (C5O5és C6O6) vélhetően instabilak.
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben aDiolcímű angol Wikipédia-szócikkezen változatánakfordításán alapul.Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Jegyzetek
[szerkesztés]- ↑March, Jerry(1985),Advanced Organic Chemistry: Reactions, Mechanisms, and Structure(3rd ed.), New York: Wiley,ISBN 0-471-85472-7
- ↑trans-cyclohexanediolOrganic Syntheses,Coll. Vol. 3, p.217 (1955); Vol. 28, p.35 (1948)http:// orgsynth.org/orgsyn/pdfs/CV3P0217.pdf.
- ↑Advantages of Synthesizing trans-1,2-Cyclohexanediol in a Continuous Flow Microreactor over a Standard Glass ApparatusAndreas Hartung, Mark A. Keane, and Arno KraftJ. Org. Chem.2007,72, 10235-10238doi:10.1021/jo701758p