Metabolisme


Metabolisme(bahasa Yunani:μεταβολισμος,metabolismos,'perubahan') adalah seluruhreaksibiokimiayang bertujuan untuk mempertahankankehidupanpada suatuorganisme.Proses ini memungkinkan organisme untuk tumbuh, bereproduksi, mempertahankan struktur, dan merespons lingkungannya. Metabolisme juga dapat diartikan sebagai semua reaksi kimia yang terjadi pada organisme hidup, di antaranyapencernaandan perpindahan zat di dalam sel dan di antara sel yang berbeda. Di dalam sel, reaksi kimia terjadi secara berantai sehingga produk yang dihasilkan oleh suatu reaksi akan memasuki reaksi lain. Reaksi-reaksi yang saling terhubung ini disebut metabolisme perantara atau metabolisme intermediat dan setiap reaksinyadikatalisisolehenzim.
Secara umum, metabolisme memiliki dua arah lintasan reaksikimia organik,yaitukatabolisme(reaksi untuk menghasilkan energi dengan cara menguraisenyawa organik), seperti pemecahanglukosamenjadiasam piruvatoleh prosesrespirasi selulerdananabolisme(reaksi yang memerlukan energi untuk menyusun [sintesis] senyawa organik sepertiprotein,karbohidrat,lipid,danasam nukleatdari molekul-molekul yang diperlukan).[1]Tiga tujuan utama metabolisme yaitu mengonversi makanan menjadienergiuntuk menjalankan proses pada tingkat seluler, mengonversi makanan menjadi bahan baku penyusun protein, lipid, asam nukleat, dan beberapa jenis karbohidrat, serta mengeliminasizat sisa metabolisme.
Reaksi kimia pada proses metabolisme terbagi atas beberapalintasan metabolikyang mengubah suatu senyawa menjadi senyawa yang berbeda melalui beberapa tahapan. Tiap tahapan dalam lintasan difasilitasi denganenzimyang bersifat spesifik. Fungsi enzim sangat penting pada metabolisme karena membantu organisme menjalankan reaksi yang dinginkan karena reaksi ini membutuhkan energi dan tidak terjadi secara otomatis. Enzim memasangkan reaksi yang difasilitasinya denganreaksi spontanyang menghasilkan energi sehingga enzim berfungsi sebagai katalis yang mempercepat terjadinya reaksi sekaligus mengatur laju reaksi metabolik. Reaksi kimia dalam metabolisme muncul sebagai respons atas perubahan lingkungan sel atau sinyal dari sel lain.
Pada setiap proses dalam metabolisme, reaksi kimia juga melibatkan sejumlahsubstratyang bereaksi dengan enzim sebagaikatalispada jenjang-jenjang reaksi guna menghasilkansenyawa intermediat,yang menjadisubstratpada jenjang reaksi berikutnya. Keseluruhanpereaksi kimiayang terlibat pada suatu jenjang reaksi disebutmetabolom.Semua ini dipelajari pada suatu cabang ilmubiologiyang disebutmetabolomika.Laju metabolisme basalsuatu organisme adalah ukuran jumlah energi yang dikonsumsi oleh semua reaksi kimia yang terjadi.
Sistem metabolisme suatu organisme menentukan senyawa mana yang merupakannutrisidan senyawa mana yangberacunbagi tubuh. Sebagai contoh, beberapa jenisprokariotamemakaihidrogen sulfidasebagai nutrien walaupungasini bersifat racun bagi hewan. Namun, terdapat ciri khusus dari metabolisme yang umumnya ditemukan pada hampir seluruh spesies yang berbeda, seperti gugusasam karboksilatyang diketahui merupakan sebagai zat antara padasiklus asam sitratpada semua organisme yang diketahui manusia. Senyawa ini juga ditemukan pada spesies yang sangat berbeda struktur biologisnya, seperti bakteri uniselulerEschirichia colidan organismemultiselulerberukuran besar sepertigajah.Kesamaan yang terdapat pada lintasan metabolisme ini mungkin terjadi akibat keberadaan senyawa-senyawa tersebut pada awalsejarah evolusidan retensi kemunculan mereka yang tinggi pada beragam jenis hewan karenaefikasiyang ditimbulkan. Metabolisme sel kanker sangat berbeda dengan sel normal dan perbedaanya ini dapat digunakan sebagai intervensi terapeutik pada penyakitkanker.
Sejarah[sunting|sunting sumber]
Etimologi[sunting|sunting sumber]
Terminologi metabolisme diturunkan daribahasa Prancis"métabolisme"ataubahasa Yunani Kunoμεταβολή– "Metabole"yang dialihbahasakan menjadi" sebuah perubahan "yang diturunkan dari kataμεταβάλλ– "Metaballein"yang dialihbahasakan menjadi" untuk mengubah ".[2]
Filsafat Yunani[sunting|sunting sumber]

Buku karya dariAristotelesberjudulDe Partibus Animaliummenjelaskan cukup detail tentangpandangannya terhadap metabolismeyang digambarkan dengan sebuah model diagram alir terbuka. Dia mempercayai bahwa pada setiap langkah di dalam proses saat materi dari makanan ditransformasikan, panas keluar sebagaielemen klasikdari api dan materi residu dieksresikan sebagaiurine,empedu,atautinja.[3]
Ilmu kedokteran oleh ilmuwan Islam[sunting|sunting sumber]
Ibnu al-Nafismenjelaskan metabolisme pada abad ke-13 dengan menyatakan, "Baiktubuhdan bagian-bagiannya berada dalam kondisi penguraian dan pemberiannutrisisecara berkesinambungan sehingga mereka mengalami perubahan permanen yang tidak dapat dihindari. "[4]
Eksperimen awal[sunting|sunting sumber]

Eksperimen terkontrol terhadap metabolisme pada manusia pertama kali diterbitkan olehSantorio Santoriopada tahun 1614 di dalam bukunya,Ars de statica medecinayang membuatnya terkenal diEropa.Dia mendeskripsikan rangkaian percobaan yang dilakukannya, yang melibatkan penimbangan dirinya sendiri pada sebuah kursi yang digantung pada sebuah timbangan besar (lihat gambar) sebelum dan sesudahmakan,tidur,bekerja,berhubungan seksual,berpuasamakan atauminum,danbuang air besar.Dia menemukan bahwa bagian terbesar makanan yang dimakannya hilang dari tubuh melaluiperspiratio insensibilis(mungkin dapat diterjemahkan sebagai "keringatan yang tidak tampak").[5]
Pada studi awal, mekanisme proses metabolisme tidak dapat diidentifikasi dan dipercaya bahwaenergi vitalmenggerakkan kehidupan.[6]Pada abad ke-19,Louis Pasteurmengambil kesimpulan bahwafermentasimengkatalisis senyawa di dalam selkhamiryang dia sebut "fermen" ketika dia mempelajari proses fermentasi gula menjadi alkohol oleh khamir. Dia menulis bahwa "fermentasi alkohol merupakan suatu kondisi yang berkorelasi dengan kehidupan dan pengaturan oleh sel khamir, bukan kematian atau pembusukan sel tersebut".[7]Penemuan ini selaras dengan publikasiFriedrich Wöhlerpada tahun 1828 dalam karya tulisnya tentang sintesis kimiawiurea,yang dikenal sebagai senyawa organik pertama yang dipersiapkan dari prekursor anorganik lengkap. Penelitian ini membuktikan bahwa senyawa organik dan reaksi kimia yang ditemukan di dalam sel tidak berbeda secara prinsip dengan reaksi kimiawi yang berlangsung di tempat lain.[8]
Penemuan enzim pada awal abad ke-20 olehEduard Buchneryang memisahkan studi reaksi kimiawi metabolisme dari studi sel biologis lain menjadi awal mula daribiokimia.[9]Pengetahuan biokimia berkembang pesat selama awal abad ke-20. Salah satu ahli biokimia modern yang paling terkemuka ialahHans Krebsyang memberikan kontibusi besar kepada studi metabolisme. Dia menemukan siklus urea dan kemudian bekerja sama denganHans Kornbergmenemukansiklus asam sitratdansiklus glioksilat.[10]Penelitian biokimia modern telah berkembang dengan pesat setelah penemuankromatografipada tahun 1904,[11]difraksi sinar-X,spektroskopi resonansi magnet inti,pelabelan isotop,mikroskop elektron,dansimulasi dinamika molekular.
Senyawa biokimia kunci[sunting|sunting sumber]
Sebagian besar struktur yang menyusun hewan, tumbuhan, dan mikroorganisme tersusun atas empat gugus molekul dasar: asam amino, karbohidrat, asam nukleat, danlipid.Karena keempatnya sangat vital bagi kehidupan, reaksi metabolik bertujuan untuk membentuk molekul-molekul tersebut selama proses penyusunanseldan jaringan, atau menguraikan dan menggunakan mereka untuk mendapatkan energi melalui proses pencernaan. Senyawa-senyawa biokimia ini dapat digabungkan untuk membentukpolimersepertiDNAdan protein yang merupakanmakromolekulesensial bagi kehidupan.[12]
| Jenis molekul | Nama monomer | Nama polimer | Contoh bentuk polimer |
|---|---|---|---|
| Asam amino | Asam amino | Protein (tersusun ataspolipeptida) | Protein seratdanprotein globular |
| Karbohidrat | Monosakarida | Polisakarida | Amilum,glikogen,danselulosa |
| Asam nukleat | Nukleotida | Polinukleotida | DNA danRNA |
Asam amino dan protein[sunting|sunting sumber]
Protein terdiri dari rangkaian asam amino yang disusun menjadi sebuah rantai yang disatukan olehikatan peptida.Sebagian besar protein berfungsi sebagai enzim yang dapatmengkatalisisreaksi kimia pada proses metabolisme. Protein-protein lainnya memiliki fungsi struktural atau mekanik seperti sebagai penyusunsitoskeleton,suatu sistemperancahyang berfungsi untuk mempertahankan bentuk sel.[13]Beberapa fungsi protein yang lain di antaranya memproduksi cahaya pada kunang-kunang, membantu transpor oksigen dalam darah, serta menjadi komponen penyusunkeratin.[14]Asam amino berkontribusi dalam proses metabolisme energi seluler sebagai penyedia sumber karbon untuk memulai siklus asam sitrat, terutama ketika sumber energi utama sepertiglukosamenipis atau ketika sel mengalami represi katabolit kembali, misalnya akibat stres metabolik.[15]
Lipid[sunting|sunting sumber]

Lipid adalah gugus senyawa biokimia yang paling beragam. Fungsi struktural utamanya adalah sebagai bagian darimembran biologis,baik sebagai membran internal (misalnya membran padaretikulum endoplasma), membran eksternal (sepertimembran sel), atau sebagai sumber energi dan tempat penyimpanan energi.[16]Lipid didefinisikan sebagai molekul biologis yang bersifathidrofobikatauamfifilik,tetapi dapat terlarut padapelarut lipid,sepertieter,benzena,aseton,ataukloroform.[17]Lipid adalah gugus besar senyawa yang mengandungasam lemakdangliserol;gliserol yang melekat pada asam lemakesterdikenal dengan namatriasilgliserida[18]Selain itu, terdapat banyak variasi bentuk lipid yang lain, misalnyasfingosinayang merupakan rantai utamasfingomielindan gugushidrofiliksepertifosfatyang ada padafosfolipid.Steroidmerupakan salah satu kelompok utama dari lipid.[19]
Karbohidrat[sunting|sunting sumber]

Karbohidrat adalah senyawaaldehidadanketondengan banyak gugushidroksilyang menempel dalam bentuk rantai lurus atau cincin. Karbohidrat adalah molekul biologis paling berlimpah dan memiliki banyak fungsi, seperti tempat penyimpanan atau transpor energi (amilum danglikogen) dan juga merupakan komponen penyusun dari suatu senyawa pada organisme (selulosapada tumbuhan dankitinpada hewan).[20]Unit paling sederhana dari karbohidrat dikenal dengan namamonosakarida.Terdapat tiga jenis monosakarida, yaitugalaktosa,fruktosadan senyawa yang paling penting bagi organisme, yaituglukosa.Monosakarida akan saling terikat dengan monoskarida lain dan membentukpolisakaridadalam pelbagai bentuk yang tak terhitung jumlahnya.[21]
Nukleotida[sunting|sunting sumber]
Dua jenis asam nukleat, yaitu DNA dan RNA merupakan polimer dari nukleotida. Tiap nukleotida disusun atas fosfat yang menempel pada gugus gularibosaataudeoksiribosayang menempel padabasa nitrogen.Asam nukleat memiliki fungsi penting sebagai media penyimpanan dan penggunaan informasi genetik yang akan dinterpretasi melalui prosestranskripsidantranslasidalam prosesbiosintesis protein.[22]Informasi genetik yang terkandung di dalam asam nukleat dilindungi oleh mekanismeperbaikan DNAdan diperbanyak pada prosesreplikasi DNA.Banyakvirusmemilikigenom RNA,sepertiHIV,yang menggunakan prosestranskripsi balikuntuk membuat templat DNA dari genom virus RNA-nya.[23]Molekul RNA yang berada di dalamribozim,sepertispliseosomatau ribosom, bekerja mirip dengan enzim yang mampu mengkatalisis reaksi kimia.Nukleosidaadalah penyusun nukleotida yang merupakanbasa nukleotidayang menempel pada gula ribosa. Basa nukleotida memiliki bentuk cincinheterosiklikyang mengandung nitrogen yang diklasifisikasikan menjadi dua macam, yaitupurinaataupirimidina.Nukleotida juga dapat berfungsi sebagaikoenzimpada reaksi transfer gugus metabolis.[24]
Koenzim[sunting|sunting sumber]

Metabolisme melibatkan banyak reaksi kimia, tetapi sebagian besar reaksi tersebut dikategorikan ke dalam jenis reaksi sederhana yang melibatkan perpindahangugus fungsionalsuatu atom serta ikatannya di dalam suatu molekul.[25]Kimia sederhana ini memungkinkan pengunaaan kelompok senyawa intermediat untuk membawa gugus senyawakimiaini berpindah di antara reaksi-reaksi yang berbeda.[26]Kelompok senyawa intermediat yang berfungsi untuk memindahkan gugus tersebut dikenal dengan nama koenzim. Tiap kelompok reaksi dikendalikan oleh suatu koenzim tertentu, yang menjadisubstratuntuk kelompok enzim yang memproduksinya sekaligus enzim yang memakainya. Koenzim ini terus-menerus dibuat, dipakai, dan didaur ulang.[27]

Salah satu koenzim utama yang ada di dalam tubuh ialah ATP (adenosina trifosfat) yang merupakan sumber energi universal di dalam sel. Jenis nukleotida ini digunakan untuk memindahkan energi kimiawi di antara reaksi-reaksi kimia yang berbeda. Hanya ada sedikit ATP di dalam tubuh, tetapi ATP terus-menerus diregenerasi sehingga tubuh manusia dapat menggunakan ATP dengan jumlah yang setara dengan berat badan tubuhnya.[27][28]ATP bertindak sebagai jembatan penghubung katabolisme dan anabolisme. Katabolisme menguraikan molekul dan katabolisme menyatukannya kembali. Reaksi katabolisme menghasilkan ATP dan reaksi anabolis memakainya. ATP juga berfungsi sebagai pembawa gugus fosfat dalam reaksifosforilasi.[29]
Vitaminmerupakan senyawa organik yang dibutuhkan dalam jumlah sedikit dan tidak dapat diproduksi oleh sel di dalam tubuh manusia. Padanutrisi manusia, vitamin berfungsi sebagai koenzim, setelah mengalami modifikasi. Misalnya, vitamin larut air akan mengalami fosforilasi dan berpasangan dengan nukleotida ketika dipakai oleh sel.[30]Nikotinamida adenina dinukleotida(NAD+) adalah senyawa turunan vitamin B3(niasin) yang merupakan koenzim penting yang bertindak sebagai reseptor molekul hidrogen. Ratusan jenis enzimdehidrogenasemelepas elektron dari substrat danmereduksiNAD+menjadi NADH. Koenzim yang telah direduksi ini kemudian menjadi substrat bagi enzim reduktase di dalam sel untuk mereduksi substrat.[31]Nikotinamida adenina dinukleotidaeksis dalam bentuk yang saling berhubungan di dalam sel, yaitu NADH dan NADPH. Bentuk NAD+/NADH lebih penting pada reaksi katabolis, sedangkan NADP+/NADPH dipakai pada reaksi anabolik.[32]
Mineral dan kofaktor[sunting|sunting sumber]

Senyawa anorganik memiliki peran penting pada proses metabolisme. Beberapa senyawa berada dalam jumlah yang berlimpah (natriumdankalium), sedangkan senyawa yang lain hanya berfungsi dalam konsentrasi yang kecil di dalam tubuh. Sekitar 99% berat badan pada manusia terdiri darikarbon,nitrogen,kalsium,natrium, kalium,klorin,hidrogen,oksigen,danfosfor.Senyawa organikpenyusun tubuh, seperti lipid, protein, dan karbohidrat mengandung sebagian besar karbon dan nitrogen sebagai salah satu penyusunnya. Sebagian besar molekul oksigen dan hidrogen berada dalam bentuk air di dalam tubuh.[33]
Senyawa anorganik berfungsi sebagaielektrolitdi dalam tubuh. Elektrolit penting dalam tubuh terdiri atas enam elektrolit, yaituiodin,kalium,klorida,bikarbonat,fosfat,dankalsium.Gradien konsentrasi ionyang stabil padamembran seldiperlukan untuk mempertahankantekanan osmotikdanpH.[34]Ion memiliki fungsi penting padaototdansarafsebagaipotensial aksidi dalam jaringan yang dihasilkan oleh pertukaran ion antaracairan ektraselulerdan cairan di dalam sel, yaitusitosol.[35]Elektrolit keluar masuk melalui protein di dalam membran sel yang disebutsaluran ion.Contohnya, yaitu pada proseskontraksi ototyang ditentukan oleh perpindahan kalsium, iodin, dan kalium melalui saluran ion di dalam membran sel dantubulus T[36]
Logam transisibiasanya terdapat dalam bentukunsur kelumitdi dalam organisme.Sengdanbesiadalah unsur paling berlimpah dari kategori tersebut.[37]Logam-logam ini berfungsi sebagai kofaktor pada beberapa jenis protein yang bersifat esensial untuk aktivitas enzimkatalasedan protein pembawa protein, yaitu hemoglobin.[38]Kofaktor logam terikat dengan situs spesifik di dalam protein, meskipun akan berubah seiring proses katalisis. Zat ini akan kembali menjadi bentuk semula pada akhir reaksi katalisis. Mikronutrien logam masuk ke dalam organisme dengan menggunakan transporter spesifik dan terikat dengan protein penyimpanan, sepertiferitindanmetalotioneinketika tidak digunakan.[39][40]
Katabolisme[sunting|sunting sumber]
Katabolisme adalah serangkaian reaksi pada proses metabolisme yang menguraikan molekul-molekul besar. Reaksi-reaksi yang dimaksud ialah mengurai dan mengoksidasi molekul makanan. Tujuan dari reaksi katabolik adalah untuk menyediakan energi dan komponen yang dibutuhkan oleh reaksi anabolik untuk rangka menyusun molekul.[41]Keadaan alamiah suatu reaksi katabolis berbeda-beda tergantung organismenya. Organisme-organisme tersebut dapat diklasifikasikan berdasarkan sumber energi dan karbon (pengelompokansumber nutrisi primer) yang dapat dilihat pada tabel dibawah. Molekul organik digunakan sebagai sumber energi oleh kelompokorganotrof,sedangkanlitotrofmenggunakan molekul anorganik sebagai substratnya.Fototrofmenangkap sinar matahari sebagaisumber energi kimiawi.[42]Walaupun begitu, seluruh bentuk reaksi metabolisme yang berbeda bergantung pada reaksiredoksyang melibatkan transfer elektron dari donor molekul yang telah tereduksi, sepertimolekul organik,air,amonia,hidrogen sulfidaatauion feroterhadap molekul aseptor, yaituoksigen,nitrat,atausulfat.[43]
Klasifikasi organisme berdasarkan metabolismenya[44]
| Sumber Energi | cahaya matahari | foto- | -trof | ||
| molekul yang belum terbentuk | kemo- | ||||
| Donor elektron | Senyawa organik | organo- | |||
| Senyawa anorganik | lito- | ||||
| Carbon source | Senyawa organik | hetero- | |||
| Senyawa anorganik | auto- | ||||
Pada umumnya, reaksi katabolis pada hewan dapat dibedakan menjadi tiga tahap utama. Pertama, makromolekul seperti protein,polisakarida,danlipiddicerna menjadi komponen yang lebih kecil di luar sel. Selanjutnya, molekul-molekul kecil ini diambil oleh sel untuk dikonversi menjadi molekul yang lebih kecil lagi yang biasanya dalam bentukasetil koenzim A(Asetil-KoA) yang menghasilkan energi. Akhirnya, gugus asetil pada KoA dioksidasi oleh air dan karbondioksida melalui prosessiklus asam sitratdanrantai transpor elektronyang menghasilkan energi yang telah tersimpan dengan cara mereduksinikotinamida adenina dinukleotida(NAD+) menjadi NADH.[45]
Pencernaan[sunting|sunting sumber]

Makromolekul, seperti pati, selulosa atau protein tidak dapat langung masuk ke dalam sel sehingga harus diurai menjadi ukuran lebih kecil untuk dapat digunakan dalam reaksi metabolisme di dalam sel. Beberapa kelompok enzim berbeda berfungsi mencerna polimer-polimer tersebut.Enzim-enzim pencernaantersebut ialahproteaseyang mencerna protein menjadi asam amino, sekaligus kelompok enzimglikosida hidrolaseyang mencerna polisakarida menjadi gula yang lebih sederhana, yaitumonosakarida.[46]
Mikroorganisme menghasilkan enzim pencernaan ke sekelilingnya,[47][48]sedangkan hewan menghasilkan enzim dari sel spesifik di dalam usus, termasuk di antaranyalambungdanpankreassertakelenjar saliva.[49]Asam amino dikeluarkan oleh enzim ekstraseluler, lalu dipompa ke dalam sel oleh proteintranspor aktif.[50][51]
Katabolisme karbohidrat[sunting|sunting sumber]
Glikolisis[sunting|sunting sumber]
Glikolisisadalah proses metabolisme yang mengubah glukosa menjadi piruvat, menghasilkan dua mol ATP, dua mol NADH, dan dua molasam piruvatper mol glukosa.[52]Glikolisis dimulai dengan pengambilan glukosa ekstraseluler dan pengolahan glukosa intraseluler berikutnya dalam sitosol untuk akhirnya menghasilkan piruvat bersama dengan berbagai produk lainnya yang akan dikonversi menjadi ATP sebagai sumber energi.[53]Asam piruvat merupakan senyawa intermediat pada beberapa lintasan metabolis. Mayoritasnya dipakai dalam keadaanaerobikuntuk dikonversi menjadi asetil-KoA dalam proses glikolisis yang selanjutkan dipakai dalamsiklus asam sitrat.Meskipun sebagian besar ATP dihasilkan dari siklus asam sitrat tetapi NADH merupakan produk terpenting. NADH diproduksi melalui oksidasi asetil-Koa menggunakan bahan baku NAD+Proses oksidasi ini mengeluarkan karbondioksida sebagai zat sisanya.[54]Dalam kondisi anaerobik, piruvat direduksi menjadilaktatolehlaktat dehidrogenase.Dengan adanya oksigen,mitokondriadapat sepenuhnya mengoksidasi piruvat dan NADH dari glikolisis, menghasilkan hingga 36 mol ATP per mol glukosa menggunakanfosforilasi oksidatif.[55]
Lintasan pentosa fosfat[sunting|sunting sumber]
Lintasan pentosa fosfatatau lintasan fosfoglukonat adalah lintasan alternatif penguraian glukosa yang terjadi di sitosol dan menyediakan beberapa tujuan utama yang mendukungproliferasidan kelangsungan hidup sel. Pertama, dan yang paling terkenal, lintasan pentosa fosfat memungkinkan pengalihan senyawa antara dari lintasan glikolitik menuju produksi prekursor nukleotida dan asam amino yang diperlukan untuk pertumbuhan dan proliferasi sel. lintasan ini melibatkan cabang nonoksidatif dari lintasan pentosa fosfat. Fungsi kunci kedua dari lintasan pentosa fosfat yaitu menghasilkan reduksi ekuivalen NADPH, yang memiliki peran penting dalam pemeliharaan lingkungan redoks seluler yang menguntungkan dan juga diperlukan untuk sintesis asam lemak. lintasan ini melibatkan cabang oksidatif dari cabang pentosa fosfat.[56]
Glikogenolisis[sunting|sunting sumber]
Glikogenadalah bentuk penyimpanan polimer dari senyawa glukosa.Glikogenolisisyaitu proses pemecahan glikogen yang terjadi di sel otot dan sel hati dalam merespons hormonepinefrindanglukagon.Pada kondisi kelaparan atau bahaya, tubuh membutuhkan glukosa dalam jumlah yang tinggi. Kondisi ini menyebabkan selalfa pankreasakan merilis glukagon, sementara itukelenjar adrenalakan merilis epinefrin. Di dalam hati, glukagon dan epinefrin berikatan padaGPCRyang berbeda, namun keduanya berinteraksi dan mengaktifkansubunit protein alfa Gsyang sama. Karena itu, kedua hormon menghasilkan respons metabolisme yang sama, yaitu aktivasiadenilat siklasedan peningkatan levelcAMP.[57]
Glikogenolisis melibatkan proses pembuangan residu glukosa dari satu ujung polimer dengan reaksifosforolisis,yang dikatalisis olehglikogen fosforilase(GP) untuk menghasilkan glukosa-1-fosfat.Glukosa-1-fosfatselanjutnya dikonversi menjadiglukosa-6-fosfat.Proses ini terjadi baik di sel otot maupun sel hati. Pada sel otot, glukosa-6-fosfat masuk ke dalam siklus glikolisis dan dimetabolisme mejadi ATP yang digunakan untukkontraksi otot.Sedangkan di sel hati, glukosa-6-fosfat diubah menjadi glukosa. Kondisi ini disebabkan oleh enzim bernamafosfataseyang ada di sel hati. Enzim ini mampu menghidrolisis glukosa-6-fosfat menjadi glukosa sehingga di hati, penyimpanan glikogen diuraikan menjadi glukosa, lalu dengan cepat dikeluarkan ke darah, lalu disebar ke jaringan lain, seperti otot dan otak, untuk memberi makan sel-sel tersebut.[57]
Kinase protein A(PKA) aktif mendorong konversi glikogen menjadi glukosa-1-fosfat melalui dua cara yaitu menghambat sintesis glikogen dan menstimulasi degradasi glikogen. Untuk cara pertama, PKA memfosforilasi enzim penting dalam sintesis glikogen yaituglikogen sintase(GS), di mana jika enzim ini difosforilasi (diberi fosfat) membuat enzim tidak aktif. Untuk cara kedua, PKA memfosforilasi enzim perantara penting, yaitu glikogen fosforilase kinase (GPK). Bedanya dengan enzim GS, fosforilasi justru membuat GPK aktif. GPK yang aktif ini kemudian memfosforilasi enzim berikutnya yaitu glikogen fosforilase (GP) pada residu serin14 yang selanjutnya memecah glikogen menjadi glukosa-1-fosfat.[57]
Katabolisme lipid[sunting|sunting sumber]
Oksidasi asam lemak[sunting|sunting sumber]
lintasan oksidasi asam lemak memungkinkan konversi asam lemak yang ada di mitokondria menjadi banyak produk yang selanjutnya dapat digunakan sel untuk menghasilkan energi, termasuk asetil-KoA, NADH danFADH2. Langkah awal oksidasi asam lemak adalah 'aktivasi' asam lemak dalam sitosol melalui reaksi yang diperantarai enzim dengan ATP untuk akhirnya menghasilkan asam lemak asil-KoA. Mekanisme oksidasi asam lemak selanjutnya tergantung pada panjang ekoralifatikdalam asam lemak.[56]
Asam lemak rantai pendek, yang didefinisikan memiliki kurang dari enam karbon di ekor alifatik bisa berdifusi masuk ke mitokondria secara pasif. Pertama-tama, asam lemak rantai panjang dan sedang harus dalam kondisi terkonjugasi kekarnitinamelaluikarnitina palmitoiltransferase I(CPT1). Setelah ini, asam lemak rantai panjang terkonjugasi karnitina kemudian dipindahkan ke mitokondria di mana ia diubah kembali menjadi asam lemak asil-KoA melalui penghilangan karnitina olehkarnitina palmitoil transferase II(CPT2). Pada tahap ini, β-oksidasi asam lemak asil-CoA dimulai, menghasilkan sejumlah besar asetil-KoA, NADH dan FADH2 yang selanjutnya digunakan dalam siklus TCA dan rantai transpor elektron untuk menghasilkan ATP.[56]
CPT1 A bertindak sebagai langkah regulator utama dalam reaksi oksidasi asam lemak, karena membatasi laju yang dihambat oleh zat intermediat sintesis lipidmalonil-KoA,sehingga mencegah reaksi oksidasi lipid ketika sel secara aktif mensintesis lipid. Secara keseluruhan, oksidasi asam lemak dapat memungkinkan produksi ATP dalam jumlah yang luar biasa. Reaksi oksidasi β lengkap dari molekulpalmitattunggal (asam lemak utama dalam sel mamalia) yang memiliki potensi untuk menghasilkan lebih dari 100 molekul ATP.[56]
Pemecahan kolesterol[sunting|sunting sumber]
Pada orang dewasa, banyak jaringan mampu menyintesis kolesterol. Produk hewani merupakan sumber kolesterol, sedangkan tumbuhan tidak memiliki kolesterol. Namun, membran pada sel tumbuhan mengandungfitosterol,yang secara struktural mirip dengan kolesterol dan berguna dalam pengobatan diethiperkolesterolemiakarena mereka berkompetisi saat penyerapan kolesterol. Hati dan usus merupakan situs kuantitatif yang paling penting untuk metabolisme kolesterol pada manusia, meskipun sejumlah kecil kolesterol juga hilang melalui siklus pergantian kulit.[58]
Katabolisme asam amino[sunting|sunting sumber]
Metabolisme asam amino memiliki beberapa peran penting dalam beberapa aspek biologis pada sel. Bermacam-macam jenis asam amino berperan dalam lintasan metabolis yang beragam yang menggunakannya sebagai substrat.Asam aminodigunakan dalam proses sintesis protein dan biomolekul lainnya atau dioksidasi menjadiureadan karbondioksida sebagai sumber energi.Glutaminadapat berperan aktif dalam proliferasi sel sebagai sumber alternatif pada siklus asam sitrat yang berfungsi untuk mendukung produksi ATP atau sumbersitratpada reaksi sintesis asam lemak. Asam amino lainnya, sepertiargininadantriptofandimetabolisasi melalu lintasan yang berbeda untuk mendukungproliferasi seldan pertumbuhan anabolis.[56][59]
lintasan oksidasi gugus asam amino dimulai dengan melepaskangugus aminaoleh enzimtransaminase.Gugus amina masuk ke dalamsiklus ureayang meninggalkan rangka karbon yang telahdideaminasidalam bentuk asam keto. Beberapa asam keto menjadi intermediat di dalam siklus asam sitrat, seperti deaminasiglutamatmenjadi bentuk alfa-ketoglutarat. Asam amino glukogenik dapat dikonversi menjadi glukosa dalam prosesglukoneogenesis.[60]
Transformasi energi[sunting|sunting sumber]
Fosforilasi oksidatif[sunting|sunting sumber]

Pada reaksi fosforilasi oksidatif, elektron dilepas dari molekul organik seperti NADH dan FADH2, lalu dipindahkan ke oksigen dan energi yang dihasilkan akan digunakan untuk membuat ATP.[12]Reaksi ini berlangsung padaeukariota melalui protein berantai di dalam membran dimitokondriayang disebut dengan namarantai transpor elektron,sedangkan padaprokariota,protein-protein ini ditemukan padamembran dalam.[61]Protein-protein ini menggunakan energi yang dikeluarkan dari elektron yang lewat yang
berasal dari molekul yang tereduksi, seperti NADH ke dalamoksigenuntuk memompaprotonmelewati membran.[62]
Proton yang dipompa keluar dari mitokondria menciptakanperbedaan konsentrasimelewati membran yang menghasilkangaya gerak proton.[63]Gaya ini menggerakkan proton kembali ke dalam mitokondria melalui basa sebuah enzim yang disebut denganATP Sintase.Aliran proton membuat tangkai subunit berotasi sehingga menyebabkansitus aktifdomain sintase berubah bentuk dan memosforilasiadenosina difosfatmenjadi ATP[27]
Energi dari senyawa anorganik[sunting|sunting sumber]
Kemolitotrofadalah jenis metabolisme yang ditemukan pada prokariota yang menggunakan energi yang didapatkan dari proses oksidasisenyawa anorganik.Organisme ini dapat menggunakanhidrogen,[64]senyawabelerangyang tereduksi (sulfida,hidrogen sulfidadantiosulfat),[65]besi (II) oksida[66]atauamoniak[67]sebagai sumber energi dengan mengoksidasi senyawa tersebut dengan elektron aseptor, seperti oksigen ataunitrit.[68]Proses mikrobial ini penting bagidaur biogeokimia,sepertiasetogenesis,nitrifikasidandenitrifikasisekaligus berfungsi penting untukkesuburan tanah[69][70]
Energi dari cahaya[sunting|sunting sumber]
Energi yang berasal dari sinar matahari ditangkap olehtumbuhan,sianobakteri,bakteri ungu,chlorobidan beberapa jenisprotista.Proses ini dipasangkan dengan konversi karbondioksida menjadi senyawa organik sebagai bagian proses fotosintesis. Penangkapan energi dan fiksasi karbon bisa beroperasi secara terpisah pada prokariota, sedangkan bakteri ungu fdan chlorobi bisa menggunakan sinar matahari sebagai sumber energi, ketika menukar reaksi di antara reaksi fiksasi karbon atau fermentasi senyawa organik.[71][72]
Pada banyak organisme, penangkapan energi sinar matahari memilik prinsip yang sama dengan fosforilasi oksidatif yang melibatkan penyimpanan energi sebagai gradien konsentrasi proton. Gaya gerak proton ini lah yang akan menggerakan sintesis ATP[73].Elektron yang dibutuhkan untuk menggerakan rantai transpor elektron berasal dari protein yang mengumpulkan cahaya yang disebutpusat reaksi fotosintesis.Kelompok pusat reaksi ini dibagi menjadi dua tipe tergantung sifatpigmen fotosintesisnyadi mana bakteri hanya memiliki satu tipe, sedangkan tumbuhan dan sianobakteri punya dua[74]
Pada tumbuhan, alga, dan sianobakteri,fotosistem IImenggunakan energi cahaya untuk melepaskan elektron dari molekul air dan melepaskan oksigen sebagai zat sisa. Lalu, elektron masuk ke dalamkompleks sitokrom b6fyang menggunakan energi tersebut untuk memompa proten melewati membrantilakoidyang ada di dalam membran kloroplas..[75]Proton ini kembali melalui membran untuk menggerakan ATP sintase seperti sebelumnya.Elektron masuk melaluifotosistem Idan bisa juga digunakan untuk mereduksi koenzim NADP+[76]Koenzim ini dapat digunakan di dalamsiklus Calvinatau didaur ulang untuk menghasilkan ATP selanjutnya.
Anabolisme[sunting|sunting sumber]
Anabolisme adalah sekelompok proses reaksi metabolis yang menggunakan energi yang dihasilkan dari proses katabolisme untuk menyintesis molekul kompleks. Pada umumnya, molekul kompleks terdiri dari struktur seluler yang disusun secara bertahap dari prekursor yang kecil dan sederhana. Anabolisme melibatkan tiga tahap dasar. Pertama, sintesis prekursor, seperti asam amino, monosakarida danisoprenoid,dan nukleotida. Tahap kedua ialah aktivasi bentuk reaktif menggunakan energi yang berasal dari ATP. Tahap ketiga ialah penyusunan prekursor menjadi molekul yang lebih kompleks, seperti protein, polisakarida, lipid, danasam nukleat.[77]
Anabolism di dalam organisme dapat berbeda tergantung bahan baku konstruksi molekul yang terjadi di dalam sel organisme tersebut.Autotrofseperti tanaman dapat menyusun molekul organik kompleks di dalam sel seperti polisakarida dan protein hanya dari molekul sederhana seperti karbondioksida dan air. Sedangkan,Heterotrofmembutuhkan senyawa yang lebih kompleks dibandingkan autotrof, seperti monosakarida dan asam amino untuk menghasilkan molekul yang lebih kompleks. Organisme ini dapat diklasifikasikan lebih jauh dengan berdasarkan sumber energi, yaitu fotoautotrof and fotoheterotrof yang mendapatkan energi dari cahaya, sedangkan kemoautotrof dan kemoheterotrof mendapatkan energi dari reaksi oksidasi senyawa anorganik.[77]
Fiksasi karbon[sunting|sunting sumber]

perbFotosintesis adalah reaksi sintesis karbohidrat dari cahaya dan karbondioksida. Pada tanaman, sianobakteri danalga,fotosintesis oksigenik menguraikan molekul air,dengan oksigen sebagai zat sisa.Proses ini menggunakan ATP dan NADPH yang diproduksi olehpusat reaksi fotosintesisuntuk mengonversi CO2menjadigliserat-3-fosfatyang akan dikonversi menjadi glukosa. Reaksi fiksasi karbon ini akan dibantu oleh enzimRubiscosebagai bagiansiklus Calvin[78]Ada tiga tipe fotosintesis yang terjadi pada tanaman, yaitufiksasi karbon C3,C4danFotosintesis CAM.Perbedaan ketiga tipe tanaman dapat dibedakan dari lintasan masuknya karbondioksida ke dalam siklus Calvin.Tanaman C3 memiksasi CO2secara langsung, sedangkan C4 dan CAM memasukkan CO2ke dalam senyawa lain terlebih dahulu sebagai bentuk adaptasi terhadap sinar matahari yang menyengat atau kondisi kering atau kurang air.[79]
Pada prokariota fotosintetik, mekanisme fiksasi karbon lebih beragam. Fiksasi dapat terjadi dengan beberapa reaksi seperti, siklus Calvin,siklus Krebs terbalik,[80]atau karboksilasi asetil-KoA[81].[82]Prokariotakemoautotrofjuga memiksasi melalui siklus Calvin tetapi menggunakan energi dari senyawa anorganik untuk menggerakkan reaksi.[83]
Karbohidrat and glikan[sunting|sunting sumber]
Pada proses anabolisme karbohidrat, asam organik sederhana dapat dikonversi menjadi monosakarida seperti glukosa, dan dapat disusun menjadi polisakarida seperti pati. Produksi glukosa dapat dilakukan menggunakan bahan bakuasam piruvat,asam laktat,gliserol,gliserat-3-fosfat dan asam amino dalam reaksi yang disebutglukoneogenesis.Glukoneogenesis mengonversi asam piruvat menjadi glukosa-6-fosfat melalui serangkaian senyawa intermediat yang ada juga di dalam reaksiglikolisis[53]
Meskipun begitu, lintasan ini tidak sama dengan reaksi glikolisis yang berlangsung secara terbalik karena beberapa langkah dalam reaksi ini dikatalisis oleh enzim non-glikolitik. Kondisi ini penting untuk memungkinkan pembentukan dan penguraian glukosa berjalan dalam siklus yang berbeda dan mencegah terjadinya kedua lintasan berjalan secara bersamaan di dalam sebuahsiklus yang sia-sia.[84][85]Dalam keadaan berlimpah, glukosa dapat dikoversi menjadi glikogen melalui reaksi yang disebutglikogenesissebagai bentuk penyimpanan energi selain lemak yang biasanya digunakan untuk mempertahankan glukosa di dalam darah[86]
Polisakarida danglikantersusun dengan penambahan secara bertahap suatu monosakarida oleh reaksiglikosiltransferasedari gula pendonor aktif fosfat, sepertiuridina difosfat glukosa(UDP-Glc) terhadap suatu gugushidroksilaseptor pada polisakarida yang diinginkan. Selama gugus hidroksil pada cincin subtrat dapat menjadi aseptor, polisakarida yang diproduksi akan memiliki cabang struktur yang lurus atau bercabang.[87]Polisakarida yang terbentuk dapat memiliki fungsi pada bentuk aslinya atau dapat dipindahkan ke lipid atau protein menggunakan enzimoligasakariltransferase[88][89]
Sintesis lipid[sunting|sunting sumber]
biLintasan sintesis asam lemak memungkinkan sel untuk menghasilkan lipid yang diperlukan untuk pertumbuhan sel dan proliferasi dari prekursor yang berasal dari lintasan metabolisme intrinsik lainnya. Aktivitas lintasan sintesis asam lemak sangat terkait dengan pensinyalanmTOR,yang telah terbukti mendorong sintesis asam lemak melalui regulasi banyak enzim utama yang bertanggung jawab untuk sintesis lipidde novo,termasukSREBP(protein pengikat elemen pengatur sterol), FASN (asam lemak sintase) dan ACC (asetil-KoA karboksilase) yang diinduksi oleh SREBP.[56]Enzim pada proses biosintesis asam lemak dibagi menjadi dua kelompok. Padafungidan hewan, seluruh reaksi asam lemak sintase dilakukan oleh satu jenis protein tunggal multifungsi yang mengandung semua pusat reaksi di dalamnya yang disebut FAS I.Plastidtumbuhan, bakteri danparasitmemiliki sistem terpisah yang setiap komponennya disandi oleh gen berbeda yang menghasilkan suatu protein unik yang mengkatalisis satu langkah di dalam lintasan tersebut yang diberi nama FAS II.[90][91]
Sintesis asam lemak menggunakan produk yang berasal dari beberapa lintasan metabolisme lainnya, terutama glikolisis, siklus TCA, dan lintasan pentosa fosfat. Untuk sintesis asam lemak rantai lurus,asam sitratyang berasal dari siklus TCA dapat diekspor darimitokondriake sitosol melalui pembawa sitrat, di manaATP sitrat liasemengubahnya menjadi asetil-koA, bersama denganoksaloasetat.Asetil-KoA yang berasal dari proses ini kemudian dapat dikarboksilasi oleh ACC untuk menghasilkanmalonil-KoA.Selanjutnya, FASN bertindak dalam cara yang tergantung pada NADPH untuk memperpanjang rantai asam lemak yang baru terbentuk sampai produk seperti asam palmitat disintesis. Asam lemak dengan panjang rantai alternatif dapat disintesis menggunakan asam palmitat sebagai substrat untuk pemanjangan, sementara reaksi desaturasi dapat dilakukan untuk menghasilkan asam lemak tak jenuh.[56]Sintesis asam lemak rantai cabang berbeda dengan sintesis asam lemak lurus, yaitu membutuhkan asam amino rantai cabang seperti valin dan leusin sebagai substrat untuk perpanjangan. Lebih lanjut, asam lemak dapat dikondensasikan dengan gliserol produk dari glikolisis untuk menghasilkan banyak kemungkinan kombinasi triasilgliserol dan fosfolipid, yang merupakan komponen kunci dari banyak struktur seluler.[56]
Selain asam lemak, proses anabolisme juga terjadi pada mamalia juga yang menggunakan gliserol dalam bentuk G-3-P yang dihasilkan dari reaksifosforilasi gliserol olehgliserol kinaseatau reduksidihidroksiaseton fosfatmenggunakan enzimgliseraldehida 3-fosfat dehidrogenase.Dihidroksiasaseton fosfat dapat diturunkan dari senyawa glukosa atau piruvat. Pada kondisi normal, trigliserida ataugliserol-3-fosfatdihasilkan dari proses glikolisis dengan prekursor glukosa. Akantetapi, ketika konsentrasi glukosa menurun di dalam sitosol, gliserol dihasilkan dari proses reaksigliseroneogenesis.Reaksi ini menggunakan asam piruvat, asam laktat,alanina,dananiondari siklus asam sitrat sebagai prekursor pengganti.Fosfoenolpiruvat karboksikinase(PEPC-K) adalah enzim regulator utama yang berfungsi sebagai katalisator reaksidekarboksilasioksaloasetat menjadifosfoenolpiruvat.[92]
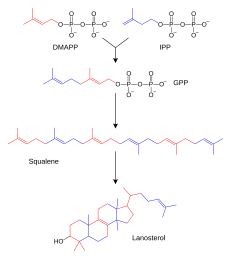
Terpenaadalah kelompok lipid,sepertikarotenoidyang membentuk kelompok terbesarproduk alamidari tumbuhan.[93]Senyawa ini disusun atas susunan dan modifikasi unitisoprenayang diberikan oleh prekursor reaktifisopentenil pirofosfatdandimetilalil pirofosfat[94]Prekursor ini dapat disusun dengan dua cara. Pada hewan danarkea,lintasan mevalonatmenghasilkan senyawa ini dari asetil KoA,[95]sedangkan pada tumbuhan dan bakteri, piruvat dan (G-3-P) digunakan sebagai substrat padalintasan nonmevalonat.[94][96]Salah satu reaksi penting yang mengunakan donor isoprena aktif ini adalahbiosintesis sterol.Reaksi ini menyatukan unit isoprena untuk menyusunskualena,lalu dilipat dan membentuk kelompok cincin yang menyusunlanosterol[97]Lanosterol bisa dikonversi menjadi sterol lainnya, sepertikolesteroldanergosterol[97][98]
Fosfatidilkolin merupakan kelompok fosfolipid yang disintesis melalui lintasan sitidin 5-difosfat (CDP)-kolin yang memfosforilasi kolin i menjadi fosfokolin oleh kolin kinase kemudian dikonversi menjadi CDP-kolin oleh CPT:fosfokolin sitidiltransferase. Selanjutnya, CDP-kolin dikombinasikan dengan diasilgliserol oleh dua enzim yang terintegrasi ke retikulum endoplasma: CDP-kolin:1,2-diasilgliserol kolinfosfotransferase (CPT) dan CDP-kolin: 1,2-diasilgliserol kolin/etanolamin fosfotransferase (CEPT). lintasan CDP-kolin terdapat di semua sel mamalia berinti. Namun, di hati, hingga 30% fosfatidilkolin dihasilkan oleh konversi fosfatidletanolamin menjadi fosfatidilkolin oleh fosfatidiletanolamin N-metiltransferase (PEMT).[99]Selain sintesis fosfatidlkolin, fosfatidiletanolamin juga merupakan golongan fosfolipdid yang disintesis makhluk hidup melalui dua lintasan utama: lintasan CDP-etanolamin di retikulum endoplasma dan lintasan fosfatidilserin dekarboksilase (PSD) di mitokondria. lintasan CDP-etanolamin mirip dengan sintesis fosfatidilkolin. Fosfoetanolamin diubah menjadi CDP-etanolamin oleh CTP:fosfoetanolamin sitidiltransferase kemudian ditambahkan ke diasilgliserol oleh CEPT untuk membentuk fosfatidiletanolamin. lintasan PSD terjadi secara eksklusif di mitokondria, di mana fosfatidilserin didekarboksilasi oleh PSD untuk membentuk fosfatidiletanolamin. Sintesis fosfatidilserin, yang dikendalikan oleh dua sintase fosfatidilserin, merupakan langkah pembatas laju untuk sintesis fosfatidiletanolamin pada lintasan PSD.[99]
Protein[sunting|sunting sumber]
Organisme memiliki kemampuan berbeda untuk mensintesis 20 jenis asam amino. Sebagian besar bakteri dan tumbuhan mampu semua jenis 20 asam amino. Namun, mamamalia hanya mampu mensintesis 11 asam amino nonesensial, sedangkan 9asam amino esensiallainnya didapatkan dari makanan.[100]Beberapa parasit sederhana, seperti bakteriMycoplasma pneumoniae,tidak mempunyai kemampuan untuk mensintesis seluruh asam amino dan mengambil asam amino langsung dari inangnya.[101]Seluruh asam amino disintesis dari senyawa intermediat di dalam proses reaksi glikolisis, siklus asam sitrat atau lintasan pentosa fosfar, Nitrogen disediakan olehasam glutamatdanglutamina.Sintesis asam amino non esensial bergantung pada pembentuk asam alfa-keto yang sesuai yang akanditransaminasiuntuk membentuk asam amino.[102]
Asam amino disusun menjadi protein yang disatukan bersama menjadi sebuahrantai ikatan peptida.Tiap protein yang berbeda memiliki sekuens yang unik dari residu asam amino yang merupakanstruktur primernya.Asam amino dapat disambungkan dalam sekuens yang beragam untuk membentuk banyak variasi protein. Protein disusun dari asam amino yang diaktivasi oleh penempelan olem molekulTransfer RNAmelalui ikatanester.Prekursoraminoasil-tRNAdihasilkan oleh sebuah reaksi yang menggunakan ATP yang dilakukan oleh enzimsintetase aminoasll-tRNA[103]Selanjutnya, aminoasil-tRNA ini menjadi substrat untukribosomyang menyatukan asam amino menjadi rantai protein memanjang menggunakan sekuens yang ada di dalam MRNA.[104][105]
Sintesis nukleotida dan penghematan[sunting|sunting sumber]
Nukleotida disusun dari asam amino, karbondioksida danasam formatdi lintasan yang membutuhkan energi metabolis dalam jumlah besar.[106][107]Karena itu, sebagian besar organisme mempunyai sistem yang efisien untuk menghemat nukleotida yang belum terbentuk.[106][107][108]Purinadisintesis menjadi nukleosida ( basa yang melekat kepadaribosa)[109]Adeninadanguaninadisusun dari prekursornukleosidainosinamonofosfat yang disintesis menggunakan atom dari asam aminoglisina,glutaminadanasam aspartatsertaasam formatyang dipindahkan dari koenzimtetrahidrofolat.Sedangkan,pirimidinadisintesis dari basaorotatyang dibentuk dari glutamina dan asam aspartat.[110]
Xenobiotika dan metabolisme redoks[sunting|sunting sumber]
Seluruh organisme secara konstan terpapar oleh senyawa yang mereka tidak bisa gunakan sebagai nutrisi dan dapat berbahaya, jika berakumulasi di dalam sel karena tidak memiliki fungsi metabolis. Senyawa yang berpotensi membahayakan ini disebut xenobiotik.[111]Xenobiotik, sepertiobat sintetis,racun alami,danantibiotikdidetokfisikasi oleh serangkaian enzim metabolis.Pada manusia,termasuk di antaranyasitokrom P450 oksidase,[112][113]UDP-glukuronosiltransferase,[114]andglutationS-transferase.[115]Sistem ini terbagi menjadi tiga langkah. Langkah pertama ialah mengoksidasi xenobiotik (fase I) dan mengonjungasi gugus berbahan dasar air terhadap molekul (fase II). Xenobiotik larut air yang telah temodikasi dapat dipompa keluar dari sel dan organisme multiseluler akan mencerna lebih jauh, sebelum senyawa tersebut dieskresikan (fase III). Pada ilmuekologi,reaksi ini sangat penting dalam prosesbiodegradasipolutan oleh mikrob danbioremediasilahan yang terkontaminasi serta tumpahan minyak.[116]Banyak reaksi mikrob yang juga ada pada organisme multiseluler. Akan tetapi, dikarenakan diversitas jenis mikrob, organisme ini dapat menangani xenobiotik dalam jangkauan yang lebih luas dibandingkan dengan organisme multiseluler. Organisme ini juga dapat mendegradasipolutan organik persistenseperti senyawaorganoklorida.[117]
Masalah serupa untuk xenobiotik terjadi untukorganisme aerobikadalahstres oksidatif.[118]Stres oksidatif dimulai dengan reaksifosforilasi oksidatifdan pembentukanikatan disulfidaselamapelipatan proteinyang menghasilkanspesi oksigen reaktif,sepertihidrogen peroksida[119]Oksidan yang bersifat merusak ini dihilangkan oleh metabolit antioksidan sepertiglutationdan enzimkatalasedanperoksidase.[120][121]
Termodinamika organisme[sunting|sunting sumber]
Organisme hidup harus mematuhihukum termodinamikayang mengatur perpindahan panas danusaha.Hukum termodinamika keduamenyatakan bahwa di dalamsistem tertutup,jumlahentropitidak dapat berkurang. Walaupun kompleksitas organisme hidup terlihat berkontradiksi terhadap hukum tersebut, kehidupan hanya terjadi karena seluruh organisme merupakansistem terbukayang menukarmateridanenergike lingkungannya. Jadi, sistem kehidupan tidak berada di dalam kesetimbangan, tetapi berada di dalamsistem disipatifyang mempertahankan keadaan kompleksitas tinggi yang menyebabkan peningkatan entropi sekitar.[122]Metabolisme mencapai kondisi ini dengan memasangkan reaksi katabolisme yangspontandengan reaksi nonspontan dari anabolisme. Padaterminologitermodinamika, metabolisme mempertahankan keteraturan dengan menciptakan ketidakteraturan.[123]
Regulasi dan kontrol[sunting|sunting sumber]
Karena lingkungan sebagian besar organisme terus berubah, reaksi metabolisme harus diatur dengan baik untuk mempertahankan serangkaian kondisi konstan dalam sel. Kondisi ini disebuthomeostasis.[124][125]Ada dua konsep yang saling berhubungan dekat dan harus dimengerti untuk memahami bagaimana lintasan metabolisme dapat dikontrol. Pertama, regulasi suatu enzim di dalam lintasan dilihat dari bagaimana aktivitasnya meningkat dan berkurang sebagai respons terhadap sinyal. Kedua, seberapa besar efek perubahan aktivitas yang dilakukan oleh enzim mempunyai pengaruh pada keseluruhan lintasan yang terjadi (jumlahfluksyang terjadi pada lintasan)[126]Misalnya, ketika suatu enzim menunjukkan perubahan yang besar pada suatu aktivitas, tetapi perubahan ini hanya mempunyai efek yang kecil pada fluks yang ada di lintasan metabolisme, maka enzim ini tidak terlibat sebagai kontrol lintasan.[127]

Ada beberapa tingkatan dari regulasi metabolisme. Pada regulasi intrinsik, lintasan metabolisme meregulasi dirinya sendiri sebagai respons terhadap perubahan jumlah substrat atau produk. Misalnya, berkurangnya jumlah produk akan meningkatkan flux yang ada di lintasan sebagai kompensasi.[126]Jenis regulasi ini sering melibatkanregulasi alosterikdari beberapa enzim yang ada di lintasan.[128]Kontrol ekstrinsi melibatkan suatu sel yang ada di dalam organisme multiseluler yang mengubah metabolismenya sebagai respons terhadap sinyal dari sel lain, Sinyal ini biasanya dalam bentuk pengirim pesan larut air, seperti hormon danfaktor pertumbuhanyang dapat dideteksi olehreseptorspesifik yang ada di permukaan sel.[129]Sinyal ini akan ditransmisikan ke dalam sel olehsistem penghantar keduayang biasanya melibatkan reaksifosforilasiprotein.[130]
Suatu contoh yang dapat menggambarkan kontrol ekstrinsik ialah regulasi metabolisme glukosa oleh hormoninsulin.[131]Insulin dihasilkan sebagai respons dari kenaikankonsentrasi gula darah.Melekatnya hormon padareseptor insulinmengaktifkan kinase protein secara berurutan yang menyebabkan sel mengambil glukosa dan mengonversinya menjadi bentuk simpanan glukosa, seperti asam lemak dan glikogen.[132]Metabolisme glikogen dikontrol oleh aktivitas enzimfosforilaseyang menguraikan glikogen dan enzimglikogen sintaseyang mensintesisnya, Enzim ini diregulasi di dalam sebuah proses timbal balik dengan reaksi fosforilasi yang menghambat glikogen sintase, tetapi mengaktifkan fosforilase. Insulin menyebabkan sintesis glikogen dengan mengaktifkanprotein fosfatasedan menganghasilkan penurunan fosfforilasi enzim ini.[133]
Evolusi[sunting|sunting sumber]

Lintasan metabolisme utama yang telah dijelaskan di atas, seperti glikolisis dan siklus asam sitrat ada pada seluruhtiga domainmakhluk hidup dan juga ada padaleluhur universal terakhir.[134][135]Sel leluhur universal merupakanprokariotadan mungkin merupakan suatumetanogenyang memiliki metabolisme asam amino, nukleotida, karbohidrat, dan lipid yang ekstensif.[136][137]Retensi keberadaan lintasan purba padaevolusimakhluk hidup setelahnya mungkin merupakan hasil dari reaksi yang memiliki solusi optimum untuk masalah metabolisme tertentu dengan lintasan, seperti glikolisis dan siklus asam sitrat yang menghasilkan produk akhir dengan efisiensi yang tinggi dan dengan langkah dalam jumlah minimum.[138][139]Lintasan metabolisme berbasis enzim pertama mungkin merupakan bagian dari metabolisme nukleotida purina, sedangkan lintasan metabolisme sebelumnya merupakan bagian daridunia RNA purba.[140]
Banyak model yang diusulkan untuk menjelaskan bagaimana lintasan metabolisme baru berevolusi. Model ini termasuk penambahan secara berurutan enzim baru kepada lintasan purba yang pendek, duplikasi, lalu menyebarkan ke seluruh lintasan sekaligus memasukkan enzim yang telah ada dan menyusunnya menjadi lintasan reaksi yang baru.[141]Kepentingan relatif dari mekanisme ini masih belum jelas, tetapi studigenomikamenunjukkan bahwa enzim yang ada di dalam lintasan kemungkinan mempunyai leluhur yang sama. Mekanisme ini menyatakan kemungkinan bahwa banyak lintasan berevolusi secara tahap demi tahap dengan fungsi baru yang diciptakan oleh tahap yang sebelumnya ada di dalam lintasan.[142][143]Sebuah model alternatif berasal dari studi tentang jejak evolusi struktur protein di dalam jaringan metabolisme. Studi ini menyatakan kemungkinan bahwa enzim perlahan bergabung dengan meminjam enzim dengan fungsi yang sama pada jalur metabolisme yang berbeda (ada di dalambasis data MANET)[144]Proses bergabungnya enzim ini menghasilkan sebuah mosaik enzim evolusioner.[145]Kemungkinan ketiga ialah sebagian metabolisme mungkin ada sebagai 'modul' yang dapat digunakan kembali di dalam lintasan berbeda dan melakukan fungsi yang sama pada molekul berbeda[146]
Evolusi juga dapat menyebabkan hilangnya fungsi metabolisme. Sebagai contoh, beberapa proses metabolisme pada parasit yang tidak esensial untuk bertahan hidup menjadi hilang sehingga kebutuhan asam amino, nukleotida, dan karbohidrat mereka ambil dariinang.[147][148]Kondisi yang sama juga dapat dilihat pada organismeendosimbiotik.[149]
Investigasi dan manipulasi[sunting|sunting sumber]

Secara klasik, metabolisme dipelajari dengan pendekatanreduksionisyang berfokus pada lintasan metabolisme tunggal. Pendekatan ini menggunakanpelacak radioaktifpada tingkat organisme, jaringan, atau sel. Lintasan metabolisme dari prekursor hingga produk akhir didefinisikan dengan mengidentifikasi berbagai senyawa intermediat dan produk yang memiliki label senyawa radioaktif.[150]Enzim-enzim yang mengatalisis reaksi-reaksi kimiadimurnikansehinggakinetikadan responsnya terhadapinhibitordapat dipelajari. Pendekatan paralel juga dilakukan untuk mengidentifikasi molekul-molekul kecil di dalam sel dan jaringan; serangkaian molekul lengkap ini dikenal dengan namametabolom.Meskipun dapat memberikan gambaran yang baik tentang struktur dan lintasan metabolisme sederhana, studi ini tidak memadai ketika diterapkan pada sistem yang lebih kompleks, seperti metabolisme pada sebuah sel lengkap.[151]
Kompleksitasjejaring metabolismedi dalam sel yang mengandung ribuan enzim berbeda dapat dilihat pada ilustrasi yang menampilkan reaksi 43 protein dan 40 metabolit: urutan genom pada gambar tersebut mengandung hingga 26.000 gen.[152]Datagenomikaseperti ini dapat digunakan untuk mengonstruksi kembali jejaring reaksi biokimia yang lengkap dan menghasilkan model matematika yang lebih komprehensif untuk menjelaskan dan memprediksi bagaimana reaksi ini bekerja.[153]Model ini ampuh ketika digunakan untuk mengintegrasikan data lintasan dan metabolit yang didapatkan melalui metode klasik dengan dataekspresi genyang didapatkan dari studiproteomikasertaDNAmicroarray[154]Dengan teknik ini, model metabolisme manusia dapat dibentuk yang selanjutnya mengarahkan penemuan obat dan penelitian biokimia.[155]Model ini juga digunakan dalamanalisis jejaringuntuk mengklasifikasikan penyakit manusia menjadi kelompok-kelompok berdasarkan kesamaan protein dan metabolit mereka.[156][157]
Jejaring metabolisme bakteri adalah contoh yang sangat baik dari organisasidasi kupu-kupu,[158][159][160]suatu proses yang masukannya adalah berbagai nutrien yang sangat beragam dan keluarannya adalah berbagai produk dan makromolekul kompleks yang sangat bervariasi meskipun prosesnya hanya melibatkan senyawa intermediat yang jenisnya relatif sedikit.Rekayasa metabolismemerupakan penerapan teknologi paling utama dari informasi ini. Organisme sepertikhamir,tumbuhan, dan bakteri direkayasa genetiknya agar mereka lebih berguna dalam prosesbioteknologidan produksi obat-obatan seperti antibotik atau produksi bahan kimia industri sepertietilena glikoldanasam sikimat.[161][162][163]
Lihat pula[sunting|sunting sumber]
Referensi[sunting|sunting sumber]
- ^(Inggris)"Overview of Metabolism".ElmHurst College.Diakses tanggal12 Juni2023.
- ^"metabolism (n.)".Online Etymology Dictionary(dalam bahasa Inggris).Diakses tanggal12 Juni2023.
- ^Leroi, Armand Marie. (2014).The lagoon: how Aristotle invented science.New York: Bloomsbury. hlm. 400–401.ISBN978-0-698-17039-1.OCLC883341616.Diarsipkandari versi asli tanggal 2020-07-06.Diakses tanggal2020-07-24.
- ^Fernie, Alisdair R.; Pichersky, Eran (2015)."Focus Issue on Metabolism: Metabolites, Metabolites Everywhere".Plant Physiology.169(3): 1421–1423.doi:10.1104/pp.15.01499.ISSN1532-2548.PMC4634105
 .PMID26531677.
.PMID26531677.
- ^Eknoyan, Garabed (1999)."Santorio Sanctorius (1561–1636) – Founding Father of Metabolic Balance Studies".American Journal of Nephrology(dalam bahasa english).19(2): 226–233.doi:10.1159/000013455.ISSN0250-8095.PMID10213823.
- ^William HA (1904).Modern Development of the Chemical and Biological Sciences.A History of Science: in Five Volumes.IV.New York: Harper and Brothers. hlm. 184–185.
- ^Manchester, Keith L. (Desemer 1995)."Louis Pasteur (1822–1895) — chance and the prepared mind".Trends in Biotechnology(dalam bahasa Inggris).13(12): 511–515.doi:10.1016/S0167-7799(00)89014-9.ISSN0167-7799.Diarsipkandari versi asli tanggal 2018-11-07.Diakses tanggal2020-07-28.
- ^Kinne-Saffran, E.; Kinne, R. K. H. (1999)."Vitalism and Synthesis of Urea".American Journal of Nephrology(dalam bahasa english).19(2): 290–294.doi:10.1159/000013463.ISSN0250-8095.PMID10213830.
- ^Barnett, James A.; Lichtenthaler, Frieder W. (2001)."A history of research on yeasts 3: Emil Fischer, Eduard Buchner and their contemporaries, 1880–1900".Yeast(dalam bahasa Inggris).18(4): 363–388.doi:10.1002/1097-0061(20010315)18:43.0.CO;2-R.ISSN1097-0061.Diarsipkandari versi asli tanggal 2021-02-06.Diakses tanggal2020-07-28.
- ^Chawla R (2017).Textbook of Medical Biochemistry(edisi ke-2). New Delhi: Wolters Kluwer India. hlm. 4.ISBN9789351298250.
- ^Stone, David (4 Juli 2020)."Chromatography Resources Technique, Theory, and Instrumentation".Analytical Science Resources Instrumentation, Theory, Tutorials, and Virtual Tours.Diakses tanggal12 Juni2023.
- ^abCooper, Geoffrey M. (2000)."The Molecular Composition of Cells".The Cell: A Molecular Approach. 2nd edition(dalam bahasa Inggris).Diarsipkandari versi asli tanggal 2020-08-27.Diakses tanggal2020-06-25.
- ^Michie, Katharine A.; Löwe, Jan (2006-06)."Dynamic Filaments of the Bacterial Cytoskeleton".Annual Review of Biochemistry(dalam bahasa Inggris).75(1): 467–492.doi:10.1146/annurev.biochem.75.103004.142452.ISSN0066-4154.Diarsipkan dariversi aslitanggal 2020-02-06.Diakses tanggal2020-06-06.
- ^Nelson & Cox 2017,hlm. 187.
- ^Hothersall, John S.; Ahmed, Aamir (2013-02-04)."Metabolic Fate of the Increased Yeast Amino Acid Uptake Subsequent to Catabolite Derepression".Journal of Amino Acids(dalam bahasa Inggris).doi:10.1155/2013/461901.PMC3575661
 .PMID23431419.Diarsipkandari versi asli tanggal 2020-06-06.Diakses tanggal2020-06-06.
.PMID23431419.Diarsipkandari versi asli tanggal 2020-06-06.Diakses tanggal2020-06-06.
- ^Nelson & Cox 2017,hlm. 225.
- ^Attwood T K, Campbell P N, Parish J H, Smith A D, Stirling J L, Vella F (2006).Oxford dictionary of biochemistry and molecular biology.Cammack, Richard, Ph. D. (edisi ke-Rev. ed). Oxford: Oxford University Press. hlm. 388.ISBN978-0-19-852917-0.OCLC65467611.
- ^"Lipid nomenclature Lip-1 & Lip-2".www.qmul.ac.uk.Diarsipkandari versi asli tanggal 2020-06-06.Diakses tanggal2020-06-06.
- ^Berg JM, Tymoczko, JL, Gatto GJ Jr, Stryer L. (8 April 2015).Biochemistry(edisi ke-8). New York: W. H. Freeman. hlm. 362.ISBN978-1-4641-2610-9.OCLC913469736.Diarsipkandari versi asli tanggal 2019-09-15.Diakses tanggal2020-06-06.
- ^Nelson & Cox 2017,hlm. 324-336.
- ^Raman, Rahul; Raguram, S.; Venkataraman, Ganesh; Paulson, James C.; Sasisekharan, Ram (21 Oktober 2005)."Glycomics: an integrated systems approach to structure-function relationships of glycans".Nature Methods(dalam bahasa Inggris).2(11): 817–824.doi:10.1038/nmeth807.ISSN1548-7105.Diarsipkandari versi asli tanggal 2022-07-18.Diakses tanggal2020-06-06.
- ^Nelson & Cox 2017,hlm. 717-752.
- ^Sierra, Saleta; Kupfer, Bernd; Kaiser, Rolf (2005-12-01)."Basics of the virology of HIV-1 and its replication".Journal of Clinical Virology.Focus on HIV (dalam bahasa Inggris).34(4): 233–244.doi:10.1016/j.jcv.2005.09.004.ISSN1386-6532.Diarsipkandari versi asli tanggal 2016-02-25.Diakses tanggal2020-06-08.
- ^Wimmer M, Rose I (1978). "Mechanisms of enzyme-catalyzed group transfer reactions".Annu Rev Biochem.47:1031–78.doi:10.1146/annurev.bi.47.070178.005123.PMID354490.
- ^Mitchell, Peter (Maret 1979)."Compartmentation and Communication in Living Systems. Ligand Conduction: a General Catalytic Principle in Chemical, Osmotic and Chemiosmotic Reaction Systems".European Journal of Biochemistry(dalam bahasa Inggris).95(1): 1–20.doi:10.1111/j.1432-1033.1979.tb12934.x.ISSN1432-1033.Diarsipkan dariversi aslitanggal 2020-10-30.Diakses tanggal2020-06-09.
- ^Wimmer, Mary J.; Rose, Irwin A. (1 Juni 1978)."Mechanisms of Enzyme-Catalyzed Group Transfer Reactions".Annual Review of Biochemistry.47(1): 1031–1078.doi:10.1146/annurev.bi.47.070178.005123.ISSN0066-4154.Diarsipkan dariversi aslitanggal 2022-07-18.Diakses tanggal2020-06-09.
- ^abcDimroth P, von Ballmoos C, Meier T (March 2006)."Catalytic and mechanical cycles in F-ATP synthases: Fourth in the Cycles Review Series".EMBO Rep.7(3): 276–82.doi:10.1038/sj.embor.7400646.PMC1456893
 .PMID16607397.
.PMID16607397.
- ^Dimroth, Peter; von Ballmoos, Christoph; Meier, T (1 Maret 2006)."Catalytic and mechanical cycles in F-ATP synthases".EMBO reports.7(3): 276–282.doi:10.1038/sj.embor.7400646.ISSN1469-221X.PMC1456893
 .PMID16607397.Diarsipkan dariversi aslitanggal 2020-06-09.Diakses tanggal2020-06-09.
.PMID16607397.Diarsipkan dariversi aslitanggal 2020-06-09.Diakses tanggal2020-06-09.
- ^Bonora, Massimo; Patergnani, Simone; Rimessi, Alessandro; De Marchi, Elena; Suski, Jan M.; Bononi, Angela; Giorgi, Carlotta; Marchi, Saverio; Missiroli, Sonia (12 September 2012)."ATP synthesis and storage".Purinergic Signalling(dalam bahasa Inggris).8(3): 343–357.doi:10.1007/s11302-012-9305-8.ISSN1573-9538.PMC3360099
 .PMID22528680.
.PMID22528680.
- ^Berg, Jeremy M.; Tymoczko, John L.; Stryer, Lubert (2002)."Vitamins Are Often Precursors to Coenzymes".Biochemistry. 5th edition(dalam bahasa Inggris).Diarsipkandari versi asli tanggal 2020-12-15.Diakses tanggal2020-06-09.
- ^Pollak, Nadine; Dölle, Christian; Ziegler, Mathias (1 Maret 2007)."The power to reduce: pyridine nucleotides – small molecules with a multitude of functions".Biochemical Journal(dalam bahasa Inggris).402(2): 205–218.doi:10.1042/BJ20061638.ISSN0264-6021.PMC1798440
 .PMID17295611.Diarsipkandari versi asli tanggal 2022-06-15.Diakses tanggal2020-06-09.
.PMID17295611.Diarsipkandari versi asli tanggal 2022-06-15.Diakses tanggal2020-06-09.
- ^Fatih, Yildiz (2009).Advances in food biochemistry.Boca Raton: CRC Press. hlm. 228.ISBN978-1-4200-0769-5.OCLC607553259.
- ^Heymsfield, S. B.; Waki, M.; Kehayias, J.; Lichtman, S.; Dilmanian, F. A.; Kamen, Y.; Wang, J.; Pierson, R. N. (1991-08-01)."Chemical and elemental analysis of humans in vivo using improved body composition models".American Journal of Physiology-Endocrinology and Metabolism(dalam bahasa Inggris).261(2): E190–E198.doi:10.1152/ajpendo.1991.261.2.E190.ISSN0193-1849.
- ^"ELECTROLYTE BALANCE".opentextbc.Diarsipkan dariversi aslitanggal 2020-06-02.Diakses tanggal23 June2020.
- ^Lodish, Harvey; Berk, Arnold; Zipursky, S. Lawrence; Matsudaira, Paul; Baltimore, David; Darnell, James (2000)."The Action Potential and Conduction of Electric Impulses".Molecular Cell Biology. 4th edition(dalam bahasa Inggris).Diarsipkandari versi asli tanggal 2020-05-30.Diakses tanggal2020-06-23– via NCBI.
- ^Dulhunty, A. F. (2006)."EXCITATION–CONTRACTION COUPLING FROM THE 1950s INTO THE NEW MILLENNIUM".Clinical and Experimental Pharmacology and Physiology(dalam bahasa Inggris).33(9): 763–772.doi:10.1111/j.1440-1681.2006.04441.x.ISSN1440-1681.Diarsipkandari versi asli tanggal 2021-07-01.Diakses tanggal2020-06-23.
- ^Quiroz & Antonio 2018,hlm. 151.
- ^Craig & Leonard 2019,hlm. 190-196.
- ^Cousins, Robert J.; Liuzzi, Juan P.; Lichten, Louis A. (2006-08-25)."Mammalian Zinc Transport, Trafficking, and Signals".Journal of Biological Chemistry(dalam bahasa Inggris).281(34): 24085–24089.doi:10.1074/jbc.R600011200.ISSN0021-9258.
- ^Dunn, Louise L.; Rahmanto, Yohan Suryo; Richardson, Des R. (2007-02-01)."Iron uptake and metabolism in the new millennium".Trends in Cell Biology(dalam bahasa Inggris).17(2): 93–100.doi:10.1016/j.tcb.2006.12.003.Diarsipkandari versi asli tanggal 2020-06-27.Diakses tanggal2020-06-24.
- ^Alberts, Bruce; Johnson, Alexander; Lewis, Julian; Raff, Martin; Roberts, Keith; Walter, Peter (2002)."How Cells Obtain Energy from Food".Molecular Biology of the Cell. 4th edition(dalam bahasa Inggris).Diarsipkandari versi asli tanggal 2021-07-05.Diakses tanggal2020-06-25– via NCBI.
- ^Raven, Ja (2009-09-03)."Contributions of anoxygenic and oxygenic phototrophy and chemolithotrophy to carbon and oxygen fluxes in aquatic environments".Aquatic Microbial Ecology(dalam bahasa Inggris).56:177–192.doi:10.3354/ame01315.ISSN0948-3055.Diarsipkandari versi asli tanggal 2020-06-25.Diakses tanggal2020-06-25.
- ^"Electron Source - an overview | ScienceDirect Topics".www.sciencedirect.com.Diarsipkandari versi asli tanggal 2020-06-25.Diakses tanggal2020-06-25.
- ^Madigan, Michael T., Martinko, John M (2006).Brock Mikrobiologie(edisi ke-11., überarb. Aufl). München: Pearson Studium. hlm. 604,621.ISBN3-8273-7187-2.OCLC162303067.Diarsipkandari versi asli tanggal 2020-06-25.Diakses tanggal2020-06-25.
- ^Alberts, Bruce; Johnson, Alexander; Lewis, Julian; Raff, Martin; Roberts, Keith; Walter, Peter (2002)."How Cells Obtain Energy from Food".Molecular Biology of the Cell. 4th edition(dalam bahasa Inggris).Diarsipkandari versi asli tanggal 2021-07-05.Diakses tanggal2020-06-25.
- ^Demirel, Yaşar, (2016).Energy: production, conversion, storage, conservation, and coupling(edisi ke-Second edition). Cham: Springer. hlm. 431.ISBN978-3-319-29650-0.OCLC945435943.Diarsipkandari versi asli tanggal 2020-08-31.Diakses tanggal2020-06-26.
- ^Häse, C. C.; Finkelstein, R. A. (1993-12-01)."Bacterial extracellular zinc-containing metalloproteases".Microbiology and Molecular Biology Reviews(dalam bahasa Inggris).57(4): 823–837.doi:10.1128/mmbr.57.4.823-837.1993.ISSN1092-2172.PMID8302217.Diarsipkandari versi asli tanggal 2020-06-27.Diakses tanggal2020-06-26.
- ^Gupta, R.; Gupta, N.; Rathi, P. (2004-06-01)."Bacterial lipases: an overview of production, purification and biochemical properties".Applied Microbiology and Biotechnology(dalam bahasa Inggris).64(6): 763–781.doi:10.1007/s00253-004-1568-8.ISSN1432-0614.
- ^Hoyle, Terence (1997-12-11)."The digestive system: linking theory and practice".British Journal of Nursing(dalam bahasa Inggris).6(22): 1285–1291.doi:10.12968/bjon.1997.6.22.1285.ISSN0966-0461.
- ^Souba, Wiley W.; Pacitti, Anthony J. (1992-11-01)."Review: How Amino Acids Get Into Cells: Mechanisms, Models, Menus, and Mediators".Journal of Parenteral and Enteral Nutrition(dalam bahasa Inggris).16(6): 569–578.doi:10.1177/0148607192016006569.ISSN1941-2444.Diarsipkandari versi asli tanggal 2020-06-28.Diakses tanggal2020-06-26.
- ^Barrett, Michael P; Walmsleyt, Adrian R; Gould, Gwyn W (1999-08-01)."Structure and function of facultative sugar transporters".Current Opinion in Cell Biology(dalam bahasa Inggris).11(4): 496–502.doi:10.1016/S0955-0674(99)80072-6.ISSN0955-0674.Diarsipkandari versi asli tanggal 2015-09-24.Diakses tanggal2020-06-26.
- ^"Glycolysis Summary".chemistry.elmhurst.edu.Diarsipkandari versi asli tanggal 2020-06-24.Diakses tanggal2020-06-27.
- ^abBouché, Clara; Serdy, Shanti; Kahn, C. Ronald; Goldfine, Allison B. (2004-10-01)."The Cellular Fate of Glucose and Its Relevance in Type 2 Diabetes".Endocrine Reviews(dalam bahasa Inggris).25(5): 807–830.doi:10.1210/er.2003-0026.ISSN0163-769X.Diarsipkandari versi asli tanggal 2020-06-30.Diakses tanggal2020-06-27.
- ^Alfarouk, Khalid O.; Verduzco, Daniel; Rauch, Cyril; Muddathir, Abdel Khalig; Bashir, Adil H. H.; Elhassan, Gamal O.; Ibrahim, Muntaser E.; Orozco, Julian David Polo; Cardone, Rosa Angela (2014-12-18)."Glycolysis, tumor metabolism, cancer growth and dissemination. A new pH-based etiopathogenic perspective and therapeutic approach to an old cancer question".Oncoscience(dalam bahasa Inggris).1(12): 777.doi:10.18632/oncoscience.109.ISSN2331-4737.PMC4303887
 .PMID25621294.
.PMID25621294.
- ^Salway, J. G. (2004).Metabolism at a glance(edisi ke-3rd ed). Malden, Mass.: Blackwell Pub. hlm. 20–21.ISBN1-4051-0716-2.OCLC53178315.
- ^abcdefghO'Neill, Luke A. J.; Kishton, Rigel J.; Rathmell, Jeff (09 2016)."A guide to immunometabolism for immunologists".Nature Reviews. Immunology.16(9): 553–565.doi:10.1038/nri.2016.70.ISSN1474-1741.PMC5001910
 .PMID27396447.Diarsipkandari versi asli tanggal 2019-02-01.Diakses tanggal2019-02-01.
.PMID27396447.Diarsipkandari versi asli tanggal 2019-02-01.Diakses tanggal2019-02-01.
- ^abcLodish, Harvey; Berk, Arnold; Kaiser, Chris A.; Krieger, Monty; Bretscher, Anthony; Ploegh, HIddle; Amon, Angelika (2016).Molecular cell biology(edisi ke-Eighth edition). New York: WH Freeman and Company. hlm. 705.ISBN9781464183393.OCLC949909675.
- ^Shlomo,, Melmed,; S.,, Polonsky, Kenneth; Reed,, Larsen, P.; Henry,, Kronenberg,.Williams textbook of endocrinology(edisi ke-Thirteenth edition). Philadelphia, PA.ISBN0323341578.OCLC932080537.p1664
- ^Sakami, W; Harrington, H (1963-06)."Amino Acid Metabolism".Annual Review of Biochemistry(dalam bahasa Inggris).32(1): 355–398.doi:10.1146/annurev.bi.32.070163.002035.ISSN0066-4154.Diarsipkan dariversi aslitanggal 2021-03-08.Diakses tanggal2020-06-30.
- ^Brosnan, John T. (2000-04-01)."Glutamate, at the Interface between Amino Acid and Carbohydrate Metabolism".The Journal of Nutrition(dalam bahasa Inggris).130(4): 988S–990S.doi:10.1093/jn/130.4.988S.ISSN0022-3166.Diarsipkandari versi asli tanggal 2010-11-06.Diakses tanggal2020-06-30.
- ^"Eukaryotic Cells | Learn Science at Scitable".www.nature.com.Diarsipkandari versi asli tanggal 2020-08-06.Diakses tanggal2020-07-01.
- ^Schultz, Brian E.; Chan, Sunney I. (2001-06-01)."Structures and Proton-Pumping Strategies of Mitochondrial Respiratory Enzymes".Annual Review of Biophysics and Biomolecular Structure.30(1): 23–65.doi:10.1146/annurev.biophys.30.1.23.ISSN1056-8700.Diarsipkan dariversi aslitanggal 2022-07-19.Diakses tanggal2020-07-01.
- ^Capaldi R, Aggeler R (2002). "Mechanism of the F(1)F(0)-type ATP synthase, a biological rotary motor".Trends Biochem Sci.27(3): 154–60.doi:10.1016/S0968-0004(01)02051-5.PMID11893513.
- ^Friedrich, B.; Schwartz, E. (1993-10-01)."Molecular biology of hydrogen utilization in aerobic chemolithotrophs".Annual Review of Microbiology.47(1): 351–383.doi:10.1146/annurev.mi.47.100193.002031.ISSN0066-4227.Diarsipkan dariversi aslitanggal 2022-07-19.Diakses tanggal2020-07-02.
- ^Friedrich, Cornelius G. (-01-01 1997). Poole, R. K., ed.Advances in Microbial Physiology(dalam bahasa Inggris).39.Academic Press. hlm. 235–289.doi:10.1016/s0065-2911(08)60018-1.ISBN978-0-12-027739-1.ISSN0065-2911.Diarsipkandari versi asli tanggal 2015-09-24.Diakses tanggal2020-07-02.
- ^Weber, Karrie A.; Achenbach, Laurie A.; Coates, John D. (01-10-2006)."Microorganisms pumping iron: anaerobic microbial iron oxidation and reduction".Nature Reviews Microbiology(dalam bahasa Inggris).4(10): 752–764.doi:10.1038/nrmicro1490.ISSN1740-1526.Diarsipkandari versi asli tanggal 2021-03-08.Diakses tanggal2020-07-02.
- ^Jetten, Mike S.M.; Strous, Marc; van de Pas-Schoonen, Katinka T.; Schalk, Jos; van Dongen, Udo G.J.M.; van de Graaf, Astrid A.; Logemann, Susanne; Muyzer, Gerard; van Loosdrecht, Mark C.M. (1998-12-01)."The anaerobic oxidation of ammonium".FEMS Microbiology Reviews(dalam bahasa Inggris).22(5): 421–437.doi:10.1111/j.1574-6976.1998.tb00379.x.ISSN1574-6976.Diarsipkandari versi asli tanggal 2021-12-31.Diakses tanggal2020-07-02.
- ^Simon, Jörg (2002-08-01)."Enzymology and bioenergetics of respiratory nitrite ammonification".FEMS Microbiology Reviews(dalam bahasa Inggris).26(3): 285–309.doi:10.1111/j.1574-6976.2002.tb00616.x.ISSN1574-6976.Diarsipkandari versi asli tanggal 2021-10-19.Diakses tanggal2020-07-02.
- ^Barea, José-Miguel; Pozo, María José; Azcón, Rosario; Azcón-Aguilar, Concepción (2005-07-01)."Microbial co-operation in the rhizosphere".Journal of Experimental Botany(dalam bahasa Inggris).56(417): 1761–1778.doi:10.1093/jxb/eri197.ISSN1460-2431.Diarsipkandari versi asli tanggal 2021-12-31.Diakses tanggal2020-07-02.
- ^Conrad, R (1996-12-01)."Soil microorganisms as controllers of atmospheric trace gases (H2, CO, CH4, OCS, N2O, and NO)".Microbiological reviews(dalam bahasa Inggris).60(4): 609–640.doi:10.1128/MMBR.60.4.609-640.1996.ISSN0146-0749.Diarsipkandari versi asli tanggal 2020-07-02.Diakses tanggal2020-07-02.
- ^van der Meer, Marcel T. J.; Schouten, Stefan; Bateson, Mary M.; Nübel, Ulrich; Wieland, Andrea; Kühl, Michael; de Leeuw, Jan W.; Sinninghe Damsté, Jaap S.; Ward, David M. (2005-07)."Diel Variations in Carbon Metabolism by Green Nonsulfur-Like Bacteria in Alkaline Siliceous Hot Spring Microbial Mats from Yellowstone National Park".Applied and Environmental Microbiology(dalam bahasa Inggris).71(7): 3978–3986.doi:10.1128/AEM.71.7.3978-3986.2005.ISSN0099-2240.PMC1168979
 .PMID16000812.Diarsipkan dariversi aslitanggal 2020-07-04.Diakses tanggal2020-07-03.
.PMID16000812.Diarsipkan dariversi aslitanggal 2020-07-04.Diakses tanggal2020-07-03.
- ^Tichi, Mary A.; Tabita, F. Robert (2001-11-01)."Interactive Control of Rhodobactercapsulatus Redox-Balancing Systems during Phototrophic Metabolism".Journal of Bacteriology(dalam bahasa Inggris).183(21): 6344–6354.doi:10.1128/JB.183.21.6344-6354.2001.ISSN1098-5530.PMC100130
 .PMID11591679.Diarsipkan dariversi aslitanggal 2021-03-08.Diakses tanggal2020-07-03.
.PMID11591679.Diarsipkan dariversi aslitanggal 2021-03-08.Diakses tanggal2020-07-03.
- ^Alberts, Bruce; Johnson, Alexander; Lewis, Julian; Raff, Martin; Roberts, Keith; Walter, Peter (2002)."Energy Conversion: Mitochondria and Chloroplasts".Molecular Biology of the Cell. 4th edition(dalam bahasa Inggris).Diarsipkandari versi asli tanggal 2020-12-15.Diakses tanggal2020-07-03.
- ^Allen, J. P.; Williams, J. C. (08-12-1998)."Photosynthetic reaction centers".FEBS Letters(dalam bahasa Inggris).438(1-2): 5–9.doi:10.1016/S0014-5793(98)01245-9.ISSN1873-3468.Diarsipkan dariversi aslitanggal 2022-04-11.Diakses tanggal2020-07-03.
- ^Nelson, Nathan; Ben-Shem, Adam (2004-12-01)."The complex architecture of oxygenic photosynthesis".Nature Reviews Molecular Cell Biology(dalam bahasa Inggris).5(12): 971–982.doi:10.1038/nrm1525.ISSN1471-0072.Diarsipkandari versi asli tanggal 2021-03-08.Diakses tanggal2020-07-03.
- ^Munekage, Yuri; Hashimoto, Mihoko; Miyake, Chikahiro; Tomizawa, Ken-Ichi; Endo, Tsuyoshi; Tasaka, Masao; Shikanai, Toshiharu (2004-06)."Cyclic electron flow around photosystem I is essential for photosynthesis".Nature(dalam bahasa Inggris).429(6991): 579–582.doi:10.1038/nature02598.ISSN0028-0836.Diarsipkandari versi asli tanggal 2022-08-03.Diakses tanggal2020-07-03.
- ^abMandal, Ananya (2009-11-26)."What is Anabolism?".News-Medical.net(dalam bahasa Inggris).Diarsipkandari versi asli tanggal 2020-07-05.Diakses tanggal2020-07-04.
- ^Miziorko, H M; Lorimer, G H (1983-06)."Ribulose-1,5-Bisphosphate Carboxylase-Oxygenase".Annual Review of Biochemistry(dalam bahasa Inggris).52(1): 507–535.doi:10.1146/annurev.bi.52.070183.002451.ISSN0066-4154.Diarsipkan dariversi aslitanggal 2021-03-08.Diakses tanggal2020-07-07.
- ^Dodd, Antony N.; Borland, Anne M.; Haslam, Richard P.; Griffiths, Howard; Maxwell, Kate (2002-04-01)."Crassulacean acid metabolism: plastic, fantastic".Journal of Experimental Botany(dalam bahasa Inggris).53(369): 569–580.doi:10.1093/jexbot/53.369.569.ISSN0022-0957.Diarsipkandari versi asli tanggal 2020-07-07.Diakses tanggal2020-07-07.
- ^Hügler, Michael; Wirsen, Carl O.; Fuchs, Georg; Taylor, Craig D.; Sievert, Stefan M. (2005-05-01)."Evidence for Autotrophic CO2 Fixation via the Reductive Tricarboxylic Acid Cycle by Members of the ε Subdivision of Proteobacteria".Journal of Bacteriology(dalam bahasa Inggris).187(9): 3020–3027.doi:10.1128/JB.187.9.3020-3027.2005.ISSN0021-9193.PMC1082812
 .PMID15838028.Diarsipkan dariversi aslitanggal 2020-09-21.Diakses tanggal2020-07-07.
.PMID15838028.Diarsipkan dariversi aslitanggal 2020-09-21.Diakses tanggal2020-07-07.
- ^Strauss, Gerhard; Fuchs, Georg (1993-08)."Enzymes of a novel autotrophic CO2 fixation pathway in the phototrophic bacterium Chloroflexus aurantiacus, the 3-hydroxypropionate cycle".European Journal of Biochemistry(dalam bahasa Inggris).215(3): 633–643.doi:10.1111/j.1432-1033.1993.tb18074.x.ISSN0014-2956.
- ^Wood, Harland G. (1991-02)."Life with CO or CO 2 and H 2 as a source of carbon and energy".The FASEB Journal(dalam bahasa Inggris).5(2): 156–163.doi:10.1096/fasebj.5.2.1900793.ISSN0892-6638.
- ^Shively, Jessup M.; van Keulen, Geertje; Meijer, Wim G. (1998-10)."SOMETHING FROM ALMOST NOTHING: Carbon Dioxide Fixation in Chemoautotrophs".Annual Review of Microbiology(dalam bahasa Inggris).52(1): 191–230.doi:10.1146/annurev.micro.52.1.191.ISSN0066-4227.Diarsipkan dariversi aslitanggal 2021-06-07.Diakses tanggal2020-07-07.
- ^"Design of glycolysis".Philosophical Transactions of the Royal Society of London. B, Biological Sciences(dalam bahasa Inggris).293(1063): 5–22. 1981-06-26.doi:10.1098/rstb.1981.0056.ISSN0080-4622.Diarsipkandari versi asli tanggal 2019-10-26.Diakses tanggal2020-07-08.
- ^Pilkis, S. J.; El-Maghrabi, M. R.; Claus, T. H. (1990-06-01)."Fructose-2,6-Bisphosphate in Control of Hepatic Gluconeogenesis: From Metabolites to Molecular Genetics".Diabetes Care(dalam bahasa Inggris).13(6): 582–599.doi:10.2337/diacare.13.6.582.ISSN0149-5992.Diarsipkandari versi asli tanggal 2022-08-16.Diakses tanggal2020-07-08.
- ^Evans, Rhys D.; Heather, Lisa C. (2016-06)."Metabolic pathways and abnormalities".Surgery (Oxford).34(6): 266–272.doi:10.1016/j.mpsur.2016.03.010.ISSN0263-9319.
- ^Freeze, Hudson H.; Hart, Gerald W.; Schnaar, Ronald L. (2015). Varki, Ajit; Cummings, Richard D.; Esko, Jeffrey D.; Stanley, Pamela; Hart, Gerald W.; Aebi, Markus; Darvill, Alan G.; Kinoshita, Taroh; Packer, Nicolle H., ed.Essentials of Glycobiology(edisi ke-3). Cold Spring Harbor (NY): Cold Spring Harbor Laboratory Press.PMID28876856.Diarsipkandari versi asli tanggal 2022-02-24.Diakses tanggal2020-07-08.
- ^Opdenakker, Ghislain; Rudd, Pauline M.; Ponting, Christopher P.; Dwek, Raymond A. (1993-11)."Concepts and principles of glycobiology".The FASEB Journal(dalam bahasa Inggris).7(14): 1330–1337.doi:10.1096/fasebj.7.14.8224606.ISSN0892-6638.
- ^McConville, Malcolm J.; Menon, Anant K. (2000-01)."Recent developments in the cell biology and biochemistry of glycosylphosphatidylinositol lipids (Review)".Molecular Membrane Biology(dalam bahasa Inggris).17(1): 1–16.doi:10.1080/096876800294443.ISSN0968-7688.
- ^White, Stephen W.; Zheng, Jie; Zhang, Yong-Mei; Rock, Charles O. (2005-06)."THE STRUCTURAL BIOLOGY OF TYPE II FATTY ACID BIOSYNTHESIS".Annual Review of Biochemistry(dalam bahasa Inggris).74(1): 791–831.doi:10.1146/annurev.biochem.74.082803.133524.ISSN0066-4154.Diarsipkan dariversi aslitanggal 2020-07-11.Diakses tanggal2020-07-10.
- ^Ohlrogge, John B.; Jaworski, Jan G. (1997-06)."REGULATION OF FATTY ACID SYNTHESIS".Annual Review of Plant Physiology and Plant Molecular Biology(dalam bahasa Inggris).48(1): 109–136.doi:10.1146/annurev.arplant.48.1.109.ISSN1040-2519.Diarsipkan dariversi aslitanggal 2020-05-02.Diakses tanggal2020-07-10.
- ^Nye CK; Hanson, Richard W.; Kalhan, Satish C. (2008-10-10)."Glyceroneogenesis Is the Dominant Pathway for Triglyceride Glycerol Synthesis in Vivo in the Rat".Journal of Biological Chemistry(dalam bahasa Inggris).283(41): 27565–27574.doi:10.1074/jbc.M804393200.ISSN0021-9258.PMC2562054
 .PMID18662986.
.PMID18662986.
- ^Dubey, Vinod Shanker; Bhalla, Ritu; Luthra, Rajesh (2003-09)."An overview of the non-mevalonate pathway for terpenoid biosynthesis in plants"(PDF).Journal of Biosciences(dalam bahasa Inggris).28(5): 637–646.doi:10.1007/BF02703339.ISSN0250-5991.Archived from the original on 2007-04-15.Diakses tanggal2020-07-11.
- ^abKuzuyama, Tomohisa; Seto, Haruo (2003-03-25)."Diversity of the biosynthesis of the isoprene units".Natural Product Reports.20(2): 171–183.doi:10.1039/b109860h.
- ^Grochowski, Laura L.; Xu, Huimin; White, Robert H. (2006-05-01)."Methanocaldococcus jannaschii Uses a Modified Mevalonate Pathway for Biosynthesis of Isopentenyl Diphosphate".Journal of Bacteriology(dalam bahasa Inggris).188(9): 3192–3198.doi:10.1128/JB.188.9.3192-3198.2006.ISSN0021-9193.PMC1447442
 .PMID16621811.Diarsipkan dariversi aslitanggal 2020-07-12.Diakses tanggal2020-07-11.
.PMID16621811.Diarsipkan dariversi aslitanggal 2020-07-12.Diakses tanggal2020-07-11.
- ^Lichtenthaler, Hartmut K. (1999-06-01)."The 1-deoxy-d-xylulose-5-phosphate pathway of isoprenoid biosynthesis in plants".Annual Review of Plant Physiology and Plant Molecular Biology.50(1): 47–65.doi:10.1146/annurev.arplant.50.1.47.ISSN1040-2519.Diarsipkan dariversi aslitanggal 2021-07-15.Diakses tanggal2020-07-11.
- ^abSchroepfer, G J (1981-06-01)."Sterol Biosynthesis".Annual Review of Biochemistry.50(1): 585–621.doi:10.1146/annurev.bi.50.070181.003101.ISSN0066-4154.Diarsipkan dariversi aslitanggal 2020-07-11.Diakses tanggal2020-07-11.
- ^Lees, N. D.; Skaggs, B.; Kirsch, D. R.; Bard, M. (1995-03)."Cloning of the late genes in the ergosterol biosynthetic pathway ofSaccharomyces cerevisiae—A review".Lipids(dalam bahasa Inggris).30(3): 221–226.doi:10.1007/BF02537824.ISSN0024-4201.
- ^abYang, Qin; Vijayakumar, Archana; Kahn, Barbara B. (2018-10)."Metabolites as regulators of insulin sensitivity and metabolism".Nature Reviews. Molecular Cell Biology.19(10): 654–672.doi:10.1038/s41580-018-0044-8.ISSN1471-0080.PMID30104701.Diarsipkandari versi asli tanggal 2019-02-01.Diakses tanggal2019-02-01.
- ^Nelson DL, Cox MM (2005).Lehninger principles of biochemistry(edisi ke-4). New York: W.H. Freeman and Company. hlm. 841.ISBN0-7167-4339-6.OCLC55476414.
- ^Himmelreich, R.; Hilbert, H.; Plagens, H.; Pirkl, E.; Li, B.-C.; Herrmann, R. (1996-11-01)."Complete Sequence Analysis of the Genome of the Bacterium Mycoplasma Pneumoniae".Nucleic Acids Research(dalam bahasa Inggris).24(22): 4420–4449.doi:10.1093/nar/24.22.4420.ISSN0305-1048.PMC146264
 .PMID8948633.Diarsipkandari versi asli tanggal 2021-12-31.Diakses tanggal2020-07-13.
.PMID8948633.Diarsipkandari versi asli tanggal 2021-12-31.Diakses tanggal2020-07-13.
- ^Guyton, AC, Hall JE (2006).Textbook of medical physiology(PDF)(edisi ke-11th ed). Philadelphia: Elsevier Saunders. hlm. 855.ISBN0-7216-0240-1.OCLC56661571.Diarsipkan dariversi asli(PDF)tanggal 2020-07-14.Diakses tanggal2020-07-13.
- ^Ibba M, Söll D (2001-05-01)."The renaissance of aminoacyl-tRNA synthesis".EMBO reports.2(5): 382–387.doi:10.1093/embo-reports/kve095.ISSN1469-221X.PMC1083889
 .PMID11375928.Diarsipkan dariversi aslitanggal 2020-07-13.Diakses tanggal2020-07-13.
.PMID11375928.Diarsipkan dariversi aslitanggal 2020-07-13.Diakses tanggal2020-07-13.
- ^Lengyel, P.; Söll, D. (1969-06-01)."Mechanism of protein biosynthesis".Microbiology and Molecular Biology Reviews(dalam bahasa Inggris).33(2): 264–301.doi:10.1128/mmbr.33.2.264-301.1969.ISSN1092-2172.PMID4896351.Diarsipkandari versi asli tanggal 2020-07-14.Diakses tanggal2020-07-13.
- ^Lengyel P, Söll D (June 1969)."Mechanism of protein biosynthesis".Bacteriological Reviews.33(2): 264–301.doi:10.1128/MMBR.33.2.264-301.1969.PMC378322
 .PMID4896351.
.PMID4896351.
- ^abRudolph, Frederick B. (1994-01-01)."The Biochemistry and Physiology of Nucleotides".The Journal of Nutrition(dalam bahasa Inggris).124(suppl_1): 124S–127S.doi:10.1093/jn/124.suppl_1.124S.ISSN0022-3166.Diarsipkandari versi asli tanggal 2021-03-08.Diakses tanggal2020-07-14.
- ^abZrenner, Rita; Stitt, Mark; Sonnewald, Uwe; Boldt, Ralf (Mei 2005)."Pyrimidine and purine biosynthesis and degradation in plants".Annual Review of Plant Biology.57(1): 805–836.doi:10.1146/annurev.arplant.57.032905.105421.ISSN1543-5008.Diarsipkan dariversi aslitanggal 2021-03-08.Diakses tanggal2020-07-14.
- ^Stasolla, Claudio; Katahira, Riko; Thorpe, Trevor A.; Ashihara, Hiroshi (January 2003)."Purine and pyrimidine nucleotide metabolism in higher plants".Journal of Plant Physiology(dalam bahasa Inggris).160(11): 1271–1295.doi:10.1078/0176-1617-01169.ISSN0176-1617.Diarsipkandari versi asli tanggal 2020-07-14.Diakses tanggal2020-07-14.
- ^Davies, Oluwafemi; Mendes, Pedro; Smallbone, Kieran; Malys, Naglis (April 2012)."Characterisation of multiple substrate-specific (d)ITP/(d)XTPase and modelling of deaminated purine nucleotide metabolism".BMB Reports.45(4): 259–264.doi:10.5483/BMBRep.2012.45.4.259.ISSN1976-670X.Diarsipkandari versi asli tanggal 2020-07-15.Diakses tanggal2020-07-14.
- ^Smith, Janet L (Desember 1995)."Enzymes of nucleotide synthesis".Current Opinion in Structural Biology(dalam bahasa Inggris).5(6): 752–757.doi:10.1016/0959-440X(95)80007-7.ISSN0959-440X.Diarsipkandari versi asli tanggal 2015-09-24.Diakses tanggal2020-07-14.
- ^Testa, Bernard; Krämer, Stefanie D. (Oktober 2006)."The Biochemistry of Drug Metabolism – An Introduction".Chemistry & Biodiversity(dalam bahasa Inggris).3(10): 1053–1101.doi:10.1002/cbdv.200690111.ISSN1612-1880.Diarsipkandari versi asli tanggal 2020-07-16.Diakses tanggal2020-07-16.
- ^Danielson, P. B. (Desember 2002)."The Cytochrome P450 Superfamily: Biochemistry, Evolution and Drug Metabolism in Humans".Current Drug Metabolism(dalam bahasa Inggris).doi:10.2174/1389200023337054.Diarsipkandari versi asli tanggal 2020-07-19.Diakses tanggal2020-07-16.
- ^Danielson PB (December 2002). "The cytochrome P450 superfamily: biochemistry, evolution and drug metabolism in humans".Current Drug Metabolism.3(6): 561–97.doi:10.2174/1389200023337054.PMID12369887.
- ^King, C. D.; Rios, G. R.; Tephly, M. D. Green and T. R. (Agustus 2000)."UDP-Glucuronosyltransferases".Current Drug Metabolism(dalam bahasa Inggris).doi:10.2174/1389200003339171.Diarsipkandari versi asli tanggal 2020-07-16.Diakses tanggal2020-07-16.
- ^Sheehan, D.; Meade, G.; Foley, V. M.; Dowd, C. A. (November 2001)."Structure, function and evolution of glutathione transferases: implications for classification of non-mammalian members of an ancient enzyme superfamily".The Biochemical Journal.360(Pt 1): 1–16.doi:10.1042/0264-6021:3600001.ISSN0264-6021.PMC1222196
 .PMID11695986.Diarsipkandari versi asli tanggal 2020-06-29.Diakses tanggal2020-07-16.
.PMID11695986.Diarsipkandari versi asli tanggal 2020-06-29.Diakses tanggal2020-07-16.
- ^Galvão, Teca Calcagno; Mohn, William W.; Lorenzo, Víctor de (Oktober 2005)."Exploring the microbial biodegradation and biotransformation gene pool".Trends in Biotechnology(dalam bahasa English).23(10): 497–506.doi:10.1016/j.tibtech.2005.08.002.ISSN0167-7799.PMID16125262.Diarsipkandari versi asli tanggal 2013-10-14.Diakses tanggal2020-07-16.
- ^Janssen, Dick B.; Dinkla, Inez J. T.; Poelarends, Gerrit J.; Terpstra, Peter (2005)."Bacterial degradation of xenobiotic compounds: evolution and distribution of novel enzyme activities".Environmental Microbiology(dalam bahasa Inggris).7(12): 1868–1882.doi:10.1111/j.1462-2920.2005.00966.x.ISSN1462-2920.Diarsipkan dariversi aslitanggal 2022-04-11.Diakses tanggal2020-07-16.
- ^Rice-Evans, C.; Halliwell, B.; Lunt, G. G.; Davies, Kelvin J. A. (November 1995)."Oxidative stress: the paradox of aerobic life".Biochemical Society Symposia(dalam bahasa Inggris).61:1–31.doi:10.1042/bss0610001.ISSN0067-8694.Diarsipkandari versi asli tanggal 2020-07-17.Diakses tanggal2020-07-16.
- ^Tu, Benjamin P.; Weissman, Jonathan S. (Februari 2004)."Oxidative protein folding in eukaryotes".The Journal of Cell Biology.164(3): 341–346.doi:10.1083/jcb.200311055.ISSN0021-9525.PMC2172237
 .PMID14757749.Diarsipkandari versi asli tanggal 2021-03-08.Diakses tanggal2020-07-16.
.PMID14757749.Diarsipkandari versi asli tanggal 2021-03-08.Diakses tanggal2020-07-16.
- ^Sies, H (Maret 1997)."Oxidative stress: oxidants and antioxidants".Experimental Physiology(dalam bahasa Inggris).82(2): 291–295.doi:10.1113/expphysiol.1997.sp004024.
- ^Vertuani S; Manfredini S; Angusti A (Mei 2004)."The Antioxidants and Pro-Antioxidants Network: An Overview".Current Pharmaceutical Design(dalam bahasa Inggris).doi:10.2174/1381612043384655.Diarsipkandari versi asli tanggal 2020-07-16.Diakses tanggal2020-07-16.
- ^von Stockar, U.; Liu, J. -S. (Agustus 1998)."Does microbial life always feed on negative entropy? Thermodynamic analysis of microbial growth".Biochimica et Biophysica Acta (BBA) - Bioenergetics(dalam bahasa Inggris).1412(3): 191–211.doi:10.1016/S0005-2728(99)00065-1.ISSN0005-2728.Diarsipkandari versi asli tanggal 2020-07-18.Diakses tanggal2020-07-17.
- ^Demirel, Y.; Sandler, S. I. (2002-06-19)."Thermodynamics and bioenergetics".Biophysical Chemistry(dalam bahasa Inggris).97(2): 87–111.doi:10.1016/S0301-4622(02)00069-8.ISSN0301-4622.Diarsipkandari versi asli tanggal 2015-09-24.Diakses tanggal2020-07-17.
- ^Albert R (2005)."Scale-free networks in cell biology".J Cell Sci.118(Pt 21): 4947–57.arXiv:q-bio/0510054
 .doi:10.1242/jcs.02714.PMID16254242.Diarsipkandari versi asli tanggal 2007-04-12.Diakses tanggal2023-03-09.
.doi:10.1242/jcs.02714.PMID16254242.Diarsipkandari versi asli tanggal 2007-04-12.Diakses tanggal2023-03-09.
- ^Brand M (1997)."Regulation analysis of energy metabolism".J Exp Biol.200(Pt 2): 193–202.PMID9050227.Diarsipkandari versi asli tanggal 2007-03-29.Diakses tanggal2019-01-31.
- ^abSalter, M.; Knowles, R. G.; Pogson, C. I. (1994)."Metabolic control".Essays in Biochemistry.28:1–12.ISSN0071-1365.PMID7925313.Diarsipkandari versi asli tanggal 2020-07-19.Diakses tanggal2020-07-18.
- ^Westerhoff, Hans V.; Groen, Albert K.; Wanders, Ronald J. A. (January 1984)."Modern theories of metabolic control and their applicationsReview".Bioscience Reports(dalam bahasa Inggris).4(1): 1–22.doi:10.1007/BF01120819.ISSN0144-8463.Diarsipkandari versi asli tanggal 2020-07-19.Diakses tanggal2020-07-18.
- ^Fell DA, Thomas S (October 1995)."Physiological control of metabolic flux: the requirement for multisite modulation".The Biochemical Journal.311 ( Pt 1) (Pt 1): 35–9.doi:10.1042/bj3110035.PMC1136115
 .PMID7575476.
.PMID7575476.
- ^Hendrickson WA (November 2005). "Transduction of biochemical signals across cell membranes".Quarterly Reviews of Biophysics.38(4): 321–30.doi:10.1017/S0033583506004136.PMID16600054.
- ^Cohen, Philip (Desember 2000)."The regulation of protein function by multisite phosphorylation – a 25 year update".Trends in Biochemical Sciences(dalam bahasa English).25(12): 596–601.doi:10.1016/S0968-0004(00)01712-6.ISSN0968-0004.PMID11116185.Diarsipkandari versi asli tanggal 2013-10-12.Diakses tanggal2020-07-18.
- ^Lienhard, G. E.; Slot, J. W.; James, D. E.; Mueckler, M. M. (1992-01)."How cells absorb glucose".Scientific American.266(1): 86–91.doi:10.1038/scientificamerican0192-86.ISSN0036-8733.PMID1734513.Diarsipkandari versi asli tanggal 2020-07-16.Diakses tanggal2020-07-18.
- ^Roach, Peter J. (Maret 2002)."Glycogen and its metabolism".Current Molecular Medicine.2(2): 101–120.doi:10.2174/1566524024605761.ISSN1566-5240.PMID11949930.Diarsipkandari versi asli tanggal 2020-07-18.Diakses tanggal2020-07-18.
- ^Newgard, C. B.; Brady, M. J.; O'Doherty, R. M.; Saltiel, A. R. (Desember 2000)."Organizing glucose disposal: emerging roles of the glycogen targeting subunits of protein phosphatase-1".Diabetes(dalam bahasa Inggris).49(12): 1967–1977.doi:10.2337/diabetes.49.12.1967.ISSN0012-1797.PMID11117996.Diarsipkandari versi asli tanggal 2020-07-19.Diakses tanggal2020-07-18.
- ^Smith, Eric; Morowitz, Harold J. (September 2004)."Universality in intermediary metabolism".Proceedings of the National Academy of Sciences(dalam bahasa Inggris).101(36): 13168–13173.doi:10.1073/pnas.0404922101.ISSN0027-8424.PMC516543
 .PMID15340153.Diarsipkandari versi asli tanggal 2020-12-04.Diakses tanggal2020-07-20.
.PMID15340153.Diarsipkandari versi asli tanggal 2020-12-04.Diakses tanggal2020-07-20.
- ^Romano, AH; Conway, T (Juli 1996)."Evolution of carbohydrate metabolic pathways".Research in Microbiology(dalam bahasa Inggris).147(6): 448–455.doi:10.1016/0923-2508(96)83998-2.ISSN0923-2508.Diarsipkandari versi asli tanggal 2020-11-01.Diakses tanggal2020-07-20.
- ^Koch, Arthur L. (Januari 1998). Poole, R. K., ed.Advances in Microbial Physiology.Advances in Microbial Physiology (dalam bahasa Inggris).40.Academic Press. hlm. 353–399.doi:10.1016/s0065-2911(08)60135-6.Diarsipkandari versi asli tanggal 2015-09-24.Diakses tanggal2020-07-20.
- ^Ouzounis, Christos; Kyrpides, Nikos (Juli 1996)."The emergence of major cellular processes in evolution".FEBS Letters(dalam bahasa Inggris).390(2): 119–123.doi:10.1016/0014-5793(96)00631-X.ISSN1873-3468.Diarsipkan dariversi aslitanggal 2021-03-02.Diakses tanggal2020-07-20.
- ^Ebenhöh, Oliver; Heinrich, Reinhart (January 2001)."Evolutionary optimization of metabolic pathways. Theoretical reconstruction of the stoichiometry of ATP and NADH producing systems".Bulletin of Mathematical Biology(dalam bahasa Inggris).63(1): 21–55.doi:10.1006/bulm.2000.0197.ISSN1522-9602.
- ^Meléndez-Hevia, Enrique; Waddell, Thomas G.; Cascante, Marta (September 1996)."The puzzle of the Krebs citric acid cycle: Assembling the pieces of chemically feasible reactions, and opportunism in the design of metabolic pathways during evolution".Journal of Molecular Evolution(dalam bahasa Inggris).43(3): 293–303.doi:10.1007/BF02338838.ISSN1432-1432.
- ^Caetano-Anollés, Gustavo; Kim, Hee Shin; Mittenthal, Jay E. (2007-05-29)."The origin of modern metabolic networks inferred from phylogenomic analysis of protein architecture".Proceedings of the National Academy of Sciences(dalam bahasa Inggris).104(22): 9358–9363.doi:10.1073/pnas.0701214104.ISSN0027-8424.PMC1890499
 .PMID17517598.Diarsipkandari versi asli tanggal 2020-12-06.Diakses tanggal2020-07-20.
.PMID17517598.Diarsipkandari versi asli tanggal 2020-12-06.Diakses tanggal2020-07-20.
- ^Schmidt, Steffen; Sunyaev, Shamil; Bork, Peer; Dandekar, Thomas (Juni 2003)."Metabolites: a helping hand for pathway evolution?".Trends in Biochemical Sciences(dalam bahasa English).28(6): 336–341.doi:10.1016/S0968-0004(03)00114-2.ISSN0968-0004.Diarsipkandari versi asli tanggal 2013-10-13.Diakses tanggal2020-07-20.
- ^Light, Sara; Kraulis, Per (February 2004)."Network analysis of metabolic enzyme evolution in Escherichia coli".BMC Bioinformatics.5(1): 15.doi:10.1186/1471-2105-5-15.ISSN1471-2105.PMC394313
 .PMID15113413.
.PMID15113413.
- ^Alves, Rui; Chaleil, Raphael A. G; Sternberg, Michael J. E (Juli 2002)."Evolution of Enzymes in Metabolism: A Network Perspective".Journal of Molecular Biology(dalam bahasa Inggris).320(4): 751–770.doi:10.1016/S0022-2836(02)00546-6.ISSN0022-2836.Diarsipkandari versi asli tanggal 2015-09-24.Diakses tanggal2020-07-20.
- ^Kim, Hee Shin; Mittenthal, Jay E.; Caetano-Anollés, Gustavo (2006-07-19)."MANET: tracing evolution of protein architecture in metabolic networks".BMC Bioinformatics.7(1): 351.doi:10.1186/1471-2105-7-351.ISSN1471-2105.PMC1559654
 .PMID16854231.
.PMID16854231.
- ^Teichmann, Sarah A.; Rison, Stuart C. G.; Thornton, Janet M.; Riley, Monica; Gough, Julian; Chothia, Cyrus (2001-12-01)."Small-molecule metabolism: an enzyme mosaic".Trends in Biotechnology(dalam bahasa English).19(12): 482–486.doi:10.1016/S0167-7799(01)01813-3.ISSN0167-7799.PMID11711174.
- ^Spirin, Victor; Gelfand, Mikhail S.; Mironov, Andrey A.; Mirny, Leonid A. (2006-06-06)."A metabolic network in the evolutionary context: Multiscale structure and modularity".Proceedings of the National Academy of Sciences(dalam bahasa Inggris).103(23): 8774–8779.doi:10.1073/pnas.0510258103.ISSN0027-8424.PMC1482654
 .PMID16731630.Diarsipkandari versi asli tanggal 2020-12-05.Diakses tanggal2020-07-20.
.PMID16731630.Diarsipkandari versi asli tanggal 2020-12-05.Diakses tanggal2020-07-20.
- ^Lawrence, Jeffrey G (Desember 2005)."Common themes in the genome strategies of pathogens".Current Opinion in Genetics & Development.Genomes and evolution (dalam bahasa Inggris).15(6): 584–588.doi:10.1016/j.gde.2005.09.007.ISSN0959-437X.
- ^Wernegreen, Jennifer J (Desember 2005)."For better or worse: genomic consequences of intracellular mutualism and parasitism".Current Opinion in Genetics & Development.Genomes and evolution (dalam bahasa Inggris).15(6): 572–583.doi:10.1016/j.gde.2005.09.013.ISSN0959-437X.Diarsipkandari versi asli tanggal 2015-09-24.Diakses tanggal2020-07-20.
- ^Pál, Csaba; Papp, Balázs; Lercher, Martin J.; Csermely, Péter; Oliver, Stephen G.; Hurst, Laurence D. (2006-03)."Chance and necessity in the evolution of minimal metabolic networks".Nature(dalam bahasa Inggris).440(7084): 667–670.doi:10.1038/nature04568.ISSN1476-4687.Diarsipkandari versi asli tanggal 2021-02-12.Diakses tanggal2020-07-20.
- ^Rennie, Michael J. (November 1999)."An introduction to the use of tracers in nutrition and metabolism".Proceedings of the Nutrition Society(dalam bahasa Inggris).58(4): 935–944.doi:10.1017/S002966519900124X.ISSN1475-2719.Diarsipkandari versi asli tanggal 2020-08-31.Diakses tanggal2020-07-22.
- ^Phair, Robert D. (1997-12)."Development of kinetic models in the nonlinear world of molecular cell biology".Metabolism.46(12): 1489–1495.doi:10.1016/s0026-0495(97)90154-2.ISSN0026-0495.
- ^Sterck, Lieven; Rombauts, Stephane; Vandepoele, Klaas; Rouzé, Pierre; Van de Peer, Yves (April 2007)."How many genes are there in plants (… and why are they there)?".Current Opinion in Plant Biology.Genome Studies and Molecular Genetics / Edited by Stefan Jansson and Edward S Buckler (dalam bahasa Inggris).10(2): 199–203.doi:10.1016/j.pbi.2007.01.004.ISSN1369-5266.Diarsipkandari versi asli tanggal 2020-07-22.Diakses tanggal2020-07-22.
- ^Borodina, Irina; Nielsen, Jens (June 2005)."From genomes to in silico cells via metabolic networks".Current Opinion in Biotechnology.Environmental biotechnology/Systems biology (dalam bahasa Inggris).16(3): 350–355.doi:10.1016/j.copbio.2005.04.008.ISSN0958-1669.
- ^Gianchandani EP, Brautigan DL, Papin JA (May 2006). "Systems analyses characterize integrated functions of biochemical networks".Trends in Biochemical Sciences.31(5): 284–91.doi:10.1016/j.tibs.2006.03.007.PMID16616498.
- ^Duarte, Natalie C.; Becker, Scott A.; Jamshidi, Neema; Thiele, Ines; Mo, Monica L.; Vo, Thuy D.; Srivas, Rohith; Palsson, Bernhard Ø (Februari 2007)."Global reconstruction of the human metabolic network based on genomic and bibliomic data".Proceedings of the National Academy of Sciences(dalam bahasa Inggris).104(6): 1777–1782.doi:10.1073/pnas.0610772104.ISSN0027-8424.PMC1794290
 .PMID17267599.Diarsipkandari versi asli tanggal 2020-07-01.Diakses tanggal2020-07-22.
.PMID17267599.Diarsipkandari versi asli tanggal 2020-07-01.Diakses tanggal2020-07-22.
- ^Goh, Kwang-Il; Cusick, Michael E.; Valle, David; Childs, Barton; Vidal, Marc; Barabási, Albert-László (Mei 2007)."The human disease network".Proceedings of the National Academy of Sciences(dalam bahasa Inggris).104(21): 8685–8690.doi:10.1073/pnas.0701361104.ISSN0027-8424.PMC1885563
 .PMID17502601.Diarsipkandari versi asli tanggal 2020-07-22.Diakses tanggal2020-07-22.
.PMID17502601.Diarsipkandari versi asli tanggal 2020-07-22.Diakses tanggal2020-07-22.
- ^Lee, D.- S.; Park, J.; Kay, K. A.; Christakis, N. A.; Oltvai, Z. N.; Barabasi, A.- L. (Juli 2008)."The implications of human metabolic network topology for disease comorbidity".Proceedings of the National Academy of Sciences(dalam bahasa Inggris).105(29): 9880–9885.doi:10.1073/pnas.0802208105.ISSN0027-8424.PMC2481357
 .PMID18599447.
.PMID18599447.
- ^Csete, Marie; Doyle, John (September 2004)."Bow ties, metabolism and disease".Trends in Biotechnology(dalam bahasa English).22(9): 446–450.doi:10.1016/j.tibtech.2004.07.007.ISSN0167-7799.PMID15331224.Diarsipkandari versi asli tanggal 2013-10-14.Diakses tanggal2020-07-22.
- ^Zhao, Jing; Yu, Hong; Luo, Jian-Hua; Cao, Zhi-Wei; Li, Yi-Xue (Agustus 2006)."Hierarchical modularity of nested bow-ties in metabolic networks".BMC Bioinformatics.7(1): 386.doi:10.1186/1471-2105-7-386.ISSN1471-2105.PMC1560398
 .PMID16916470.
.PMID16916470.
- ^Ma, Hong-Wu; Zeng, An-Ping (Juli 2003)."The connectivity structure, giant strong component and centrality of metabolic networks".Bioinformatics(dalam bahasa Inggris).19(11): 1423–1430.doi:10.1093/bioinformatics/btg177.ISSN1367-4803.Diarsipkandari versi asli tanggal 2020-07-22.Diakses tanggal2020-07-22.
- ^Thykaer, Jette; Nielsen, Jens (Januari 2003)."Metabolic engineering of β-lactam production".Metabolic Engineering(dalam bahasa Inggris).5(1): 56–69.doi:10.1016/S1096-7176(03)00003-X.ISSN1096-7176.
- ^González-Pajuelo, María; Meynial-Salles, Isabelle; Mendes, Filipa; Andrade, Jose Carlos; Vasconcelos, Isabel; Soucaille, Philippe (September 2005)."Metabolic engineering of Clostridium acetobutylicum for the industrial production of 1,3-propanediol from glycerol".Metabolic Engineering(dalam bahasa Inggris).7(5): 329–336.doi:10.1016/j.ymben.2005.06.001.ISSN1096-7176.
- ^Krämer, Marco; Bongaerts, Johannes; Bovenberg, Roel; Kremer, Susanne; Müller, Ulrike; Orf, Sonja; Wubbolts, Marcel; Raeven, Leon (October 2003)."Metabolic engineering for microbial production of shikimic acid".Metabolic Engineering(dalam bahasa Inggris).5(4): 277–283.doi:10.1016/j.ymben.2003.09.001.ISSN1096-7176.Diarsipkandari versi asli tanggal 2011-08-28.Diakses tanggal2020-07-22.
Bacaan lebih lanjut[sunting|sunting sumber]
- Aryulina, Diah (2007).Biologi 3 SMA dan MA Untuk Kelas XII.Jakarta: Esis/Erlangga.ISBN 974-734-551-3.(Indonesia)
Pranala luar[sunting|sunting sumber]
- (Inggris)Eksperimen-eksperimen Santorio Santorio
- (Inggris)Interactive Flow Chart of the Major Metabolic PathwaysDiarsipkan2006-02-18 diWayback Machine.

