Oksima

Oksimaadalah suatusenyawa kimiayang termasuk dalam kelompokimina,dengan rumus umum R1R2C=NOH,di mana R1adalah suaturantai sampingorganikdan R2dapat berupa hidrogen, membentuk suatualdoksima,atau gugus organik lain, membentuk suatuketoksima.Oksima tersubstitusi-O membentuk suatu keluarga senyawa yang terkait erat.Amidoksimaadalah oksimaamidadengan struktur umum RC(=NOH)(NRR').
Oksima biasanya dihasilkan oleh reaksihidroksilaminadenganaldehidaatauketon.Istilah oksima berasal dari abad 19, merupakan kombinasi kataoksigendanimina.[1]
Struktur dan sifat
[sunting|sunting sumber]Jika kedua rantai samping pada karbon sentral berbeda satu sama lain, oksima dapat memiliki dua bentukstereoisomerikgeometris: isomersyndan isomeranti,tergantung dari mana kedua rantai samping lebih dekat dengan hidroksil. Kedua bentuk tersebut sering kali cukup stabil untuk dipisahkan satu sama lain dengan teknik standar.
Oksima memiliki tiga pita karakteristik dalam spektruminframerah,pada panjang gelombang 3600 cm−1(O−H), 1665 cm−1(C=N) dan 945 cm−1(N−O).[2]
Dalam larutan berair, oksima alifatik adalah 102- hingga 103-kali lebih resisten terhadap hidrolisis dibandingkan analog hidrazon.[3]
Preparasi
[sunting|sunting sumber]Oksima dapat disintesis dengankondensasidari aldehida atau keton denganhidroksilamina.Kondensasi aldehida dengan hidroksilamina memberikan aldoksin, dan ketoksi dihasilkan dari keton dan hidroksilamina. Secara umum, oksima hadir sebagaikristaltidak berwarna dan tidak larut dalam air. Oleh karena itu, oksima dapat digunakan untuk identifikasi keton atau aldehida.
Oksida juga dapat diperoleh dari reaksinitritsepertiisoamil nitritdengan senyawa yang mengandung atom hidrogen asam. Contohnya adalah reaksietil asetoasetatdannatrium nitritdalamasam asetat,[4][5]reaksimetil etil ketondenganetil nitritdalamasam klorida.[6]dan reaksi serupa denganpropiofenon,[7]reaksifenasil klorida,[8]reaksimalononitrildengan natrium nitrit dalam asam asetat[9]
Reaksi konseptual terkait adalahreaksi Japp–Klingemann.
Reaksi
[sunting|sunting sumber]Hidrolisisdari oksima berlangsung dengan mudah dengan memanaskan dengan adanya berbagaiasam anorganik,dan oksima terurai menjadi keton atau aldehida, dan hidroksilamina. Reduksi oksima oleh logamnatrium,[10]amalgamnatrium,hidrogenasi,atau reaksi dengan pereaksihidridamenghasilkanamina.[11]Biasanyareduksialdoksima menghasilkan amina primer dan amina sekunder; namun, kondisi reaksi dapat diubah (seperti penambahankalium hidroksidadalam rasio molar 1/30) untuk menghasilkan amina primer semata-mata.[12]
Secara umum, oksima dapat diubah menjadi turunanamidayang sesuai dengan pengobatan dengan berbagai asam. Reaksi ini disebutpenataan ulang Beckmann.Dalam reaksi ini, gugushidroksildipertukarkan dengan gugus yang berada dalam posisi anti gugus hidroksil. Derivatif amida yang diperoleh dengan penataan ulang Beckmann dapat diubah menjadiasam karboksilatdengan cara hidrolisis (katalis asam atau basa) serta amina dengan degradasi Hoffman amida dengan keberadaan hipoklorit alkali pada suhu 80 derajat celcius, degradasi itu sendiri rentan terhadap reaksi samping, yaitu pembentukan biuret atau polimer sianat. Untuk menghindari reaksi samping ini, kontrol suhu yang ketat perlu dilakukan; Reaksi harus dilakukan pada suhu yang cukup untuk isomerisasi sianat menjadi isosianat.
Selain itu, solvasi yang baik juga penting untuk mensukseskan reaksi tersebut. Penataan ulang Beckmann digunakan untuk sintesis industrikaprolaktam(lihat aplikasi di bawah).
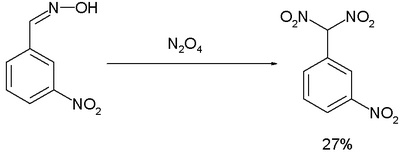
Reaksi Ponzio(1906)[13]mengenai konversim-nitrobenzaldoksima menjadim-nitrofenildinitrometana dengandinitrogen tetroksidamerupakan hasil penelitian bahan peledak tinggi seperti-TNT:[14]
DalamPenataan ulang Neberoksima tertentu dikonversi menjadi keton alfa-amino yang sesuai.
Oksima dapat didehidrasimenggunakananhidrida asamuntuk menghasilkannitrilyang sesuai.
Amidoksima tertentu bereaksi denganbenzenasulfonil kloridamenjadiureatersubstitusi dalamPenataan ulang Tiemann:[15][16]
Kegunaan
[sunting|sunting sumber]Dalam aplikasi terbesar mereka, oksima adalah zat antara dalam produksi industrikaprolaktam,pendahuluNilon 6.Sekitar setengah dari pasokansikloheksanondunia, lebih dari satu miliar kilogram per tahun, diubah menjadi oksima. Dengan adanyakatalisasam sulfat,oksima menjalanipenataan ulang Beckmannuntuk menghasilkan kaprolaktam amida siklik:[17]
Lihat pula
[sunting|sunting sumber]Referensi
[sunting|sunting sumber]- ^Nama "oksima" berasal dari "oksimida" (yaitu, oksi- + amida). Menurut ahli kimia organik JermanVictor Meyer(1848-1897) – yang, dengan Alois Janny, mensintesis oksima pertama – suatu "oksimida" adalah suatu senyawa yang mengandung gugus (=N−OH) yang menempel pada atom karbon. Keberadaan oksimida dipertanyakan pada waktu itu (sekitar tahun 1882). (Lihat halaman 1164 dari: Victor Meyer und Alois Janny (1882a)"Ueber stickstoffhaltige Acetonderivate"(On nitrogenous derivatives of acetone),Berichte der Deutschen chemischen Gesellschaft,15:1164–1167.) Namun, pada tahun 1882, Meyer dan Janny berhasil mensintesis metilglioksima (CH3C(=NOH)CH(=NOH)), yang mereka namai "Acetoximsäure" (asam asetoksimat) (Meyer & Janny, 1882a, hal. 1166). Selanjutnya, mereka mensintesis 2-propanon, oksima ((CH3)2C=NOH), yang mereka namai "Acetoxim" (asetoksima), analog dengan Acetoximsäure. Dari Victor Meyer dan Alois Janny (1882b)"Ueber die Einwirkung von Hydroxylamin auf Aceton"(On the effect of hydroxylamine on acetone),Berichte der Deutschen chemischen Gesellschaft,15:1324–1326, page 1324: "Die Substanz, welche wir, wegen ihrer nahen Beziehungen zur Acetoximsäure, und da sie keine sauren Eigenschaften besitzt, vorläufig Acetoxim nennen wollen,…" (The substance, which we – on account of its close relations to acetoximic acid, and since it possesses no acid properties – will, for the present, name "acetoxime,"… )
- ^Reusch, W."Infrared Spectroscopy".Virtual Textbook of Organic Chemistry.Michigan State University. Diarsipkan dariversi aslitanggal 2010-06-21.Diakses tanggal2017-07-10.
- ^Kalia, J.; Raines, R. T. (2008)."Hydrolytic stability of hydrazones and oximes".Angew. Chem. Int. Ed.47(39): 7523–7526.doi:10.1002/anie.200802651.PMC2743602
 .PMID18712739.
.PMID18712739.
- ^Fischer, Hans(1943). "2,4-Dimethyl-3,5-dicarbethoxypyrrole".Org. Synth.;Coll. Vol.2:202.
- ^Fischer, Hans (1955). "Kryptopyrrole".Org. Synth.;Coll. Vol.3:513.
- ^Semon, W. L. and Damerell, V. R. (1943). "Dimethoxyglyoxime".Org. Synth.;Coll. Vol.2:204.
- ^Hartung, Walter H. and Crossley, Frank (1943). "Isonitrosopropiophenone".Org. Synth.;Coll. Vol.2:363.
- ^Levin, Nathan and Hartung, Walter H. (1955). "ω-chloroisonitrosoacetophenone".Org. Synth.;Coll. Vol.3:191.
- ^Ferris, J. P.; Sanchez, R. A. and Mancuso, R. W. (1973). "p-toluenesulfonate".Org. Synth.;Coll. Vol.5:32.
- ^Suter, C. M.; Moffett, Eugene W. (1934). "The Reduction of Aliphatic Cyanides and Oximes with Sodium and n-Butyl Alcohol".Journal of the American Chemical Society.56(2): 487–487.doi:10.1021/ja01317a502.
- ^George, Frederick; Saunders, Bernard (1960).Practical Organic Chemistry, 4th Ed.London: Longman. hlm. 93 & 226.ISBN9780582444072.
- ^Hata, Kazuo (1972).New Hydrogenating Catalysts.New York: John Wiley & Sons Inc. hlm. 193.ISBN9780470358900.
- ^Ponzio, Giacomo (1906). "Einwirkung von Stickstofftetroxyd auf Benzaldoxim".J. Prakt. Chem.73:494.doi:10.1002/prac.19060730133.
- ^Fieser, Louis F. andDoering, William von E.(1946). "Aromatic-Aliphatic Nitro Compounds. III. The Ponzio Reaction; 2,4,6-Trinitrobenzyl Nitrate".J. Am. Chem. Soc.68(11): 2252.doi:10.1021/ja01215a040.
- ^Tiemann, Ferdinand(1891). "Ueber die Einwirkung von Benzolsulfonsäurechlorid auf Amidoxime".Chemische Berichte.24(2): 4162–4167.doi:10.1002/cber.189102402316.
- ^Plapinger, Robert; Owens, Omer (1956). "Notes – The Reaction of Phosphorus-Containing Enzyme Inhibitors with Some Hydroxylamine Derivatives".J. Org. Chem.21(10): 1186.doi:10.1021/jo01116a610.
- ^Ritz, Josef; Fuchs, Hugo; Kieczka, Heinz; Moran, William C. (2005), "Caprolactam",Ullmann's Encyclopedia of Industrial Chemistry,Weinheim: Wiley-VCH,doi:10.1002/14356007.a05_031.pub2