Biosintesis
Biosintesis adalah suatu proses banyak-tahap, yang dikatalisis-enzim di mana substrat diubah menjadi produk yang lebih kompleks dalam organisme hidup[1]. Dalam biosintesis, senyawa dimodifikasi, diubah menjadi senyawa lain, atau digabungkan bersama untuk membentuk makromolekul. Proses ini terkadang terdiri dari jalur metabolik. Beberapa dari jalur biosintesis ini berlokasi didalam organel sel tunggal, sementara lainnya melibatkan enzim yang berlokasi di dalam organel sel ganda. Contoh dari jalur biosintesis ini diantaranya pada produksi komponen membran lipida dan nukleotida. Biosintesis biasanya bersinonim dengan anabolisme.[2]
Unsur-unsur prasyarat untuk biosintesis meliputi: senyawa prekursor, energi kimia (misalnya ATP), dan enzim katalitik yang mungkin memerlukan koenzim (misalnya NADH, NADPH). Elemen-elemen ini menciptakan monomer, suatu blok pembangun untuk makromolekul. Beberapa makromolekul biologis penting meliputi: protein, yang terdiri dari monomer asam amino yang bergabung melalui ikatan peptida, dan molekul DNA, yang terdiri dari nukleotida yang bergabung melalui ikatan fosfodiester.[3]
Sifat reaksi kimia
[sunting | sunting sumber]Biosintesis terjadi karena serangkaian reaksi kimia. Agar reaksi-reaksi ini terjadi, unsur-unsur berikut ini diperlukan:[4][5]
- Senyawa prekursor: senyawa-senyawa ini adalah molekul awal atau substrat dalam suatu reaksi. Prekursor ini juga dapat dilihat sebagai reaktan dalam proses kimia tertentu.[4]
- Energi kimia: energi kimia dapat ditemukan dalam bentuk molekul energi tinggi. Molekul-molekul ini diperlukan untuk reaksi yang tidak menguntungkan secara energi. Lebih lanjut, hidrolisis senyawa ini mendorong reaksi ke depan. Molekul berenergi tinggi, seperti ATP, memiliki tiga fosfat. Seringkali, fosfat terminal terpecah selama hidrolisis dan dipindahkan ke molekul lain.[4]
- Enzim katalitik: molekul-molekul ini adalah protein khusus yang mengkatalisasi suatu reaksi dengan meningkatkan laju reaksi dan menurunkan energi aktivasi.[4]
- Koenzim atau kofaktor: kofaktor adalah molekul yang membantu dalam reaksi kimia. Konfaktor tersebut mungkin merupakan suatu ion logam, turunan vitamin seperti NADH dan asetil KoA, atau turunan non-vitamin seperti ATP. Dalam kasus NADH, molekul mentransfer hidrogen, sedangkan asetil KoA mentransfer gugus asetil, dan ATP mentransfer fosfat.[4]
Dalam pengertian yang paling sederhana, reaksi yang terjadi dalam biosintesis memiliki format berikut:[6]
Lipida
[sunting | sunting sumber]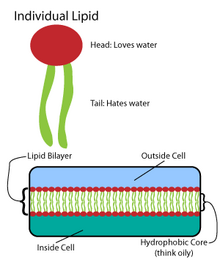
Banyak makromolekul rumit disintesis dalam pola struktur berulang yang sederhana.[7] Sebagai contoh, struktur lipida yang paling sederhana adalah asam lemak. Asam lemak adalah turunan hidrokarbon; mereka mengandung "kepala" gugus karboksil dan "ekor" rantai hidrokarbon.[7] Asam lemak ini menciptakan komponen yang lebih besar, yang pada gilirannya menggabungkan interaksi nonkovalen untuk membentuk lapisan ganda lipida.[7] Rantai asam lemak ditemukan dalam dua komponen utama lipid membran: fosfolipida dan sfingolipida. Komponen membran utama ketiga, kolesterol, tidak mengandung unit asam lemak ini.[8]
Nukleotida
[sunting | sunting sumber]Biosintesis nukleotida melibatkan reaksi yang dikatalisis-enzim yang mengubah substrat menjadi produk yang lebih kompleks.[4] Nukleotida adalah blok pembangun DNA dan RNA. Nukleotida terdiri dari cincin beranggota lima yang terbentuk dari gula ribosa dalam RNA, dan gula deoksiribosa dalam DNA; gula-gula ini terkait dengan basa purin atau pirimidin dengan ikatan glikosida dan gugus fosfat di lokasi 5' pada gula.[9]
DNA
[sunting | sunting sumber]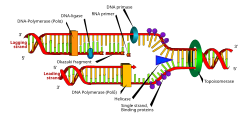
DNA terdiri dari nukleotida yang bergabung dengan ikatan fosfodiester.[7] Sintesis DNA, yang terjadi di inti, adalah proses semikonservatif, yang berarti bahwa molekul DNA yang dihasilkan mengandung untai asli dari induknya struktur dan untai baru.[10] Sintesis DNA dikatalisis oleh keluarga DNA polimerase yang membutuhkan empat deoksinukleosida trifosfat, untai templat, dan primer dengan 3 'OH bebas yang menggabungkan nukleotida.[11]
Agar replikasi DNA terjadi, garpu replikasi dibuat oleh enzim yang disebut helikase yang melepaskan heliks DNA.[11] Topoisomerase yang berada di garpu replikasi menghapus superkoil yang disebabkan oleh DNA yang tidak mengikat, dan protein pengikat untai tunggal mempertahankan dua templat DNA untai tunggal distabilkan sebelum replikasi.[9]
Asam amino
[sunting | sunting sumber]Protein adalah polimer yang tersusun dari asam amino yang dihubungkan oleh ikatan peptida. Ada lebih dari 300 asam amino yang ditemukan di alam dan hanya dua puluh diantaranya, yang dikenal sebagai asam amino esensial, adalah blok pembangun untuk protein.[12] Hanya tumbuhan hijau dan sebagian besar mikrob yang mampu mensintesis semua dari 20 asam amino esensial yang dibutuhkan oleh semua spesies hidup. Mamalia hanya dapat mensintesis sepuluh dari dua puluh asam amino esensial. Asam amino lainnya, valin, metionin, leusin, isoleusin, fenilalanin, lisin, treonin dan triptofan untuk orang dewasa dan histidin, serta arginin untuk bayi diperoleh melalui makanan.[13]
Protein
[sunting | sunting sumber]Sintesis protein terjadi melalui proses yang disebut translasi.[14] Selama proses translasi, materi genetik yang disebut mRNA dibaca oleh ribosom untuk menghasilkan rantai protein polipeptida.[14] Proses ini membutuhkan transfer RNA (tRNA) yang berfungsi sebagai adaptor dengan mengikat asam amino di satu sisi dan berinteraksi dengan mRNA di ujung lainnya; pasangan yang terakhir antara tRNA dan mRNA memastikan bahwa asam amino yang benar ditambahkan ke rantai.[14] Sintesis protein terjadi dalam tiga fase: inisiasi, elongasi, dan terminasi.[9]
Lihat pula
[sunting | sunting sumber]Referensi
[sunting | sunting sumber]- ^ Parker, SYbil, P (1984). McGraw-Hill Dictionary of Biology. McGraw-Hill Company.
- ^ Stincone A, Prigione A, Cramer T, Wamelink MM, Campbell K, Cheung E, Olin-Sandoval V, Grüning NM, Krüger A, Tauqeer Alam M, Keller MA, Breitenbach M, Brindle KM, Rabinowitz JD, Ralser M. (2015). "The return of metabolism: biochemistry and physiology of the pentose phosphate pathway". Biol Rev Camb Philos Soc. (dalam bahasa Inggris). 90 (3): 927–63. doi:10.1111/brv.12140. PMC 4470864
 . PMID 25243985.
. PMID 25243985.
- ^ Graupner, Marion; White, Robert H. (2001). "Biosynthesis of the Phosphodiester Bond in Coenzyme F420 in the Methanoarchaea". Biochemistry (dalam bahasa Inggris). doi:10.1021/bi0107703.
- ^ a b c d e f Alberts, Bruce (2007). Molecular biology of the cell. New York: Garland Science. ISBN 978-0815341055.
- ^ Pratt, Donald Voet, Judith G. Voet, Charlotte W. (2013). Fundamentals of biochemistry : life at the molecular level (edisi ke-4). Hoboken, NJ: Wiley. ISBN 978-0470547847.
- ^ Zumdahl, Steven S. Zumdahl, Susan A. (2008). Chemistry (edisi ke-8th). CA: Cengage Learning. ISBN 978-0547125329.
- ^ a b c d Lodish, Harvey; et al. (2007). Molecular cell biology (edisi ke-6). New York: W.H. Freeman. ISBN 978-0716743668.
- ^ Cox, David L. Nelson, Michael M. (2008). Lehninger principles of biochemistry (edisi ke-5). New York: W.H. Freeman. ISBN 9780716771081.
- ^ a b c Watson, James D.; et al. (2007). Molecular biology of the gene (edisi ke-6th). San Francisco, Calif.: Benjamin Cummings. ISBN 978-0805395921.
- ^ Geer, Gerald Karp ; responsible for the revision of chapter 15 Peter van der (2004). Cell and molecular biology : concepts and experiments (edisi ke-4th ed., Wiley International). New York: J. Wiley & Sons. ISBN 978-0471656654.
- ^ a b Griffiths, Anthony J. F. (1999). Modern genetic analysis (edisi ke-2. print.). New York: Freeman. ISBN 978-0716731184.
- ^ Wu, G (May 2009). "Amino acids: metabolism, functions, and nutrition". Amino Acids. 37 (1): 1–17. doi:10.1007/s00726-009-0269-0. PMID 19301095.
- ^ Mousdale, D. M.; Coggins, J. R. (1991). Amino Acid Synthesis. Target Sites for Herbicide Action. hlm. 29–56. doi:10.1007/978-1-4899-2433-9_2. ISBN 978-1-4899-2435-3.
- ^ a b c Weaver, Robert F. (2005). Molecular biology (edisi ke-3). Boston: McGraw-Hill Higher Education. ISBN 978-0-07-284611-9.

![{\displaystyle {\ce {Reaktan ->[][enzim] Produk}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/02569b02726472cc52f277b847ee2a8673659e11)