Polonium
84Po Polonium | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Konfigurasi elektron polonium | |||||||||||||||||||||||||
Garis spektrum polonium | |||||||||||||||||||||||||
| Sifat umum | |||||||||||||||||||||||||
| Pengucapan | /polonium/[1] | ||||||||||||||||||||||||
| Alotrop | α (alfa), β (beta) | ||||||||||||||||||||||||
| Penampilan | keperakan | ||||||||||||||||||||||||
| Polonium dalamtabel periodik | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Nomor atom(Z) | 84 | ||||||||||||||||||||||||
| Golongan | golongan 16 (kalkogen) | ||||||||||||||||||||||||
| Periode | periode 6 | ||||||||||||||||||||||||
| Blok | blok-p | ||||||||||||||||||||||||
| Kategori unsur | logam miskin | ||||||||||||||||||||||||
| Nomor massa | [209] | ||||||||||||||||||||||||
| Konfigurasi elektron | [Xe] 6s24f145d106p4 | ||||||||||||||||||||||||
| Elektron per kelopak | 2, 8, 18, 32, 18, 6 | ||||||||||||||||||||||||
| Sifat fisik | |||||||||||||||||||||||||
| FasepadaSTS(0 °C dan 101,325kPa) | padat | ||||||||||||||||||||||||
| Titik lebur | 527K(254 °C, 489 °F) | ||||||||||||||||||||||||
| Titik didih | 1235 K (962 °C, 1764 °F) | ||||||||||||||||||||||||
| Kepadatanmendekatis.k. | α-Po: 9,196 g/cm3 β-Po: 9,398 g/cm3 | ||||||||||||||||||||||||
| Kalor peleburan | sekitar 13kJ/mol | ||||||||||||||||||||||||
| Kalor penguapan | 102,91 kJ/mol | ||||||||||||||||||||||||
| Kapasitas kalor molar | 26,4 J/(mol·K) | ||||||||||||||||||||||||
Tekanan uap
| |||||||||||||||||||||||||
| Sifat atom | |||||||||||||||||||||||||
| Bilangan oksidasi | −2,+2,+4,+5,[2]+6 (oksidaamfoter) | ||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 2,0 | ||||||||||||||||||||||||
| Energi ionisasi | ke-1: 8121 kJ/mol | ||||||||||||||||||||||||
| Jari-jari atom | empiris: 168pm | ||||||||||||||||||||||||
| Jari-jari kovalen | 140±4 pm | ||||||||||||||||||||||||
| Jari-jari van der Waals | 197 pm | ||||||||||||||||||||||||
| Lain-lain | |||||||||||||||||||||||||
| Kelimpahan alami | dari peluruhan | ||||||||||||||||||||||||
| Struktur kristal | kubus α-Po | ||||||||||||||||||||||||
| Struktur kristal | rombohedron β-Po | ||||||||||||||||||||||||
| Ekspansi kalor | 23,5 µm/(m·K) (suhu 25 °C) | ||||||||||||||||||||||||
| Konduktivitas termal | 20 W/(m·K) (?) | ||||||||||||||||||||||||
| Resistivitas listrik | α-Po: 0,40 µΩ·m (suhu 0 °C) | ||||||||||||||||||||||||
| Arah magnet | nonmagnetik | ||||||||||||||||||||||||
| Nomor CAS | 7440-08-6 | ||||||||||||||||||||||||
| Sejarah | |||||||||||||||||||||||||
| Penamaan | dariPolonia,Latin untukPolandia,negara asal Marie Curie | ||||||||||||||||||||||||
| Penemuan | P. CuriedanM. Curie(1898) | ||||||||||||||||||||||||
| Isolasi pertama | W. Marckwald(1902) | ||||||||||||||||||||||||
| Isotop poloniumyang utama | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
Poloniumadalah sebuahunsur kimiadenganlambangPodannomor atom84. Sebuahlogamlangka yang sangatradioaktiftanpaisotopstabil, polonium adalah sebuahkalkogendan secara kimiawi mirip denganseleniumdantelurium,meskipun karakter logamnya mirip dengantetangga horizontalnyaditabel periodik:talium,timbal,danbismut.Karenawaktu paruhsemua isotopnya pendek, keterjadian alaminya terbatas pada jejak kecilpolonium-210yang cepat meluruh (dengan waktu paruh 138 hari) dalambijihuranium,karena ia merupakananak kedua terakhirdariuranium-238yang alami. Meskipun ada isotop yang berumur sedikit lebih lama, mereka jauh lebih sulit untuk diproduksi. Saat ini, polonium biasanya diproduksi dalam jumlah miligram melaluiiradiasi neutronoleh bismut. Karena radioaktivitasnya yang kuat, yang menghasilkanradiolisisdalam ikatan kimia dan pemanasan radioaktif sendiri, sifat kimianya sebagian besar telah diselidiki hanya pada skala kecil.
Polonium ditemukan pada Juli 1898 olehMarie Skłodowska-CuriedanPierre Curie,ketika ia diekstraksi dari bijih uraniumuraninitdan teridentifikasi hanya dengan radioaktivitasnya yang kuat: ia adalah unsur pertama yang ditemukan melalui sifat radioaktifnya. Polonium dinamai dari negara asal Marie Curie,Polandia.Polonium memiliki beberapa aplikasi, dan itu terkait dengan radioaktivitasnya: pemanas diprob antariksa,perangkat antistatis,sumberneutrondanpartikel alfa,sertaracun.Polonium sangatlah berbahaya bagi manusia.
Karakteristik
[sunting|sunting sumber]210Po adalah sebuahpemancar alfayang memiliki waktu paruh 138,4 hari; ia meluruh langsung menjadiisotop anaknyayang stabil,206Pb.Satu miligram (5curie)210Po memancarkan partikel alfa per detik sebanyak 5 gram226Ra,[4]yang berarti ia 5.000 kali lebih radioaktif daripada radium. Beberapacurie(1 curie sama dengan 37gigabecquerel,1 Ci = 37 GBq) dari210Po memancarkan cahaya biru yang disebabkan olehionisasiudara di sekitarnya.
Sekitar satu dari 100.000 pancaran alfa menyebabkan eksitasi pada inti yang kemudian menghasilkan pancaransinar gamadengan energi maksimum 803 keV.[5][6]
Bentuk wujud padat
[sunting|sunting sumber]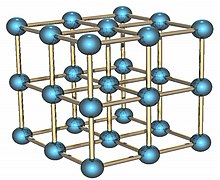
Polonium adalah unsur radioaktif yang ada dalam duaalotropmetalik.Bentuk alfa adalah satu-satunya contoh yang diketahui dari struktur kristalkubik sederhanadalam basis atom tunggal padaSTP,dengan panjang tepi 335,2pikometer;bentuk beta adalahrombohedral.[7][8][9]Struktur polonium telah dicirikan olehdifraksisinar-X[10][11]dandifraksi elektron.[12]
210Po (sama dengan238Pu[butuh rujukan]) memiliki kemampuan untukmengudara dengan mudah:jika sebuah sampel dipanaskan di udara hingga 55 °C (131 °F), 50% darinya menguap dalam 45 jam untuk membentuk molekul Po2diatomik,meskipun titik lebur polonium adalah 254 °C (489 °F) dan titik didihnya adalah 962 °C (1.764 °F).[13][14][2] Ada lebih dari satu hipotesis tentang bagaimana polonium melakukan ini; satu pendapat mengemukakan bahwa gugus kecil atom poloniumterkelupasoleh peluruhan alfa.[15]
Sifat Kimia
[sunting|sunting sumber]Sifat kimia polonium mirip dengantelurium,meskipun ia juga menunjukkan beberapa kesamaan dengan tetangganyabismutkarena karakter logamnya. Polonium mudah larut dalamasamencer tetapi hanya sedikitlarutdalamalkali.Larutanpolonium mula-mula berwarna merah muda oleh ion Po2+,tetapi kemudian dengan cepat menjadi kuning karena radiasi alfa dari polonium yang mengionisasi pelarut dan mengubah Po2+menjadi Po4+.Karena polonium juga memancarkan partikel alfa setelah disintegrasi maka proses ini disertai dengan gelembung dan emisi panas dan cahaya olehperalatan kacakarena partikel alfa yang terserap; akibatnya, larutan polonium bersifat volatil dan akan menguap dalam beberapa hari kecuali disegel.[16][17]Pada pH sekitar 1, ion polonium mudah dihidrolisis dan dikomplekskan oleh asam sepertiasam oksalat,asam sitrat,danasam tartarat.[18]
Senyawa
[sunting|sunting sumber]Polonium tidak memiliki senyawa umum, dan hampir semua senyawanya dibuat secara sintetis; lebih dari 50 di antaranya telah diketahui.[19]Golongan senyawa polonium yang paling stabil adalahpolonida,yang dibuat melalui reaksi langsung dua unsur.Na2Pomemiliki strukturantifluorit,polonidaCa,Ba,Hg,Pb dan lantanida membentuk kisi NaCl,BePodanCdPomemiliki strukturwurtzit,danMgPomemiliki strukturnikel arsenida.Sebagian besar polonida terurai pada pemanasan hingga sekitar 600 °C, kecuali HgPo yang terurai pada ~300 °C dan polonidalantanida,yang tidak terurai tetapi melebur pada suhu di atas 1000 °C. Misalnya, polonidapraseodimium(PrPo) melebur pada 1250 °C, dan polonidatulium(TmPo) melebur pada 2200 °C.[20]PbPoadalah salah satu dari sangat sedikit senyawa polonium alami, karena polonium meluruh melaluipeluruhan alfamenjaditimbal.[21]
Polonium hidrida(PoH2) adalah cairan yang mudah menguap pada suhu kamar yang rentan terhadap disosiasi; ia tidak stabil secara termal.[20]Airadalah satu-satunyahidrogen kalkogenidalain yang diketahui berbentuk cair pada suhu kamar; namun, hal ini dikarenakan ikatan hidrogen. Tiga oksida,PoO,PoO2,danPoO3,adalah produk dari oksidasi polonium.[22]
Halidadari struktur PoX2,PoX4dan PoF6telah diketahui. Mereka larut dalam hidrogen halida yang sesuai, yaitu, PoClXdalam HCl, PoBrXdalam HBr, dan PoI4dalam HI.[23]Polonium dihalida dibentuk oleh reaksi langsung dari unsur-unsur yang sesuai atau dengan reduksi PoCl4dengan SO2dan dengan PoBr4dengan H2S pada suhu kamar. Tetrahalida dapat diperoleh dengan mereaksikan polonium dioksida dengan HCl, HBr atau HI.[24]
Senyawa polonium lainnya termasukkalium polonitsebagaipolonit,polonat,asetat,bromat,karbonat,sitrat,kromat,sianida,format,(II)dan(IV) hidroksida,nitrat,selenat,selenit,monosulfida,sulfat,disulfat,dansulfit.[23][25]
Kimia organopoloniumterbatas telah diketahui, sebagian besar terbatas pada dialkil dan diaril polonida (R2Po), triarilpolonium halida (Ar3PoX), dan diarilpolonium dihalida (Ar2PoX2).[26][27]Polonium juga membentuk senyawa yang larut dengan beberapaagen pengelat,seperti2,3-butanedioldantiourea.[26]
| Rumus | Warna | t.l.(°C) | Suhu sublimasi(°C) |
Simetri | Lambang Pearson | Grup ruang | No | a (pm) | b(pm) | c(pm) | Z | ρ(g/cm3) | ref |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| PoO | hitam | ||||||||||||
| PoO2 | kuning pucat | 500 (dec.) | 885 | fcc | cF12 | Fm3m | 225 | 563,7 | 563,7 | 563,7 | 4 | 8,94 | [29] |
| PoH2 | -35,5 | ||||||||||||
| PoCl2 | merah rubi gelap | 355 | 130 | ortorombik | oP3 | Pmmm | 47 | 367 | 435 | 450 | 1 | 6,47 | [30] |
| PoBr2 | coklat ungu | 270 (dec.) | [31] | ||||||||||
| PoCl4 | kuning | 300 | 200 | monoklinik | [30] | ||||||||
| PoBr4 | merah | 330 (dec.) | fcc | cF100 | Fm3m | 225 | 560 | 560 | 560 | 4 | [31] | ||
| PoI4 | hitam | [32] |
Isotop
[sunting|sunting sumber]Polonium memiliki 42 isotop yang diketahui, semuanya bersifatradioaktif.Mereka memilikimassa atomyang berkisar antara 186 hingga 227u.210Po(waktu paruh 138,376 hari) adalah yang paling banyak tersedia dan dibuat melalui penangkapan neutron olehbismutalami.209Po yang berumur lebih panjang (waktu paruh125,2±3,3tahun, berumur paling panjang dari semua isotop polonium)[33]dan208Po (waktu paruh 2,9 tahun) dapat dibuat melalui pemborbardiran alfa, proton, atau deuteron terhadaptimbalatau bismut dalamsiklotron.[34]
Sejarah
[sunting|sunting sumber]
Terkadang disebut "radium F",polonium ditemukan olehMariedan Pierre Curie pada bulan Juli 1898,[35][36]dan diberi nama dari tanah kelahiran Marie Curie diPolandia(bahasa Latin:Polonia).[37][38]Polandia pada saat itu berada di bawahpartisiRusia,Jerman,danAustria-Hungaria,dan tidak eksis sebagai negara merdeka. Itu adalah harapan Curie bahwa penamaan unsur ini setelah tanah airnya akan mempublikasikan kurangnya kemerdekaan.[39]Polonium mungkin merupakan unsur pertama yang disebutkan untuk menyoroti kontroversi politik.[39]
Unsur ini adalah yang pertama kali ditemukan oleh Curie saat mereka menyelidiki penyebabradioaktivitasuraninit.Uraninit, setelah penghilangan unsur radioaktifuraniumdantorium,menjadi lebih radioaktif daripada gabungan uranium dan torium. Ini mendorong Curie untuk mencari unsur radioaktif tambahan. Mereka pertama kali memisahkan polonium dari uraninit pada Juli 1898, dan lima bulan kemudian, juga mengisolasiradium.[16][35][40]Ilmuwan JermanWilly Marckwaldberhasil mengisolasi 3 miligram polonium pada tahun 1902, meskipun pada saat itu dia yakin itu adalah unsur baru, yang dia juluki "radio-telurium", dan baru pada tahun 1905 terbukti sama dengan polonium.[41][42]
Di Amerika Serikat, polonium diproduksi sebagai bagian dariProyek Dayton,bagian dariProyek Manhattan,selamaPerang Dunia II.Polonium danberiliumadalah bahan utama dari inisiator 'Urchin' di tengahlubangbola bom.[43]'Urchin' memprakarsaireaksi berantai nuklirpada saatkekritisan yang cepatuntuk memastikan bahwa senjata itu tidakgagal.'Urchin' digunakan dalam senjata A.S. awal; senjata A.S. selanjutnya menggunakan generator pulsa neutron untuk tujuan yang sama.[43]
Sebagian besar fisika dasar poloniumdirahasiakansampai setelah perang. Fakta bahwa ia digunakan sebagai inisiator dirahasiakan hingga tahun 1960-an.[44]
Komisi Energi AtomdanProyek Manhattanmendanaieksperimen manusiamenggunakan polonium pada lima orang diUniversitas Rochesterantara tahun 1943 dan 1947. Orang-orang tersebut diberikan antara 9 dan 22microcurie(330 dan 810kBq) polonium untuk mempelajariekskresinya.[45][46][47]
Keterjadian dan produksi
[sunting|sunting sumber]Polonium adalah unsur yang sangat langka di alam karenawaktu paruhsemua isotopnya pendek. Tujuh isotop terjadi dalam jumlahjejaksebagaiproduk peluruhan:210Po,214Po, dan218Po terjadi dalamrantai peluruhan238U;211Po dan215Po terjadi dalam rantai peluruhan235U;212Po dan216Po terjadi dalam rantai peluruhan232Th.Dari mereka,210Po adalah satu-satunya isotop dengan waktu paruh lebih dari 3 menit.[48]
Polonium dapat ditemukan dalam bijihuraniumsekitar 0,1 mg perton metrik(1 bagian dalam 1010),[49][50]yang merupakan sekitar 0,2% dari kelimpahan radium. Jumlahnya di kerak bumi tidak berbahaya. Polonium telah ditemukan dalamasap tembakaudari daun tembakau yang ditanam dengan pupukfosfat.[51][52][53]
Karena ia hadir dalam konsentrasi kecil, isolasi polonium dari sumber alami merupakan proses yang sangat lama. Kumpulan polonium terbesar yang pernah diekstraksi, dilakukan pada paruh pertama abad ke-20, hanya mengandung 40 Ci (1,5 TBq) (9 mg)polonium-210dan diperoleh dengan mengolah 37 ton residu dari produksi radium.[54]Polonium sekarang biasanya diperoleh dengan menyinari bismut dengan neutron atau proton berenergi tinggi.[16][55]
Pada tahun 1934, sebuah percobaan menunjukkan bahwa ketika209Bidibombardir denganneutron,210Bi dibuat, yang kemudian meluruh menjadi210Po melalui peluruhan beta-minus. Pemurnian akhir dilakukan secara pirokimia diikuti dengan teknik ekstraksi cair-cair.[56]Polonium sekarang dapat dibuat dalam jumlah miligram dalam prosedur ini yang menggunakan fluks neutron tinggi yang ditemukan direaktor nuklir.[55]Hanya sekitar 100 gram yang diproduksi setiap tahun, hampir seluruhnya di Rusia, membuat polonium sangatlah langka.[57][58]
Proses ini dapat menyebabkan masalah dalamreaktor berpendingin logam cairberbasistimbal-bismutseperti yang digunakan padaK-27milikAngkatan Laut Soviet.Langkah-langkah harus diambil dalam reaktor tersebut untuk mengatasi kemungkinan210Po yang tidak diinginkan dilepaskan dari pendingin.[59][60]
Isotop polonium yang berumur lebih panjang,208Po dan209Po, dapat dibentuk oleh pemborbardiranprotonataudeuteronterhadap bismut menggunakansiklotron.Isotop lain yang lebih memiliki sedikit neutron dan lebih tidak stabil dapat dibentuk dengan iradiasi platina dengan intikarbon.[61]
Aplikasi
[sunting|sunting sumber]Sumber partikel alfa berbasis polonium diproduksi diUni Soviet.[62]Sumber tersebut diterapkan untuk mengukur ketebalan lapisan industri melalui atenuasi radiasi alfa.[63]
Karena radiasi alfa yang kuat, satu gram sampel210Po akan secara spontan memanas hingga di atas 500 °C (932 °F) menghasilkan daya sekitar 140 watt. Oleh karena itu,210Po digunakan sebagai sumber panas atom untuk menggerakkangenerator termoelektrik radioisotopmelalui bahantermoelektrik.[4][16][64][65]Misalnya, sumber panas210Po digunakan padawahana penjelajah BulanLunokhod1 (1970) dan Lunokhod 2 (1973) untuk menjaga komponen internalnya tetap hangat selama malam bulan, serta satelitKosmos 84dan 90 (1965).[62][66]
Partikel alfa yang dipancarkan oleh polonium dapat diubah menjadi neutron menggunakan berilium oksida, dengan laju 93 neutron per juta partikel alfa.[64]Campuran Po-BeO digunakan sebagaisumber neutronpasif dengan rasio produksisinar gama-ke-neutronsebesar 1,13 ± 0,05, lebih rendah daripada sumber neutron berbasisfisi nuklir.[67]Contoh campuran ataupaduanPo-BeO yang digunakan sebagai sumber neutron adalahpemicu atau inisiator neutronuntuksenjata nuklir[16][68]dan untuk inspeksi sumur minyak. Sekitar 1500 sumber jenis ini, dengan aktivitas individual sebesar 1.850 Ci (68 TBq), telah digunakan setiap tahun di Uni Soviet.[69]
Polonium juga merupakan bagian dari kuas atau alat yang lebih rumit yang menghilangkan muatan statis pada pelat fotografi, pabriktekstil,gulungan kertas, lembaran plastik, dan pada substrat (seperti otomotif) sebelum penerapan pelapisan.[70]Partikel alfa yang dipancarkan oleh polonium mengionisasi molekul udara yang menetralkan muatan pada permukaan terdekat.[71][72]Beberapa sikat antistatis mengandung hingga 500 microcurie (20 MBq)210Po sebagai sumber partikel bermuatan untuk menetralkan listrik statis.[73]Di A.S., perangkat dengan tidak lebih dari 500 μCi (19 MBq)210Po per unit (yang disegel) dapat dibeli dalam jumlah berapa pun di bawah "lisensi umum",[74]yang berarti pembeli tidak perlu didaftarkan oleh otoritas mana pun. Polonium perlu diganti di perangkat tersebut hampir setiap tahun karena waktu paruhnya yang pendek; ia juga sangat radioaktif dan oleh karena itu sebagian besar telah digantikan oleh sumberpartikel betayang lebih tidak berbahaya.[4]
Sejumlah kecil210Po kadang-kadang digunakan di laboratorium dan untuk tujuan pengajaran—biasanya sekitar 4–40 kBq (0,11–1,08 μCi), dalam bentuk sumber tersegel, dengan polonium diendapkan pada substrat atau dalam resin atau matriks polimer—sering dikecualikan dari lisensi oleh NRC dan otoritas serupa karena tidak dianggap berbahaya. Sejumlah kecil210Po diproduksi untuk dijual ke publik di Amerika Serikat sebagai "sumber jarum" untuk eksperimen laboratorium, dan dijual eceran oleh perusahaan pemasok ilmiah. Polonium adalah lapisan pelapisan yang pada gilirannya dilapisi dengan bahan seperti emas, yang memungkinkanradiasi alfa(digunakan dalam eksperimen seperti bilik awan) untuk lewat sambil mencegah pelepasan polonium dan menghadirkan bahaya beracun.[butuh rujukan]
Busipolonium dipasarkan olehFirestonedari tahun 1940 hingga 1953. Walaupun jumlah radiasi dari busi sangat kecil dan bukan ancaman bagi konsumen, manfaat busi tersebut dengan cepat berkurang setelah sekitar satu bulan karena waktu paruh polonium yang pendek dan karena penumpukan pada konduktor akan memblokir radiasi yang meningkatkan kinerja mesin. (Alasan di balik busi polonium, serta stekerradiumprototipeAlfred Matthew Hubbardyang mendahuluinya, adalah bahwa radiasi akan meningkatkan ionisasi bahan bakar di dalam silinder dan dengan demikian memungkinkan motor menyala lebih cepat dan efisien.)[75][76]
Biologi dan toksisitas
[sunting|sunting sumber]Ikhtisar
[sunting|sunting sumber]Polonium dapat menjadi berbahaya dan tidak memiliki peran biologis.[16]Secara massa, polonium-210 sekitar 250.000 kali lebih beracun daripadahidrogen sianida(LD50untuk210Po kurang dari 1mikrogramuntuk orang dewasa rata-rata (lihat di bawah) dibandingkan dengan sekitar 250miligramuntuk hidrogen sianida[77]). Bahaya utamanya adalah radioaktivitasnya yang intens (sebagai pemancar alfa), yang membuatnya sulit ditangani dengan aman. Bahkan dalam jumlah mikrogram, penanganan210Po sangatlah berbahaya, membutuhkan peralatan khusus (sebuahkotak sarung tanganbertekanan negatif yang dilengkapi dengan filter performa tinggi), pemantauan yang memadai, dan prosedur penanganan yang ketat untuk menghindari kontaminasi. Partikel alfa yang dipancarkan oleh polonium akan merusak jaringan organik dengan mudah jika polonium tertelan, terhirup, atau diserap, meskipun partikel alfa tidak dapat menembusepidermisdan karenanya tidak berbahaya selama partikel alfa tetap berada di luar tubuh. Mengenakan sarung tangan yang tahan bahan kimia dan utuh adalah tindakan pencegahan wajib untuk menghindaridifusipolonium transkutan langsung melaluikulit.Polonium yang diberikan dalamasam nitratpekat dapat dengan mudah berdifusi melalui sarung tangan yang tidak memadai (misalnyasarung tangan lateks) atau asam itu dapat merusak sarung tangan.[78]
Polonium tidak memiliki sifat kimia beracun.[79]
Telah dilaporkan bahwa beberapamikrobadapatmemetilasipolonium dengan aksimetilkobalamin.[80][81]Ini mirip dengan cararaksa,selenium,danteluriumdimetilasi pada makhluk hidup untuk membuat senyawaorganologam.Studi menyelidiki metabolisme polonium-210 pada tikus telah menunjukkan bahwa hanya 0,002 sampai 0,009% dari polonium-210 yang tertelan diekskresikan sebagai polonium-210 volatil.[82]
Efek akut
[sunting|sunting sumber]Median dosis letal(LD50) untuk paparan radiasi akut adalah sekitar 4,5Sv.[83]Dosis efektif setara210Po adalah 0,51 µSv/Bqjika tertelan, dan 2,5 µSv/Bq jika terhirup.[84]Dosis fatal 4,5 Sv dapat disebabkan oleh menelan 88 MBq (2.400 μCi), sekitar 50 nanogram (ng), atau menghirup 18 MBq (490 μCi), sekitar 10 ng. Satu gram210Po secara teori dapat meracuni 20 juta orang, di antaranya 10 juta akan mati. Toksisitas sebenarnya dari210Po lebih rendah dari perkiraan ini karena paparan radiasi yang tersebar selama beberapa minggu (waktu paruh biologispolonium pada manusia adalah 30 hingga 50 hari[85]) agak kurang merusak daripada dosis sesaat. Diperkirakan bahwa median dosis letal210Po adalah 15 megabecquerel (0,41 mCi), atau 0,089 mikrogram (μg), jumlah yang masih sangat kecil.[86][87]Sebagai perbandingan, satu butirgaram dapuradalah sekitar 0,06 mg = 60 μg.[88]
Efek jangka panjang (kronis)
[sunting|sunting sumber]Selain efek akut, paparan radiasi (baik internal maupun eksternal) membawa risiko kematian jangka panjang akibat kanker sebesar 5–10% per Sv.[83]Populasi umum terpapar polonium dalam jumlah kecil sebagai produkradondi udara dalam ruangan; isotop214Po dan218Po diperkirakan menyebabkan mayoritas[89]dari perkiraan 15.000–22.000 kematian akibat kanker paru-paru di A.S. setiap tahunnya yang dikaitkan dengan radon dalam ruangan.[90]Merokok dengan tembakaujuga menyebabkan paparan tambahan polonium.[91]
Batas paparan dan penanganan regulasi
[sunting|sunting sumber]Beban tubuh maksimum yang diperbolehkan untuk menelan210Po hanyalah 11 kBq (300 nCi), yang setara dengan massa partikel yang hanya 6,8 pikogram. Konsentrasi maksimum yang diizinkan di tempat kerja dari210Po di udara adalah sekitar 10 Bq/m3(3×10−10µCi/cm3).[92]Organ target polonium pada manusia adalahlimpadanliver.[93]Karena limpa (150 g) dan liver (1,3 hingga 3 kg) jauh lebih kecil daripada bagian tubuh lainnya, jika polonium terkonsentrasi di organ vital ini, itu merupakan ancaman yang lebih besar bagi kehidupan daripada dosis (rata-rata) yang akan diderita oleh seluruh tubuh jika disebarkan secara merata ke seluruh tubuh, dengan cara yang sama sepertisesiumatautritium(sebagai T2O).[butuh rujukan]
210Po banyak digunakan dalam industri, dan tersedia dengan sedikit regulasi atau batasan.[butuh rujukan][94]Di A.S., sistem pelacakan yang dijalankan oleh Komisi Pengaturan Nuklir diterapkan pada tahun 2007 untuk mencatat pembelian lebih dari 16 curie (590 GBq) polonium-210 (cukup untuk membuat 5.000 dosis letal). IAEA "dikatakan sedang mempertimbangkan peraturan yang lebih ketat... Ada pembicaraan bahwa mungkin akan memperketat persyaratan pelaporan polonium dengan faktor 10, menjadi 16 curie (590 GBq)."[95]Pada 2013, ini masih satu-satunya bahan produk sampingan yang memancarkan alfa yang tersedia, sebagai Kuantitas Pengecualian NRC, yang dapat diadakan tanpa lisensi bahan radioaktif.[butuh rujukan]
Polonium dan senyawanya harus ditangani dalamkotak sarung tangan,yang selanjutnya ditutup dalam kotak lain, dijaga pada tekanan yang sedikit lebih tinggi daripada kotak sarung tangan untuk mencegah kebocoran bahan radioaktif. Sarung tangan yang terbuat darikaret alamtidak memberikan perlindungan yang memadai terhadap radiasi dari polonium; sarung tangan bedah diperlukan. Sarung tanganneoprenamelindungi radiasi dari polonium lebih baik daripada karet alam.[96]
Kasus keracunan
[sunting|sunting sumber]Terlepas dari sifat polonium yang sangat berbahaya, keadaan di mana keracunan polonium dapat terjadi, jarang terjadi. Sifatnya yang sangat langka, waktu paruh semua isotopnya yang pendek, fasilitas dan peralatan khusus yang diperlukan untuk mendapatkan kuantitas yang signifikan, dan tindakan pencegahan keselamatan terhadap kecelakaan laboratorium, membuat peristiwa paparan yang berbahaya tidak mungkin terjadi. Dengan demikian, hanya segelintir kasus keracunan radiasi yang secara khusus disebabkan oleh paparan polonium telah dikonfirmasi.[butuh rujukan]
Abad ke-20
[sunting|sunting sumber]Menanggapi kekhawatiran tentang risiko paparan polonium di tempat kerja, jumlah210Po diberikan kepada lima sukarelawan manusia di Universitas Rochester dari tahun 1944 hingga 1947, untuk mempelajari perilaku biologisnya. Studi-studi ini didanai olehProyek Manhattandan AEC. Empat pria dan seorang wanita berpartisipasi, semuanya menderita kanker stadium akhir, dan berusia antara awal tiga puluhan hingga awal empat puluhan; semuanya dipilih karena peneliti menginginkan subjek yang tidak terpapar polonium baik melalui pekerjaan atau kecelakaan.[97]210Po disuntikkan ke empat pasien rawat inap, dan secara oral diberikan kepada pasien kelima. Tak satu pun dari dosis yang diberikan (semua mulai dari 0,17 hingga 0,30 μCikg−1) mendekati jumlah yang fatal.[97][98]
Kematian pertama yang terdokumentasi secara langsung akibat keracunan polonium terjadi diUni Soviet,pada 10 Juli 1954.[99][100]Seorang pria berusia 41 tahun yang tidak dikenal datang untuk perawatan medis pada tanggal 29 Juni, dengan muntah dan demam yang parah; hari sebelumnya, dia telah bekerja selama lima jam di area di mana, tanpa dia ketahui, sebuah kapsul berisi210Po telah mengalami penurunan tekanan dan mulai menyebar dalam bentuk aerosol. Selama periode ini, total asupan210Po di udara diperkirakan mencapai 0,11 GBq (hampir 25 kali perkiraan LD50jika dihirup sebesar 4,5 MBq). Meski dirawat, kondisinya terus memburuk dan dia meninggal 13 hari setelah kejadian paparan.[99]
Juga dikemukakan bahwa kematianIrène Joliot-Curiepada tahun 1956 akibat leukemia disebabkan oleh efek radiasi polonium. Dia secara tidak sengaja terekspos pada tahun 1946 ketika sebuah kapsul polonium yang tersegel meledak di bangku laboratoriumnya.[101]
Selain itu, beberapa kematian di Israel selama 1957–1969 diduga berasal dari paparan210Po.[102]Sebuah kebocoran ditemukan di laboratoriumInstitut Weizmannpada tahun 1957. Jejak210Po ditemukan di tangan Profesor Dror Sadeh, fisikawan yang meneliti bahan radioaktif. Tes medis menunjukkan tidak adanya bahaya, tetapi tes tersebut tidak termasuk sumsum tulang. Sadeh, salah satu muridnya, dan dua rekannya meninggal karena berbagai penyakitkankerselama beberapa tahun berikutnya. Masalahnya diselidiki secara diam-diam, tetapi tidak pernah ada pengakuan resmi tentang hubungan antara kebocoran dan kematian.[103]
Abad ke-21
[sunting|sunting sumber]Penyebab kematianAlexander Litvinenkoditahun 2006,mantan agenFSBRusia yang membelot ke Britania Raya pada tahun 2001, diidentifikasi keracunan dengan dosis210Po letal;[104][105]kemudian ditentukan bahwa210Po mungkin sengaja diberikan kepadanya oleh dua mantan agen keamanan Rusia,Andrey LugovoydanDmitry Kovtun.[106][107]Dengan demikian, kematian Litvinenko adalah kejadian pertama (dan, sampai saat ini, satu-satunya) yang dikonfirmasi di mana toksisitas ekstrim polonium telah digunakan dengan niat jahat.[108][109][110]
Pada tahun 2011, muncul dugaan bahwa kematian pemimpinPalestinaYasser Arafat,yang meninggal pada tanggal 11 November 2004 tanpa sebab yang pasti, juga diakibatkan oleh keracunan polonium yang disengaja,[111][112]dan pada bulan Juli 2012, konsentrasi210Po yang sangat tinggi terdeteksi dalam pakaian dan barang-barang pribadi Arafat oleh Institut de Radiophysique di Lausanne, Swiss.[113][114]Namun, juru bicara Institut menekankan bahwa terlepas dari tes ini, laporan medis Arafat tidaklah konsisten dengan keracunan210Po,[114]dan jurnalis sainsDeborah Blummenyatakan bahwa asap tembakau mungkin lebih bertanggung jawab, karena Arafat dan banyak rekannya adalah perokok berat;[115]tes selanjutnya oleh tim Prancis dan Rusia menetapkan bahwa peningkatan kadar210Po bukanlah hasil dari keracunan yang disengaja, dan tidak menyebabkan kematian Arafat.[116][117]
Ada juga dugaan bahwaRoman Tsepovdiracun dengan polonium. Dia memiliki gejala yang mirip dengan Aleksander Litvinenko.[118]
Pengobatan
[sunting|sunting sumber]Telah dikemukakan bahwaagen pengelat,seperti British Anti-Lewisite (dimerkaprol), dapat digunakan untuk mendekontaminasi manusia.[119]Dalam satu percobaan, tikus diberi dosis fatal 1,45 MBq/kg (8,7 ng/kg)210Po; semua tikus yang tidak diobati mati setelah 44 hari, tetapi 90% tikus yang diobati dengan agen pengelat HOEtTTC tetap hidup selama 5 bulan.[120]
Deteksi dalam spesimen biologis
[sunting|sunting sumber]Polonium-210 dapat dihitung dalam spesimen biologis dengan spektrometri partikel alfa untuk mengonfirmasi diagnosis keracunan pada pasien rawat inap atau untuk memberikan bukti dalam investigasi kematian medikolegal. Ekskresi urin polonium-210 dasar pada orang sehat karena paparan rutin terhadap sumber lingkungan biasanya berkisar antara 5–15 mBq/hari. Tingkat yang melebihi 30 mBq/hari menunjukkan paparan radionuklida yang berlebihan.[121]
Keterjadian pada manusia dan biosfer
[sunting|sunting sumber]Polonium-210 tersebar luas dibiosfer,termasuk di jaringan manusia, karena posisinya dalamrantai peluruhan uranium-238.Uranium-238alami dikerak Bumimeluruh melalui serangkaian perantara radioaktif padat termasukradium-226hingga gas mulia radioaktifradon-222,beberapa di antaranya, selama waktu paruh 3,8 hari, berdifusi ke atmosfer. Di sana ia meluruh melalui beberapa tahap lagi menjadi polonium-210, yang sebagian besar, selama waktu paruh 138 hari, tersapu kembali ke permukaan Bumi, lalu memasuki biosfer, sebelum akhirnya meluruh menjaditimbal-206yang stabil.[122][123][124]
Pada awal tahun 1920-an, ahli biologi PrancisAntoine Lacassagne,dengan menggunakan polonium yang disediakan oleh rekannyaMarie Curie,menunjukkan bahwa unsur tersebut memiliki pola serapan tertentu pada jaringan kelinci, dengan konsentrasi tinggi, terutama dihati,ginjal,dantestis.[125]Bukti yang lebih baru menunjukkan bahwa perilaku ini dihasilkan dari polonium yang menggantikan kongenernya belerang, juga dalam golongan 16 dari tabel periodik, dalam asam amino yang mengandung belerang atau molekul terkait[126]dan bahwa pola distribusi yang serupa terjadi pada jaringan manusia.[127]Polonium memang merupakan unsur yang secara alami ada pada semua manusia, berkontribusi cukup besar terhadap dosis latar alami, dengan variasi geografis dan budaya yang luas, dan tingkat yang sangat tinggi pada penduduk Arktik, misalnya.[128]
Tembakau
[sunting|sunting sumber]Polonium-210dalam tembakau berkontribusi pada banyak kasuskanker paru-parudi seluruh dunia. Sebagian besar polonium ini berasal daritimbal-210yang tersimpan di daun tembakau dari atmosfer; timbal-210 adalah produk gasradon-222,yang sebagian besar tampaknya berasal dari peluruhanradium-226dari pupuk yang diberikan pada tanah tembakau.[53][129][130][131][132]
Kehadiran polonium dalam asap tembakau telah diketahui sejak awal 1960-an.[133][134]Beberapa perusahaan tembakau terbesar di dunia meneliti cara untuk menghilangkan zat tersebut—tanpa hasil—selama periode 40 tahun. Hasilnya tidak pernah dipublikasikan.[53]
Makanan
[sunting|sunting sumber]Polonium ditemukan dalam rantai makanan, terutama dalam makanan laut.[135][136]
Lihat pula
[sunting|sunting sumber]Referensi
[sunting|sunting sumber]- ^(Indonesia)"Polonium".KBBI Daring.Diakses tanggal17 Juli2022.
- ^abThayer, John S. (2010). "Relativistic Effects and the Chemistry of the Heavier Main Group Elements".Relativistic Methods for Chemists.Challenges and Advances in Computational Chemistry and Physics.10:78.doi:10.1007/978-1-4020-9975-5_2.ISBN978-1-4020-9974-8.
- ^Boutin, Chad."Polonium's Most Stable Isotope Gets Revised Half-Life Measurement".nist.gov.NIST Tech Beat.Diakses tanggal29 Juli2022.
- ^abc"Polonium"(PDF).Argonne National Laboratory. Diarsipkan dariversi asli(PDF)tanggal 3 Juli 2007.Diakses tanggal11 Maret2023.
- ^Greenwood,hlm. 250
- ^"210PO α decay".Nuclear Data Center, Korea Atomic Energy Research Institute.2000.Diakses tanggal10 Maret2023.
- ^Greenwood,hlm. 753
- ^Miessler, Gary L.; Tarr, Donald A. (2004).Inorganic Chemistry(edisi ke-3rd). Upper Saddle River, N.J.: Pearson Prentice Hall. hlm.285.ISBN978-0-13-120198-9.
- ^"The beta Po (A_i) Structure".Naval Research Laboratory.20 November 2000. Diarsipkan dariversi aslitanggal 4 Februari 2001.Diakses tanggal10 Maret2023.
- ^Desando, R. J.; Lange, R. C. (1966). "The structures of polonium and its compounds—I α and β polonium metal".Journal of Inorganic and Nuclear Chemistry.28(9): 1837–1846.doi:10.1016/0022-1902(66)80270-1.
- ^Beamer, W. H.; Maxwell, C. R. (1946)."The Crystal Structure of Polonium".Journal of Chemical Physics.14(9): 569.doi:10.1063/1.1724201.hdl:2027/mdp.39015086430371
 .
.
- ^Rollier, M. A.; Hendricks, S. B.; Maxwell, L. R. (1936)."The Crystal Structure of Polonium by Electron Diffraction".Journal of Chemical Physics.4(10): 648.Bibcode:1936JChPh...4..648R.doi:10.1063/1.1749762.
- ^Wąs, Bogdan; Misiak, Ryszard; Bartyzel, Mirosław; Petelenz, Barbara (2006)."Thermochromatographic separation of206,208Po from a bismuth target bombarded with protons "(PDF).Nukleonika.51(Suppl. 2): s3–s5.
- ^Lide, D. R., ed. (2005).CRC Handbook of Chemistry and Physics(edisi ke-86). Boca Raton (FL): CRC Press.ISBN0-8493-0486-5.
- ^Condit, Ralph H.; Gray, Leonard W.; Mitchell, Mark A. (2014).Pseudo-evaporation of high specific activity Alpha -emitting materials.EFCOG 2014 Safety Analysis Workshop.Lawrence Livermore National Laboratory.
- ^abcdefEmsley, John (2001).Nature's Building Blocks.New York: Oxford University Press. hlm. 330–332.ISBN978-0-19-850341-5.
- ^Bagnall,hlm. 206
- ^Keller, Cornelius; Wolf, Walter; Shani, Jashovam (2005), "Radionuclides, 2. Radioactive Elements and Artificial Radionuclides",Ullmann's Encyclopedia of Industrial Chemistry,Weinheim: Wiley-VCH,doi:10.1002/14356007.o22_o15
- ^Bagnall,hlm. 199
- ^abGreenwood,hlm. 766
- ^Weigel, F. (1959). "Chemie des Poloniums".Angewandte Chemie.71(9): 289–316.Bibcode:1959AngCh..71..289W.doi:10.1002/ange.19590710902.
- ^Holleman, A. F.; Wiberg, E. (2001).Inorganic Chemistry.San Diego: Academic Press.ISBN978-0-12-352651-9.
- ^abFiggins, P. E. (1961)The Radiochemistry of Polonium,National Academy of Sciences, US Atomic Energy Commission, hlm. 13–14Google Books
- ^abGreenwood,hlm. 765, 771, 775
- ^Bagnall,hlm. 212–226
- ^abZingaro, Ralph A. (2011). "Polonium: Organometallic Chemistry".Encyclopedia of Inorganic and Bioinorganic Chemistry.John Wiley & Sons. hlm. 1–3.doi:10.1002/9781119951438.eibc0182.ISBN9781119951438.
- ^Murin, A. N.; Nefedov, V. D.; Zaitsev, V. M.; Grachev, S. A. (1960)."Production of organopolonium compounds by using chemical alterations taking place during the β-decay of RaE"(PDF).Dokl. Akad. Nauk SSSR(dalam bahasa Rusia).133(1): 123–125.Diakses tanggal12 April2020.
- ^Wiberg, Egon; Holleman, A. F. and Wiberg, NilsInorganic Chemistry,Academic Press, 2001, hlm. 594,ISBN0-12-352651-5.
- ^Bagnall, K. W.; d'Eye, R. W. M. (1954). "The Preparation of Polonium Metal and Polonium Dioxide".J. Chem. Soc.:4295–4299.doi:10.1039/JR9540004295.
- ^abBagnall, K. W.; d'Eye, R. W. M.; Freeman, J. H. (1955). "The polonium halides. Part I. Polonium chlorides".Journal of the Chemical Society (Resumed):2320.doi:10.1039/JR9550002320.
- ^abBagnall, K. W.; d'Eye, R. W. M.; Freeman, J. H. (1955). "The polonium halides. Part II. Bromides".Journal of the Chemical Society (Resumed):3959.doi:10.1039/JR9550003959.
- ^Bagnall, K. W.; d'Eye, R. W. M.; Freeman, J. H. (1956). "657. The polonium halides. Part III. Polonium tetraiodide".Journal of the Chemical Society (Resumed):3385.doi:10.1039/JR9560003385.
- ^Collé, R.; Fitzgerald, R.P.; Laureano-Perez, L. (13 Agustus 2014)."A new determination of the209Po half-life ".Journal of Physics G.41(10): 105103.Bibcode:2014JPhG...41j5103C.doi:10.1088/0954-3899/41/10/105103.
- ^Emsley, John (2011).Nature's Building Blocks: An A-Z Guide to the Elements(edisi ke-New). New York, NY: Oxford University Press. hlm.415.ISBN978-0-19-960563-7.
- ^abCurie, P.; Curie, M. (1898)."Sur une substance nouvelle radio-active, contenue dans la pechblende"[Pada zat radioaktif baru yang terkandung dalam uraninit](PDF).Comptes Rendus(dalam bahasa Prancis).127:175–178. Diarsipkan dariversi asli(PDF)tanggal 23 Juli 2013.Terjemahan bahasa Inggris.
- ^Krogt, Peter van der."84. Polonium - Elementymology & Elements Multidict".elements.vanderkrogt.net.Diakses tanggal11 Maret2023.
- ^Pfützner, M. (1999). "Borders of the Nuclear World – 100 Years After Discovery of Polonium".Acta Physica Polonica B.30(5): 1197.Bibcode:1999AcPPB..30.1197P.
- ^Adloff, J. P. (2003). "The centennial of the 1903 Nobel Prize for physics".Radiochimica Acta.91(12–2003): 681–688.doi:10.1524/ract.91.12.681.23428.
- ^abKabzinska, K. (1998). "Chemical and Polish aspects of polonium and radium discovery".Przemysł Chemiczny.77(3): 104–107.
- ^Curie, P.; Curie, M.; Bémont, G. (1898)."Sur une nouvelle substance fortement radio-active contenue dans la pechblende"[Pada zat baru yang sangat radioaktif yang terkandung dalam uraninit](PDF).Comptes Rendus(dalam bahasa Prancis).127:1215–1217. Diarsipkan dariversi asli(PDF)tanggal 22 Juli 2013.Terjemahan bahasa InggrisDiarsipkan6 Agustus 2009 diWayback Machine.
- ^"Polonium and Radio-Tellurium".Nature.73(549): 549. 1906.Bibcode:1906Natur..73R.549..doi:10.1038/073549b0
 .
.
- ^Neufeldt, Sieghard (2012).Chronologie Chemie: Entdecker und Entdeckungen.John Wiley & Sons.ISBN9783527662845.
- ^abNuclear Weapons FAQ, Section 4.1, Version 2.04: 20 Februari 1999.Nuclearweaponarchive.org. Diakses tanggal 11 Maret 2023.
- ^KEPUTUSAN DEKLASIFIKASI DATA TERBATAS, 1946 SAMPAI SEKARANG (RDD-7),1 Januari 2001, Kantor Deklasifikasi Departemen Energi A.S., via fas.org
- ^American nuclear guinea pigs: three decades of radiation experiments on U.S. citizensDiarsipkan30 Juli 2013 diWayback Machine.. United States. Congress. House. of the Committee on Energy and Commerce. Subcommittee on Energy Conservation and Power, published by U.S. Government Printing Office, 1986, Identifier Y 4.En 2/3:99-NN, Electronic Publication Date 2010, at the University of Nevada, Reno, unr.edu
- ^"Studies of polonium metabolism in human subjects", Chapter 3 inBiological Studies with Polonium, Radium, and Plutonium,National, Nuclear Energy Series, Volume VI-3, McGraw-Hill, New York, 1950, cited in "American Nuclear Guinea Pigs...", 1986 House Energy and Commerce committee report
- ^Moss, William and Eckhardt, Roger (1995)"The Human Plutonium Injection Experiments",Los Alamos Science, Number 23.
- ^Carvalho, F.; Fernandes, S.; Fesenko, S.; Holm, E.; Howard, B.; Martin, P.; Phaneuf, P.; Porcelli, D.; Pröhl, G.; Twining, J. (2017).The Environmental Behaviour of Polonium.Technical Reports Series - International Atomic Energy Agency.Technical reports series.484.Vienna: International Atomic Energy Agency. hlm. 1.ISBN978-92-0-112116-5.ISSN0074-1914.
- ^Greenwood,hlm. 746
- ^Bagnall,hlm. 198
- ^Kilthau, Gustave F. (1996). "Cancer risk in relation to radioactivity in tobacco".Radiologic Technology.67(3): 217–222.PMID8850254.
- ^"Alpha Radioactivity (210 Polonium) and Tobacco Smoke".Diarsipkan dariversi aslitanggal 9 Juni 2013.Diakses tanggal11 Maret2023.
- ^abcMonique, E. Muggli; Ebbert, Jon O.; Robertson, Channing; Hurt, Richard D. (2008)."Waking a Sleeping Giant: The Tobacco Industry's Response to the Polonium-210 Issue".American Journal of Public Health.98(9): 1643–50.doi:10.2105/AJPH.2007.130963.PMC2509609
 .PMID18633078.
.PMID18633078.
- ^Adloff, J. P.; MacCordick, H. J. (1995)."The Dawn of Radiochemistry".Radiochimica Acta.70/71: 13–22.doi:10.1524/ract.1995.7071.special-issue.13.,reprinted inAdloff, J. P. (1996).One hundred years after the discovery of radioactivity.hlm. 17.ISBN978-3-486-64252-0.[pranala nonaktif permanen]
- ^abGreenwood,hlm. 249
- ^Schulz, Wallace W.; Schiefelbein, Gary F.; Bruns, Lester E. (1969). "Pyrochemical Extraction of Polonium from Irradiated Bismuth Metal".Ind. Eng. Chem. Process Des. Dev.8(4): 508–515.doi:10.1021/i260032a013.
- ^"Q&A: Polonium-210".RSC Chemistry World. 27 November 2006.Diakses tanggal11 Maret2023.
- ^"Most Polonium Made Near the Volga River".The Moscow Times – News. 11 Januari 2007.
- ^Usanov, V. I.; Pankratov, D. V.; Popov, É. P.; Markelov, P. I.; Ryabaya, L. D.; Zabrodskaya, S. V. (1999). "Long-lived radionuclides of sodium, lead-bismuth, and lead coolants in fast-neutron reactors".Atomic Energy.87(3): 658–662.doi:10.1007/BF02673579.
- ^Naumov, V. V. (November 2006).За какими корабельными реакторами будущее?.Атомная стратегия(dalam bahasa Rusia).26.
- ^Atterling, H.; Forsling, W. (1959). "Light Polonium Isotopes from Carbon Ion Bombardments of Platinum".Arkiv för Fysik.15(1): 81–88.OSTI4238755.
- ^ab"Радиоизотопные источники тепла".Diarsipkan dariversi aslitanggal 1 Mei 2007.Diakses tanggal11 Maret2023.(dalam bahasa Rusia). npc.sarov.ru
- ^Bagnall,hlm. 225
- ^abGreenwood,hlm. 251
- ^Hanslmeier, Arnold (2002).The sun and space weather.Springer. hlm. 183.ISBN978-1-4020-0684-5.
- ^Wilson, Andrew (1987).Solar System Log.London: Jane's Publishing Company Ltd. hlm.64.ISBN978-0-7106-0444-6.
- ^Ritter, Sebastian (2021). "Comparative Study of Gamma to Neutron Ratios of various ( Alpha, neutron) Neutron Sources".arΧiv:2111.02774[nucl-ex].
- ^Rhodes, Richard (2002).Dark Sun: The Making of the Hydrogen Bomb.New York: Walker & Company. hlm.187–188.ISBN978-0-684-80400-2.
- ^Красивая версия "самоубийства" Литвиненко вследствие криворукости(dalam bahasa Rusia). stringer.ru (26 November 2006).
- ^Boice, John D.; Cohen, Sarah S.; et al. (2014). "Mortality Among Mound Workers Exposed to Polonium-210 and Other Sources of Radiation, 1944–1979".Radiation Research.181(2): 208–28.Bibcode:2014RadR..181..208B.doi:10.1667/RR13395.1.ISSN0033-7587.OSTI1286690.PMID24527690.
- ^"Static Control for Electronic Balance Systems"(PDF).Diarsipkan dariversi asli(PDF)tanggal 10 November 2013.Diakses tanggal11 Maret2023.
- ^"BBC News: College breaches radioactive regulations".12 Maret 2002.Diakses tanggal11 Maret2023.
- ^"Staticmaster Ionizing Brushes".AMSTAT Industries. Diarsipkan dariversi aslitanggal 26 September 2009.Diakses tanggal11 Maret2023.
- ^"General domestic licenses for byproduct material".Diakses tanggal11 Maret2023.
- ^"Radioactive spark plugs".Oak Ridge Associated Universities. 20 Januari 1999.Diakses tanggal11 Maret2023.
- ^Pittman, Cassandra (3 februari 2017)."Polonium".The Instrumentation Center.University of Toledo.Diakses tanggal11 Maret2023.
- ^"Safety data for hydrogen cyanide".Physical & Theoretical Chemistry Lab, Oxford University.Diarsipkan dariversi aslitanggal 11 Februari 2002.
- ^Bagnall,hlm. 202–6
- ^"Polonium-210: Effects, symptoms, and diagnosis".Medical News Today.28 Juli 2017.
- ^Momoshima, N.; Song, L. X.; Osaki, S.; Maeda, Y. (2001). "Formation and emission of volatile polonium compound by microbial activity and polonium methylation with methylcobalamin".Environ Sci Technol.35(15): 2956–2960.Bibcode:2001EnST...35.2956M.doi:10.1021/es001730.PMID11478248.
- ^ Momoshima, N.; Song, L. X.; Osaki, S.; Maeda, Y. (2002). "Biologically induced Po emission from fresh water".J Environ Radioact.63(2): 187–197.doi:10.1016/S0265-931X(02)00028-0.PMID12363270.
- ^Li, Chunsheng; Sadi, Baki; Wyatt, Heather; Bugden, Michelle; et al. (2010). "Metabolism of210Po in rats: volatile210Po in excreta ".Radiation Protection Dosimetry.140(2): 158–162.doi:10.1093/rpd/ncq047.PMID20159915.
- ^ab"Health Impacts from Acute Radiation Exposure"(PDF).Pacific Northwest National Laboratory.Diakses tanggal11 Maret2023.
- ^"Nuclide Safety Data Sheet: Polonium–210"(PDF).hpschapters.org.Diakses tanggal11 Maret2023.
- ^Naimark, D.H. (4 Januari 1949). "Effective half-life of polonium in the human".Technical Report MLM-272/XAB, Mound Lab., Miamisburg, OH.OSTI7162390.
- ^Carey Sublette (14 Desember 2006)."Polonium Poisoning".Diakses tanggal11 Maret2023.
- ^Harrison, J.; Leggett, Rich; Lloyd, David; Phipps, Alan; et al. (2007). "Polonium-210 as a poison".J. Radiol. Prot.27(1): 17–40.Bibcode:2007JRP....27...17H.doi:10.1088/0952-4746/27/1/001.PMID17341802.
Kesimpulan yang dicapai adalah bahwa 0,1–0,3 GBq atau lebih yang terserap ke dalam darah pria dewasa cenderung berakibat fatal dalam waktu 1 bulan. Ini sesuai dengan konsumsi 1–3 GBq atau lebih, dengan asumsi penyerapan sebesar 10% ke darah
- ^Yasar Safkan."Approximately how many atoms are in a grain of salt?".PhysLink: Physics & Astronomy.
- ^Health Risks of Radon and Other Internally Deposited Alpha-Emitters: BEIR IV.National Academy Press. 1988. hlm. 5.ISBN978-0-309-03789-1.
- ^Health Effects Of Exposure To Indoor Radon.Washington: National Academy Press. 1999. Diarsipkan dariversi aslitanggal 19 Juni 2006.
- ^"The Straight Dope: Does smoking organically grown tobacco lower the chance of lung cancer?".28 September 2007.Diakses tanggal11 Maret2023.
- ^"Nuclear Regulatory Commission limits for210Po ".U.S. NRC. 12 Desember 2008.Diakses tanggal11 Maret2023.
- ^"PilgrimWatch – Pilgrim Nuclear – Health Impact".Diarsipkan dariversi aslitanggal 5 Januari 2009.Diakses tanggal11 Maret2023.
- ^Bastian, R.K.; Bachmaier, J.T.; Schmidt, D.W.; Salomon, S.N.; Jones, A.; Chiu, W.A.; Setlow, L.W.; Wolbarst, A.W.; Yu, C. (1 Januari 2004). "Radioactive Materials in Biosolids: National Survey, Dose Modeling & POTW Guidance".Proceedings of the Water Environment Federation.2004(1): 777–803.doi:10.2175/193864704784343063.ISSN1938-6478.
- ^Zimmerman, Peter D. (19 Desember 2006)."The Smoky Bomb Threat".The New York Times.Diakses tanggal11 Maret2023.
- ^Bagnall,hlm. 204
- ^abMoss, William; Eckhardt, Roger (1995)."The human plutonium injection experiments"(PDF).Los Alamos Science.23:177–233.
- ^Fink, Robert (1950).Biological studies with polonium, radium, and plutonium.National Nuclear Energy Series (dalam bahasa Rusia).VI–3.McGraw-Hill.ISBN5-86656-114-X.
- ^abGasteva, G. N. (2001). "Ostraja lučevaja boleznʹ ot postuplenija v organizm polonija" [Penyakit radiasi akut dengan menelan polonium ke dalam tubuh]. Dalam Ilʹin, L. A.Radiacionnaja medicina: rukovodstvo dlja vračej-issledovatelej i organizatorov zdravooxranenija, Tom 2 (Radiacionnye poraženija čeloveka)[Pengobatan radiasi: panduan untuk peneliti medis dan manajer layanan kesehatan, Volume 2 (Kerusakan radiasi pada manusia)] (dalam bahasa Rusia). IzdAT. hlm. 99–107.ISBN5-86656-114-X.
- ^Harrison, John; Leggett, Rich; Lloyd, David; Phipps, Alan; Scott, Bobby (2 March 2007). "Polonium-210 as a poison".Journal of Radiological Protection.27(1): 17–40.Bibcode:2007JRP....27...17H.doi:10.1088/0952-4746/27/1/001.PMID17341802.
- ^Manier, Jeremy (4 Desember 2006)."Innocent chemical a killer".The Daily Telegraph (Australia). Diarsipkan dariversi aslitanggal 6 Januari 2009.Diakses tanggal11 Maret2023.
- ^Karpin, Michael (2006).The bomb in the basement: How Israel went nuclear and what that means for the world.Simon and Schuster.ISBN978-0-7432-6594-2.
- ^Maugh, Thomas; Karen Kaplan (1 Januari 2007)."A restless killer radiates intrigue".Los Angeles Times.Diakses tanggal11 Maret2023.
- ^Geoghegan, Tom (24 November 2006)."The mystery of Litvinenko's death".BBC News.
- ^"UK requests Lugovoi extradition".BBC News.28 Mei 2007.Diakses tanggal11 Maret2023.
- ^"Report".The Litvinenko Inquiry.Diakses tanggal11 Maret2023.
- ^Addley, Esther; Harding, Luke (21 Januari 2016)."Litvinenko 'probably murdered on personal orders of Putin'".The Guardian.Diakses tanggal11 Maret2023.
- ^Boggan, Steve (5 Juni 2007)."Who else was poisoned by polonium?".The Guardian.Diakses tanggal11 Maret2023.
- ^Poort, David (6 November 2013)."Polonium: a silent killer".Al Jazeera News.Diakses tanggal11 Maret2023.
- ^Froidevaux, Pascal; Bochud, François; Baechler, Sébastien; Castella, Vincent; Augsburger, Marc; Bailat, Claude; Michaud, Katarzyna; Straub, Marietta; Pecchia, Marco; Jenk, Theo M.; Uldin, Tanya; Mangin, Patrice (Februari 2016)."²¹⁰Po poisoning as possible cause of death: forensic investigations and toxicological analysis of the remains of Yasser Arafat".Forensic Science International.259:1–9.doi:10.1016/j.forsciint.2015.09.019.PMID26707208.Diakses tanggal11 Maret2023.
- ^"الأخبار - ضابط فلسطيني: خصوم عرفات قتلوه عربي".Al Jazeera.17 Januari 2011. Diarsipkan dariversi aslitanggal 4 Juli 2012.Diakses tanggal11 Maret2023.
- ^"George Galloway and Alex Goldfarb on Litvinenko inquiry".Newsnight.21 Januari 2016. Berlangsung pada 1:53.BBC.Diarsipkan dariversi aslitanggal 30 Oktober 2021.Diakses tanggal11 Maret2023.
- ^Froidevaux, P.; Baechler, S. B.; Bailat, C. J.; Castella, V.; Augsburger, M.; Michaud, K.; Mangin, P.; Bochud, F. O. O. (2013). "Improving forensic investigation for polonium poisoning".The Lancet.382(9900): 1308.doi:10.1016/S0140-6736(13)61834-6.PMID24120205.
- ^abBart, Katharina (3 Juli 2012).Swiss institute finds polonium in Arafat's effectsDiarsipkan7 Oktober 2015 diWayback Machine.. Reuters.
- ^"Yasser Arafat and the radioactive cigarette".Wired.12 Juni 2012.Diakses tanggal11 Maret2023.
- ^Isachenkov, Vadim (27 Desember 2013)Russia: Arafat's death not caused by radiation.Associated Press.
- ^"Arafat did not die of poisoning, French tests conclude".Reuters.3 Desember 2013.Diakses tanggal11 Maret2023.
- ^"The Putin bodyguard riddle".The Sunday Times.3 Desember 2006.
- ^"Guidance for Industry. Internal Radioactive Contamination — Development of Decorporation Agents"(PDF).US Food and Drug Administration.Diakses tanggal11 Maret2023.
- ^Rencováa J.; Svoboda V.; Holuša R.; Volf V.; et al. (1997). "Reduction of subacute lethal radiotoxicity of polonium-210 in rats by chelating agents".International Journal of Radiation Biology.72(3): 341–8.doi:10.1080/095530097143338.PMID9298114.
- ^Baselt, R.Disposition of Toxic Drugs and Chemicals in ManDiarsipkan16 Juni 2013 diWayback Machine., edisi ke-10, Biomedical Publications, Seal Beach, CA.
- ^Hill, C. R. (1960). "Lead-210 and Polonium-210 in Grass".Nature.187(4733): 211–212.Bibcode:1960Natur.187..211H.doi:10.1038/187211a0.PMID13852349.
- ^Hill, C. R. (1963)."Natural occurrence of unsupported radium-F (Po-210) in tissue".Health Physics.9:952–953.PMID14061910.
- ^Heyraud, M.; Cherry, R. D. (1979). "Polonium-210 and lead-210 in marine food chains".Marine Biology.52(3): 227–236.doi:10.1007/BF00398136.
- ^Lacassagne, A. & Lattes, J. (1924)Bulletin d'Histologie Appliquée à la Physiologie et à la Pathologie,1,279.
- ^Vasken Aposhian, H.; Bruce, D. C. (1991). "Binding of Polonium-210 to Liver Metallothionein".Radiation Research.126(3): 379–382.Bibcode:1991RadR..126..379A.doi:10.2307/3577929.JSTOR3577929.PMID2034794.
- ^Hill, C. R. (1965). "Polonium-210 in man".Nature.208(5009): 423–8.Bibcode:1965Natur.208..423H.doi:10.1038/208423a0.PMID5867584.
- ^Hill, C. R. (1966). "Polonium-210 Content of Human Tissues in Relation to Dietary Habit".Science.152(3726): 1261–2.Bibcode:1966Sci...152.1261H.doi:10.1126/science.152.3726.1261.PMID5949242.
- ^Martell, E. A. (1974)."Radioactivity of tobacco trichomes and insoluble cigarette smoke particles".Nature.249(5454): 214–217.Bibcode:1974Natur.249..215M.doi:10.1038/249215a0.PMID4833238.Diarsipkan dariversi aslitanggal 2016-07-01.Diakses tanggal11 Maret2023.
- ^Martell, E. A. (1975). "Tobacco Radioactivity and Cancer in Smokers: Alpha interactions with chromosomes of cells surrounding insoluble radioactive smoke particles may cause cancer and contribute to early atherosclerosis development in cigarette smokers".American Scientist.63(4): 404–412.Bibcode:1975AmSci..63..404M.JSTOR27845575.PMID1137236.
- ^Tidd, M. J. (2008)."The big idea: polonium, radon and cigarettes".Journal of the Royal Society of Medicine.101(3): 156–7.doi:10.1258/jrsm.2007.070021.PMC2270238
 .PMID18344474.
.PMID18344474.
- ^Birnbauer, William (7 September 2008)"Big Tobacco covered up radiation danger".The Age,Melbourne, Australia
- ^Radford EP Jr; Hunt VR (1964). "Polonium 210: a volatile radioelement in cigarettes".Science.143(3603): 247–9.Bibcode:1964Sci...143..247R.doi:10.1126/science.143.3603.247.PMID14078362.
- ^Kelley TF (1965). "Polonium 210 content of mainstream cigarette smoke".Science.149(3683): 537–538.Bibcode:1965Sci...149..537K.doi:10.1126/science.149.3683.537.PMID14325152.
- ^Ota, Tomoko; Sanada, Tetsuya; Kashiwara, Yoko; Morimoto, Takao; et al. (2009)."Evaluation for Committed Effective Dose Due to Dietary Foods by the Intake for Japanese Adults".Japanese Journal of Health Physics.44:80–88.doi:10.5453/jhps.44.80
 .
.
- ^Smith-Briggs, JL; Bradley, EJ (1984). "Measurement of natural radionuclides in U.K. diet".Science of the Total Environment.35(3): 431–40.Bibcode:1984ScTEn..35..431S.doi:10.1016/0048-9697(84)90015-9.PMID6729447.
Bibliografi
[sunting|sunting sumber]- Bagnall, K. W. (1962)."The Chemistry of Polonium".Advances in Inorganic Chemistry and Radiochemistry.4.New York:Academic Press.hlm. 197–226.doi:10.1016/S0065-2792(08)60268-X.ISBN978-0-12-023604-6.Diakses tanggal11 Maret2023.
- Greenwood, Norman N.; Earnshaw, Alan (1997).Chemistry of the Elements(edisi ke-2). Butterworth–Heinemann.ISBN978-0080379418.
Pranala luar
[sunting|sunting sumber]- (Inggris)PoloniumdiThe Periodic Table of Videos(Universitas Nottingham)
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||



