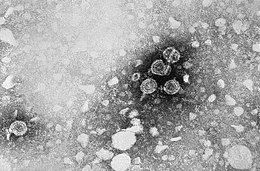
Epatite B
L'epatite Bè unamalattia infettiva,causata dalvirusHBV,appartenente alla famigliaHepadnaviridae,che colpisce ilfegatodeglihominoidea.La malattia, nota in origine come "epatite da siero"[1],è causa diepidemiein alcune parti dell'Asiae inAfricaed è a carattereendemicoinCina[2].Circa un quarto della popolazione mondiale, più di due miliardi di persone, è stato contagiato dal virus dell'epatite B[3]ed esistono circa 350 milioni di portatori cronici del virus[4].
| Epatite B | |
|---|---|
 | |
| Specialità | infettivologia |
| Eziologia | Infettiva |
| Sede colpita | Fegato |
| Classificazione e risorse esterne (EN) | |
| ICD-9-CM | 070.2e070.3 |
| ICD-10 | B16,B18.0eB18.1 |
| OMIM | 610424 |
| MeSH | D006509 |
| MedlinePlus | 000279 |
| eMedicine | 177632e964662 |
La trasmissione di epatite B avviene tramite esposizione asangueinfetto o a fluidi corporei comespermae liquidivaginali,mentre ilDNAvirale è stato rilevato anche nellasaliva,nellelacrimee nell'urinadi portatori cronici con alto titolo nelsiero sanguigno[3][5].Il virus dell'epatite B non può essere però trasmesso attraverso il contatto casuale, come per esempio il tocco delle mani, la condivisione di posate o bicchieri, l'allattamento, baci, abbracci, tosse o starnuti[6].Il virus è comunque in grado di sopravvivere fino a 7 giorni nell'ambiente.
La malattia provoca un'infiammazione acuta del fegato,vomito,itteroe, di rado, può portare allamorte.L'epatite B cronica può causarecirrosi epaticaecancro al fegato,una malattia mortale con una scarsa risposta allachemioterapia[7].L'infezione si può prevenire con lavaccinazione[8].Si stima che ogni anno muoiano circa 750 000 persone per le conseguenze dell'epatite B[3].
Nel caso l'infezione coinvolga un bambino nonvaccinato,evento possibile per varie cause (alla nascita dalla madre infetta anche se asintomatica, per contatto con tagli o ferite aperte di adulti o altri bambini infetti, ecc.), lo sviluppo di condizioni croniche avviene con una frequenza variabile tra l'80 e il 90% in caso di infezione nel primo anno di vita, e tra il 50 e il 60% nel caso di infezione prima dei 6 anni[3].Per prevenire questi rischi, la posizione ufficiale dell'Organizzazione mondiale della sanitàè che tutti i neonati dovrebbero ricevere la loro prima dose di vaccino entro le prime 24 ore dalla nascita[9];ilvaccino antiepatite Bè efficace nel 95% dei casi nel prevenire l'infezione e le sue conseguenze croniche, ed è stato il primo vaccino a essere sviluppato come forma di prevenzione contro gravitumori.Il vaccino antiepatite B è considerato particolarmente sicuro[3];gli effetti collaterali, come per gli altri vaccini, sono rari e particolarmente blandi (arrossamento della pelle nel punto dell'iniezione,febbreleggera di breve durata); nonostante numerosi studi a lungo termine, non è mai emersa evidenza di gravi eventi avversi connessi in modo causale alla vaccinazione[10].
Storia
modificaIlvirus dell'epatite Bha infettato l'uomo almeno dall'età del bronzo[11][12].Le prove di ciò sono state ottenute dall'analisi di resti umani risalenti a 4 500 anni fa[12].Secondo uno studio pubblicato nel 2018, igenomivirali ottenuti mediantesequenziamento shotgunsono i più antichi mai recuperati davertebrati[12].Inoltre, è stato scoperto che alcuni antichi ceppi virali dell'epatite sono ancora responsabili di infezione negli esseri umani, mentre altri si sono estinti[12].Ciò ha smentito la teoria in cui si voleva che l'epatite B avesse avuto origine nelNuovo Mondoe che si fosse poi diffusa in Europa intorno alXVI secolo[12].Un altro studio, sempre del 2018, effettuato sui resti di un bambinomummificatotrovato nellaBasilica di San Domenico MaggioreaNapoliha concluso che questi, vissuto nel XVI secolo, accusava una forma di HBV e che ilvirusfosse strettamente correlato alle varianti moderne[13].Gli studi genomici confermano, tuttavia, un'origine più antica nell'uomo. Un particolare sottogenotipo, detto C4, dell'epatite B risulta presente negliaborigeni australianie in nessun altro luogo nel sud-est asiatico, suggerendo un'origine antica stimabile in 50 000 anni[14][15].Ulteriori studi hanno confermato che il virus fosse presente negli esseri umani 40 000 anni fa per poi diffondersi insieme a loro[16].
La prima testimonianza di un'epidemia provocata dal virus dell'epatite B la si deve a Lürman nel1885[17].Un'epidemia divaiolosi era verificata aBremanel 1883 tra i 1 289 dipendenti di un cantiere che erano stativaccinaticon ilsierodi altre persone. Dopo diverse settimane, e fino a otto mesi più tardi, 191 dei lavoratori vaccinati si ammalarono di itterizia e fu loro diagnosticata epatite da siero. Gli altri dipendenti che erano stati inoculati con differenti lotti di siero rimasero sani. Uno scritto di Lürman, oggi considerato un classico esempio distudio epidemiologico,dimostrò che il siero contaminato era stato l'origine del focolaio. In seguito, numerosi focolai simili furono riportati a seguito dell'introduzione, nel 1909, diaghi ipodermiciche venivano riutilizzati per il trattamento dellasifilide.Il virus non fu comunque scoperto fino al1965,quandoBaruch Blumberg,che allora lavorava presso ilNational Institutes of Health,scoprì l'antigene Australia(più tardi conosciuto per essereantigenedi superficie dell'epatite B, o HBsAg) nel sangue diaborigeni australiani[18].Un virus era comunque stato sospettato a partire dallo studio pubblicato da MacCallum nel1947[19].Nel 1970, grazie almicroscopio elettronicovenne visualizzato il virus e nei primianni ottantail genoma del virus è stato sequenziato[20]e furono testati i primi vaccini[21].
Epidemiologia
modificaAlta:prevalenzasuperiore a 8%
Moderata: tra il 2 e il 7%
Bassa: inferiore al 2%
Nel 2004 si stimava che ci fossero 350-400 milioni di portatori cronici dell'epatite B in tutto il mondo e che un terzo della popolazione mondiale sia portatrice di anticorpi specifici del virus (e che quindi abbia contratto il virus nel corso della propria vita). La prevalenza di malati varia da oltre il 10% in Asia allo 0,5% negli Stati Uniti e in Europa settentrionale. Si stima che ogni anno 4,5 milioni di soggetti contraggano il virus e che solo una parte di essi vada incontro a epatite cronica,cirrosiedepatocarcinomacellulare; secondo l'Organizzazione mondiale della sanità,l'epatite B provoca oltre 600 000 decessi annui per le conseguenze croniche della malattia[23].
Le vie di infezione includono latrasmissione verticale(ad esempio attraverso ilparto), la trasmissione orizzontale nei primi anni di vita (morsi, lesioni e le abitudini sanitarie) e da adulti (contatto sessuale,uso di droghe per via endovenosa)[24].In zone a bassa prevalenza, come i territori continentali degli Stati Uniti e l'Europa occidentale, l'iniezione di droghe e i rapporti sessuali non protetti sono le vie principali di infezione, anche se altri fattori possono risultare importanti[25].In aree di prevalenza moderata, che comprendono l'Europa orientale, Russia e Giappone, in cui 2-7% della popolazione è cronicamente infetta, la malattia è diffusa soprattutto tra i bambini. Nelle zone di alta prevalenza come la Cina e Sud-est asiatico, la trasmissione durante il parto è la modalità più frequente[26].La prevalenza dell'infezione cronica da HBV nelle aree di alta endemicità è almeno l'8%. Nel 2010 la Cina aveva 120 milioni di persone infette, seguita da India e Indonesia, rispettivamente con 40 e 12 milioni[27].
La maggioranza dei soggetti infetti nei paesi dell'Europa occidentaleha un'infezione di lunga durata, sostenuta dalceppomutante sull' "e"oe-minus,questo poiché l'introduzione capillare della vaccinazione ha notevolmente ridotto i nuovi casi di infezione. Nei paesi dell'Europa dell'Est,inAsiaeAfrica,dove invece la frequenza di nuove infezioni è ancora alta, la maggioranza dei soggetti è infetta dal cepposelvaticoowild-type[28][29][30].
Eziologia
modificaIl virus dell'epatite B appartiene alla famigliaHepadnaviridaee presenta un genoma a DNA a doppio filamento circolare e un virioneicosaedricorivestito.Per la replicazione sfrutta latrascrittasi inversa,fa perciò parte dei virus a DNA a trascrizione inversa (detti ancheretrovirus a DNA), del gruppo VII dellaclassificazione di Baltimore,attraverso una forma intermedia aRNAe l'uso di unatrascrittasi inversache lo fa assomigliare airetrovirus[31].Se ne conoscono quattro sierotipi: adr, ADW, Ayr, ayw[31][32][33].
Anche se la replicazione avviene nel fegato, il virus si diffonde nel sangue dove, nelle persone infette, si possono trovare leproteinespecifiche del virus e i suoi corrispondentianticorpi.Esami del sangueper queste proteine e anticorpi sono utilizzati per diagnosticare l'infezione[34].
Patogenesi
modificaIl virus dell'epatite B interferisce soprattutto con le funzioni del fegato replicandosi nelle sue cellule, gliepatociti.Il recettore non è ancora noto[35][36].I virioni di HBV si legano alla cellula ospite tramite l'antigene di superficiee in seguito vengono interiorizzati perendocitosi.Recettori specifici HBV sono presenti soprattutto sugli epatociti, tuttavia il DNA virale e le proteine sono state rilevate anche in siti extraepatici, suggerendo che i recettori cellulari per l'HBV possano esistere anche su cellule extraepatiche[37].
Durante l'infezione da HBV larisposta immunitariacausa sia il danno epatocellulare sia la clearance virale. Anche se la risposta immunitaria innata non gioca un ruolo significativo in questi processi, la risposta immunitaria, con ilinfociticitotossici in particolare, contribuisce alla maggior parte dei danni al fegato associati con l'infezione da HBV[38].
La trasmissione di epatite da virus B deriva da esposizione a sangue infetto o fluidi corporei contenenti sangue. Si può trasmettere per[39]:
- via parenterale(dalgrecoparà ènteron,ovvero "al di fuori dell'intestino" ), ossia con il contatto su mucose o ferite di sangue infetto, con lesioni accidentali da aghi o altri taglienti infetti, strumentario medico chirurgico non opportunamente sterilizzato e infine, evenienza assai rara oggi dal momento che si fanno controlli sierologici, con la pratica delle emotrasfusioni;
- via parenterale inapparente,ossia tramite l'uso di oggetti che possono creare microtraumi cutanei, per esempio rasoi e forbici da unghie infetti;
- via transplacentare e perinatale, al neonato da parte di madre infetta;
- via sessuale;
- contatto o convivenza con animali di fogna (blatte) che si trovano soprattutto in Paesi poveri come l'Africa, l'India o la Cina.
L'HBV può essere trasmesso tra familiari all'interno delle famiglie, prevalentemente per il contatto di pelle non intatta o delle mucose con secrezioni o saliva contenente HBV[40][41].Tuttavia, almeno il 30% delle segnalazioni di epatite B tra gli adulti non può essere associato ad alcun fattore di rischio identificabile[42].
La storia naturale dell'infezione è completamente diversa a seconda che l'infezione venga contratta nella prima infanzia, nel qual caso si assiste a una percentuale di cronicizzazione in oltre il 90% dei casi, o in età adulta[43].In quest'ultimo caso la guarigione avviene in oltre il 90% dei casi. La guarigione si manifesta dal punto di vista laboratoristico con la scomparsa dellaproteinaHBsAg e con la comparsa di un livello dianticorpicontro questa proteina, detti HBsAb, protettivo, cioè maggiore di 10 mUI/ml. La persistenza dell'HBsAg, e quindi dell'infezione, oltre 6 mesi definisce lo stato di epatite B cronica[44].
La presenza dell'anticorpo HBeAb e di una bassa carica virale nelsanguetrasforma il soggetto da un paziente con epatite B attiva a un "portatore inattivo", non capace di infettare altri soggetti, ma comunque a rischio di possibile futura riattivazione virale, e in una situazione minimamente evolutiva se non per nulla evolutiva. A questo punto, dopo la comparsa dell'HBeAb e la fine del processo epatitico si possono verificare due circostanze[45] [46]:
- Nel primo caso il soggetto può sviluppare anche l'anticorpo contro la proteina HBsAg (HBsAb) e quindi guarire. Questo avviene soprattutto entro i primi 6 mesi dall'infezione (ma non solo) ed è il meccanismo attraverso cui la maggior parte dei soggetti affetti guarisce.
- Nel secondo caso il soggetto può restare anni nello stato di portatore cronico inattivo. Tuttavia la pressione selettiva esercitata dal sistema immunitario attraverso l'HBeAb può indurre il virus amutare.Il nuovo ceppo virale mutante impara a replicare senza esprimere l'HBeAg ma attraverso altre vie non ancora note. Questo ceppo, dettomutante sull' "e"oe-minus,è responsabile del ritorno del soggetto dallo stato di portatore inattivo allo stato di soggetto epatitico cronico con epatite attiva, caratterizzata dal nuovo incremento dellaviremia,cioè dell'HBV-DNA nel sangue, nonostante la permanenza dell'anticorpo antiHBe.
Clinica
modificaSegni e sintomi
modificaL'infezione acuta da virus dell'epatite B provoca un'epatite viraleacuta, una condizione che si presenta inizialmente consegniesintomivariegati, come una perdita di appetito,nausea,vomito,dolori muscolari,febbrelieve eurinescure, per poi progredire fino a sviluppareittero(colorazione giallastra dellacute). Tale sintomatologia dura in genere alcune settimane per poi, nella maggior parte delle persone colpite, migliorare gradualmente. Alcuni pazienti possono, invece, sviluppare una forma più grave di epatite che può portare ad unainsufficienza epaticafulminante con il conseguente rischio di decesso. Talvolta, l'infezione può essere del tutto asintomatica e non essere riconosciuta[47].
L'infezione cronica da virus dell'epatite B può essere anch'essa asintomatica o presentare un'infiammazione cronica del fegato (epatite cronica), con probabile conseguente sviluppo dicirrosidopo alcuni anni. Questa situazione è anche responsabile di un notevole aumento della probabilità di incorrere in uncarcinoma epatocellulare(tumore del fegato). In Europa, si stima che l'epatite B eCsiano responsabili di circa il 50% dei carcinomi epatocellulari[48][49].Pertanto, i portatori cronici del virus HBV sono incoraggiati a evitare il consumo dibevande alcolichepoiché queste aumentano ulteriormente il rischio di incorrere in una cirrosi e tumore del fegato. L'infezione da virus dell'epatite B è stato anche correlato allo sviluppo dellaglomerulonefrite membranosa(MGN)[50].
In circa l'1-10% di persone con infezione da HBV sono stati riscontriati sintomi che non coinvolgono il fegato, come unareazione simile alla malattia da siero,la vasculite necrotizzante acuta (poliarterite nodosa), laglomerulonefrite membranosae l'acrodermatite papulare dell'infanzia (sindrome di Gianotti-Crosti)[51][52].La reazione simile alla malattia da siero si verifica nel contesto dell'epatite B acuta e spesso precede l'insorgenza dell'ittero[53].Le caratteristiche cliniche sono febbre,rash cutaneoepoliarterite nodosa.I sintomi spesso regrediscono poco dopo la comparsa dell'ittero, ma possono persistere per tutta la fase acuta dell'infezione[54].Circa il 30-50% delle persone con vasculite necrotizzante acuta (poliarterite nodosa) sono portatori di HBV[55].La nefropatia associata all'HBV è stata descritta negli adulti ma è più comune nei bambini[56][57]mentre la glomerulonefrite membranosa è la forma più comune[54].Altri disturbi ematologici immuno-mediati, come lacrioglobulinemia mista essenzialee l'anemia aplasticasono stati individuati come parte delle manifestazioni extraepatiche dell'infezione da HBV, ma la loro correlazione non è stata ben definita, pertanto, probabilmente non dovrebbero essere consideratieziologicamentelegati all'infezione da HBV[54].
Diagnosi
modificaLa corretta diagnosi di epatite B può però essere fatta solo studiando il dosaggio deimarkervirali specifici. Le prove per la rilevazione di infezione da virus dell'epatite B prevedono analisi del siero o del sangue che rilevano entrambi gli antigeni virali (proteine prodotte dal virus) o anticorpi prodotti dal soggetto ospitante. L'interpretazione di questi test è complessa[34].
L'antigene di superficie dell'epatite B (HBsAg) è quello più usato per individuare la presenza dell'infezione, essendo il primo antigene virale ad apparire tra quelli rilevabili. Tuttavia, all'inizio di un'infezione, questo antigene può non essere presente e può essere rilevabile soltanto più tardi poiché eliminato dall'ospite. Ilvirioneinfettivo contiene al suo interno una "particella core" che racchiude ilgenomavirale. La particella coreicosaedricaè costituita da 180 o 240 copie della proteina del core, conosciuta comeantigene core dell'epatite Bo HBcAg. Durante questo periodo finestra, in cui l'ospite è infettivo ma sta combattendo con successo contro il virus, gli anticorpiIgMspecifici dell'antigene core (anti-HBc IgM) possono essere l'unica prova sierologica della malattia e pertanto la maggior parte dei test diagnostici per l'epatite B comprendono la conta degli HBsAg e degli anti-HBc (sia IgM che IgG)[58].
Poco dopo la comparsa di HBsAg, compare un altro antigene chiamato antigene "e" dell'epatite B (HBeAg). Di solito, la presenza di HBeAg nel siero di un ospite è associata a tassi molto più alti della replicazione virale e a una maggiore infettività, tuttavia esistono varianti del virus dell'epatite B che non producono l'antigene "e" e quindi questa regola non risulta sempre vera[59].Durante il corso naturale di un'infezione, l'HBeAg può essere eliminato e successivamente possono formarsi anticorpi contro l'antigene "e" (anti-HBe). Questa conversione è di solito associata con un drastico declino della replicazione virale[60].
Se il portatore è in grado di eliminare l'infezione, alla fine l'HBsAg diventa inosservabile e saranno invece presenti gli anticorpiIgGper l'antigene di superficie dell'epatite B e l'antigene core (anti-HBs e anti HBc IgG)[32].Il tempo intercorso tra la scomparsa dell'antigene HBsAg e la comparsa degli anticorpi anti-HBs è chiamato "periodo finestra". Una persona che risultasse negativa per HBsAg ma positiva per gli anti-HBs significherebbe che o ha superato un'infezione o è stata vaccinata in precedenza[61].
Le persone che rimangono HBsAg positivi per almeno sei mesi sono considerate portatori di epatite B.[62]I portatori del virus potrebbero avere l'epatite B cronica, che si riflette in elevati livelli serici dialanina aminotransferasi(ALT) e infiammazione al fegato, rilevabile con unabiopsia.I portatori che presentano sieroconversione HBeAg negativa, in particolare quelli che hanno acquisito l'infezione da adulti, hanno assai poca moltiplicazione virale e, quindi, possono essere a minor rischio di complicanze a lungo termine o di trasmettere l'infezione ad altri[63].
La tecnica dellareazione a catena della polimerasi(PCR) può essere utilizzata per rilevare e misurare la quantità di DNA del virus HBV, chiamata carica virale, in campioni clinici. Questi test sono usati per valutare lo stato infettivo di una persona e per monitorarne il trattamento[64].Gli individui con elevata carica virale tipicamente presentano "epatociti concitoplasmaa vetro smerigliato "evidenziati tramite l'analisi di unabiopsiaepatica[65].
Riassumendo, i marker virologici infettivi sono:[66][67][68]
- HBsAg: antigene Australia o di superficie, positivo al contatto colvirusanche nel periodo antecedente alla manifestazione dei segni e sintomi della malattia;
- HBsAb: anticorpi contro l'antigene di superficie prodotti dailinfociti B,positivo dopo la guarigione della malattia o nei soggettivaccinati;
- HBcAb: anticorpi contro l'antigene delcorevirale (HBcAg), può esistere di due diverse classi diimmunoglobuline:la classe IgM è dosabile in fase acuta mentre la classe IgG lo è per tutta la vita;
- HBeAg: antigene non corpuscolato del core virale; indica attività della malattia e della replicazione virale, è presente in fase acuta e in alcuni tipi di portatore cronico attivo;
- HBeAb: anticorpo contro l'antigene non corpuscolato del core virale, compare nell'epatite acuta quando comincia a risolversi; è presente anche nel portatore cronico sia attivo sia inattivo.
La tabella riassume la diagnosi in base alla presenza dei marker virologici nel siero:[66][67][68]
| HBsAg | anti-HBc IgM | anti-HBc IgG | HBV-DNA | HBeAg | anti-HBe | anti-HBs | |
|---|---|---|---|---|---|---|---|
| Epatite acuta | + | + | + | +/- | +/- | - | - |
| Termine dell'epatite acuta | - | + | + | - | - | + | + |
| Epatite cronica attiva | + | - | + | + | + | - | - |
| Portatore sano | + | - | + | - | - | + | - |
| Vaccinazione | - | - | - | - | - | - | + |
Trattamento
modificaL'infezione acuta da epatite B generalmente non richiede un trattamento poiché la maggior parte degli adulti è in grado di eliminare l'infezione spontaneamente[69].Il precoce trattamento antivirale può essere utile solo per meno dell'1% dei pazienti, il cui contagio avviene con un decorso molto aggressivo (epatite fulminante) oppure per soggettiimmunocompromessi.In caso di presunta infezione, il prima possibile e preferibilmente entro 24-72 ore si può eseguire una profilassi passiva con iniezioni di immunoglobuline anti-HBV ovvero anticorpi diretti contro il virus e cominciare la vaccinazione completa. D'altra parte, il trattamento dell'infezione cronica può rendersi necessario per ridurre il rischio di cirrosi e cancro al fegato. Gli individui con infezione cronica che presentano elevati valori dialanina transaminasi,unmarkerdi danno epatico, sono candidati alla terapia[70]. Nei pazienti che presentano elevata carica virale e malattia epatica grave il trattamento farmacologico è raccomandato anche se i livelli dialanina transaminasi(ALT) rientrano nella norma[71].
Anche se nessuno deifarmaciattualmente disponibili può eliminare l'infezione, alcuni possono bloccare la replicazione del virus, riducendo così al minimo i danni al fegato. Attualmente, ci sono sette farmaci autorizzati per il trattamento dell'infezione da virus dell'epatite B. Questi includono i farmaciantivirali:lamivudina(Epivir),adefovir-dipivoxil(Hepsera),tenofovir(Viread), latelbivudina(Sebivo),entecavir(Baraclude) e i modulatori del sistema immunitariointerferone α-2aepeginterferone α-2a(Pegasys). L'uso di interferone, che richiede iniezioni giornaliere o almeno di tre volte alla settimana, è stato soppiantato dall'azione prolungata dell'interferone pegilato che viene iniettato una sola volta alla settimana[72].Tuttavia, alcuni individui risultano essere molto più propensi a rispondere rispetto ad altri alla terapia e questo potrebbe essere dovuto al diverso genotipo del virus o alla storia del paziente. Il trattamento riduce significativamente la replicazione virale nel fegato e riduce così la quantità di particelle virali misurate nel sangue[73].
I bambini nati da madri malate di epatite B possono essere trattati con anticorpi del virus dell'epatite B (HBIg). Se gli anticorpi vengono somministrati entro dodici ore dalla nascita, il rischio di contrarre l'epatite B viene ridotta del 90%[74].La terapia consente inoltre a una madre di allattare il suo bambino in modo sicuro.
Nel luglio 2005, alcuni ricercatori hanno identificato un'associazione tra una proteina che lega il DNA e la capacità di replicazione dell'HBV nel fegato. Il controllo del livello di produzione di questa proteina potrebbe essere utilizzato per il trattamento dell'infezione[75].
Il trattamento dura da 6 mesi a un anno, a seconda del farmaco e del genotipo del virus[76].
Prognosi
modificano dati
<10
10–20
20–40
40–60
60–80
80–100
100–125
125–150
150–200
200–250
250–500
>500
L'infezione da virus dell'epatite B può essere acuta o cronica. I pazienti con infezione acuta possono eliminare il virus spontaneamente nel giro di settimane o mesi.[77]
I bambini hanno meno probabilità degli adulti di eliminare l'infezione. Più del 95% delle persone che si infettano da adulti sono in grado di guarire completamente e sviluppare l'immunità al virus. Questo dato, tuttavia, scende al 30% per i bambini più piccoli e solo il 5% dei neonati che acquisiscono l'infezione dalla madre al momento della nascita sono in grado di eliminare l'infezione[78].Questi presenteranno un rischio del 40% di morte, di sviluppare cirrosi o carcinoma epatocellulare[72].Il 70% dei bambini di età compresa tra uno e sei anni infetti riuscirà ad eliminare il virus.[79]
L'epatite D(HDV) può avvenire solo in concomitanza con l'infezione da epatite B, poiché l'HDV utilizza l'antigene di superficie dell'HBV per formare ilcapside[80].La co-infezione con virus dell'epatite D aumenta il rischio di cirrosi epatica e tumore del fegato[81].Lapoliarterite nodosarisulta essere più comune nelle persone con infezione da epatite B.
Riassumendo, l'infezione da virus dell'epatite B evolve in quattro situazioni correlate con la risposta immunitaria del soggetto infetto:[77][82]
- Decorso acuto (ma spesso asintomatico) con completo recupero e acquisizione della immunità dall'infezione (89% dei casi);
- Epatite fulminante con mortalità del 90%: può richiedere iltrapianto di fegato(1% dei casi);
- Infezione cronica: persistenza del virus nell'organismo con danno epatico (5-10% dei casi); in questo caso la malattia ha un andamento cronico e può compromettere la funzionalità epatica nel giro di 10-30 anni con l'insorgenza dicirrosi epaticao di carcinoma epatocellulare primitivo (di solito dopo che è già presente la cirrosi);
- Stato di portatore inattivo (5% dei casi): il virus persiste nel fegato ma non provoca danno epatico; può rimanere in questo stato anche tutta la vita, senza arrecare danni nemmeno a lungo termine. Risulta essere poco contagioso.
Cirrosi
modificaSono disponibili diversi test per determinare il grado di cirrosi. L'elastografia epatica(FibroScan) è il test preferito ma è particolarmente costoso[83].L'aspartato aminotransferasi rispetto all'indice del rapporto piastrinico può essere utilizzato quando il costo da affrontare risulta un problema[83].
Riattivazione
modificaIlDNAdel virus dell'epatite B rimane nell'organismo dopo l'infezione e, in alcune persone, comprese quelle che non hanno quantitativi rilevabili di HBsAg, la malattia può ripresentarsi[84][85].Sebbene sia un evento raro, la riattivazione si osserva più spesso nel caso di uso di alcol o didroghe,[86]o in individui con ridotta immunità[87].L'HBV attraversa cicli direplicazionee non replicazione e circa il 50% dei portatori conclamati sperimenta una riattivazione acuta. I maschi conalanina transaminasi(ALT) basale di 200 UL/L hanno una probabilità tre volte maggiore di sviluppare una riattivazione rispetto a coloro che presentano livelli inferiori. Sebbene la riattivazione possa avvenire spontaneamente,[88]le persone che si sottopongono achemioterapiahanno un rischio maggiore[89].I farmaci immunosoppressori favoriscono un aumento della replicazione dell'HBV mentre inibiscono la funzione deilinfociti T citotossicinel fegato[90].Il rischio di riattivazione varia anche a seconda del profilo sierologico: coloro che hanno quantitativi di HBsAg rilevabile nel sangue presentano un maggior rischio, ma anche colore con solo anticorpi contro l'antigene core sono a rischio. La presenza di anticorpi contro l'antigene di superficie, che sono considerati unmarkerdi immunità, non preclude la riattivazione[89].Il trattamento diprofilassiconfarmaci antiviralipuò prevenire la gravemorbilitàassociata alla riattivazione della malattia da HBV[89].
Postumi e follow up
modificaPoiché l'epatite B cronica è una malattia a rischio di complicanze sul lungo periodo (fibrosi,cirrosiecarcinoma epatico), i pazienti devono essere costantemente monitorati per seguire l'evoluzione della malattia. Inoltre, la presenza di malattie del fegato di origine alcolica, autoimmunitaria, o metabolica, può indurre un peggioramento del quadro clinico del paziente. L'ecografiadel fegato permette di evidenziare la formazione di eventuali lesioni sospette riconducibili atumore epatico.A differenza infatti di quanto si verifica in caso diepatite C,il carcinoma epatico da virus dell'epatite B si può manifestare anche in un fegato senza cirrosi[71]:il motivo è che HBV produce la proteina X, che ha un'azione cancerogena diretta sul fegato, a prescindere dallo sviluppo di cirrosi epatica[91].
Prevenzione
modificaA differenza dell'epatite A,l'epatite B non è generalmente diffusa attraverso acqua e cibo. Invece essa si trasmette attraverso i fluidi del corpo. La prevenzione è quindi focalizzata a evitare questo tipo di trasmissione: rapporti sessuali non protetti, trasfusioni di sangue, riutilizzo di aghi contaminati e trasmissione verticale durante il parto, sono alcune delle situazioni più a rischio. I neonati possono essere vaccinati alla nascita[92].
Vaccino
modificaPer la prevenzione dell'infezione da virus dell'epatite B sono stati sviluppati diversi vaccini a partire dagli anni 1980. Questi si basano sull'uso di una delle proteine dell'involucro del virus (antigene di superficie dell'epatite Bo HBsAg). Il vaccino è stato originariamente ottenuto dalplasmadi pazienti che avevano contratto da lungo tempo l'infezione da virus dell'epatite B. Tuttavia, dal 1996, viene realizzato grazie a una tecnologia di sintesi delDNA ricombinanteche non contiene derivati del sangue. Non si può essere infettati con il virus dell'epatite B da questo vaccino[93].Il vaccino contro l'epatite B è stato il primo vaccino considerato in grado di prevenire il cancro, in particolare quello del fegato[94].
La maggior parte dei vaccini viene somministrata in tre dosi nell'arco di giorni. Una risposta protettiva al vaccino è definita come una concentrazione di anticorpi anti-HBs di almeno 10 mUI/ml nel siero del ricevente. Il vaccino risulta essere più efficace nei bambini e nel 95% di coloro che si sono vaccinati si rilevano livelli protettivi di anticorpi. Il dato scende a circa il 90% a 40 anni di età e a circa il 75% in coloro che hanno più di 60 anni. La protezione offerta dalla vaccinazione è di lunga durata, perdurando anche dopo che i livelli di anticorpi scendono al di sotto dei 10 mUI/ml. Per i neonati di madri HBsAg-positive il solo vaccino per l'epatite B, la sola immunoglobulina per l'epatite B o la combinazione dei due, prevengono l'insorgenza della malattia[95].Inoltre, l'efficacia della combinazione di vaccino più immunoglobuline per l'epatite B è superiore al vaccino da solo[95].Questa combinazione impedisce la trasmissione dell'HBV al momento della nascita nell'86%-99% dei casi[96].
IlTenofovirsomministrato nel secondo o terzo trimestre può ridurre del 77% il rischio di trasmissione da madre a figlio se combinato con l'immunoglobulina dell'epatite B e il vaccino contro l'epatite B, soprattutto per le donne in gravidanza con livelli elevati di DNA virale[97].Tuttavia, non vi sono prove sufficienti a sostegno che la sola somministrazione di immunoglobuline durante la gravidanza possa ridurre le probabilità di trasmissione al neonato[98].Al 2021 non è stato ancora condotto alcuno studio di controllo randomizzato per valutare gli effetti del vaccino contro l'epatite B durante la gravidanza per prevenire l'infezione infantile[99].
Tutti coloro che sono a rischio di esposizione a fluidi corporei, come il sangue, dovrebbero essere vaccinati contro l'epatite B[100].Si raccomanda di eseguire test per verificare l'efficacia dell'immunizzazione e di somministrare ulteriori dosi di vaccino a coloro che non risultano sufficientemente immunizzati[100].
Negli studi difollow-upa 10-22 anni non si sono riscontrati casi di epatite B tra i soggetti vaccinati con un sistema immunitario normale. Sono state documentate solo rare infezioni croniche[101].La vaccinazione è particolarmente raccomandata per i gruppi ad alto rischio, tra cui: operatori sanitari, persone coninsufficienza renale cronicae uomini che hanno rapporti sessuali con uomini[102][103][104].
Entrambi i tipi di vaccino contro l'epatite B, il vaccino plasma-derivato (PDV) e il vaccino ricombinante (RV) hanno dimostrato un'efficacia simile nel prevenire l'infezione sia negli operatori sanitari che nei gruppi di insufficienza renale cronica[102].Nel gruppo degli operatori sanitari è stata trovata un'unica differenza relativamente alla via di somministrazione, con quella intramuscolare dimostratasi significativamente più efficace rispetto a quella intradermica[102].
Altro
modificaNellaprocreazione assistita,illavaggio dello spermanon è sufficiente per i maschi con epatite B per prevenire la trasmissione a meno che lapartnerfemminile non sia stata vaccinata in modo efficace[105].Nelle femmine con epatite B, il rischio di trasmissione da madre a figlio confecondazione in vitronon è diverso da quello riscontrabile nel concepimento spontaneo[105].
Coloro che presentano un alto rischio di essere infetti dovrebbero essere sottoposti a test[106].Loscreeningviene raccomandato a coloro che non sono stati vaccinati e che siano: persone provenienti da aree geografiche in cui l'epatite B si verifica in più del 2% della popolazione, persone conHIV,tossicodipendentiche assumono stupefacenti per via endovenosa, uomini che hanno rapportiomosessualinon protetti e coloro che vivono con qualcuno con la malattia[106].Negli Stati Uniti è raccomandato loscreeningdurante la gravidanza[107].
Note
modifica- ^Barker LF,et al.,Transmission of serum hepatitis. 1970,inJournal of the American Medical Association,vol. 276, n. 10, 1996, pp. 841–844,DOI:10.1001/jama.276.10.841,PMID8769597.
- ^Williams R,Global challenges in liver disease,inHepatology (Baltimore, Md.),vol. 44, n. 3, 2006, pp. 521–526,DOI:10.1002/hep.21347,PMID16941687.
- ^abcdeHepatitis B,suwho.int,World Health Organization.URL consultato il 24 aprile 2014(archiviatoil 17 ottobre 2019).
- ^FAQ about Hepatitis B,suliver.stanford.edu,Stanford School of Medicine, 10 luglio 2008.URL consultato il 19 settembre 2009(archiviato dall'url originaleil 9 febbraio 2009).
- ^Kidd-Ljunggren K, Holmberg A, Bläckberg J, Lindqvist B,High levels of hepatitis B virus DNA in bodynm fluids from chronic carriers,inThe Journal of Hospital Infection,vol. 64, n. 4, dicembre 2006, pp. 352–7,DOI:10.1016/j.jhin.2006.06.029,PMID17046105.
- ^Hepatitis B,suncbi.nlm.nih.gov,National Institute of Health.URL consultato il 23 novembre 2010(archiviatoil 6 febbraio 2011).
- ^Chang M,Hepatitis B virus infection,inSemin Fetal Neonatal Med,vol. 12, n. 3, giugno 2007, pp. 160–167,DOI:10.1016/j.siny.2007.01.013,PMID17336170.
- ^Pungpapong S, Kim WR, Poterucha JJ,Natural History of Hepatitis B Virus Infection: an Update for Clinicians,inMayo Clinic Proceedings,vol. 82, n. 8, agosto 2007, p. 967,DOI:10.4065/82.8.967,PMID17673066.
- ^( "All infants should receive their first dose of hepatitis B vaccine as soon as possible after birth, preferably within 24 hours" -WHO Hepatitis B Vaccines Position Paper(PDF)(archiviato dall'url originaleil 2 dicembre 2015).)
- ^(EN)World Health Organization - Hepatitis B Vaccines Position Paper(PDF), suwho.int.URL consultato il 24 aprile 2014(archiviatoil 2 dicembre 2015).
- ^Mühlemann B, Jones TC, Damgaard PB, Allentoft ME, Shevnina I, Logvin A, Usmanova E, Panyushkina IP, Boldgiv B, Bazartseren T, Tashbaeva K, Merz V, Lau N, Smrčka V, Voyakin D, Kitov E, Epimakhov A, Pokutta D, Vicze M, Price TD, Moiseyev V, Hansen AJ, Orlando L, Rasmussen S, Sikora M, Vinner L, Osterhaus AD, Smith DJ, Glebe D, Fouchier RA, Drosten C, Sjögren KG, Kristiansen K, Willerslev E,Ancient hepatitis B viruses from the Bronze Age to the Medieval period,inNature,vol. 557, n. 7705, maggio 2018, pp. 418–423,Bibcode:2018Natur.557..418M,DOI:10.1038/s41586-018-0097-z,PMID29743673.URL consultato il 6 ottobre 2021(archiviatoil 22 luglio 2021).
- ^abcdeBen Guarino,New strains of hepatitis B virus discovered in ancient human remains,inThe Washington Post,9 maggio 2018.URL consultato il 9 gennaio 2018(archiviatoil 5 luglio 2018).
- ^(DE) Lurman A,Eine icterus epidemic,inBerl Klin Woschenschr,vol. 22, 1885, pp. 20–3.
- ^Jane Davis,Molecular Epidemiology of Hepatitis B in the Indigenous People of Northern Australia,inJournal of Gastroenterology and Hepatology,2013 July, n. 7, 2013, pp. 1234–41,DOI:10.1111/jgh.12177,PMID23432545.
- ^Wolfram Gerlich,Medical Virology of Hepatitis B: how it began and where we are now,inVirology Journal,2013, 10, 2013, p. 239,DOI:10.1186/1743-422X-10-239,PMC3729363,PMID23870415.
- ^Dimitrios Paraskevis,Dating the Origin and Dispersal of Hepatitis B Virus Infection in Humans and Primates,inHepatology,vol. 2013, n. 3, 2013, pp. 908–16,DOI:10.1002/hep.26079,PMID22987324.
- ^(DE) Lürman A.,Eine icterus epidemic,inBerl Klin Wochenschr.,vol. 22, 1885, pp. 20–3.
- ^Alter H, Blumberg BS,Further studies on a "new" human isoprecipitin system (Australia antigen),inBlood,vol. 27, n. 3, 1966, pp. 297–309,PMID5930797.
- ^MacCallum, F.O.,Homologous serum hepatitis,inLancet,vol. 2, 1947, p. 691.
- ^Galibert F, Mandart E, Fitoussi F, Tiollais P, Charnay P,Nucleotide sequence of the hepatitis B virus genome (subtype ayw) cloned in E. Coli,inNature,vol. 281, n. 5733, 1979, p. 646,Bibcode:1979Natur.281..646G,DOI:10.1038/281646a0,PMID399327.
- ^Hepatitis B vaccine,inLancet,vol. 2, n. 8206, 6 dicembre 1980, pp. 1229–1230,PMID6108398.
- ^Hepatitis B incidence rate,suOur World in Data.URL consultato il 5 marzo 2020(archiviatoil 26 settembre 2019).
- ^(EN)World Health Organization - Epatite B,suwho.int.URL consultato il 4 giugno 2011(archiviatoil 19 maggio 2011).
- ^Custer B, Sullivan S, Hazlet T, Kowdley U, Veenstra D, Iloeje K,Global epidemiology of hepatitis B virus,inJournal of Clinical Gastroenterology,vol. 38, 10 Suppl 3, novembre-dicembre 2004, pp. S158–S168,DOI:10.1097/00004836-200411003-00008,PMID15602165.
- ^Redd J, Baumbach J, Kohn W, Nainan O, Khristova M, Williams I,Patient-to-patient transmission of hepatitis B virus associated with oral surgery,inThe Journal of infectious diseases,vol. 195, n. 9, 1º maggio 2007, pp. 1311–1314,DOI:10.1086/513435,PMID17397000.
- ^Alter M,Epidemiology and prevention of hepatitis B,inSeminars in liver disease,vol. 23, n. 1, febbraio 2003, pp. 39–46,DOI:10.1055/s-2003-37583,PMID12616449.
- ^(EN)Healthcare stumbling in RI's Hepatitis fight,inThe Jakarta Post,13 gennaio 2011(archiviato dall'url originaleil 4 marzo 2016).
- ^Gaeta GB, Stornaiuolo G, Precone DF,Type B and D viral hepatitis: epidemiological changes in Southern Europe,PMID11948358.
- ^Marcelo El Khouri e Vera Aparecida dos Santos,Hepatis B: epidemiological, immunological and serological considerations emphasizing mutation,PMID15361988.
- ^Hadziyannis SJ, Papatheodoridis GV, Vassilopoulos D,Precore mutant chronic hepatitis B - approach to management,ottobre 2003,PMID14745348.
- ^abLocarnini S,Molecular virology of hepatitis B virus,inSeminars in liver disease,24 Suppl 1, 2004, pp. 3–10,DOI:10.1055/s-2004-828672,PMID15192795.
- ^abZuckerman AJ,Hepatitis Viruses. In:Baron's Medical Microbiology(Baron S.et al.,eds.),4th, Univ of Texas Medical Branch, 1996,ISBN0-9631172-1-1.URL consultato il 1º maggio 2019(archiviatoil 14 luglio 2009).
- ^Kramvis A, Kew M, François G,Hepatitis B virus genotypes,inVaccine,vol. 23, n. 19, 31 marzo 2005, pp. 2409–2423,DOI:10.1016/j.vaccine.2004.10.045,PMID15752827.
- ^abBonino F, Chiaberge E, Maran E, Piantino P,Serological markers of HBV infectivity,inAnnali dell'Istituto superiore di sanità,vol. 24, n. 2, 1987, pp. 217–223,PMID3331068.
- ^Shuping Tong, Jisu Li, Jack R. Wands,Carboxypeptidase D Is an Avian Hepatitis B Virus Receptor[collegamento interrotto],inJournal of Virology,vol. 73, n. 10, ottobre 1999, pp. 8696–8702,PMC112890,PMID10482623.URL consultato il 19 settembre 2009.
- ^Glebe D, Urban S,Viral and cellular determinants involved in hepadnaviral entry,inWorld Journal of Gastroenterology,vol. 13, n. 1, 7 gennaio 2007, pp. 22–38,PMID17206752.URL consultato il 3 giugno 2011(archiviatoil 9 settembre 2011).
- ^Coffin CS, Mulrooney-Cousins PM, van Marle G, Roberts JP, Michalak TI, Terrault NA,Hepatitis B virus (HBV) quasispecies in hepatic and extrahepatic viral reservoirs in liver transplant recipients on prophylactic therapy,inLiver Transpl,aprile 2011, pp. n/a–n/a,DOI:10.1002/lt.22312,PMID21462295.
- ^Iannacone M,et al,Platelets mediate cytotoxic T lymphocyte-induced liver damage,inNature medicine,vol. 11, n. 11, novembre 2005, pp. 1167–1169,DOI:10.1038/nm1317,PMC2908083,PMID16258538.URL consultato il 1º maggio 2019(archiviatoil 10 maggio 2017).
- ^(EN)Hepatitis B - the facts,suideas.health.vic.gov.au,Department of Health, Victoria, Australia.URL consultato il 3 aprile 2012(archiviatoil 18 settembre 2011).
- ^Petersen N,et al,Hepatitis B surface antigen in saliva, impetiginous lesions, and the environment in two remote Alaskan villages,inApplied and environmental microbiology,vol. 32, n. 4, ottobre 1976, pp. 572–574,PMC170308,PMID791124.
- ^Hepatitis B – the facts: IDEAS – Victorian Government Health Information, Australia,suhealth.vic.gov.au,State of Victoria, 28 luglio 2009.URL consultato il 19 settembre 2009(archiviato dall'url originaleil 28 febbraio 2009).
- ^Shapiro CN,Epidemiology of hepatitis B,inThe Pediatric infectious disease journal,vol. 12, n. 5, maggio 1993, pp. 433–437,DOI:10.1097/00006454-199305000-00036,PMID8392167.
- ^levaccinazioni.it.URL consultato il 4 giugno 2011(archiviato dall'url originaleil 28 luglio 2012).
- ^Epatite B,suavismontenero.it.URL consultato il 4 giugno 2011(archiviatoil 23 marzo 2013).
- ^Epac - Epatite B,Significato dei vari componenti di HBV,suepatiteb.com.URL consultato il 26 maggio 2022.
- ^Villari D, Pollicino T, Spinella S, Russo F, Campo S, Rodino G, Squadrito G, Longo G, Raimondo G,Hepatitis B E antigen detection in formalin-fixed liver biopsy specimens. A tool to investigate wild-type and E-minus variant HBV infection,inAm J Clin Pathol,vol. 103, n. 2, febbraio 1995, pp. 136–40,DOI:10.1093/ajcp/103.2.136,PMID7856554.
- ^Terrault N, Roche B, Samuel D,Management of the hepatitis B virus in the liver transplantation setting: a European and an American perspective,inLiver Transplant.,vol. 11, n. 7, luglio 2005, pp. 716–32,DOI:10.1002/lt.20492,PMID15973718.
- ^El-Serag HB, Rudolph KL,Hepatocellular carcinoma: epidemiology and molecular carcinogenesis,inGastroenterology,vol. 132, n. 7, giugno 2007, pp. 2557–76,DOI:10.1053/j.gastro.2007.04.061,PMID17570226.
- ^El-Serag HB,Hepatocellular carcinoma,inNew England Journal of Medicine,vol. 365, n. 12, 22 settembre 2011, pp. 1118–27,DOI:10.1056/NEJMra1001683,PMID21992124.
- ^Gan SI, Devlin SM, Scott-Douglas NW, Burak KW,Lamivudine for the treatment of membranous glomerulopathy secondary to chronic hepatitis B infection,inCanadian Journal of Gastroenterology,vol. 19, n. 10, ottobre 2005, pp. 625–9,DOI:10.1155/2005/378587,PMID16247526.
- ^Dienstag JL,Hepatitis B as an immune complex disease,inSeminars in Liver Disease,vol. 1, n. 1, febbraio 1981, pp. 45–57,DOI:10.1055/s-2008-1063929,PMID6126007.
- ^Trepo C, Guillevin L,Polyarteritis nodosa and extrahepatic manifestations of HBV infection: the case against autoimmune intervention in pathogenesis,inJournal of Autoimmunity,vol. 16, n. 3, maggio 2001, pp. 269–74,DOI:10.1006/jaut.2000.0502,PMID11334492.
- ^Alpert E, Isselbacher KJ, Schur PH,The pathogenesis of arthritis associated with viral hepatitis. Complement-component studies,inThe New England Journal of Medicine,vol. 285, n. 4, luglio 1971, pp. 185–9,DOI:10.1056/NEJM197107222850401,PMID4996611.
- ^abcLiang TJ,Hepatitis B: the virus and disease,inHepatology,vol. 49, 5 Suppl, maggio 2009, pp. S13–21,DOI:10.1002/hep.22881,PMC2809016,PMID19399811.
- ^Gocke DJ, Hsu K, Morgan C, Bombardieri S, Lockshin M, Christian CL,Association between polyarteritis and Australia antigen,inLancet,vol. 2, n. 7684, dicembre 1970, pp. 1149–53,DOI:10.1016/S0140-6736(70)90339-9,PMID4098431.
- ^Lai KN, Li PK, Lui SF, Au TC, Tam JS, Tong KL, Lai FM,Membranous nephropathy related to hepatitis B virus in adults,inThe New England Journal of Medicine,vol. 324, n. 21, maggio 1991, pp. 1457–63,DOI:10.1056/NEJM199105233242103,PMID2023605.
- ^Takekoshi Y, Tanaka M, Shida N, Satake Y, Saheki Y, Matsumoto S,Strong association between membranous nephropathy and hepatitis-B surface antigenaemia in Japanese children,inLancet,vol. 2, n. 8099, novembre 1978, pp. 1065–8,DOI:10.1016/S0140-6736(78)91801-9,PMID82085.URL consultato il 5 ottobre 2021(archiviatoil 28 agosto 2021).
- ^Karayiannis P, Thomas HC,Desk Encyclopedia of Human and Medical Virology,Boston, Academic Press, 2009, p.110.,ISBN978-0-12-375147-8.
- ^Liaw YF, Brunetto MR, Hadziyannis S,The natural history of chronic HBV infection and geographical differences,inAntiviral Therapy,vol. 15, 2010, pp. 25–33,DOI:10.3851/IMP1621,PMID21041901.URL consultato il 28 novembre 2021(archiviatoil 24 giugno 2021).
- ^(EN) Mayo CLinic,Hepatitis B e Antigen and Hepatitis B e Antibody, Serum,sumayocliniclabs.com.URL consultato il 28 novembre 2021(archiviatoil 28 novembre 2021).
- ^Keechilot CS, Shenoy V, Kumar A, Biswas L, Vijayrajratnam S, Dinesh K, Nair P,Detection of occult hepatitis B and window period infection among blood donors by individual donation nucleic acid testing in a tertiary care center in South India,inPathog Glob Health,vol. 110, n. 7-8, 2016, pp. 287–291,DOI:10.1080/20477724.2016.1248171,PMC5189866,PMID27788631.
- ^Lok AS, Mcmahon BJ,Chronic hepatitis B,inHepatology (Baltimore, Md.),vol. 45, n. 2, febbraio 2007, pp. 507–539,DOI:10.1002/hep.21513,PMID17256718.
- ^Chu CM, Liaw YF,Predictive factors for reactivation of hepatitis B following hepatitis B e antigen seroconversion in chronic hepatitis B,inGastroenterology,vol. 133, n. 5, novembre 2007, pp. 1458–1465,DOI:10.1053/j.gastro.2007.08.039,PMID17935720.
- ^Zoulim F,New nucleic acid diagnostic tests in viral hepatitis,inSeminars in liver disease,vol. 26, n. 4, novembre 2006, pp. 309–317,DOI:10.1055/s-2006-951602,PMID17051445.
- ^Cohen C,"Ground-glass" hepatocytes,inS Afr Med J,vol. 49, n. 34, agosto 1975, pp. 1401–3,PMID1162516.
- ^ab(EN) Vanessa Towell e Benjamin Cowieeditore=Australian Family Physician,Hepatitis B serology,suracgp.org.au.URL consultato il 28 novembre 2021(archiviatoil 13 novembre 2021).
- ^ab(EN)Centers for Disease Control and Prevention,Interpretation of Hepatitis B Serologic Test Results(PDF), sucdc.gov.URL consultato il 28 novembre 2021(archiviatoil 2 novembre 2021).
- ^abSonal Kumar,Epatite B, acuta,sumsdmanuals.com.URL consultato il 28 novembre 2021(archiviatoil 28 novembre 2021).
- ^Hollinger FB, Lau DT,Hepatitis B: the pathway to recovery through treatment,inGastroenterology Clinics of North America,vol. 35, n. 4, dicembre 2006, pp. 895–931,DOI:10.1016/j.gtc.2006.10.002,PMID17129820.
- ^Lai CL, Yuen MF,The natural history and treatment of chronic hepatitis B: a critical evaluation of standard treatment criteria and end points,inAnnals of Internal Medicine,vol. 147, n. 1, luglio 2007, pp. 58–61,DOI:10.7326/0003-4819-147-1-200707030-00010,PMID17606962.
- ^abPharmamedix: Epatite Bhttp://www.pharmamedix.com/patologiavoce.php?pat=Epatite+B&vo=AvvertenzeArchiviatoil 10 maggio 2013 inInternet Archive.
- ^abDienstag JL,Hepatitis B virus infection,inThe New England journal of medicine,vol. 359, n. 14, 2008, pp. 1486–1500,DOI:10.1056/NEJMra0801644,PMID18832247.URL consultato il 4 giugno 2011(archiviatoil 1º febbraio 2010).
- ^Pramoolsinsup C,Management of viral hepatitis B,inJournal of Gastroenterology and Hepatology,17 Suppl, febbraio 2002, pp. S125–45,DOI:10.1046/j.1440-1746.17.s1.3.x,PMID12000599.
- ^Libbus MK, Phillips LM,Public health management of perinatal hepatitis B virus[collegamento interrotto],inPublic Health Nursing (Boston, Mass.),vol. 26, n. 4, luglio-agosto 2009, pp. 353–61,DOI:10.1111/j.1525-1446.2009.00790.x,PMID19573214.
- ^Ng LF, Chan M, Chan SH, Cheng PC, Leung EH, Chen WN, Ren EC,Host heterogeneous ribonucleoprotein K (hnRNP K) as a potential target to suppress hepatitis B virus replication,inPLos medicine,vol. 2, n. 7, luglio 2005, pp. e163,DOI:10.1371/journal.pmed.0020163,ISSN1549-1277,PMC1181871,PMID16033304.
- ^(EN)Hepatitis B Foundation: Approved Drugs for Adults,suhepb.org.URL consultato il 4 giugno 2011(archiviato dall'url originaleil 7 luglio 2011).
- ^abMinistero della Salute,Epatite B,susalute.gov.it.URL consultato il 28 novembre 2021(archiviatoil 28 novembre 2021).
- ^Bell SJ, Nguyen T,The management of hepatitis B,inAust Prescr,vol. 23, n. 4, 2009, pp. 99–104(archiviato dall'url originaleil 10 maggio 2011).
- ^Kerkar N,Hepatitis B in children: complexities in management,inPediatric Transplantation,vol. 9, n. 5, 2005, pp. 685–691,DOI:10.1111/j.1399-3046.2005.00393.x,PMID16176431.
- ^Taylor J,Hepatitis delta virus,inVirology,vol. 344, n. 1, 2006, pp. 71–76,DOI:10.1016/j.virol.2005.09.033,PMID16364738.
- ^Olivieri F, Brunetto MR, Bonino G, Actis GC,Pathobiology of chronic hepatitis virus infection and hepatocellular carcinoma (HCC),inThe Italian journal of gastroenterology,vol. 23, n. 8, 1991, pp. 498–502,PMID1661197.
- ^Prométhée,Epatiti B e C(PDF), supromethee-hepatites.org.URL consultato il 28 novembre 2021(archiviatoil 28 novembre 2021).
- ^abGUIDELINES FOR THE PREVENTION, CARE AND TREATMENT OF PERSONS WITH CHRONIC HEPATITIS B INFECTION,World Health Organization, Mar 2015,ISBN978924154905-9.URL consultato il 6 dicembre 2021(archiviatoil 19 marzo 2015).
- ^Peters MG,Hepatitis B Virus Infection: What Is Current and New,inTopics in Antiviral Medicine,vol. 26, n. 4, gennaio 2019, pp. 112–116,PMC6372357,PMID30641484.
- ^Vierling JM,The immunology of hepatitis B,inClin Liver Dis,vol. 11, n. 4, novembre 2007, pp. 727–759, vii–759,DOI:10.1016/j.cld.2007.08.001,PMID17981227.
- ^Villa E, Fattovich G, Mauro A, Pasino M,Natural history of chronic HBV infection: special emphasis on the prognostic implications of the inactive carrier state versus chronic hepatitis,inDigestive and Liver Disease,vol. 43, Suppl 1, gennaio 2011, pp. S8–14,DOI:10.1016/S1590-8658(10)60686-X,PMID21195374.
- ^Katz LH, Fraser A, Gafter-Gvili A, Leibovici L, Tur-Kaspa R,Lamivudine prevents reactivation of hepatitis B and reduces mortality in immunosuppressed patients: systematic review and meta-analysis,inJ. Viral Hepat.,vol. 15, n. 2, febbraio 2008, pp. 89–102,DOI:10.1111/j.1365-2893.2007.00902.x,PMID18184191.
- ^Roche B, Samuel D,The difficulties of managing severe hepatitis B virus reactivation,inLiver International,vol. 31, Suppl 1, gennaio 2011, pp. 104–10,DOI:10.1111/j.1478-3231.2010.02396.x,PMID21205146.
- ^abcMastroianni CM, Lichtner M, Citton R, Del Borgo C, Rago A, Martini H, Cimino G, Vullo V,Current trends in management of hepatitis B virus reactivation in the biologic therapy era,inWorld Journal of Gastroenterology,vol. 17, n. 34, settembre 2011, pp. 3881–7,DOI:10.3748/wjg.v17.i34.3881,PMC3198017,PMID22025876.
- ^Maurizio, MD Bonacini,Hepatitis B Reactivation,susurgery.usc.edu,University of Southern California Department of Surgery.URL consultato il 24 gennaio 2009(archiviato dall'url originaleil 27 novembre 2008).
- ^S. Liu, SS. Koh; CG. Lee,Hepatitis B Virus X Protein and Hepatocarcinogenesis.,inInt J Mol Sci,vol. 17, n. 6, 2016,DOI:10.3390/ijms17060940,PMID27314335.
- ^John O'Connor,Hepatitis B Prevention – The Body,suthebody.com,Body Health Resources Corporation, 3 ottobre 2008.URL consultato il 30 gennaio 2009(archiviatol'8 febbraio 2009).
- ^Hepatitis B Vaccine,suhepb.org,Doylestown, Pennsylvania, Hepatitis B Foundation, 31 gennaio 2009.URL consultato il 13 marzo 2010(archiviato dall'url originaleil 13 marzo 2010).
- ^Chan SL, Wong VW, Qin S, Chan HL,Infection and Cancer: The Case of Hepatitis B,inJournal of Clinical Oncology,vol. 34, n. 1, gennaio 2016, pp. 83–90,DOI:10.1200/JCO.2015.61.5724,PMID26578611.
- ^abLee C, Gong Y, Brok J, Boxall EH, Gluud C,Hepatitis B immunisation for newborn infants of hepatitis B surface antigen-positive mothers,inThe Cochrane Database of Systematic Reviews,n. 2, aprile 2006, pp. CD004790,DOI:10.1002/14651858.CD004790.pub2,PMID16625613.
- ^Wong F, Pai R, Van Schalkwyk J, Yoshida EM,Hepatitis B in pregnancy: a concise review of neonatal vertical transmission and antiviral prophylaxis,inAnnals of Hepatology,vol. 13, n. 2, 2014, pp. 187–95,DOI:10.1016/S1665-2681(19)30881-6,PMID24552860.
- ^Hyun MH, Lee YS, Kim JH, Je JH, Yoo YJ, Yeon JE, Byun KS,Systematic review with meta-analysis: the efficacy and safety of tenofovir to prevent mother-to-child transmission of hepatitis B virus,inAlimentary Pharmacology & Therapeutics,vol. 45, n. 12, giugno 2017, pp. 1493–1505,DOI:10.1111/apt.14068,PMID28436552.
- ^Eke AC, Eleje GU, Eke UA, Xia Y, Liu J,Hepatitis B immunoglobulin during pregnancy for prevention of mother-to-child transmission of hepatitis B virus,inThe Cochrane Database of Systematic Reviews,vol. 2, febbraio 2017, pp. CD008545,DOI:10.1002/14651858.CD008545.pub2,PMC6464495,PMID28188612.
- ^Sangkomkamhang US, Lumbiganon P, Laopaiboon M,Hepatitis B vaccination during pregnancy for preventing infant infection,inThe Cochrane Database of Systematic Reviews,n. 11, novembre 2014, pp. CD007879,DOI:10.1002/14651858.CD007879.pub3,PMC7185858,PMID25385500.
- ^abSchillie S, Murphy TV, Sawyer M, Ly K, Hughes E, Jiles R, de Perio MA, Reilly M, Byrd K, Ward JW,CDC guidance for evaluating health-care personnel for hepatitis B virus protection and for administering postexposure management,inMMWR. Recommendations and Reports,vol. 62, RR-10, dicembre 2013, pp. 1–19,PMID24352112(archiviato dall'url originaleil 19 giugno 2017).
- ^Shepard CW, Simard EP, Finelli L, Fiore AE, Bell BP,Hepatitis B virus infection: epidemiology and vaccination,inEpidemiologic Reviews,vol. 28, 2006, pp. 112–25,DOI:10.1093/epirev/mxj009,PMID16754644.
- ^abcChen W, Gluud C,Vaccines for preventing hepatitis B in health-care workers,inThe Cochrane Database of Systematic Reviews,n. 4, ottobre 2005, pp. CD000100,DOI:10.1002/14651858.CD000100.pub3,PMID16235273.
- ^Schroth RJ, Hitchon CA, Uhanova J, Noreddin A, Taback SP, Moffatt ME, Zacharias JM,Hepatitis B vaccination for patients with chronic renal failure,inThe Cochrane Database of Systematic Reviews,vol. 2010, n. 3, 19 luglio 2004, pp. CD003775,DOI:10.1002/14651858.CD003775.pub2,PMC8406712,PMID15266500.
- ^(EN)Men Who Have Sex with Men | Populations and Settings | Division of Viral Hepatitis | CDC,sucdc.gov,31 maggio 2015.URL consultato il 13 dicembre 2017(archiviatoil 26 luglio 2008).
- ^abLutgens SP, Nelissen EC, van Loo IH, Koek GH, Derhaag JG, Dunselman GA,To do or not to do: IVF and ICSI in chronic hepatitis B virus carriers,inHuman Reproduction,vol. 24, n. 11, 22 luglio 2009, pp. 2676–8,DOI:10.1093/humrep/dep258,PMID19625309.
- ^abLeFevre ML,Screening for hepatitis B virus infection in nonpregnant adolescents and adults: U.S. Preventive Services Task Force recommendation statement,inAnnals of Internal Medicine,vol. 161, n. 1, luglio 2014, pp. 58–66,DOI:10.7326/M14-1018,PMID24863637.
- ^Owens DK, Davidson KW, Krist AH, Barry MJ, Cabana M, Caughey AB, Doubeni CA, Epling JW, Kemper AR, Kubik M, Landefeld CS, Mangione CM, Pbert L, Silverstein M, Simon MA, Tseng CW, Wong JB,Screening for Hepatitis B Virus Infection in Pregnant Women: US Preventive Services Task Force Reaffirmation Recommendation Statement,inJAMA,vol. 322, n. 4, luglio 2019, pp. 349–354,DOI:10.1001/jama.2019.9365,PMID31334800.
Bibliografia
modifica- Patologia medica Piccin. Aggiornamento 1989,PICCIN, 1989, pp. 57–,ISBN978-88-299-0793-9.
- Emilio Arisi,Farmaci in gravidanza,Elsevier srl, 2002, pp. 123–,ISBN978-88-86457-48-4.
- (EN) Brian I. Carr,Hepatocellular Carcinoma: Diagnosis and Treatment,Springer, 29 settembre 2009, pp. 236–,ISBN978-1-60327-373-2.
- (EN) Henryk Dancygier, Scott L. (FRW) Friedman, H. D. (CON) Allescher, U. (CON) Beuers,Clinical Hepatology: Principles and Practice of Hepatobiliary Diseases,Springer, 1º gennaio 2010, pp. 692, 752,ISBN978-3-642-04509-7.
- S. Fagiuoli,Dalle epatiti virali al trapianto di fegato: problemi aperti in epatologia,PICCIN, 2001, pp. 145–,ISBN978-88-299-1597-2.
- (EN) C. Fauquet e International Committee on Taxonomy of Viruses,Virus taxonomy: classification and nomenclature of viruses: eighth report of the International Committee on the Taxonomy of Viruses,Academic Press, 2005, pp. 381–,ISBN978-0-12-249951-7.
- (EN) Ralph D. Feigin,Textbook of pediatric infectious diseases,Elsevier Health Sciences, 2004, pp. 1871–,ISBN978-0-7216-9329-3.
- Luigi Grazioli e Lucio Olivetti,Diagnostica per immagini delle malattie del fegato e delle vie biliari,Elsevier srl, 2005, pp. 497–,ISBN978-88-214-2729-9.
- (EN) F. Blaine Hollinger,Viral hepatitis,Surendra Kumar, 2002, pp. 103–,ISBN978-0-7817-4055-5.
- Mauro Moroni, Roberto Esposito e Fausto De Lalla,Malattie infettive,Elsevier srl, 2008, pp. 585–,ISBN978-88-214-2980-4.
- (EN) John Nicholas,Human Cancer Viruses: Principles of Transformation and Pathogenesis,Karger Publishers, 2008, pp. 98–,ISBN978-3-8055-8576-7.
- (EN) Hans-Jörg Senn,Clinical Cancer Prevention,Springer, 14 gennaio 2011, pp. 75–,ISBN978-3-642-10856-3.
- (EN) Sheila Sherlock, Sheila Sherlock e James Dooley,Diseases of the liver and biliary system,Wiley-Blackwell, 2002, pp. 285–,ISBN978-0-632-05582-1.
- Michele Stefani,Lezioni di anatomia patologica,PICCIN, 1996, pp. 380–,ISBN978-88-299-1184-4.
Altri progetti
modifica- Wikiversitàcontiene risorse suepatite B
- Wikimedia Commonscontiene immagini o altri file suepatite B
Collegamenti esterni
modifica- (EN) Kara Rogers,hepatitis B,suEnciclopedia Britannica,Encyclopædia Britannica, Inc.
- Epatite b sintomi.URL consultato il 18 maggio 2011(archiviato dall'url originaleil 21 aprile 2011).,descrizione completa.
- Hepatitis B Pathogen Profile,suppdictionary.com.
- Conoscere e prevenire le malattie del fegato,sumalattiedelfegato.blogspot.com.
- Fegato e benessere: epatite B,sufegatoebenessere.blogspot.com.
- (EN)MST - Epatite virale B: sintomi e trattamento.URL consultato il 3 marzo 2018(archiviato dall'url originaleil 22 dicembre 2014).da Giovincelli in salute
- (FR)Epatite virale C: Informazione,sujeunesensante.ca.URL consultato l'8 ottobre 2008(archiviato dall'url originalel'8 febbraio 2009).
- (EN)[1]MEDHELP forums to share information among doctors and patients on HBV
- Epatite virale.URL consultato il 18 maggio 2011(archiviato dall'url originaleil 23 aprile 2011).,descrizione completa.
| Controllo di autorità | Thesaurus BNCF22624·LCCN(EN)sh85060295·GND(DE)4159548-8·BNE(ES)XX548510(data)·BNF(FR)cb11938386s(data)·J9U(EN,HE)987007558059405171·NDL(EN,JA)00986940 |
|---|