Anilina
| Anilina | |
|---|---|
 | |
 | |
| NomeIUPAC | |
| anilina | |
| Abbreviazioni | |
| Ph-NH2 | |
| Nomi alternativi | |
| fenilammina amminobenzene benzenammina | |
| Caratteristiche generali | |
| Formula brutaomolecolare | C6H7N |
| Massa molecolare(u) | 93,13 |
| Aspetto | liquido incolore (da giallo a bruno se impura) |
| Numero CAS | |
| Numero EINECS | 200-539-3 |
| PubChem | 6115 |
| DrugBank | DBDB06728 |
| SMILES | C1=CC=C(C=C1)N |
| Proprietà chimico-fisiche | |
| Densità(g/cm3,inc.s.) | 1,03 |
| Costante di dissociazione basicaa 293 K | 3,81×10−10 |
| Solubilitàinacqua | 36 g/l a 293 K |
| Temperatura di fusione | −6,2 °C (266,9 K) |
| Temperatura di ebollizione | 184 °C (457 K) |
| ΔebH0(kJ·mol−1) | 47,3 |
| Proprietà termochimiche | |
| ΔfH0(kJ·mol−1) | 31,6 |
| C0p,m(J·K−1mol−1) | 191,9 |
| Indicazioni di sicurezza | |
| Punto di fiamma | 76 °C (349 K) |
| Limiti di esplosione | 1,2 - 11% vol. |
| Temperatura di autoignizione | 540 °C (813 K) |
| Simboli di rischio chimico | |
    
| |
| pericolo | |
| Frasi H | 351-341-331-311-301-372-318-317-400 |
| Consigli P | 273-280-308+313-302+352-305+351+338-309+310[1] |
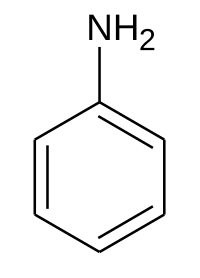
L'anilina,nota anche comefenilamminaoamminobenzene,è uncomposto aromaticoavente formula bruta C6H7N. È un'amminaprimaria la cui struttura è quella di unbenzene,in cui un atomo di idrogeno è stato sostituito da un gruppo NH2.A temperatura ambiente si presenta come un liquido incolore quando è molto pura. Data la facilità con cui siossidaall'aria, l'anilina tende col tempo a scurirsi fino ad annerire.
Storia
[modifica|modifica wikitesto]L'anilina fu isolata per la prima volta nel1826daOtto Unverdorbenper distillazione dei prodotti di decomposizione dell'indaco.Fu inizialmente chiamatacristallina.
Nel1834F. Rungeisolò dalcatrameuna sostanza capace di produrre un'intensa colorazionebluper trattamento con la calce e la battezzòcianolo.
Nel1841C. J. Fritzsche diede il nome dianilinaall'olio ottenuto per trattamento dell'indacoconpotassa caustica.Prese il nome dalla pianta diIndigofera anil,da cui l'indaco viene ricavato. A sua voltaanilderiva dalsanscritonīla,blu scuro, enīlā,la pianta dell'indaco. Più o meno nello stesso periodo il chimicorussoNikolaj Nikolaevič Zininscoprì che per riduzione del nitrobenzene si ottiene un composto basico che chiamòbenzidam.
Fu infineAugust Wilhelm von Hofmannnel1855a dimostrare l'identità di questi preparati, tutti riconducibili ad un'unica sostanza, chiamata quindianilinaofenilammina.
La prima produzione su scala industriale dell'anilina fu impiegata come intermedio della sintesi dellamauveina,un coloranteviolascoperto nel1856daWilliam Henry Perkin.Viene utilizzato anche per il "nero inferno", un colorante per le pelli usato dai calzolai.
Sintesi
[modifica|modifica wikitesto]L'anilina può essere prodotta dalbenzenein due passaggi. Dapprima il benzene vienenitrato,cioè fatto reagire con una miscela diacido nitricoeacido solforicoconcentrati per dare ilnitrobenzenetramite una reazione disostituzione elettrofila.Quindi il nitrobenzene vieneridottoad anilina per reazione con diversi reagenti riducenti; tra essi l'idrogenoin presenza di uncatalizzatoreo un metallo (ferro,zincoostagno) in presenza diacidi.
Molti derivati dell'anilina possono essere sintetizzati in modo simile.
Proprietà e reattività chimica
[modifica|modifica wikitesto]L'anilina è una sostanza velenosa con possibili effetticancerogeni(frase di rischio R40). È un liquido oleoso dall'odore caratteristico e dall'aspetto incolore, tuttavia nel tempo si ossida e produce impurezze resinose di colore rosso-bruno. Brucia facilmente con fiamma grande e fumosa. Dal punto di vista chimico è unabasedebole. Le ammine aromatiche come l'anilina sono in genere meno basiche delle ammine alifatiche, questo perché ildoppietto elettronicodell'atomo di azoto è parzialmente condiviso con l'anello aromatico perrisonanzaed è pertanto meno disponibile per essere ceduto a specie chimicheacide.
- L'anilina reagisce con gli acidi forti a dare sali dianilinioC6H5-NH3+che generalmente per riscaldamento si decompongono liberandoammoniaca;reagisce inoltre con glialogenuri acilici,come ilcloruro di acetileCH3COCl, o con gliacidi carbossiliciin ambiente disidratante a dare leammidi.Le ammidi dell'anilina sono spesso chiamateanilidi;CH3-CO-NH-C6H5,ad esempio, è l'acetanilide.[2]
- Per reazione coniodurialchilicil'anilina forma ammine secondarie e terziarie; per bollitura consolfuro di carboniodà lasolfocarbanilide(difeniltiourea,CS(NHC6H5)2) che può essere decomposta intiocianato di fenileC6H5CNS etrifenilguanidinaC6H5N=C(NHC6H5)2.
- Come ilfenoloanche l'anilina subisce facilmente reazioni disostituzione elettrofilasull'anello aromatico in posizioneparaeorto.Per reazione con l'acido solforicoa 180 °C dà l'acido solfanilicop-NH2-C6H4-SO3H le cui ammidi costituiscono la classe dei farmacisulfamidici,antibatterici comunemente usati all'inizio delXX secolo.
- L'anilina ed i suoi derivati sostituiti sull'anello aromatico reagiscono facilmente con l'acido nitrosoper dare i corrispondentisali di diazonio;attraverso essi il gruppo -NH2dell'anilina può essere convertito in altrigruppi funzionaliquali -OH, -CN o unalogenooppure possono venire sintetizzati composti coloranti, detticoloranti diazoici.
- Con l'acroleinal'anilina reagisce secondo lasintesi di Skraupcome seguito:
- L'anilina viene facilmente ossidata sia sul gruppo -NH2sia sull'anello aromatico; in ambiente alcalino l'ossidazione dell'anilina produce l'azobenzene;con l'acido arsenicosi ottiene il coloranteviola di anilina,con l'acido cromicoviene convertita nel corrispondentechinone,mentre per ossidazione concloratiin presenza di sali metallici, specialmente divanadio,si ottiene il colorantenero di anilina.
- L'ossidazione conacido cloridricoeclorato di potassiodà ilcloranile;l'ossidazione conpermanganato di potassioin soluzioneneutrala trasforma innitrobenzene,in soluzione alcalina la ossida a azobenzene, ammoniaca edacido ossalico,in soluzione acida la trasforma in nero di anilina.
- La reazione conacido ipoclorosodà4-amminofenoloe4-ammino-difenilammina.
Saggi
[modifica|modifica wikitesto]L'anilina ed i suoi sali possono essere identificati in unasoluzione acquosaper aggiunta di poche gocce disoluzione saturadiipoclorito di calcio;si ottiene colorazione.
Utilizzi
[modifica|modifica wikitesto]Il valore commerciale dell'anilina è legato alla sua versatilità come intermedio nelle sintesi chimiche industriali di prodotti quali farmaci, ausiliari e coloranti.
A partire dal1858l'anilina è stata la materia prima impiegata nella produzione di centinaia di sostanze coloranti tra cui lafucsina,lasafranina,l'indacoe molte altre.
Industrialmente l'anilina è prodotta per riduzione del nitrobenzene con ferro e acido cloridrico, purificandola successivamente perdistillazionein corrente di vapore.
L'anilina fu inizialmente considerata come propellente per razzi, ma fu abbandonata a causa dell'alta temperatura di fusione.
Effetti per la salute
[modifica|modifica wikitesto]L'anilina è uno dei primicancerogeniriconosciuti per l'uomo.[3]Ludwig Rehn, nel 1895, associò l'incidenza del tumore alla vescica all'esposizione dei lavoratori dell'industria tedesca dei coloranti artificiali.[3]Provoca soprattuttotumori della vescicae anche tumori renali, cutanei, epatici e del sangue. La molecola non è cancerogena in quanto tale, ma lo diventa a seguito della sua metabolizzazione nelfegatoattraverso processi di idrossilazione ad opera di enzimi dipendenti dalcitocromoP450 (catena ossidativa dei microsomi). I principali derivati dell'anilina sono il para-ammino-fenolo e la 2,4-diossi-anilina; a loro volta questi intermedi devono andare incontro a reazioni diossido-riduzioneper potersi trasformare nei loro rispettivichinoni:para-iminochinone e 2-idrossi-para-iminochinone.
Sono queste ultime molecole, assai reattive (elettrofili), che reagiscono prontamente con specifici residui di proteine e con gli acidi nucleici instaurando un legame di tipo covalente. Nel caso delle proteine se si tratta di enzimi questi possono essere permanentemente inattivati e devono essere degradati. Nel caso degli acidi nucleici, soprattutto delDNA,si verificano interazioni covalenti con le basiguaninaedadenina,reazioni che portano sia a legami crociati tra le eliche del DNA sia a rotture delle stesse. A seconda dei geni interessati e della sede al loro interno si potranno avere variabili alterazioni del fenotipo cellulare, per esempio alterazioni in geni oncosoppressori possono rendere la cellula più soggetta a trasformazioni neoplastiche. Un triste esempio della carcinogenicità dell'anilina è la fabbricaIPCAdi Ciriè, comune della città metropolitana di Torino.
Note
[modifica|modifica wikitesto]- ^scheda dell'anilina suIFA-GESTIS(archiviato dall'url originaleil 16 ottobre 2019).
- ^(EN)IUPAC Gold Book, "anilides".
- ^ab(EN)The Epidemiological Imagination: A Reader - 1994, Page 77 | Online Research Library: Questia[collegamento interrotto],suquestia.com.URL consultato il 15 agosto 2017.
Bibliografia
[modifica|modifica wikitesto]- (EN) Klaus Weissermel, Hans-Jürgen Arpe, Charlet R. Lindley,Industrial organic chemistry,4ª ed., Wiley-VCH, 2003, pp. 376-379,ISBN3-527-30578-5.
Altri progetti
[modifica|modifica wikitesto] Wikizionariocontiene il lemma di dizionario «anilina»
Wikizionariocontiene il lemma di dizionario «anilina» Wikimedia Commonscontiene immagini o altri file suanilina
Wikimedia Commonscontiene immagini o altri file suanilina
Collegamenti esterni
[modifica|modifica wikitesto]- Anilina, ulla Matrice di esposizione a cancerogeni - MATline,sudors.it.
- (EN)aniline/aniline dye,suEnciclopedia Britannica,Encyclopædia Britannica, Inc.
| Controllo di autorità | Thesaurus BNCF30854·LCCN(EN)sh85005157·GND(DE)4142482-7·BNF(FR)cb12359525w(data)·J9U(EN,HE)987007294056505171 |
|---|
