Catalizzatore di Crabtree
| Catalizzatore di Crabtree | |
|---|---|
 | |
 | |
| NomeIUPAC | |
| esafluoridofosfato(1−) di (SP-4)tris(cicloesil)fosfano [(1-2-η:5-6-η)-ciclootta-1,5-diene] piridinairidio(1+) | |
| Caratteristiche generali | |
| Formula brutaomolecolare | C31H50F6IrNP2 |
| Massa molecolare(u) | 804,89 |
| Aspetto | solido cristallino arancione |
| Numero CAS | |
| Numero EINECS | 636-356-4 |
| PubChem | 2734563 |
| SMILES | C1CCC(CC1)P(C2CCCCC2)C3CCCCC3.C1CC=CCCC=C1.C1=CC=NC=C1.F[P-](F)(F)(F)(F)F.[Ir] |
| Proprietà chimico-fisiche | |
| Densità(g/cm3,inc.s.) | 1,67 |
| Solubilitàinacqua | insolubile |
| Temperatura di fusione | 175 °C (448 K) dec |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
| Frasi R | 36/38 |
| Frasi S | 26-37 |
Catalizzatore di Crabtreeè il nome comune delcomplessodiiridio[Ir(COD)(PCy3)(py)]+,dove l'iridio instato di ossidazione+1 è legato a1,5-cicloottadiene(COD), tris-cicloesilfosfina (PCy3) epiridina(py). Incondizioni normalisi presenta come un solido cristallino arancione. I leganti circondano l'atomo di iridio con una geometriaplanare quadrata,come atteso per uno ione d8.Il complesso è uncatalizzatoreomogeneoper reazioni diidrogenazione,[1]ed è stato sviluppato daRobert H. Crabtreeall'Università di Yale.[2]
Questo catalizzatore fu scoperto negli anni settanta all'Istituto di Chimica delle Sostanze Naturali diGif-sur-Yvette,vicino aParigi,dove Crabtree e lo studente laureato George Morris stavano lavorando su composti di iridio analoghi alcatalizzatore di Wilkinson,che è a base dirodio.Uno dei vantaggi del catalizzatore di Crabtree è che è circa 100 volte più attivo di quello di Wilkinson, e può idrogenare anchealchenitri- e tetrasostituiti.
Il catalizzatore di Crabtree è stato usato anche come base per lo sviluppo di ulteriori catalizzatori, dato che modificando i leganti si possono variare le proprietà del catalizzatore. Ad esempio, l'uso di legantichiraliha permesso lo sviluppo di catalizzatorienantioselettivi.
Confronto con catalizzatori tradizionali
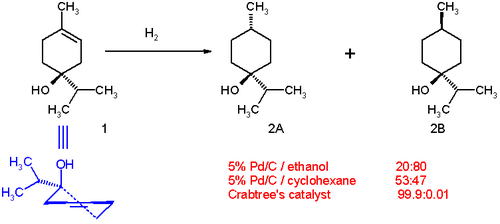
[modifica|modifica wikitesto]Nella reazione di idrogenazione di alcuni terpen-4-oli si osserva che:[3]
- Usando come catalizzatorepalladio su carbone(Pd/C) inetanoloil prodotto principale della reazione è l'isomero trans (rapporto 20:80, composto2Bnello schema seguente). Il lato polare con il gruppo idrossilico interagisce con ilsolventepolare e il lato apolare è libero di interagire con la superficie del catalizzatore.
- Usando il solvente apolarecicloesanola distribuzione diventa 53:47 indicando che il lato polare ha una leggera preferenza per il catalizzatore.
- Usando il catalizzatore di Crabtree indiclorometanola distribuzione dei prodotti cambia totalmente a favore dell'isomero cis2A.Questo effetto direzionante è dovuto all'interazione di legame tra il gruppo idrossilico e il centro di iridio. Anche i gruppi carbonilici mostrano lo stesso effetto direzionante nelle reazioni di idrogenazione con il catalizzatore di Crabtree.
Sicurezza
[modifica|modifica wikitesto]Il composto è irritante per la pelle e gli occhi. Non ci sono dati che indichino proprietà cancerogene. Non è consideratopericoloso per l'ambiente.[4]
Note
[modifica|modifica wikitesto]- ^Brown 1987
- ^Crabtree 1979
- ^Crabtree e Davis 1986
- ^Alfa Aesar,Scheda di dati di sicurezza del catalizzatore di Crabtree(PDF), sualfa.com.URL consultato l'11 ottobre 2011.
Bibliografia
[modifica|modifica wikitesto]- J. M. Brown,Directed homogeneous hydrogenation,inAngew. Chem. Int. Ed.,vol. 26, n. 3, 1987, pp. 190–203,DOI:10.1002/anie.198701901.URL consultato il 10 ottobre 2011.
- R. Crabtree,Iridium compounds in catalysis,inAcc. Chem. Res.,vol. 12, n. 9, 1979, pp. 331–337,DOI:10.1021/ar50141a005.URL consultato il 10 ottobre 2011.
- R. H. Crabtree, M. W. Davis,Directing effects in homogeneous hydrogenation with [Ir(cod)(PCy3)(py)]PF6,inJ. Org. Chem.,vol. 51, n. 14, 1986, pp. 2655–2661,DOI:10.1021/jo00364a007.URL consultato il 10 ottobre 2011.
Altri progetti
[modifica|modifica wikitesto] Wikimedia Commonscontiene immagini o altri file suCatalizzatore di Crabtree
Wikimedia Commonscontiene immagini o altri file suCatalizzatore di Crabtree