1,3-bis(difenilfosfino)propano
| 1,3-bis(difenilfosfino)propano | |
|---|---|
 | |
 | |
| Nomi alternativi | |
| dppp | |
| Caratteristiche generali | |
| Formula brutaomolecolare | C27H26P2 |
| Massa molecolare(u) | 412,44 |
| Aspetto | polvere cristallina bianca |
| Numero CAS | |
| Numero EINECS | 229-791-2 |
| PubChem | 81219 |
| SMILES | C1=CC=C(C=C1)P(CCCP(C2=CC=CC=C2)C3=CC=CC=C3)C4=CC=CC=C4 |
| Proprietà chimico-fisiche | |
| Solubilitàinacqua | insolubile |
| Temperatura di fusione | 62-64 °C (335-337 K) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| Frasi H | 315-319-335 |
| Consigli P | 261-305+351+338-302+352-321-405-501 |
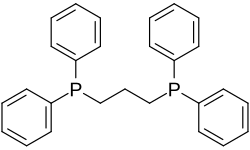
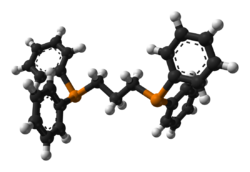
Il1,3-bis(difenilfosfino)propanoè unafosfinaconformulaPh2P-CH2-CH2-CH2-PPh2(Ph =fenile). Il nome è generalmente abbreviato comedppp.Incondizioni normaliè un solido di colore bianco sensibile all'ossigeno atmosferico. Viene comunemente usato comelegantebidentato inchimica inorganicaechimica metallorganica.Il dppp funziona nella maggior parte dei casi come legantechelato,ma può fare anche da legante a ponte tra due metalli.[1]
Sintesi e reattività
[modifica|modifica wikitesto]Per preparare il dppp si fa reagire difenilfosfuro di litio (LiPPh2) e 1,3-dicloropropano:[2]
- 2LiPPh2+ CH2Cl-CH2-CH2Cl → Ph2P-CH2-CH2-CH2-PPh2+ 2LiCl
Chimica di coordinazione
[modifica|modifica wikitesto]Il dppp è usato come legante in molti complessi che trovano applicazioni catalitiche. Normalmente preferisce agire da legantechelato.Ad esempio:
- [Rh(CO)Cl(dppp)] e [Rh(dppp)2]Cl catalizzano la decarbonilazione di aldeidi.[3]
- NiCl2(dppp) catalizza il cross-coupling di reagenti di Grignard (Kumada[4]-Corriu[5]coupling) per sintetizzare alchilareni da cloruri arilici.
- In catalizzatori dipalladio(II) catalizza lacopolimerizzazionedimonossido di carbonioedetileneper ottenerepolichetoni,una famiglia dipolimeri termoplasticiad elevate prestazioni.
In un numero più limitato di casi il dppp può fungere anche da legante a ponte tra due metalli, ad esempio nei cluster [Au6(dppp)4](NO3)2e [Au11(dppp)5](SCN)3[6]
Indicazioni di sicurezza
[modifica|modifica wikitesto]Il composto è disponibile in commercio. È irritante per gli occhi, la pelle e le vie respiratorie. Non ci sono dati che indichino proprietà cancerogene. È considerato poco pericoloso per l'ambiente.[7]
Note
[modifica|modifica wikitesto]- ^Albéniz ed Espinet 2006.
- ^Hewertson e Watson 1962.
- ^Jardine 2006.
- ^Tamao et al. 1972.
- ^Corriu e Masse 1972.
- ^Vittal e Puddephatt 2006.
- ^Alfa Aesar,Scheda di dati di sicurezza del dppp(PDF), sualfa.com.URL consultato il 22 novembre 2011.
Bibliografia
[modifica|modifica wikitesto]- A. C. Albéniz e P. Espinet,Palladium: Inorganic & Coordination Chemistry,inEncyclopedia of Inorganic Chemistry,Wiley, 2006,DOI:10.1002/0470862106.ia178.
- R. J. P. Corriu e J. P. Masse,Activation of Grignard reagents by transition-metal complexes. A new and simple synthesis of trans-stilbenes and polyphenyls,inJ. Chem. Soc., Chem. Commun.,n. 3, 1972, pp. 144a,DOI:10.1039/C3972000144A.URL consultato il 22 novembre 2011.
- F. H. Jardine,Decarbonylation Catalysis,inEncyclopedia of Inorganic Chemistry,Wiley, 2006,DOI:10.1002/0470862106.ia061.
- W. Hewertson e H. R. Watson,283. The preparation of di- and tri-tertiary phosphines,inJ. Chem. Soc.,1962, pp. 1490–1494,DOI:10.1039/JR9620001490.URL consultato il 14 novembre 2011.
- K. Tamao, K. Sumitani e M. Kumada,Selective carbon-carbon bond formation by cross-coupling of Grignard reagents with organic halides. Catalysis by nickel-phosphine complexes,inJ. Am. Chem. Soc.,vol. 94, n. 12, 1972, pp. 4374–4376,DOI:10.1021/ja00767a075.URL consultato il 22 novembre 2011.
- J. J. Vittal e R. J. Puddephatt,Gold: Inorganic & Coordination Chemistry,inEncyclopedia of Inorganic Chemistry,Wiley, 2006,DOI:10.1002/0470862106.ia081.
Altri progetti
[modifica|modifica wikitesto] Wikimedia Commonscontiene immagini o altri file su1,3-bis(difenilfosfino)propano
Wikimedia Commonscontiene immagini o altri file su1,3-bis(difenilfosfino)propano
