Malaria
| Malaria | |
|---|---|
 | |
| Specialità | infettivologia,medicina tropicaleeparassitologia |
| Eziologia | Plasmodium falciparum,Plasmodium vivax,Plasmodium malariae,Plasmodium ovaleePlasmodium knowlesi |
| Classificazione e risorse esterne (EN) | |
| OMIM | 248310 |
| MeSH | D008288 |
| MedlinePlus | 000621 |
| eMedicine | 221134e784065 |
| Sinonimi | |
| paludismo | |
| Eponimi | |
| dottrina miasmatico-umorale zona umida | |
Lamalaria(detta anchepaludismo) è unaparassitosi,malattia provocata da parassitiprotozoidelgenerePlasmodium(regnoProtista,phylumApicomplexa,classeSporozoea,ordineEucoccidiida). Fra le varie specie di parassitaPlasmodium,quattro sono le più diffuse, ma la più pericolosa è ilPlasmodium falciparum,con il più altotasso di mortalitàfra i soggetti infestati. Il serbatoio del parassita è costituito dagli individui infettati in maniera cronica. I vettori sonozanzaredel genereAnopheles.
La malaria è la più diffusa fra tutte le parassitosi, con il suo quadro clinico di malattia febbrile acuta che si manifesta consegnidi gravità diversa a seconda della specie infettante.[1]La sua diffusione attuale non si limita alle aree tropicali dell'America del sud,dell'Africae dell'Asia,ma interessa sporadicamente anche gliUSAe alcuni paesi europei, in cui casi clinici della malattia possono apparire a seguito di spostamenti di persone che contraggono la malattia in zone in cui essa è endemica.[2][3]
Si pensa che la malaria sia stata tra le cause dell’affermazione dellatalassemiaminor (e conseguentemajor) poiché, durante il medioevo, la malaria era molto diffusa in Europa e lamutazione spontaneadel gene corrispondente allatalassemiaapportava il vantaggio di rendere la riproduzione del patogeno più complessa nel corpo umano.[4]
Poiché i sintomi della malaria sono aspecifici, e la diagnosi e il trattamento devono essere tempestivi, la malaria deve essere sospettata in tutti i pazienti con segni febbrili di ritorno daitropici.
Etimologia del nome
[modifica|modifica wikitesto]L'etimologiadi "malaria" deriva da un termine medievale italiano "mal aria" ovvero cattiva aria[5]mentre il termine "paludismo" deriva dalla convinzione che la malattia fosse provocata dai miasmi provenienti dallezone paludose.Questo termine venne utilizzato nelSettecentoanche fuori dall'Italia per descrivere una febbre che compariva solo d'estate e che era spesso mortale.[6]
Storia
[modifica|modifica wikitesto]La malaria, secondo studi che hanno verificato la presenza del morbo anche negliscimpanzé,[7]infetterebbe l'umanità da oltre 50 000 anni.[8]Le prime testimonianze verificate le troviamo nel 2700 a.C. in Cina,[9]mentre la prima descrizione delquadro clinicodella malaria risale aIppocrateche nelleEpidemiee negliAforismidescrive la tipicafebbreintermittente.[10]
Lo sviluppo della malaria si spostò in seguito verso l'Italia, dove la sua diffusione venne ostacolata dall'abilità deiRomaninel curare i campi agricoli e dalle loro opere di bonifica.[6]AlV secolo d.C.,pressappoco in coincidenza con la data convenzionale dicaduta dell'Impero romano d'Occidente,risale la prima evidenza storico-archeologica dell'arrivo inEuropadelPlasmodium falciparum,individuata a seguito degli scavi dellaNecropoli dei bambinidiLugnano in Teverina,nei pressi di unavilla romanadella mediavalle del Tevere.Quando l'impero romano perse i suoi antichi fasti, i focolai fecero nuovamente la loro comparsa, una circostanza che comportò una lunga opera di bonifica fino alMedioevo.[6] Secondo uno studio del 2016[11]esistono evidenze anche precedenti. I ricercatori (Canada,Italia e Australia) hanno analizzato 58 denti di individui adulti provenienti da tre cimiteri (Isola Sacra - Portus Romae, I–III secolo, Velia I–II secolo, e Vagnari I–IV secolo[12].In 11 individui è stata trovata la presenza diPlasmodiumspp.[13]mentre in due è stata provata la presenza diPlasmodium falciparum.
Il primomedicoche intuì il coinvolgimento delle zanzare nella diffusione della malattia fuGiovanni Maria Lancisi.Alla fine dell'Ottocento si avevano inItalia15 000 morti all'anno per malaria, con febbri estivo-autunnali, soprattutto nel Sud e nelle isole. La malaria in Italia è stata eradicata intorno aglianni cinquanta,con campagne di eradicazione finanziate dallaRockefeller Foundation.Nel1880Alphonse Laveran[14],aCostantinainAlgeria,osservò per primo il parassita nelle cellule delsangueperiferico umano delle persone che soffrivano di tale malattia. Egli propose che il morbo fosse causato da quelprotozoo,intuizione che gli valse ilpremio Nobel per la medicinanel1907.Ettore MarchiafavaeAngelo Celli[15],un anno dopo aRoma,studiarono il protozoo e lo denominaronoPlasmodium.

Nel1885,aPavia,Camillo Golgi,insignito delpremio Nobelnel1906,dimostrò l'associazione tra periodicità delle febbri malariche e il ciclo del plasmodio. Riuscì a provare come i due diversi tipi di febbre malarica, la terzana e la quartana, fossero provocati da due distinte specie di plasmodio:Plasmodium vivax,responsabile della terzana benigna, ePlasmodium malariae,responsabile della quartana. Nel1889dimostrò che gli attacchi febbrili si verificavano nel momento in cui gli sporozoiti (stadio del ciclo del plasmodio) rompevano iglobuli rossie si liberavano nelcircolo sanguigno.Ettore Marchiafava,Angelo Celli,Amico BignamieGiuseppe Bastianelli,aRoma,dimostrarono l'esistenza delPlasmodium falciparum,responsabile della terzana maligna. Nel1894Patrick Manson,inCina,ipotizzò per primo che ilPlasmodiumfosse trasmesso all'uomo da unazanzara.Questa tesi fu dimostrata nel1897daRonald Ross(Nobel1902), inIndia.[16]

Nel1898Giovanni Battista Grassi[17],aRoma,identificò ilvettoredella malaria, gliAnopheles,e ottenne la prima trasmissione sperimentale. Nel1899descrisse il ciclo completo delle varie specie diPlasmodium.Nel1905,Carlos Chagas,che per primo aveva notato e studiato la trasmissione intradomiciliare del plasmodio, organizzò all'età di 26 anni, e mise in atto aItatinga,nell'interno dellostato di San Paolo(Brasile), la prima efficace campagna diprofilassiantimalarica nella storia. Al1925risale la realizzazione aRomadella "Stazione Sperimentale per la Lotta Antimalarica", diretta dall'italianoAlberto Missirolie dall'americanoLewis Hackett.
Sempre nel1925nell'ambito del Primo Congresso Internazionale della Malaria tenutosi a Roma si avanzò la necessità di un istituto internazionale di malariologia, secondo quanto suggerito dallaSocietà delle Nazioni;il Governo italiano non accolse il suggerimento, ma convertì la proposta fondando nel1927un nuovo Ente per la ricerca contro la malaria; la Scuola di Malariologia di Roma, fondata e diretta dal clinico prof. Vittorio Ascoli, che per anni aveva studiato e pubblicato letteratura medica circa la malaria. Alla sua morte, nel1931,la Scuola venne poi diretta daGiuseppe Bastianelli.Nel1933la Scuola divenne l'Istituto di Malariologia, teso alla formazione di medici malariologi.
Epidemiologia
[modifica|modifica wikitesto]
La malaria è la più importante parassitosi e la seconda malattia infettiva al mondo per morbilità e mortalità dopo latubercolosi,con oltre 200 milioni di nuovi casi clinici all'anno e 438 000 decessi all'anno (dati 2015)[18].
Il 40% della popolazione mondiale vive in zone in cui la malaria è endemica, situate in aree tropicali e subtropicali e a un'altitudine inferiore ai 1 800ms.l.m..[19]
Ogni anno circa 10 000-30 000 viaggiatorieuropeieamericanisi ammalano di malaria.
Le donne ingravidanzasono particolarmente soggette a tale malattia e, malgrado gli sforzi per ridurre la trasmissione aumentando il trattamento, l'effetto ottenuto non corrisponde a quello sperato.[20]
La sua frequenza è dovuta ad una serie di fattori fra le quali le condizioni climatiche favorevoli alla malattia e il numero di soggetti portatori di gametociti nel sangue periferico umano che si trovano nell'area di contagio, anche se uno studio esatto è molto complesso vista l'estensione delle zone coinvolte.[21]
L'ambiente climatico influenza le caratteristiche epidemiologiche:
- Nelle zone disavanaafricana la trasmissione è perenne, con variazioni stagionali, più sensibili a mano a mano che ci si allontana dall'equatore;dominaP. falciparume la morbilità e mortalità sono prevalenti nei bambini e nelledonne gravide;è molto diffusa la farmaco-resistenza.
- Nellepianuree nelle valli di America centrale,Cinae India, la trasmissione è variabile e moderata, con forti variazioni stagionali e rischio di epidemie. PrevaleP. vivaxe la farmaco-resistenza è abbastanza stabile.
- Suglialtopiani,nelle areesemidesertichee nelle isole (Sahel,Sud-Est Asiatico,Sudafrica,Isole del Pacifico,Caraibi) il rischio di epidemie è dovuto ad aberrazioni climatiche, a fenomeni migratori da aree malariche altamente endemiche e a cambiamenti nelle abitudini agricole.
- In aree di recente sviluppo agricolo (Africa,Asia,Sudamerica) l'irrigazioneinagricolturapuò aumentare la trasmissione del plasmodio, con conseguente rischio di malaria stagionale con epidemie tra lavoratori immigrati non-immuni.
- Nelle aree urbane e periurbane delle città africane la trasmissione e la popolazione immune sono molto variabili anche a piccole distanze.

Rischio molto limitato
Rischio di malaria daP. vivaxo daP. falciparumclorochino sensibile
Rischio di malaria con possibile presenza di ceppi clorochino resistenti
Alto rischio di malaria daP. falciparumchemio-resistente, o moderato/basso rischio di malaria daP. falciparumcon alta diffusione di ceppi chemio-resistenti.
Criteri statistici
[modifica|modifica wikitesto]Per valutare le aree di maggiore diffusione della malaria sono stati istituiti degli indici di prevalenza; essi sono innumerevoli ma i più importanti sono:[22]
- Indice splenico: il numero di bambini che presentano determinatisintomi
- Indice parassitario: il rapporto fra la quantità di specie del singolo parassita paragonato al numero totale di casi di malaria
- Densità parassitaria: numero medio della presenza nel sangue dei protozoi infetti
- Indice sporozoitico: numero di zanzare presenti che siano potenzialmente pericolose per l'uomo
- Tasso di inoculazione entomologica: collegato all'indice sporozoitico, misura anche la quantità di punture che le persone normalmente subiscono
- Human Blood Index(HBI): misura quante zanzare in una determinata regione posseggono sangue umano (è un indice studiato anche per comprendere gli effetti di determinati alimenti o minerali[23])
Eziologia
[modifica|modifica wikitesto]La maggior parte delle infezioni malariche sono dovute a quattro specie diPlasmodium:ilP. falciparum[24],ilP. vivax[25],ilP. ovale[26]e ilP. malariae.[27]
Ladiagnosidi specie è importante perché la malaria daP. falciparumè potenzialmente mortale.
Inizialmente si pensava che soltanto queste quattro specie di protozoi potessero interessare l'uomo e trasportare l'infezione,ma recentemente si sono studiate anche altre specie, anch'esse causa della malaria, come ilPlasmodium simiovalee ilPlasmodium knowlesi,di difficile diagnosi, la cui epidemiologia risulta confinata nel sud-Asia[28]e in particolare nellaMalaysia.[29]I vettori dell'infezione sono costituiti daAnopheles latense daAnopheles hackeri.[30]
Esistono anche altre forme derivate dalla prime che si manifestano negli animali come ilPlasmodium brasilianum,molte scimmie sudamericane sono infettate da questo parassita che sembra essere un derivato dalla formamalariae.Esso si è adattato per svilupparsi nelle scimmie, probabilmente dopo la scoperta del continente.[31]
- InAfrica settentrionalela malaria è poco presente e predominaP. vivax.[32]
- InAfrica centraleeorientalepredominaP. falciparum,ma sono presenti ancheP. vivaxeP. malariae.
- InAfrica occidentalepredominaP. falciparum,ma è molto diffuso ancheP. ovale;presente ma raro ancheP. vivax.
- Nelleisoledell'Oceano Indianoe nelSudest AsiaticopredominaP. falciparum,ma sono presenti ancheP. vivaxeP. malariae.
- Nelsubcontinente indianopredominaP. vivax,ma è presente ancheP. falciparum.
- Nelle isole dell'Oceano Pacificoe inAmerica centralesono presenti siaP. vivax,siaP. falciparum,molto più diffusi inAmazzonia.
La cosiddetta "malaria da aeroporto" è causata da zanzare infette, che provengono dai paesi epidemici, che infettano persone in paesi non soggetti normalmente all'epidemia: il primo caso si è avuto nel 1977 e da allora si sono registrati quasi un centinaio di casi in Europa.[33][34][35]
Patogenesi
[modifica|modifica wikitesto]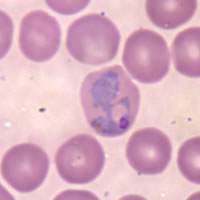
Nella maggior parte dei casi si mantiene un equilibrio tra infezione erisposta immunitaria.
Nelle infezioni daP. falciparuml'equilibrio è precario: la malattia può precipitare in qualsiasi momento e la parassitemia aumentare in modo incontrollabile, provocando unadisfunzione multiorgano(MOF, “multi-organ failure” ), o una subacuta progressivaemolisi intravascolare.In entrambi i casi si può avere la morte. La mortalità in un paziente non-immune e non trattato può arrivare fino al 20%.
Le forme di malaria daP. falciparumsono più gravi perché il plasmodio infetta tutti gli eritrociti e provoca parassitemie più alte, a differenza diP. vivaxeP. ovaleche infettano i reticolociti (eritrociti giovani) e diP. malariaeche infetta quelli vecchi.
Nella malariacerebrale,gli eritrociti parassitati vengono sequestrati nel microcircolo cerebrale, diventano più rigidi e indeformabili, aderiscono agli eritrociti sani, formando ammassi a forma dirosette,e agli endoteli deicapillarie dellevenulecerebrali, e si impacchettano, ostruendone il lume. La citoaderenza è determinata da proteine che vengono espresse sulla membrana delle emazie parassitate formando tubercoli evidenziabili solamente al microscopio elettronico. Di conseguenza si hanno congestione cerebrale e, in fasi avanzate, emorragie intraparenchimali. Alterazione della permeabilità dei vasi cerebrali è causata dalla produzione endogena di sostanze vasoattive (NO,TNF,IFNγ).
L'anemiaè di tipo emolitico, normocromico e normocitico. Possono aversi drammatici cali dell'emoglobinemia, durante gli attacchi acuti, per emolisi da rottura dei globuli rossi da parte degli schizonti. Gli eritrociti parassitati aderiscono a quelli sani e gli ammassi vengono insiemefagocitatie distrutti. L'anemia non è necessariamente proporzionale alla parassitemia. Gli eritrociti eventualmente trasfusi vengono distrutti più rapidamente. Si verifica diseritropoiesi (distruzione di eritrociti prima del loro rilascio dalmidollo osseo) e sequestro diferro,poiché il TNF stimola lafagocitosie deprime l'eritropoiesi.[36]
Modalità di trasmissione e ciclo vitale del Plasmodio
[modifica|modifica wikitesto]
La forma infettante del plasmodio è lo sporozoita il quale è presente all'interno delleghiandole salivaridizanzarefemmine appartenenti algenereAnophelesda cui vengono inoculati nell'ospite durante il pasto ematico.
LeAnopheles labranchiae,A. superpictus,A. maculipennis,A. atroparvuserano le zanzare vettore in Europa prima dell'eradicazione. Attualmente le specie coinvolte nella trasmissione sono:Anopheles gambiaeeA. funestusin Africa equatoriale;Anopheles culicifacies,A. minimuseA. maculatusin Asia;Anopheles darlingieA. acquasalisin America del Sud. Il numero di sporozoiti rilasciati dalla zanzara è alquanto variabile ma si ritiene che possa raggiungere un massimo di 100 per ilPlasmodium falciparum.Dopo una breve permanenza nel circolo ematico, entro 45 minuti dal pasto ematico gli sporozoiti invadono gliepatociti(celluledelfegato), per i quali hanno un tropismo elevato.
A questo punto, all'interno dell'epatocita ha inizio la prima fase di moltiplicazione asessuata (fase esoeritrocitaria, ovvero esterna aiglobuli rossi) detta anche schizogonica. Tale fase ha una durata variabile a seconda della specie in quanto va dai 5-7 giorni perP. falciparuma circa 15 perP. malariaee determina la formazione d'uno schizonte, che si rompe e che a seguito della lisi dell'epatocita, riversa in circolo migliaia di merozoiti mononucleati, che vanno a infettare glieritrociti(il più delle volte un merozoita per emazia ma in alcune infezioni daP. falciparumsi può arrivare fino a 4).
All'interno delle emazie (fase intraeritrocitaria) comincia un nuovo ciclo di riproduzione asessuata.[37][38][39][40]Il merozoite, infatti, si muta in trofozoite (forma vegetativa) morfologicamente distinguibile in trofozoite immaturo (con una forma ad anello) e maturo (concitoplasmapiù allargato ed accumulo diemozoina).
Successivamente il trofozoite si trasforma in uno schizonte di dimensioni più piccole rispetto a quelli intraepatocitari e contenenti in genere fino ad un massimo di 24 merozoiti.
I merozoiti, dopo la rottura dello schizonte, determinano la lisi dellamembranadel globulo rosso infettato e si riversano in circolo pronti ad infettare nuove specie ed a incominciare un nuovo ciclo riproduttivo. Tale ciclo risulta essere regolare e, in particolare, dura 48 ore perP. falciparum,P. vivaxeP. ovale,e 72 ore perP. malariae.Durante la rottura dei globuli rossi vengono rilasciatesostanze pirogene(vedi sezione relativa alla patogenesi) che determinano la comparsa dei classici picchi febbrili qualora le infezioni degli eritrociti siano diventate sincrone.
Studi recenti hanno dimostrato come iparassitipossano causare ricadute della malattia.[41][42]Nelle infezioni daP. vivaxeP. ovalealcuni degli sporozoiti possono persistere quiescenti nelle cellule epatiche (ipnozoiti, forme "dormienti" ) e rimanere in tale stato per mesi o anni per poi potersi riattivare ciclicamente determinando la comparsa di ricadute. Un fenomeno analogo può presentarsi anche nel caso diP. falciparumeP. malariaesolo che in tali casi la causa consiste nella persistenza, nel circolo ematico, d'una parassitemia troppo bassa per essere rivelata.
Dopo vari cicli alcuni trofozoiti si differenziano in forme eritrocitarie sessuate (gametociti). Sono queste le forme che permettono il mantenimento del ciclo del plasmodio nell'ambiente: l'uomo è il serbatoio dei gametociti da dove pescano le zanzare, e tale rimane per circa un anno dopo il contagio. Il microgametocita (maschio) e il macrogametocita (femmina) vengono ingeriti dall'Anopheles alla puntura di un individuo infettato, durante un nuovo pasto ematico. Il ciclo sessuato nella zanzara è detto sporogonico.
Nello stomaco dell'insetto, i gametociti escono dal globulo rosso che li ospita: il nucleo del microgametocita subisce varie divisionimitotichee forma otto microgameti maschi,flagellati.I macrogametociti, invece, non vanno incontro a processi di divisione e, comunque, la loro popolazione è più ampia d quella dei microgametociti.
Un microgametocita flagellato penetra nel macrogametocita e successivamente, dopo una fase dimeiosi,si forma lozigoteche poi diventa più lungo e mobile (oocinete), invade la parete del mediointestinodella zanzara, dove s'incista diventando un'oocisti. Questa va incontro a riproduzione asessuata che determina la formazione di migliaia di sporozoiti allorquando l'oocisti è ormai matura. Successivamente l'oocisti si rompe e libera gli sporozoiti che raggiungono le ghiandole salivari della zanzara e vengono inoculati nell'uomo alla successiva puntura con reiterazione di tutto il ciclo.
La fase di sviluppo all'interno della zanzara dura da 8 giorni ad un mese a seconda di vari fattori tra cui la specie infettante di plasmodio ed anche fattori climatici.
Oltre alla modalità classica di trasmissione, esistono anche altre possibilità di contrarre tale malattia:
- Contatto con sangue infetto: tipico il caso di trasfusioni del sangue, per incidenti o per malattie ma anche per lo scambio di siringhe infette, pratica comune tra i tossicodipendenti; tale forma di trasmissione è infatti spesso presente nei paesi africani e comporta la diffusione di più malattie infettive contemporaneamente, come malaria eAIDS[43]Ultimamente si sta studiando un metodo per poter prevenire questa propagazione.[44]
- Trasmissione transplacentare: la madre trasmette il plasmodio al figlio durante la gravidanza
Stadi della malattia
[modifica|modifica wikitesto]Incubazione
[modifica|modifica wikitesto]
Il tempo che va dall'infezionecon la puntura dizanzarae la comparsa dei trofozoiti neglieritrociticircolanti è detto "tempo prepatente", che è fisso e costante per ogni specie:
- P. falciparum9-10 giorni
- P. vivax11-13 giorni
- P. ovale10-14 giorni
- P. malariae15-16 giorni[45]
Il tempo che va dall'infezione con la puntura di zanzara alla comparsa dei segni e dei sintomi della malaria è detto "tempo d'incubazione". Questo è variabile e più lungo o al massimo uguale al periodo prepatente e dipende dalla carica infettante iniziale di sporozoiti iniettati dalla zanzara:
- P. falciparum9-14 giorni
- P. vivax12-17 giorni (raramente il periodo è ancora più lungo)
- P. ovale16-18 giorni
- P. malariae18-40 giorni (raramente il periodo è ancora più lungo)[45]
L'infezione daP. falciparumè detta "febbre terzana maligna", quella daP. vivaxe daP. ovaleè detta "febbre terzana benigna" e quella daP. malariaeè detta "febbre quartana" in base alla frequenza di febbre intermittente. Quelle di febbre "terzana" e "quartana" sono definizioni fuorvianti, perché solo una minima parte dei casi di malaria si presenta con febbre intermittente, ogni 48 ore (terzana, ogni terzo giorno) od ogni 72 ore (quartana, ogni quarto giorno). La febbre terzana si vedeva in Europa nelle zone endemiche per ilP. vivax(terzana benigna) e negli immigrati: le navi infatti facevano viaggi di 1-2 settimane, e quando arrivavano in Europa, seguendo la storia naturale dell'infezione daP. falciparum,da intermittente irregolare la febbre si faceva terzana, se il malato non era morto nel frattempo o se non era stato trattato. La febbre terzana si vede anche nei casi in cui si sia stati infettati da un unico ceppo diP. falciparum,evento non comune nelle aree endemiche, dove si è infettati più volte in sequenza e i cicli dei vari ceppi si sovrappongono con attacchi febbrili ad andamento irregolare.
Fase invasiva
[modifica|modifica wikitesto]Corrisponde alla rottura delloschizontee alla liberazione deimerozoitiche vanno ad invadere altrieritrociti.Si manifesta con febbre intermittente, brivido scuotente, sudorazione,cefalea,artralgia,mialgia,talvolta riattivazioni diherpes labiale,prostrazione, dolore negli ipocondri, sindromi gastroenteriche (diarrea,vomito,dolore addominale). Nei bimbi si possono avere convulsioni febbrili.
Fase tardiva
[modifica|modifica wikitesto]Quando i cicli vitali dei vari ceppi presenti si sono sincronizzati, compare la febbre terzana (tipico attacco malarico): brivido scuotente seguito da rialzo termico che si risolve dopo qualche ora con sudorazione profusa e uno stato di vaga euforia, e si ripete ogni 48 ore. Lasplenomegaliadi solito compare dopo giorni o settimane; all'inizio è più comune l'epatomegalia.Pallore muco-cutaneo,ittero,urineipercromiche (fortemente colorate) sono segni prognostici sfavorevoli. Nella maggioranza dei casi non trattati la malaria si risolve spontaneamente dopo 2 settimane; raramente dura più di un anno (mai più di 2 anni).
Recrudescenza
[modifica|modifica wikitesto]È la ricaduta causata dalla persistenza in circolo di forme intra-eritrocitarie (nei globuli rossi). È tipica delle infezioni daP. falciparumtrattate in modo inadeguato (per qualità e/o durata del trattamento e per posologia) e può avere una latenza da qualche giorno a qualche settimana. Si può avere anche nelle infezioni daP. malariaecon una latenza anche di molti anni.
Recidiva
[modifica|modifica wikitesto]Per recidiva si intende una ricaduta causata dalla persistenza di merozoiti nelfegato(ipnozoiti) che ricominciano un nuovo ciclo eso-eritrocitario, 5-6 mesi dopo l'infezione. È tipica delle infezioni daP. vivaxeP. ovalenelle quali non sono state trattate le forme intraepatiche (conprimachina).
Differenze tra le specie
[modifica|modifica wikitesto]
La malaria daP. vivaxha un tempo di incubazione più lungo. Si presenta come quella daP. falciparumcon attacchi febbrili irregolari, seguiti da sudorazioni profuse e defervescenza. Si può averesplenomegalia(raramente rottura splenica). Dopo qualche attacco si esaurisce, ma può avere ricadute per la persistenza degli ipnozoiti. Allora compare la febbre terzana benigna. Se i ceppi sono due e hanno un ritmo sfasato si può avere una doppia terzana, che è quotidiana. La terapia conclorochinacura l'attacco malarico ma non previene le ricadute. Nelle regioni africane (Golfo di Guinea) dove mancano individui portatori dell'antigene eritrocitarioduffy,P. vivaxè assente ed è rimpiazzato daP. ovale.Il quadro clinico è sostanzialmente sovrapponibile a quello diP. vivax.
La malaria daP. malariaeè la forma meno grave di malaria. Il plasmodio può persistere per anni negli eritrociti, a parassitemia bassissima, e nelle recrudescenze la febbre è quartana. Tuttavia, nei bimbi tra i 4 e gli 8 anni, come conseguenza di infezioni ripetute o continue, si possono avere gravi patologierenali,comeglomerulonefritimembrano-proliferative, con proliferazione dell'endotelio glomerulare e del mesangio. Il danno è causato da deposizione di immunocomplessi a livello delle aree mesangiali e subendoteliali delglomerulo renale.Clinicamente, in fase acuta, la malattia si presenta conproteinuriaimportante,edemageneralizzato e versamento ascitico (sindrome nefrosica): nella maggior parte dei casi la nefropatia non è reversibile dopo il trattamento dell'infezione malarica. La prognosi è sfavorevole e i pazienti progrediscono verso l'insufficienza renale cronicanel giro di 5 anni dall'esordio.
Clinica
[modifica|modifica wikitesto]Segni e sintomi
[modifica|modifica wikitesto]
Il decorso classico dei sintomi nella malaria è un ciclo che prevede oscillazioni termiche e quindi brividi improvvisi (per una-due ore), che avvengono quando la temperatura corporea sale, cui fanno seguito irrigidimento e febbre; anche se la persona non avverte la sensazione di calore, ma anzi prova benessere, la febbre può superare i 40 gradi (due-sette ore). L'ultima fase è una sudorazione eccessiva (due-tre ore), quando la temperatura scende. Il ciclo, che non osserva quasi mai intervalli regolari, dura dalle quattro alle sei ore e si ripete ogni due giorni nellaP. vivaxeP. ovale,mentre ogni tre perP. malariae.[46]
LaP. falciparumpuò mostrarsi confebbre ricorrenteed alta ogni 36-48 ore o una febbre meno pronunciata e quasi continua. Per ragioni ancora sconosciute, ma che possono essere collegate con l'altapressione intracranica,bambini affetti da malaria mostrano una postura anormale, unsegnoche indica danni molto gravi al cervello.[47] La malaria severa può progredire in modo estremamente veloce e causare la morte in poche ore o in qualche giorno, ed è causata daP. falciparumda 6 a 14 giorni dopo l'infezione.[48]
- Febbre,sintomo principale della malattia è dovuta alla libera circolazione del pigmento malarico (emozoina) nel sangue. Se nessuna terapia viene adottata e non si sviluppa in forme gravi, la malaria dapprima sembra guarire spontaneamente e poi sviluppa di nuovo episodi di febbre che rimangono intermittenti nella formaP. falciparume si protraggono per 3-4 mesi.
- Epatosplenomegalia,una conseguenza dell'esasperazione del lavoro del sistema macrofagico dieritrocateresi,che è stato riscontrato con degli studi specifici nel 25% dei casi.[49]
- Epatomegalial'aumento del volume delfegato,presente in quasi la totalità delle persone coinvolte.[49]
- Tachicardiaedelirio,spesso compaiono in concomitanza con eventi febbrili acuti e ne sono, soprattutto nel caso del delirio, conseguenza specifica.
Organi coinvolti
[modifica|modifica wikitesto]- Milza,in alcune forme si presenta tumefatta e iperemica, diventando ospite di molti parassiti può apparire talmente sensibile che si riscontrano casi di rottura della stessa.
- Reni,durante la manifestazione della malaria per colpa della deposizione di immunocomplessi, si può assistere ad una loro insufficienza. Attraverso unaterapiaadeguata si può ristabilire la loro funzionalità. L'indebolimento renale può causare lafebbre emoglobinurica,dove si presenta una graveemolisie l'emoglobina fuoriesce nell'urina colorandola di nero,[50]episodio con cui viene diagnosticato, anche se i casi studiati sono molto pochi.[51]Questa manifestazione si riscontra soprattutto in casi di assunzione esagerata di chinino per profilassi o terapia, ma la sua patogenesi ancora non è chiara.[52]
Forme gravi
[modifica|modifica wikitesto]Le forme gravi sono tutte provocate daP. falciparum.La mortalità per malaria severa è maggiore nei bimbi tra i 6 mesi e 3 anni di età nelle aree endemiche. I viaggiatori non-immuni hanno un'alta mortalità indipendentemente dall'età.
Segni prognostici sfavorevoli sono lo stato comatoso non risvegliabile, l'anemia normocitica severa (ematocrito <15%, emoglobinemia <5g/dL), l'insufficienza renale(creatininemia >3 mg/dL, diuresi 24 h <400 cc negli adulti o <12 cc/kg nei bimbi), edema polmonare,ipoglicemia(<40 mg/dL), collasso cardiocircolatorio, shock, coagulopatia da consumo, sanguinamenti spontanei, convulsioni generalizzate ripetute (>2/24 h, nonostante il raffreddamento con impacchi bagnati), acidosi, emoglobinuria, iperparassitemia (>5% RBC infetti, >250 000 parassiti/cc), ittero muco-cutaneo (bilirubinemia totale >3 mg/dL), leucocitosi (non necessariamente per complicanze batteriche).
Splenomegalia malarica iperreattiva (HMS)
[modifica|modifica wikitesto]Detta in passato "sindrome splenomegalica tropicale" è una condizione patologica conseguente a una risposta immunologica aberrante agli attacchi ripetuti di malaria ed è molto diffusa nel Sudan.[53]L'HMS si manifesta con severa splenomegalia in ragazzi o adulti, alti livelli di anticorpi anti-Plasmodium, alti livellisiericidiIgM,di tipo policlonale, e risposta clinica e immunologica a un'appropriata terapia anti-malarica a lungo termine. L'ipersplenismo è responsabile dell'anemia emolitica cronica, dellaleucopeniaetrombocitopenia.Si hanno calo ponderale, astenia,tachicardia,dispnea dopo sforzo, senso di peso e dolenzia in ipocondrio sinistro. Solitamente l'esame diretto della goccia spessa del sangue periferico non rivela la presenza di plasmodi e gli esami bioumorali indicano uno spiccato stato flogistico (aumento dellaVESe delle proteine plasmatiche di fase acuta).
Malaria cerebrale
[modifica|modifica wikitesto]La malaria cerebrale è un'encefalopatiaacuta diffusa. Il paziente si presenta comatoso (varia gravità e durata da 6 a 96 ore); solitamente la parassitemia è alta e possono aversi convulsioni. Le emorragie retiniche sono associate a una prognosi peggiore. Possono aversi disturbi temporanei (strabismo divergente, riflessi patologici, lieve rigor nucale). Il quadro neurologico più comune nell'adulto è quello della lesione simmetrica delmotoneuronesuperiore. Possono aversi rigidità da decerebrazione (braccia e gambe distese), da decorticazione (braccia flesse e gambe distese),opistotono. Alla rachicentesi la pressione liquorale è solitamente normale. Illiquido cefalorachidianoè limpido (<10 cell/µL), la protidorrachia eacido latticopossono essere aumentati. L'elettro-encefalogrammamostra reperti anormali ma aspecifici. Il repertoTCè del tutto normale. I riflessi cutanei addominali sono sempre assenti. Può aversi una modesta epato-splenomegalia.
Nei bimbi l'esordio è con febbre (37,5 - 41 °C),anoressia,vomito, tosse, raramente diarrea. La sintomatologia di solito precede il coma di 1 o 2 giorni (se il coma dura più di mezz'ora dopo un episodio convulsivo febbrile bisogna sospettare la malaria cerebrale). Il respiro profondo può essere segno diacidosi metabolica.L'opistotono può essere importante e simulare iltetanoo lameningite.La pressione liquorale può aumentare molto a differenza degli adulti. Il 10% dei bimbi che sopravvivono alla malaria cerebrale hanno sequele neurologiche persistenti (emiparesi, atassia cerebellare, cecità corticale, ipotonia severa, ritardo mentale, afasia, spasticità generalizzata).
Anemia
[modifica|modifica wikitesto]Molto comune nella malaria severa, soprattutto nei bimbi africani e nelle gravide, nei quali spesso è il segno di presentazione. La parassitemia spesso è bassa, ma c'è abbondante pigmento malarico neimonociti-macrofagi.L'anemiaè spesso associata asovrinfezionibatteriche.
Nei deficit congeniti di glucosio-6-fosfato deidrogenasi e in altri difetti enzimatici (deficit di piruvato chinasi), alcuni farmaci antimalarici, a effetto ossidante (es. primachina), possono provocare emolisi intravascolare e anemia importante, anche in assenza di malaria. Si riscontrano esempi diittero,febbricola o apiressia, con minima o nulla parassitemia (a differenza dell'emolisi massiva, che è abbastanza rara, in corso di iperparassitemia). È probabilmente scatenata dalla terapia con chinino e sono stati segnalati recentemente casi associati a meflochina e alofantrina. Tuttavia iltest di Coombsdiretto è negativo, a differenza delle comuniemolisiindotte dai farmaci.
Iperparassitemia
[modifica|modifica wikitesto]Nei soggetti non immuni, parassitemie >5% con schizontemia periferica sono segno prognostico sfavorevole. Nelle aree altamente endemiche, i bimbi semi-immuni possono sopportare parassitemie anche >20%, senza segni clinici evidenti.
Insufficienza renale
[modifica|modifica wikitesto]Complicanza quasi esclusiva dell'adulto. Aumentano lacreatininemia,l'azotemia.Compaionooliguriao anuria pernecrositubulare acuta: si verifica un danno al microcircolo renale per un meccanismo simile a quello del danno cerebrale (ischemia corticale e congestione midollare). A volte può esserci poliuria. L'insufficienza renale è reversibile.
Ipoglicemia
[modifica|modifica wikitesto]L'ipoglicemiasi verifica principalmente in tre gruppi di pazienti: nei bambini, nelle donne gravide, in pazienti trattati con chinino o chinidina (iperinsulinemia iatrogena). Nei pazienti coscienti si presenta classicamente con ansietà e disturbi del sensorio, sudorazione e senso di freddo, midriasi, dispnea, tachicardia, oliguria. Può precipitare rapidamente in coma ipoglicemico e convulsioni generalizzate e spesso può sfuggire perché nascosta o confusa dai segni della malaria cerebrale.
Alterazioni idro-elettrolitiche e dell'equilibrio acido-base
[modifica|modifica wikitesto]L'ipovolemia da disidratazione si manifesta con bassa pressione venosa giugulare,ipotensione posturale,oliguria con urine concentrate e ridotto turgore cutaneo. La cosiddetta “malaria algida” consiste in un collasso cardiocircolatorio, con ipotensione sistolica (<80 mmHg), cute fredda e cianotica, vasocostrizione periferica, polso flebile e rapido. Spesso è dovuta a una complicanza settica (setticemia da batteri Gram negativi).
Acidosi lattica
[modifica|modifica wikitesto]L'acidosi lattica,ovvero l'accumulazione di acido lattico nel corpo, è una complicanza pericolosa per la prognosi della persona. Si manifesta per via della glicosi anaerobia nei tessuti infetti. si rende evidente con comparsa di respiro profondo (di Kussmaul) e iperventilazione. Si verifica nei pazienti con shock, ipoglicemia, iperparassitemia, insufficienza renale.
Edema polmonare
[modifica|modifica wikitesto]È una complicanza grave (mortalità >50%) e tipica della malaria daP. falciparum(3-10%). Ricorda la sindrome da “distress” respiratorio acuto dell'adulto (Adult Respiratory Distress Syndrome,ARDS). Ha un'insorgenza relativamente tardiva e improvvisa durante la malaria da P. falciparum, anche alcuni giorni dopo che si sia instaurata un'adeguata terapia antiparassitaria, quando le condizioni cliniche migliorano e la parassitemia periferica sta diminuendo. Tuttavia spesso è associata alle altre forme di malaria severa. Si manifesta con tachipnea edispnea.Può precipitare rapidamente con deterioramento del sensorio,convulsionie morte in poche ore. Sono stati proposti diversi meccanismi patogenetici: l'aumento della permeabilità capillare da microemboli in corso di CID, lo scompenso dei capillari alveolari, lo scompenso del microcircolo polmonare, per aumento delle resistenze vascolari, conseguenza di fenomeni immunomediati, il sovraccarico iatrogeno di fluidi, l'ipoalbuminemia. Gli alveoli polmonari vengono inondati da liquido trasudatizio rendendo impossibili gli scambi gassosi. Laradiografiadeltorace[54]nei casi più gravi, mostra diffusi bilaterali infiltrati alveolari e interstiziali, periferici e confluenti.
Coagulopatia da consumo
[modifica|modifica wikitesto]È dettacoagulazione intravascolare disseminata(CID), in senso improprio, perché si hanno manifestazioni trombotiche alternate a manifestazioni emorragiche, sanguinamenti spontanei: gengivorragie, epistassi,petecchie,emorragie sottocongiuntivali,ematemesi,melena(<10% dei casi, soprattutto nei non immuni).[55]La trombocitopenia può essere presente (sequestro splenico, consumo), ma non è la causa dei sanguinamenti (la conta piastrinica torna normale con il trattamento della malaria), i quali invece sono provocati dal consumo dei fattori della coagulazione attivati in modo incontrollato.
Ipertermia
[modifica|modifica wikitesto]Il notevoleaumento della temperatura corporea,molto comune nei bimbi, è associato a convulsioni, delirio, coma. Entra in diagnosi differenziale con il colpo di calore. Temperature corporee >42 °C possono dare danni neurologici permanenti.
Malaria in gravidanza
[modifica|modifica wikitesto]La malaria durante la gravidanza è molto pericolosa, con una mortalità fino a 10 volte più alta che nella popolazione generale, caratterizzata da alta parassitemia, con pericoli per madre e feto (stress fetale, aborto, parto prematuro, basso peso alla nascita). Le gravide sono particolarmente suscettibili all'ipoglicemia e all'edema polmonare. Nelle semi-immuni (soprattutto primigravide) è più comune l'anemia. Complicanze settiche comuni sono le polmoniti e le infezioni urinarie.[56]
Diagnosi
[modifica|modifica wikitesto]Esami di laboratorio e strumentali
[modifica|modifica wikitesto]
Esami bioumorali
[modifica|modifica wikitesto]Anemia normocromica e normocitica progressiva, aumento dei reticolociti, bassaaptoglobina,alte bilirubinemia indiretta e LDH. Trombocitopenia (100.000/mm3). Leucocitosi o leucopenia. L'aumento della transaminasemia e bilirubinemia diretta, se importanti, sono segno prognostico sfavorevole di insufficienza epatica. Fibrinogenemia elevata (se bassa è segno sfavorevole per consumo o insufficiente produzione), PCR elevata, γ-globuline elevate, albuminemia ridotta.
Esami microbiologici
[modifica|modifica wikitesto]La microscopia ottica, i test diagnostici rapidi immunocromatografici e i metodi molecolari sono ampiamente utilizzati per diagnosticare la malaria[57].La diagnosi microbiologica d'infezione da plasmodi trova tuttora il suo punto di riferimento nell'emoscopiatramite striscio sottile e goccia spessa ed opportuna colorazione (soprattutto tramitecolorazione di Giemsa,WrightoField)[58].
Il campione da sottoporre ad indagine emoscopica dovrebbe essere prelevato daicapillariperiferici (ad esempio tramite puntura su polpastrello o su lobo auricolare) ove i plasmodi tendono a concentrarsi maggiormente. Il prelievo di sanguevenosoperiferico raccolto in provette contenentianticoagulanti(tipoEDTAedeparina) potrebbe creare qualche problema in caso di bassa parassitemia, e quindi dare un risultato falsamente negativo, e dovrebbe, comunque, essere sottoposto ad indagine in breve tempo, massimo un'ora, onde evitare alterazioni nella morfologia dei globuli bianchi e dei plasmodi. È da ricordare, inoltre, che l'anticoagulante non permette una defibrinizzazione ottimale durante la preparazione d'una goccia spessa che risulterà così, maggiormente ricca di detriti e di più difficile interpretazione.
Oltre a queste metodiche se ne sono aggiunte successivamente altre le quali, comunque, possono presentare alcuni inconvenienti quali una sensibilità ridotta rispetto all'emoscopia oppure essere al di fuori della portata dei laboratori comuni soprattutto nei paesi a risorse limitate. Tra le metodologie diagnostiche alternative ritroviamo:
- lafluorescenza,
- ilbuffy coatquantitativo (Quantitative Buff Coat)
- l'immunocromatografia(test rapidi), reperibili anche in Italia, che servono per rintracciare nel sangue la glicoproteina di tipo 2 (un antigene) o altri di recente studio.[59]
- metodiche immunologiche su siero
- metodiche dibiologia molecolare,dove si effettuano studi sul dna del parassita e si somministrano enzimi a carattere restrittivo, anche se praticamente tali pratiche vengono applicate di rado nella diagnostica attuale per via dell'elevatissima tecnologia non sempre presente.[59]La diagnosi molecolare risulta utile per comprendere quali siano le resistenze ai farmaci e utilizzare quelli più appropriati.[60]
Lo striscio sottile
[modifica|modifica wikitesto]L'emoscopia tramite striscio sottile, è una metodica di facile preparazione ed alla portata di pressoché tutti i laboratori. È un esame indispensabile per la diagnosi di specie in quanto consente l'identificazione morfologica dei parassiti ematici (è da ricordare, inoltre, che tale esame viene utilizzato anche per la diagnosi delle altre emoparassitosi come latripanosomiasi,laleishmaniosie lababesiosi).[61]
Per preparare uno striscio sottile basta pungere, con un aghetto sterile, un polpastrello od un lobo auricolare, dopo averli sgrassati e disinfettati, e porre una goccia di sangue ad un'estremità d'un vetrino accuratamente pulito e sgrassato.
Si utilizza, poi, un secondo vetrino il cui bordo più piccolo viene messo a contatto della goccia formando un angolo acuto col vetrino precedente in maniera tale che la goccia si disponga lungo tutta la linea del bordo stesso. Successivamente il secondo vetrino viene strisciato sul primo in maniera tale che tutti i globuli rossi si dispongano a formare un singolo strato. A questo punto il vetrino viene asciugato all'aria, fissato inmetanoloe colorato in maniera opportuna[62].
La lettura d'uno striscio sottile richiede una buona dose d'esperienza in quanto bisogna osservare un elevato numero di campi microscopici, muovendosi a serpentina su tutto il vetrino, prima di stilare un referto di negatività e prestare molta attenzione in quanto talvolta i globuli rossi infetti possono assumere una morfologia altamente atipica e confondersi con altri elementi cellulari. Un altro fattore da considerare è la possibilità d'una carica parassitaria bassa per cui bisogna prestare molta attenzione ad individuare gli eventuali pochi globuli rossi infetti od i possibili elementi extraeritrocitari.
La metodica dello striscio sottile permette anche una quantificazione della carica parassitaria il che rappresenta un elemento utile nella valutazione della risposta terapeutica.[63]
Per effettuare la quantificazione si contano i globuli rossi parassitati in 25 campi microscopici (usando l'oculare ad immersione) e lo si rapporta al numero totali di globuli rossi negli stessi campi e si moltiplica il risultato per 100.
In caso di presenza di numerosi plasmodi, preferenzialmente in aree endemiche, si può effettuare il conteggio su 10 campi.
La goccia spessa
[modifica|modifica wikitesto]La metodica della goccia spessa permette d'esaminare una quantità di sangue molto maggiore rispetto allo striscio sottile (circa 20 volte) determinando, così, un aumento della sensibilità soprattutto in caso di parassitemia bassa. L'identificazione morfologica, invece, risulta essere molto più difficoltosa in quanto, con la rottura dei globuli rossi che si determina, vari elementi utili per la diagnosi di specie, come ad esempio le granulazioni intraeritrocitarie, vengono persi. È proprio per ovviare a tale problema che nella prassi quotidiana vengono effettuate entrambe le metodiche.
Per preparare una goccia spessa si depongono su un vetrino 2 o 3 gocce di sangue, prelevate con le stesse modalità dello striscio sottile. Con un oggetto appuntito come un aghetto o l'angolo d'un altro vetrino si eseguono movimenti circolari che miscelano le gocce e le spianano su un'area di circa 2 cm di diametro. Tale operazione risulta necessaria al fine d'eliminare i frustoletti difibrina.
Successivamente il vetrino viene lasciato all'aria per circa 12 ore e dopo di ciò si procede direttamente alla colorazione. Il vetrino non va asciugato alcalorené fissato. Ciò è dovuto al fatto che i globuli rossi durante la fase di colorazione si lisano ed un precedente fissaggio impedisce che tale fenomeno si verifichi[64].
La fase di lettura di una goccia spessa richiede un'elevata accuratezza ed esperienza in quanto i plasmodi possono confondersi con detriti cellulari epiastrine
Anche tramite la goccia spessa è possibile valutare la parassitemia. Ciò viene fatto contando via via il numero di parassiti ed il numero diglobuli bianchipresenti (si devono conteggiare almeno 200 globuli bianchi o 500). Il risultato del rapporto di questi due valori viene poi moltiplicato con il valore dei globuli bianchi per microlitro di sangue. Nel caso in cui la formula leucocitaria non sia disponibile si può usare un valore medio di 8 000 globuli bianchi per microlitro.
Parassiti/μl = (Numero parassiti contati/ Numero globuli bianchi contati (200 oppure 500)) x Numero dei globuli bianchi/μl (in mancanza di esso 8 000 globuli bianchi/μl)
È da notare che i valori di parassitemia espressa in percentuale e in numero di parassiti/μl sono intercambiabili conoscendo il numero totale dei globuli rossi oppure utilizzando un valore medio ().
Ad esempio, una parassitemia dell'1% corrisponde ad un valore di 50 000 parassiti per microlitro (infatti, 1/100= 0,01 da cui 0,01 X 5 000 000=50 000 parassiti/μl).
Metodiche basate sulla fluorescenza
[modifica|modifica wikitesto]L'utilizzo delmicroscopio a fluorescenzanella diagnostica della malaria si basa sull'uso dicolorantifluorescentiin grado di legarsi preferenzialmente alDNAo all'RNAche andranno a colorare il materiale genetico del plasmodio che spiccherà rispetto al globulo rosso[65][66].
I coloranti maggiormente utilizzati a livello internazionale sono l'arancio di acridina,labenzotiocarbossipurinaod ilDAPI-PI(4,6-diamidino-2-fenilindolo propidio ioduro).[67][68][69][70]
Larodamina-123,invece, viene utilizzata per la sua capacità di legarsi alla membrana dei plasmodi ancora attivi permettendo, pertanto, una valutazione della loro vitalità.[71]
Una variante delle metodiche a fluorescenza è stata proposta da Kawamoto nel 1991. Essa prevede non più l'uso della lampada a fluorescenza, costosa e di manutenzione difficile, ma l'uso di una serie di lenti interferenti che convogliano, sul preparato colorato con arancio di acridina, unalucedilunghezza d'ondatale da poter eccitare il colorante.[72]
Tali metodiche risultano assai rapide e facili da eseguire, presentano inoltre una sensibilità maggiore rispetto alla colorazione con Giemsa; si tratta però di metodologie che richiedono un'attrezzatura di difficile reperimento in paesi a risorse limitate, e che necessitano di operatori esperti che sappiano distinguere i plasmodi da cellule o frammenti cellulari contenenti materiale genetico.
Si consiglia, comunque, sempre un affiancamento con le metodiche dello striscio sottile e della goccia spessa.
Una metodica simile, ilquantitative buffy coat,si basa sulla valutazione del sangue in un capillare da ematocrito, centrifugato, in modo da separarne le componenti, e studiato al microscopio a fluorescenza: nello strato dei globuli rossi, separato dai globuli bianchi, risalteranno i globuli rossi parassitati.
Altre metodiche
[modifica|modifica wikitesto]L'esame emoscopico non consente sempre di fare diagnosi o di escludere la malaria. La presenza dei plasmodi nel sangue di turisti o pazienti che non vivono in zona endemica è segno inequivocabile di malaria, ma è possibile che, temporaneamente, non si trovino parassiti in circolo, perché sequestrati nei capillari, o per autotrattamenti empirici e inadeguati. Nelle zone di endemia la diagnosi di malaria può essere controversa. Gli indigeni possono vivere, con parassitemie che raggiungono anche il 20%, in completo benessere, pertanto la positività dell'esame emoscopico non consente con certezza la diagnosi di malaria. Il fatto che i sintomi tipici di malaria eventualmente regrediscano con il trattamento anti-malarico, non consente la diagnosi “ex-juvantibus”, poiché molte virosi guariscono spontaneamente e molti antimalarici hanno anche un'azione antiflogistica.
Recentemente, sfruttando le metodiche immuno-isto-chimiche, sono stati introdotti nuovi test rapidi per la diagnosi di infezione. Una si basa sulla ricerca nel siero del paziente di un antigene del plasmodio (histidine rich protein-2, HRP-2) specialmente diP. falciparumeP. vivax(es. ParaSight, ICT Pf). Un'altra si basa sulla ricerca della lattato-deidrogenasi specifica diPlasmodium(pLDH) sia evidenziando la sua attività enzimatica, sia con “immunoassay” (es. Optimal).[73]
Diagnosi differenziale
[modifica|modifica wikitesto]Uno stato di malessere generale con febbre, insorto in viaggiatori tornati da almeno un mese da zone endemiche, deve far pensare principalmente alla malaria, ma vanno considerate anche la tripanosomiasi africana (malattia del sonno), la febbre dengue, leptospirosi, la febbre tifoide e altre patologie febbrili d'importazione, influenza e altre virosi, infezione acuta da HIV, batteriemia, polmonite.
Diagnosi precoce
[modifica|modifica wikitesto]L'anamnesiè la raccolta di tutti gli elementi utili da parte del medico attraverso un interrogatorio al paziente. Il medico deve chiedere se la persona che accusa i sintomi di malaria abbia soggiornato di recente (per i turisti) in paesi ad alto rischio o se abbia soggiornato per molto tempo (per gli immigrati) in regioni endemiche per malaria. Ilmedicodeve poi comprendere quale possa essere stata l'eventuale modalità di trasmissione del microorganismo e chiedere quindi di punture di insetti otrasfusionieseguite.
Trattamento
[modifica|modifica wikitesto]Trattamento farmacologico
[modifica|modifica wikitesto]


Il farmaco più efficace nel trattamento dell'infezione daP. falciparumè l'artemisinina,in combinazione con altri antimalarici quali:[74]
- clorochinaper la malaria causata daPlasmodium falciparumsensibile,Plasmodium malariae,P.vivaxe P.ovale(associata negli ultimi due casi aprimachinaper uccidere anche gli ipnozoiti)
- chininaper oso, in caso di infezioni gravi,chinidinaendovena, associata adoxiciclina,oclindamicinanei bambini, per ridurne la durata della terapia per la malaria causata daPlasmodium falciparumresistente alla clorochina e in zone endemiche
I farmaci anti-malarici impiegati nella terapia della malaria non sono necessariamente gli stessi validi per la profilassi anti-malarica e non lo sono le posologie con cui sono impiegati. Alcuni di essi hanno importanti controindicazioni ed effetti collaterali.
I principi attivi utilizzati sono:
- Alofantrina:combatte lo stadio eritrocitario delP. falciparum
- Artemetereassociato a lumefantrina
- Chinino
- Clorochina
- Meflochina:per il trattamento chemioprofilattico delP. vivax
- Pirimetaminaassociata asulfadossina:contro ilP. falciparum
- Primachina:controP. vivaxeP. ovale
- Proguanil cloridrato:per il trattamento chemioprofilattico controP. falciparumoP. vivax.L'abbinamento adatovaquoneè detto “malarone”
Esistono anche alcuni principi attivi che sono stati utilizzati in aggiunta sperimentale:
- Doxiciclina:perP. falciparum
- Propranololo
Pattern di resistenza ai farmaci anti-malarici
[modifica|modifica wikitesto]Distribuzione dellefarmaco-resistenze:[32]
- La Zona A è caratterizzata dalla presenza di ceppi di plasmodio sensibili allaclorochina;è ormai limitata all'America centrale, ai Caraibi e alMedio Oriente.
- La Zona B è caratterizzata dalla prevalenza diP. vivax,con presenza di ceppi diP. falciparumresistenti alla clorochina, e comprende il subcontinente Indiano e l'Iran.
- La Zona C interessa tutte le altre regioni malariche, nelle quali prevalgono ceppi diP. falciparumclorochino-resistenti.
Questa è una classificazione a grandi linee, perché l'epidemiologiadella malaria e i "pattern" difarmaco-resistenzavariano molto, spesso anche a distanza di pochi chilometri, e sono in continua evoluzione, a causa dell'impiego intensivo e spesso improprio deifarmaci antimalarici,ma anche influenzati da sconvolgimentiecologicie disastri naturali (per esempiouraganietifoni). Inoltre, va considerata la recente comparsa di meflochino-resistenza nelle zone silvestri al confine traThailandiaeBirmaniae Thailandia eCambogia.[75]
Prevenzione
[modifica|modifica wikitesto]
Il sistema migliore per non ammalarsi di malaria è evitare di essere punti dalla zanzara vettore.
Comprendendo fin dai tempi antichi le cause che favoriscono il nascere della malaria negli ultimi tempi si è pensato a come prevenire l'insorgere del morbo nei paesi industrializzati come in quelli in via di sviluppo. Fino al 1945 le tecniche furono le continuebonifichee la distruzione delle larve mediante sali d'arsenico.[76]
Negli anni cinquanta e negli anni sessanta, c'è stato un notevole sforzo della sanità pubblica per eradicare la malaria distruggendo le zanzare nelle zone dove la malattia era diffusa,[77]anche se questi sforzi non sono riusciti a sradicare la malaria in molte parti del mondo, soprattutto in molte zone dell'Africa, per via dello sviluppo di zanzare che resistono agli insetticidi.
Nel1998l'OMScambiò la sua strategia istituendo la "Roll Back Malaria"dove fra le varie iniziative tuttora si tende all'istruzione della popolazioneafricana,come ad esempio a far riconoscere ai bambini lelarvedelle zanzare e convincere le madri a far visitare i loro bambini quando presentano i primi sintomi.[78]
La zanzara femmina dell'Anophelespunge preferibilmente di notte, tra il tramonto e l'alba, pertanto i viaggiatori dovrebbero evitare le punture d'insetto soprattutto in queste ore. Si consiglia di vestirsi evitando i colori scuri, coprendosi il più possibile, e di usare sulla pelle esposta (volto e mani)spraye sostanze repellenti per gli insetti, di dormire in stanze trattate precedentemente con insetticida, dormendo coperti dalle apposite reti protettive impregnate con insetticida o con repellente. Il repellente più efficace è il DEET (N,N-dietilmetatoluamide). Tra gli insetticidi si può usare lapermetrina.
Inoltre, l'aria condizionatarende gli insetti meno attivi e quindi meno pericolosi.
Immunità passiva
[modifica|modifica wikitesto]Nelle areeendemichei bimbi sono protetti per i primi 6 mesi dall'immunitàpassiva materna, data daglianticorpiereditati dalla madre, poi si ha una progressiva acquisizione di una "semi-immunità", per successive esposizioni alle infezioni del plasmodio. Si hanno ricorrenti attacchi di malaria, dall'età di pochi mesi fino a 5-10 anni, prima di raggiungere uno stato di semi-immunità. Molti bimbi soffrono di ritardo di crescita e altri muoiono. Se i bimbi sopravvivono, mantengono la semi-immunità per continue reinfezioni, per tutta la vita, finché risiedono in area endemica.
La semi-immunità può calare temporaneamente durante lagravidanza(con conseguenza anche drammatiche, soprattutto nelle primigravide) e si attenua col tempo negli individui che abbandonano le zone endemiche (scompare dopo 2 anni di distanza). Questa viene considerata una semi-immunità perché durante la vita si hanno ugualmente ricorrenti episodi di parassitemia, di breve durata e bassa carica, per lo più asintomatici o paucisintomatici (con pochi sintomi).[79]
Fenomeni genetici e biochimici
[modifica|modifica wikitesto]Mutazioni dell'emoglobina(S,C, beta e alfatalassemie), deglienzimiglucosio-6-fosfato deidrogenasiepiruvato chinasi,proteggono dalle forme gravi di malaria provocate daP. falciparumin portatorieterozigotie nel caso dell'emoglobina C soprattutto inomozigosi.Le particolari proprietà delle catene dell'emoglobina e le condizioni distress ossidativoprovocate dell'infezione stessa, possono provocare l'emolisi degli eritrociti ostacolando la maturazione dei trofozoiti. Nonostante questemutazionisiano dannose (quasi sempre in omozigosi sono letali), grazie alla protezione conferita nei confronti della malaria si trovano ad alte frequenze in popolazioni che vivono in zone endemiche (o ex endemiche) per malaria (bacino del mediterraneo, Africa sub-sahariana, sud-est asiatico). Tranne per l'emoglobina C, in queste popolazioni la frequenza delle mutazioni di resistenza è comunque destinata ad arrivare ad un valore di equilibrio (intorno al 15-20%) che rispecchia lo svantaggio dovuto alla letalità della mutazione ed il vantaggio rispetto alla malaria. Nelle zone non malariche, queste mutazioni generalmente sono molto rare o assenti poiché la loro letalità non è controbilanciata da effetti positivi.
Un esempio molto interessante è quello dell'evoluzione dell'antigene eritrocitarioDuffy,il recettore attraverso il quale i merozoiti diP. vivaxpenetrano il globulo rosso. Gli eritrociti che non hanno questo antigene (Duffy negativi) sono refrattari all'infezione da parte di quel plasmodio. In Africa occidentale, una mutazione che elimina l'antigene dalla superficie degli eritrociti ma che non ha altre conseguenze cliniche ha raggiunto (probabilmente in varie migliaia di anni) la frequenza del 100% e quindi la maggior parte degli abitanti dell'Africa centrale e occidentale non viene infettata da questa specie di plasmodio.
Chemio-profilassi
[modifica|modifica wikitesto]La chemioprofilassi antimalarica si basa sul principio secondo il quale si raggiunge e si mantiene una concentrazione plasmatica di un farmaco anti-malarico a livelli bassi per essere curativi ma sufficienti a impedire che si sviluppi la malattia dopo una puntura della zanzara e l'infezione da parte del plasmodio. Tale concentrazione deve essere mantenuta per tutto il periodo in cui si è potenzialmente esposti alla malattia, cioè per tutto il periodo di permanenza in zona malarica e fino almeno a 4 settimane dopo il ritorno, pertanto solitamente si inizia la profilassi per tempo, 1 o 2 settimane prima di partire.
- Per la profilassi in zone malariche di clorochino-sensibilità, si impiega efficacemente laclorochina300 mg base (500 mg sale) per via orale, una volta alla settimana (dose pediatrica 5 mg/kg base (8,3 mg/kg sale) per via orale, una volta alla settimana, senza superare la dose massima dell'adulto di 300 mg base. Nell'Africa francofona si usa quotidianamente la nivachina (clorochina) in pasticche da 100 mg in maniera da mantenere costante nel tempo il dosaggio del prodotto nel sangue.
- Per la profilassi in zone malariche di clorochino-resistenza, si impiega lameflochina(Lariam) 228 mg base (250 mg sale, 1 compressa) per via orale, una volta alla settimana. Le dosi pediatriche variano secondo il peso:
- sotto i 9 kg: 4,6 mg/kg base (5 mg/kg sale) per via orale, una volta alla settimana
- tra 10–19 kg: un quarto di compressa una volta alla settimana
- tra 20–30 kg: mezza compressa una volta alla settimana
- tra 31–45 kg: tre quarti di compressa una volta alla settimana
- Per la profilassi in zone malariche di clorochino-resistenza e meflochino-resistenza (per es. in zone della Thailandia) si può impiegare ladoxiciclinaper via orale 100 mg al giorno. Nei bambini è solitamente sconsigliata;
- in quelli che pesano meno di 25 kg o hanno meno di 8 anni è controindicato;
- da 25 a 35 kg di peso oppure da 8 a 10 anni: mezza compressa al giorno
- da 36 a 50 kg di peso oppure da 11 a 13 anni: tre quarti di compressa al giorno
- da 50 kg di peso in poi oppure da 14 anni in poi: 1 compressa al giorno
- In alternativa, nelle zone con multiresistenze, si può impiegare ilMalarone(Atovaquone250 mg +Proguanil100 mg, 1 compressa). La dose per adulti è 1 compressa al giorno, iniziando 1-2 giorni prima di entrare nella zona a rischio e continuando fino a una settimana dopo l'uscita dalla zona.
- Nei bambini da 11 a 20 kg di peso: un quarto di compressa degli adulti
- da 21 a 30 kg di peso: mezza compressa degli adulti
- da 31 a 40 kg di peso: tre quarti di compressa degli adulti
- oltre 40 kg dose degli adulti.
Vaccini
[modifica|modifica wikitesto]Ci sono molti progetti per lo sviluppo di un vaccino efficace, ma nessuno ancora disponibile e impiegabile in larga scala.[80]
Molte associazioni sono nate con il preciso scopo di individuare un vaccino che possa ostacolare efficacemente la malaria,[81]o sono state incaricate di farlo,[82]ma secondo la ricerca scientifica lo sviluppo di un vaccino dovrebbe essere accompagnato da un impegno parallelo per migliorare gli strumenti diagnostici e la loro disponibilità nelle zone a rischio.[83]
Molte discussioni di carattere economico nascono attorno allo studio della malaria, fra le tante alcune di esse affermano che con lo stesso importo che si sta utilizzando per la ricerca dell'AIDSsi potrebbero avere più benefici per la popolazione africana se tali entrate venissero dirottate verso lo studio del paludismo.[84]
Tra 2019 e 2021 è stato sperimentato un vaccino, realizzato dalla multinazionale farmaceuticaGlaxoSmithKline,chiamatoMosquirix,indirizzato a sviluppare immunità controP. falciparumnei bambini che vivono in paesi ad alto rischio. Si somministra in 4 dosi a partire dai 5 mesi d’età. L'Organizzazione mondiale della sanitàil 6 ottobre 2021 ne ha raccomandato l'uso di massa come primo vaccino contro la malaria per i bambini.[85][86][87][88][89][90]Il vaccino, che ha ottenuto l'autorizzazione da parte delWHO,sarà utilizzato nel 2024 sui bambini delGhana,CameruneBurkina Faso[91].
Nell’aprile 2019 è stato annunciato l’inizio della fase III di un test clinico nell’isola diBioko,cominciato all’inizio del 2020, da parte di Sanaria delvaccino PfSPZ.
Nel 2023 è stato approvato in Ghana l'uso di un nuovo vaccino che ha un'efficacia di oltre il 75%, ilR21/Matrix-M,sviluppato dall'università di Oxford.[92]Nel 2024 il vaccino è stato lanciato anche nellaCosta d'Avorio.[93]
Prevenzione primaria
[modifica|modifica wikitesto]Fra i metodi alternativi si sta studiando la possibilità disterilizzaregli insetti, in tali casi serve un'applicazione continua e rapida. Vi sono stati dei risultati, ma bisogna confrontare i dati rapportandoli ad un progetto di più lunga durata.[94]Particolarmente promettenti appaiono due filoni di ricerche nell'ambito della tecnica CRISPR Cas: uno che mira alla scomparsa delle specie di zanzara tramite la diffusione di maschi geneticamente modificati per dare una progenie esclusivamente maschile, portandole all'estinzione in circa 6 generazioni, e un altro che induce nei loro sistemi immunitari la produzione di un anticorpo anti plasmodio.
Prognosi
[modifica|modifica wikitesto]
nessun dato
<10
0–100
100–500
500–1000
1000–1500
1500–2000
2000–2500
2500–2750
2750–3000
3000–3250
3250–3500
≥3500
Se trattati correttamente gli individui colpiti da malaria possono, solitamente, aspettarsi un completo recupero.[95]Tuttavia, la malaria severa può progredire molto rapidamente e causare la morte entro poche ore o giorni.[96]Nei casi più gravi della malattia, iltasso di mortalitàpuò raggiungere il 20 %, anche con il trattamento e il ricorso allaterapia intensiva. [97]Nel lungo periodo, menomazioni di sviluppo sono state documentate nei bambini che hanno sofferto di episodi di malaria grave.[98]L'infezione cronica può verificarsi, una forma di immunodeficienza acquisita, dove ilsistema immunitarioè anche meno sensibile allaSalmonellae alvirus di Epstein-Barr.[99]
La malaria provocaanemiadiffusa durante un periodo di rapido sviluppo del cervello e danni cerebrali, anche diretti. I bambini risultano più vulnerabili a questi attacchi.[98]Alcuni superstiti di malaria cerebrale presentano un aumentato rischio di sviluppare deficit neurologici e cognitivi, disturbi del comportamento edepilessia.[100]Gli studi clinici hanno dimostrato che laprofilassidella malaria è in grado di migliorare la funzione cognitiva e il rendimento scolastico, rispetto al gruppoplacebo.[98]
Nell'arte
[modifica|modifica wikitesto]Letteratura
[modifica|modifica wikitesto]La malaria viene spesso citata nellaletteratura,spesso correlata ad ambientazioni esotiche, come nei romanzi diEmilio Salgari,ma anche in contesti occidentali, come nelleNovelle rusticanediGiovanni Verga(1883)[101].
La malattia compare anche come morbo endemico nel libro diCarlo Levi,Cristo si è fermato a Eboli:l'autore, in quanto medico, cura i malati del piccolo paese in cui trascorre il confino a causa della sua avversione al fascismo. Celebre, inoltre, è la descrizione dell'arrivo a Matera della sorella dello scrittore, a cui si fanno incontro i bambini della città chiedendo ilChinino,uno dei farmaci più efficaci di allora contro la malaria.[102]
La malattia è riportata anche nel libroEbanodel reporter polaccoRyszard Kapuściński,sia per l'esperienza personale sia per la descrizione, in poche righe ma estremamente vivida, di persone in fase terminale in un villaggio africano.
La malaria in Italia
[modifica|modifica wikitesto]Nel 1882, solo in due provincie Italiane (Imperia e Macerata) non si registrarono infezioni. La mappa delle aree malariche pubblicata nello stesso anno per volontà del senatoreLuigi Torellievidenziava come le aree dove la malattia era presente rappresentavano un terzo della superficie totale del Paese, mentre erano regolarmente colpiti 3.075 comuni su 8.362.[103]Nel 1887 i decessi dovuti alla malattia furono 21.033, di cui 18.730 nelle sole regioni meridionali e nel Lazio.[104]
Poiché oggi inItaliala malaria è stata eradicata, vi si registrano solo sporadici singoli casi autoctoni. La maggior parte degli episodi che si manifestano è di importazione: colpisceturisti,viaggiatori o immigrati provenienti dalle aree endemiche.[105]Per quanto riguarda i casi registrati internamente al paese, nel 1970 l'Organizzazione mondiale della sanità(OMS) ha dichiarato l'Italia come zona indenne dal pericolo della comparsa di focolai di malaria. Gli eventi erano già comunque molto ridotti. Nel 1962 era stato segnalato inSiciliaun focolaio autoctono di malaria daP. vivax,[106]quasi 40 anni dopo l'ultimo focolaio registrato. Ormai in Italia si verificano soltanto sporadicamente singoli casi autoctoni, soprattutto nelle regioni centro-meridionali e insulari.[107]L'ultimo decesso per malaria in Italia è stato registrato aBrescianel 2017.[108]
Note
[modifica|modifica wikitesto]- ^Gaetano Filice,Malattie infettive, 2ª edizione, pag 518,Milano, McGraw-Hill, 1998,ISBN88-386-2362-7.
- ^Douglas M. Anderson, A. Elliot Michelle,Mosby's medical, nursing, & Allied Health Dictionary sesta edizione Volume I, pag 900,New York, Piccin, 2004,ISBN88-299-1716-8.
- ^Lee Goldman e Andrew Schafer,Goldman-Cecil Medicina Interna,Edra, 30 giugno 2017, pp. 8240–,ISBN978-88-214-4185-1.
- ^Collegamento tra talassemia e malaria,sufondazioneveronesi.it.
- ^Crotti D.,A history of Malaria from and for a popular point of view,inInfez Med,vol. 4, 2005, pp. 265-270.
- ^abcClaudio Genchi, Pozio Edoardo,Parassitologia generale e umana, 13ª edizione pag 224,Milano, Ambrosiana, 2004,ISBN88-408-1269-5.
- ^Escalante A, Freeland D, Collins W, Lal A,The evolution of primate malaria parasites based on the gene encoding cytochrome b from the linear mitochondrial genome.,inProc Natl Acad Sci U S A,vol. 95, n. 14, 1998, pp. 8124-9,PMID9653151.
- ^Joy D, Feng X, Mu J,et al,Early origin and recent expansion of Plasmodium falciparum.,inScience,vol. 300, n. 5617, 2003, pp. 318-21,PMID12690197.
- ^Cox F,History of human parasitology.,inClin Microbiol Rev,vol. 15, n. 4, 2002, pp. 595-612,PMID12364371.
- ^(EN) Pappas G, Kiriaze IJ, Falagas ME.,Insights into infectious disease in the era of Hippocrates.,inInt J Infect Dis.,2008.
- ^http://www.cell.com/current-biology/fulltext/S0960-9822(16)31201-5
- ^http://www.lescienze.it/news/2016/12/06/news/malaria_impero_romano-3341709/
- ^spp. abbreviazione dispecie(plurale).
- ^Biography of Alphonse Laveran,sunobelprize.org,The Nobel Foundation.URL consultato il 15 giugno 2007.] Nobel foundation. Ultimo accesso 25 ottobre 2006
- ^(EN) Ole Daniel Enersen,Ettore Marchiafava,inWho Named It?.
- ^Biography of Ronald Ross,sunobelprize.org,The Nobel Foundation.URL consultato il 15 giugno 2007.
- ^Grassi, Giovanni Battista,sutreccani.it.URL consultato il 25 marzo 2020(archiviato dall'url originalel'11 ottobre 2019).
- ^World Health Organization,World Malaria Day 2015,suwho.int,WHO, 25 aprile 2015(archiviato dall'url originaleil 25 aprile 2016).
- ^Gaetano Filice,Malattie infettive, 2ª edizione Pag 519,Milano, McGraw-Hill, 1998,ISBN88-386-2362-7.
- ^Hay S, Guerra C, Tatem A, Noor A, Snow R,The global distribution and population at risk of malaria: past, present, and future.,inLancet Infect Dis,vol. 4, n. 6, 2004, pp. 327-36,PMID15172341.
- ^Greenwood B, Mutabingwa T,Malaria in 2002,inNature,vol. 415, 2002, pp. 670–2,PMID11832954.
- ^Claudio Genchi, Pozio Edoardo,Parassitologia generale e umana, 13ª edizione pag 236-238,Milano, Ambrosiana, 2004,ISBN88-408-1269-5.
- ^Muturi EJ, Muriu S, Shililu J, Mwangangi J, Jacob BG, Mbogo C, Githure J, Novak RJ.,Effect of Rice Cultivation on Malaria Transmission in Central Kenya,inAm J Trop Med Hyg,vol. 78, 2008, pp. 270-275.
- ^P. falciparum,sucdfound.to.it(archiviato dall'url originaleil 6 settembre 2005).
- ^P. vivax,sucdfound.to.it(archiviato dall'url originaleil 29 novembre 2005).
- ^P. ovale,sucdfound.to.it(archiviato dall'url originaleil 14 aprile 2005).
- ^P. malariae,sucdfound.to.it(archiviato dall'url originaleil 27 novembre 2005).
- ^Chin W, Contacos PG, Coatney RG, Kimbal HR.,A naturally acquired quotidian-type malaria in man transferable to monkeys,inScience,vol. 149, 1965, p. 865,PMID14332847.
- ^Singh B, Lee KS, Matusop A, Radhakrishnan A, Shamsul SSG, Cox-Singh J, Thomas A, Conway DJ,A large focus of naturally acquiredPlasmodium knowlesiinfections in human beings,inLancet,vol. 363, 2004, pp. 1017–24,DOI:10.1016/S0140-6736(04)15836-4,ISSN0140-6736.
- ^Wharton RH, Eyles DE.,Anopheles hackeri,a vector ofPlasmodium knowlesiin Malaya,inScience,vol. 134, 1961, pp. 279–80.
- ^Collins WE, Jeffery GM..,Plasmodium malariae: parasite and disease.,inClin Microbiol Rev.,vol. 4, 2007, pp. 579-92.
- ^abTravelers' Health | CDC,suwwwnc.cdc.gov.URL consultato il 7 ottobre 2021.
- ^Guillet P, Germain MC, Giacomini T, Chandre F, Akogbeto M, Faye O,Dual Origin and prevention of airport malaria in France.,inTrop Med Int Hlth,vol. 3, 1998, pp. 700-705.
- ^Giacomini T, Goudal H, Boudon P, Rennes C, Dumouchel P, Petithory JC,A propos de deux cas de paludisme à Plasmodium falciparum. Responsabilité probable d'anophèles importés par voie aérienne,inBull Soc Path Ex,vol. 70, 1977, pp. 375-379.
- ^Giacomini T,Paludisme des aéroports et de leurs alentours,inRevue du Praticien,vol. 48, 1998, pp. 264-267.
- ^Pathogenesis of Malaria and Clinically Similar Conditions,sucmr.asm.org.
- ^Immagini dei diversi stadi di P. falciparum,sudpd.cdc.gov.URL consultato il 17 marzo 2020(archiviato dall'url originaleil 21 marzo 2008).
- ^Immagini dei diversi stadi di P. malariae,sudpd.cdc.gov.URL consultato il 17 marzo 2020(archiviato dall'url originaleil 19 marzo 2008).
- ^Immagini dei diversi stadi di P. ovale,sudpd.cdc.gov.URL consultato il 17 marzo 2020(archiviato dall'url originaleil 23 marzo 2008).
- ^Immagini dei diversi stadi di P. vivax,sudpd.cdc.gov.URL consultato il 17 marzo 2020(archiviato dall'url originaleil 23 marzo 2008).
- ^Krotoski W, Collins W, Bray R,et al,Demonstration of hypnozoites in sporozoite-transmitted Plasmodium vivax infection.,inAm J Trop Med Hyg,vol. 31, n. 6, 1982, pp. 1291-3,PMID6816080.
- ^Meis J, Verhave J, Jap P, Sinden R, Meuwissen J,Malaria parasites--discovery of the early liver form.,inNature,vol. 302, n. 5907, 1983, pp. 424-6,PMID6339945.
- ^Abu-Raddad L, Patnaik P, Kublin J,Dual infection with HIV and malaria fuels the spread of both diseases in sub-Saharan Africa,inScience,vol. 314, n. 5805, 2006, pp. 1603-6,PMID17158329.
- ^Alkhunaizi AM, Al-Tawfiq JA, Al-Shawaf MH.,Transfusion-transmitted malaria in a kidney transplant recipient. How safe is our blood transfusion?,inSaudi Med J.,vol. 2, 2008, pp. 293-295.
- ^abClaudio Genchi, Pozio Edoardo,Parassitologia generale e umana, 13ª edizione pag 233,Milano, Ambrosiana, 2004,ISBN88-408-1269-5.
- ^Malaria life cycle & pathogenesisArchiviatoil 18 gennaio 2008 inInternet Archive.Malaria in Armenia. Ultimo accesso 31 ottobre 2006
- ^R Idro, Otieno G, White S, Kahindi A, Fegan G, Ogutu B, Mithwani S, Maitland K, Neville BG, Newton CR,Decorticate, decerebrate and opisthotonic posturing and seizures in Kenyan children with cerebral malaria,inMalaria Journal,vol. 4, n. 57,PMID16336645.URL consultato il 21 gennaio 2007.
- ^Trampuz A, Jereb M, Muzlovic I, Prabhu R,Clinical review: Severe malaria.,inCrit Care,vol. 7, n. 4, 2003, pp. 315-23,PMID12930555.
- ^abRanque S, Poudiougou B, Traoré A, Keita M, Oumar AA, Safeukui I, Marquet S, Cabantous S, Diakité M, Mintha D, Cissé MB, Keita MM, Dessein AJ, Doumbo OK.,Life-Threatening Malaria in African Children: A Prospective Study in a Mesoendemic Urban Setting,inPediatr Infect Dis J.,vol. 2, 2008, pp. 130-135.
- ^Da qui il nome ingleseBlackwater fever,febbre dell'acqua nera.
- ^Oumar AA, Poudiougou B, Sylla M, Sall A, Konate S, Togo B, Diakite M, Keita MM.,Blackwater Blackwater fever in children during cerebral malaria: 3 case reports in Bamako,inArch Pediatr.,vol. 8, 2005, pp. 993-5.
- ^Gobbi F, Audagnotto S, Trentini L, Nkurunziza I, Corachan M, Di Perri G.,Blackwater fever in children, Burundi.,inEmerg Infect Dis.,vol. 7, 2005, pp. 1118-20.
- ^Allam MM, Alkadarou TA, Ahmed BG, Elkhair IS, Alansary EH, Ibrahim ME, Elhassan AM, Elhassan IM.,Hyper-reactive Malarial Splenomegaly (HMS) in malaria endemic area in Eastern Sudan.,inActa Trop.,2007.
- ^immagine da sito AtlasArchiviatoil 3 settembre 2005 inInternet Archive..
- ^Immagine bambino infettoArchiviatoil 14 settembre 2005 inInternet Archive.
- ^Impact of Malaria during Pregnancy on Low Birth Weight in Sub-Saharan Africa
- ^Christian Leli, Luigi Di Matteo e Franca Gotta,Clinical Utility of Platelet Count for Screening of Malaria,inThe New Microbiologica,vol. 43, n. 2, 2020-04, pp. 89–92.URL consultato il 5 novembre 2021.
- ^PLASMODIUM FALCIPARUMArchiviatol'8 settembre 2005 inInternet Archive.
- ^abClaudio Genchi, Pozio Edoardo,Parassitologia generale e umana, 13ª edizione pag 249,Milano, Ambrosiana, 2004,ISBN88-408-1269-5.
- ^Laufer MK, Djimdé AA, Plowe CV.,Monitoring and deterring drug-resistant malaria in the era of combination therapy.,inAm J Trop Med Hyg.,vol. 77, 2007, pp. 160-169.
- ^Immagine di Babesia canisArchiviatoil 1º febbraio 2008 inInternet Archive.
- ^immagine PLASMODIUM FALCIPARUMArchiviatoil 9 aprile 2005 inInternet Archive.
- ^Immagine globuli rossi PLASMODIUM FALCIPARUMArchiviatoil 4 settembre 2005 inInternet Archive.
- ^Immagine PLASMODIUM FALCIPARUMArchiviatoil 3 settembre 2005 inInternet Archive.
- ^PLASMODIUM FALCIPARUMArchiviatoil 5 settembre 2005 inInternet Archive.
- ^PLASMODIUM FALCIPARUMArchiviatoil 5 settembre 2005 inInternet Archive.
- ^Rapid diagnosis of malaria by use of fluorescent probes,suncbi.nlm.nih.gov.
- ^Acridine orange fluorescent microscopy and the detection of malaria in populations with low-density parasitemia
- ^Detection of Plasmodium falciparum infection with the fluorescent dye, benzothiocarboxypurine
- ^Acridine orange stained blood wet mounts for fluorescent detection of malaria,suncbi.nlm.nih.gov.
- ^A method for monitoring the viability of malaria parasites (Plasmodium yoelii) freed from the host erythrocytes
- ^Rapid diagnosis of malaria by fluorescence microscopy with light microscope and interference filter,suncbi.nlm.nih.gov.
- ^Rapid Diagnostic Tests for Malaria Parasites,sucmr.asm.org.
- ^Kokwaro G (2009). "Ongoing challenges in the management of malaria". Malaria Journal. 8 (Suppl 1): S2. PMC 2760237 Freely accessible.PMID 19818169.doi:10.1186/1475-2875-8-S1-S2. open access publication – free to read
- ^Malaria - Dipartimento della sanità pubblica e dell’innovazione Direzione generale dei rapporti europei ed internazionali Ufficio III – ex DGRUERI(PDF), susalute.gov.it.URL consultato il 25 marzo 2020(archiviato dall'url originalel'8 marzo 2014).
- ^Claudio Genchi, Pozio Edoardo,Parassitologia generale e umana, 13ª edizione pag 257,Milano, Ambrosiana, 2004,ISBN88-408-1269-5.
- ^Gladwell, Malcolm.,The Mosquito Killer,The New Yorker, 2 luglio 2001(archiviato dall'url originaleil 6 febbraio 2009).
- ^Claudio Genchi, Pozio Edoardo,Parassitologia generale e umana, 13ª edizione pag 258,Milano, Ambrosiana, 2004,ISBN88-408-1269-5.
- ^Articolo,sucmr.asm.org.
- ^Sicuro ed efficace il vaccino anti-malaria,sulescienze.espresso.repubblica.it,Le Scienze, 18 novembre 2007.URL consultato il 25 gennaio 2008.
- ^(EN) Kilama WL, Chilengi R, Wanga CL.,ATowards an African-driven malaria vaccine development program: history and activities of the African Malaria Network Trust (AMANET).,inAm J Trop Med Hyg.,vol. 77, 2007, pp. 282-288..
- ^(EN) Ballou WR, Cahill CP.,Two decades of commitment to malaria vaccine development: GlaxoSmithKline Biologicals.,inAm J Trop Med Hyg.,vol. 77, 2007, pp. 289-295.
- ^(EN) Wongsrichanalai C, Barcus MJ, Muth S, Sutamihardja A, Wernsdorfer WH.,A review of malaria diagnostic tools: microscopy and rapid diagnostic test (RDT).,inAm J Trop Med Hyg.,vol. 77, 2007, pp. 119-127.
- ^Hull, Kevin. (2006) "Malaria: Fever Wars". PBS DocumentaryArchiviatoil 18 gennaio 2008 inInternet Archive.
- ^Oms approva primo vaccino contro la malaria,suL'HuffPost,6 ottobre 2021.URL consultato il 7 ottobre 2021.
- ^Sky TG24,L'Oms raccomanda il primo vaccino contro la malaria per i bambini,sutg24.sky.it.URL consultato il 7 ottobre 2021.
- ^Il primo vaccino contro la malaria,suFondazione Umberto Veronesi.URL consultato il 7 ottobre 2021.
- ^Davies L,WHO endorses use of world's first malaria vaccine in Africa,inThe Guardian,6 ottobre 2021.URL consultato il 6 ottobre 2021.
- ^Drysdale C, Kelleher K,WHO recommends groundbreaking malaria vaccine for children at risk,suwho.int,Geneva,World Health Organization.URL consultato il 6 ottobre 2021.
- ^Mandavilli A,A 'Historical Event': First Malaria Vaccine Approved by W.H.O.,inThe New York Times,6 ottobre 2021.URL consultato il 6 ottobre 2021.
- ^(EN)Could new vaccines end malaria in Africa?,sualjazeera.com.URL consultato il 15 gennaio 2024.
- ^Sara Carmignani,Un nuovo vaccino promette di rivoluzionare la lotta alla malaria,suWired Italia,14 aprile 2023.URL consultato il 18 agosto 2024.
- ^(EN)Côte d’Ivoire makes history as first nation to deploy R21/Matrix-M™ Malaria Vaccine | University of Oxford,suwww.ox.ac.uk,15 luglio 2024.URL consultato il 18 agosto 2024.
- ^(EN) Fillinger U, Kannady K, William G, Vanek MJ, Dongus S, Nyika D, Geissbuehler Y, Chaki PP, Govella NJ, Mathenge EM, Singer BH, Mshinda H, Lindsay SW, Tanner M, Mtasiwa D, de Castro MC, Killeen GF.,A tool box for operational mosquito larval control: preliminary results and early lessons from the Urban Malaria Control Programme in Dar es Salaam, Tanzania.,inMalar J,vol. 7, gennaio 2008, p. 20..
- ^Frequently Asked Questions (FAQs): If I get malaria, will I have it for the rest of my life?,sucdc.gov,US Centers for Disease Control and Prevention, 8 febbraio 2010.URL consultato il 14 maggio 2012.
- ^Trampuz A, Jereb M, Muzlovic I, Prabhu R,Clinical review: Severe malaria,inCritical Care,vol. 7, n. 4, 2003, pp. 315–23,DOI:10.1186/cc2183,PMC270697,PMID12930555.
- ^Nadjm B, Behrens RH,Malaria: An update for physicians,inInfectious Disease Clinics of North America,vol. 26, n. 2, 2012, pp. 243–59,DOI:10.1016/j.idc.2012.03.010,PMID22632637.
- ^abcFernando SD, Rodrigo C, Rajapakse S,The 'hidden' burden of malaria: Cognitive impairment following infection,inMalaria Journal,vol. 9, 2010, p. 366,DOI:10.1186/1475-2875-9-366,PMC3018393,PMID21171998.
- ^Riley EM, Stewart VA,Immune mechanisms in malaria: New insights in vaccine development,inNature Medicine,vol. 19, n. 2, 2013, pp. 168–78,DOI:10.1038/nm.3083,PMID23389617.
- ^Idro R, Marsh K, John CC, Newton CRJ,Cerebral malaria: Mechanisms of brain injury and strategies for improved neuro-cognitive outcome,inPediatric Research,vol. 68, n. 4, 2010, pp. 267–74,DOI:10.1203/PDR.0b013e3181eee738,PMC3056312,PMID20606600.
- ^Testo in rete della "malaria",sudigilander.libero.it.URL consultato il 02-08-2008.
- ^Carlo Levi,Cristo si è fermato a Eboli,Einaudi, Torino, 1945.
- ^(EN) Frank M. Snowden,The Conquest of Malaria: Italy, 1900-1962,New Haven, Yale University Press, 2006,ISBN9780300108996.
- ^On. Francesco Nitti,Inchiesta parlamentare sulle condizioni dei contadini nelle provincie meridionali e nella Sicilia,vol. 5, III, Roma, 1910, p. 357.
- ^Majori G, Sabatinelli G, Casaglia O, Cavallini C, Monzali C.,Imported malaria in Italy from 1986 to 1988,inJ R Soc Health,vol. 110, 1990, pp. 88-89.
- ^Lazzara A, Morante V, Priolo A,Microfocolaio residuo di infezione malarica in provincia di Palermo,inAnn Sanità Publica,vol. 28, 1967, pp. 725-741.
- ^Baldari M, Tamburro A, Sabatinelli G, Romi R,"Malaria in maremma, Italy",inThe Lancet,vol. 351, 1998, pp. 1248-1249.
- ^Bimba di quattro anni morta di malaria a Brescia,suansa.it.
Bibliografia
[modifica|modifica wikitesto]- Claudio Genchi, Pozio Edoardo,Parassitologia generale e umana, 13ª edizione,Milano, Ambrosiana, 2004,ISBN88-408-1269-5.
- Massimo Scaglia, Simona Gatti, Elio Guido Rondanelli,Parassiti e parassitosi umane. Dalla clinica al laboratorio,Milano, Selecta medica, 2006,ISBN88-7332-129-1.
- Gaetano Filice,Malattie infettive, 2ª edizione,Milano, McGraw-Hill, 1998,ISBN88-386-2362-7.
- Joseph C. Segen,Concise Dictionary of Modern Medicine,New York, McGraw-Hill, 2006,ISBN978-88-386-3917-3.
- Douglas M. Anderson, A. Elliot Michelle,Mosby's medical, nursing, & Allied Health Dictionary sesta edizione,New York, Piccin, 2004,ISBN88-299-1716-8.
- (BR) Roberto Focaccia, Ricardo Veronesi,Tratado de Infectologia terza edizione,São Paulo, ATHENEU RIO, 2005,ISBN85-7379-805-X.
- (EN) G. Carosi, F. Castelli (editors) Handbook of malaria infection in the Tropics: health co-operation papers, pubblicato dall' "Associazione italiana amici di R. Follerau", 1997
- (EN) G. Cook,Manson's P. Tropical Diseases.12th ed. Saunders, 1998
- (EN) Patrick R., Ph. D. Murray, Ellen Jo Baron, James H. Jorgensen, Marie Louise Landry, Michael A. Pfaller: Manual of Clinical Microbiology. American Society for Microbiology. Nona edizione
- (EN)Atlas of medical parasitology, Carlo DeNegri Foundation,sucdfound.to.it.URL consultato il 22 ottobre 2005(archiviato dall'url originaleil 13 ottobre 2005).
- (EN) Armengaud A, Legros F, et al. A case of autochthonous Plasmodium vivax malaria, Corsica, August 2006. Euro Surveill. 2006 Nov 16;11(11).
- (EN)WHO guidelines for malaria, 14 March 2023,suapps.who.int.URL consultato il 13 settembre 2023.
Storia della malaria
[modifica|modifica wikitesto]- G. Penso,Parassiti, microbi e contagi nella storia dell'umanità,Ciba-Geigy, Milano 1990
- F. Snowden,The Conquest of Malaria in Italy 1900-1962,Yale University Press, New Haven 2006
- E. Tognotti,Per una storia della malaria in Italia. Il caso della Sardegna,prefazione di Frank Snowden, Franco Angeli, Milano 2008
- Frank M. Snowden,La conquista della malaria. Una modernizzazione italiana 1900-1962,Einaudi, 2008,ISBN978-88-06-18541-1.
Voci correlate
[modifica|modifica wikitesto]- Farmaci antimalarici
- Malattie trasmesse da zanzare
- Febbre quartana
- HLA-B
- Malarioterapia
- Drug Design Optimization Lab
- Malariacontrol.net
- Rosetta@home
Altri progetti
[modifica|modifica wikitesto] Wikiquotecontiene citazioni sullamalaria
Wikiquotecontiene citazioni sullamalaria Wikizionariocontiene il lemma di dizionario «malaria»
Wikizionariocontiene il lemma di dizionario «malaria» Wikimedia Commonscontiene immagini o altri file sullamalaria
Wikimedia Commonscontiene immagini o altri file sullamalaria
Collegamenti esterni
[modifica|modifica wikitesto]- (EN)malaria,suEnciclopedia Britannica,Encyclopædia Britannica, Inc.
- (EN)Malaria,inEncyclopædia Iranica,Ehsan Yarshater Center, Columbia University.
- Aiuta l'UNICEF a combattere la malaria,suunicef.it.
- Centro Nazionale di Epidemiologia, Sorveglianza e Promozione della Salute,suepicentro.iss.it.
- Il sito del ministero della salute[collegamento interrotto],sutrapianti.ministerosalute.it.
- Società italiana di medicina tropicale,susimetweb.eu.URL consultato il 29 gennaio 2008(archiviato dall'url originaleil 13 febbraio 2009).
- (EN)Brian J. Angus, Malaria on the World Wide Web, Clinical Infectious Diseases 2001;33:651-661[collegamento interrotto],sujournals.uchicago.edu.
- (EN)CDC site on malaria,sucdc.gov.
- (EN)Doctors Without Frontiers/Medecins Sans Frontieres Malaria information pages,sudoctorswithoutborders.org.URL consultato il 17 ottobre 2005(archiviato dall'url originaleil 17 dicembre 2005).
- (EN)Sito internazionale sulla malaria,sumalaria.org.URL consultato il 29 gennaio 2008(archiviato dall'url originaleil 3 febbraio 2008).
- (EN)WHO site on malaria,sumosquito.who.int.URL consultato il 17 ottobre 2005(archiviato dall'url originaleil 6 gennaio 2006).
- (EN)Yahoo! -Malariadirectory category
- (EN)Net Gain: Free Online Book on Insecticide treated nets for the prevention of malaria,suidrc.ca.URL consultato il 17 ottobre 2005(archiviato dall'url originaleil 20 novembre 2005).
- Malaria parasite interactions with the human host,sujpgmonline.com.
- Developing artemisinin based drug combinations for the treatment of drug resistant falciparum malaria: A review,sujpgmonline.com.
- Management of severe falciparum malaria,sujpgmonline.com.
- Malaria: Le iniziative di Novartis,sunovartis.it.URL consultato il 20 agosto 2012(archiviato dall'url originaleil 30 settembre 2012).
- Malaria: cause, sintomi, ciclo vitale e trattamento,su BioPills.net
| Controllo di autorità | Thesaurus BNCF12983·LCCN(EN)sh85080038·GND(DE)4037197-9·BNE(ES)XX526064(data)·BNF(FR)cb11941348r(data)·J9U(EN,HE)987007546077605171·NDL(EN,JA)00567482 |
|---|

