Virus del papilloma umano
| Virus del papilloma umano | |
|---|---|
 | |
| Classificazione scientifica | |
| Dominio | Monodnaviria |
| Regno | Shotokuvirae |
| Phylum | Cossaviricota |
| Classe | Papovaviricetes |
| Ordine | Zurhausenvirales |
| Famiglia | Papillomaviridae |
Ivirus del papilloma umano(HPV,acronimodihuman papillomavirus) sono un insieme divirus a dsDNAappartenenti alla famigliaPapillomaviridae.Le infezioni da HPV sono estremamente diffuse nella popolazione e sono trasmesse prevalentemente per via sessuale.[1]
Solitamente l'infezione provocata da questivirusnon causa nessuna alterazione e si risolve da sola.[2]Se l'infezione si prolunga nel tempo allora possono insorgeremalattiedella cute e dellemucose.Un esempio è la lesione a livello del collo dell'utero.La maggior parte di queste lesioni cervicali guarisce spontaneamente, ma alcune, se non trattate, progrediscono lentamente verso formetumorali.
Classificazione
[modifica|modifica wikitesto]Nei campioni biologici umani sono stati individuati più di 100 genotipi di HPV differenti. Solitamente due genotipi differenti presentano anche caratteristiche antigeniche diverse. Alcuni genotipi sono associati a lesioni specifiche, altri invece vengono riuniti in gruppi ad alto o a basso rischio in base alle loro capacità cancerogene.[3]
È inoltre possibile distinguere i papillomavirus in cutanei e mucosi a seconda del tessuto per cui manifestano maggioretropismo.
La maggior parte dei virus di questa famiglia non causa sintomi o causa patologie non gravi, quali ad esempio leverruchecutanee; tuttavia alcuni genotipi possono causare lesioniiperplastichecome icondilomie altri ancora causano lesioni che possono esitare in tumori maligni come ilcancroal collo dell'utero,alcavo orale,all'ano,all'esofago[4]e allalaringe.[5]
Struttura
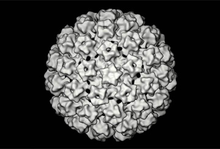
[modifica|modifica wikitesto]Gli HPV sono virus nudi (senzapericapside), possiedono un capside icosaedrico con un diametro attorno ai50nm,formato da 72 capsomeri che possono essere pentameri o esameri (60 esameri e 12 pentameri). Ciascun capsomero dà origine a una protuberanza che ha una forma simile a una stella a cinque punte con un canale al centro. Il capside contiene ungenomacostituito da DNA circolare a doppio filamento lungo 8 kb che codifica per sei geni precoci (early,da E1 a E7; N.B. non c'è E3) e due geni tardivi (late,L1 e L2). A monte dei geni precoci c'è una regione regolatrice contenente l'origine della replicazione, alcune sequenze regolanti la trascrizione e una sequenza N-terminale comune a tutte le proteine precoci. Le proteine precoci servono a modificare il metabolismo della cellula infettata per metterlo al servizio dell'HPV, mentre le tardive sono le proteine strutturali, che associandosi tra loro formano la struttura icosaedrica del capside virale. Tutti i geni di HPV sono collocati sul filamento positivo.
Proteine virali
[modifica|modifica wikitesto]Il DNA di HPV codifica per proteine precoci (early, nomenclate con la lettera E seguita da un numero) e tardive (late, nomenclate con la lettera L, seguita da un numero)[6].Le funzioni di queste proteine sono:
- La proteina L1 - proteina capsidica maggiore (codifica per componenti del capside);
- La proteina L2 - proteina capsidica minore (codifica per componenti del capside);
- La proteina E1 consente la replicazione episomale, con attività dielicasi;
- La proteina E2 partecipa alla trascrizione del promoter di E6, attiva E1 e possiede capacità transattivatrice. In particolare la trascrizione di E2 inibisce E6 ed E7; quando il DNA di HPV si integra con il genoma umano si ha la rottura delle sequenze geniche di E2, con soppressione dell'inibizione nei confronti di E6 ed E7;
- La proteina E4 è espressa nelle fasi tardive dell'infezione ed è molto importante nella maturazione e proliferazione virale. È in grado di legarsi alleproteine citoscheletriche,provocando la deformazione delle cellule infettate (coilocitosi);
- La proteina E5 blocca l'esposizione deicomplessi di istocompatibilitàdi tipo I e II, evitando la risposta cellulare T mediata e inoltre inibisce l'apoptosie altera i segnali promossi dal legame diEGFe diPDGFcon i rispettivi recettori;
- La proteina E6 si lega ap53,interferendo con la riparazione del DNA e con l'innesco dell'apoptosi;
- La proteina E7 si lega allaproteina del retinoblastoma(Rb), impedendo il blocco del ciclo cellulare.

Proteine oncogene
[modifica|modifica wikitesto]In virtù delle loro proprietà leganti e inattivantioncosoppressoricome p53 e Rb, le proteine codificate dal genoma virale promuovono un'intensa replicazione cellulare che esita verso la formazione dipapillomi,condilomi acuminati,iperplasiaepiteliale focale,verrucheecarcinomi.Tuttavia, non tutti i papillomavirus sono responsabili di forme cancerose. In particolare, i carcinomi della cervice uterina sono innescati dai genotipi 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59[7],benché i tipi 16 e 18 siano i più frequenti[8],mentre le verruche e condilomi semplici sono generati dai genotipi 2, 7 (verruche comuni), 1, 2, 4 (verruche plantari) e 3, 10 (verruche piane).
Proteine immunogeniche
[modifica|modifica wikitesto]L'oncoproteina E7 è una piccola proteina idrosolubile costituita da 98 amminoacidi, scarsamente immunogenica. Per questo, non può essere usata singolarmente comeaptenee deve essere "fusa" con complessi proteici più immunogenici. La stimolazione di una risposta immunitaria polarizzata da un vaccino contenente frammenti o proteine complessate con E6 ed E7 può essere in grado di eliminare il rischio di cancro connesso con l'infezione da HPV.[9]
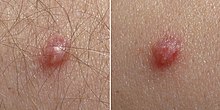
Le infezioni da HPV
[modifica|modifica wikitesto]Le infezioni da HPV si contraggono tramite contatto diretto (sessuale, orale e cutaneo) o in luoghi poco puliti (ad esempio bagni pubblici non disinfettati a norma). Sono presenti in liquidi biologici quali saliva, sperma[10]o sangue, sebbene non sia chiaro se e come sia possibile infettarsi tramite questi fluidi. Il rischio di contrarre una infezione da HPV aumenta con il numero dei partner sessuali, ed è massimo tra i giovani adulti (20-35 anni). Il virus è più frequentemente trovato tra le popolazioni promiscue e in condizioni precarie di igiene. L'uso delprofilatticonon pare avere azione protettiva completa in quanto l'infezione è spesso diffusa anche alla cute dellavulvae delperineo.
L'infezione da HPV è asintomatica nella maggior parte dei casi. In alcuni casi, si può invece manifestare concondilomi acuminatiin sede genitale (peneevulva,perineo). Le lesioni da HPV del collo uterino possono essere riconosciute mediante ilPap test,lacolposcopiao tecniche dipatologia molecolare,e le lesioni del pene mediante la penescopia. Icondilomi,generalmente provocati dal virus HPV, sono delle escrescenze della pelle di tipo verrucoso che colpiscono di preferenza le zone genitali, sia nel maschio (glande, meno frequentemente sotto ilprepuzio,corpo delpeneescroto) sia nella femmina (perineo,vulva,vaginaecerviceuterina).
Ogni anno, in Italia, sono circa 3 500 le donne che si ammalano di cancro del collo dell'utero. Si stima che il 75% della popolazione entri in contatto con il virus almeno una volta durante la sua vita. Si calcola che oltre il 70% delle donne contragga un'infezione genitale da HPV nel corso della propria vita, ma la grande maggioranza di queste infezioni è destinata a scomparire spontaneamente nel corso di pochi mesi grazie al lorosistema immunitario.Solo in caso di persistenza nel tempo di infezioni di HPV ad alto rischio oncogenico è possibile, in una minoranza dei casi e nel corso di parecchi anni, lo sviluppo di un tumore maligno del collo uterino.
Patogenesi
[modifica|modifica wikitesto]Le proteine precoci del virus hanno lo scopo di favorire la crescita e la divisione della cellula; l'HPV può infatti replicare solo nelle cellule inreplicazione,in quanto non codifica per una suaDNA polimerasie ha bisogno di quella della cellula ospite, sintetizzata nelle cellule in attiva divisione.
Le cellule bersaglio del virus sono la cute e le mucose, due tessuti che si rigenerano in continuazione. Il virus induce la crescita degli strati basale e spinoso dell'epidermide (acantosi) o dello strato superficiale della mucosa, dando origine, a seconda del luogo dell'infezione, averruchenella cute o apapillominelle mucose; promuove inoltre la sintesi delle cheratine (ipercheratosi).
L'espressione dei geni di HPV è correlata con le diverse tipologie di cheratina espresse negli strati dell'epidermide. Lo strato basale e quello spinoso dell'epidermide contengono all'interno del nucleo delle loro cellule anche il DNA virale dell'HPV, mentre i geni tardivi L1 e L2 che permettono la formazione del virione maturo sono espressi solo nello strato corneo dell'epidermide. La replicazione del virus avviene preferenzialmente nello strato granuloso. Il virus viene liberato insieme ai cheratinociti morti degli strati più superficiali dell'epidermide.
Una volta che l'HPV è entrato dentro la cellula ne sfrutta i macchinari cellulari per sintetizzare due proteine chiamate E6 e E7, che legano rispettivamentep53(mediandone la degradazione e prevenendo così l'apoptosi) e laRB protein(una proteina coinvolta nella regolazione del ciclo cellulare). Questo causa divisioni cellulari incontrollate. Si pensa che questi cambiamenti fisiologici nelle cellule infettate servano al virus per diffondersi meglio.
I tipi pericolosi di HPV (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68) si differenziano da quelli innocui (6, 11, 42, 43, 44) sia in base al sito di azione (i primi attaccano le mucose e i secondi la cute) sia in base ad alcune mutazioni dell'oncoproteinaE7(early 7). Questa differente pericolosità è dovuta al fatto che le mucose sono molto più sensibili della pelle alle infezioni da HPV perché la minore robustezza delle membrane cellulari delle cellule delle mucose facilita l'ingresso dei virus all'interno delle stesse, e in più le oncoproteineE7dei papillomavirus pericolosi hanno delle mutazioni amminoacidiche che permettono un legame e un'inibizione migliore delretinoblastomarispetto agli E7 dei tipi non pericolosi. Per esempio la differenza amminoacidica principale tra l'E7dell'HPV 16 (pericoloso) e 6 (non pericoloso) è un acido aspartico in posizione 21 presente nel primo invece di una glicina presente nel secondo; questa sola differenza fa sì che la prima proteina abbia una capacità ligante (e quindi di causare il cancro) del 41% superiore alla seconda.[11]
Infezione da HPV e gravidanza
[modifica|modifica wikitesto]È possibile che una donna contragga l'infezione da HPV in gravidanza, con conseguente preoccupazione circa l'andamento dell'infezione e la trasmissione al feto. Il rischio di contrarre l'infezione in gravidanza non è diverso rispetto alla non-gravidanza, e la distribuzione dei tipi virali ad alto e basso rischio non presenta differenze. L'infezione può tuttavia comparire la prima volta in gravidanza e dare origine a lesioni genitali che possono assumere aspetti aberranti, molto estese, giganti e friabili.
Nonostante la trasmissione materno fetale sia possibile a livello del canale del parto e possa provocarepapillomatosi respiratoria ricorrentegiovanile e condilomatosi genitale nel nato, il parto cesareo non è indicato, a meno di lesioni molto estese che ostruiscano il canale del parto.[12]
Diagnosi
[modifica|modifica wikitesto]La diagnosi dell'infezione di HPV ad alto rischio viene eseguita mediante una classe di test molecolari denominati HPV DNA Test[13].Questi test sono sempre più diffusi a livello mondiale; il Gruppo Italiano Screening del Cervicocarcinoma (GISCI) riporta:
"La ricerca scientifica ha dimostrato che il test HPV è più efficace del Pap test per la prevenzione del cervicocarcinoma, in Italia sono stati avviati i primi programmi di screening con test HPV, un esame molecolare di laboratorio che consente di individuare la presenza del virus prima che provochi alterazioni nelle cellule. Il test HPV per essere efficace deve essere fatto all’interno di un programma organizzato che garantisce protocolli e controlli di qualità adeguati. In questo nuovo programma ilPap testnon scompare ma diventa un esame di completamento (Pap test di triage) che viene letto solo nelle donne risultate positive al test HPV. "[14]
Esistono quasi duecento HPV DNA Test in commercio[15],la maggior parte dei quali si basa sull'analisi di cellule prelevate dal tessuto della cervice uterina effettuato mediante strumenti simili a quelli utilizzati per l'esecuzione del Pap test, come laspatola di Ayre.Molti dei test molecolari sono in grado di rilevare la presenza o assenza dei genotipi dei principali papillomavirus ad alto rischio, senza specificarne il genotipo. Altri test, denominati test di genotipizzazione dell'HPV, sono in grado di fornire informazioni sul ceppo presente nell'infezione, anche in caso di infezione multipla. Recenti studi hanno dimostrato che genotipi diversi di questooncovirushanno un diverso potenziale di trasformazione tumorale (cancerogenesi)[16],e ciò potrebbe essere utile in fase ditriageefollow-up[17].
In Italia, nel 2019, è stato validato clinicamente un test molecolare altamente sensibile, basato sull'auto-prelievo del solo muco vaginale, caratteristica che rende il testnon invasivo,indolore e semplice da eseguire. Inoltre il test è in grado di fornire indicazioni sul genotipo presente nel campione biologico e non richiede l'estrazione del DNA. L'auto-prelievo di muco vaginale può essere effettuato dalla donna direttamente a casa senza ulteriori procedure mediche. Il campione auto-prelevato viene poi inviato e analizzato presso il Policlinico dell'Università Campus Bio-medicodi Roma. Il referto medico viene consegnato alla donna mediante una piattaforma digitale accessibile dasmartphoneo computer. Il test è stato sviluppato dalla start-up "Ulisse Biomed" di Trieste, fondata da Rudy Ippodrino e Bruna Marini, due ricercatori perfezionatisi allaNormale di Pisa.[18][19][20]A seguito dei risultati incoraggianti della ricerca[21],era stato previsto il lancio del test entro l'autunno del 2019.[22]
Terapia
[modifica|modifica wikitesto]Come in molte infezioni virali, la terapia dell'infezione da HPV è spesso problematica. Poiché tuttavia la maggior parte delle infezioni da HPV regredisce spontaneamente, necessitando di un trattamento solo in una minoranza dei casi. Nei casi di infezione persistente del collo uterino, non esistono attualmente trattamenti non invasivi di elevata efficacia. Nel caso l'infezione sia associata a modificazioniprecancerosedell'epitelio, possono essere prese in considerazione lalaserterapiao laconizzazione,ossia la resezione di una piccola parte della cervice uterina per asportare una lesione che potrebbe essere maligna o che già lo è, ma di dimensioni ridotte. Per la rimozione dei condilomi acuminati della vulva, pene o perineo si può ricorrere allaser,all'elettrocoagulazione,allacrioterapiao ad applicazioni dipodofillina.
Prevenzione
[modifica|modifica wikitesto]Per prevenire l'infezione è opportuno attuare le comuni pratiche d'igiene e l'uso del preservativo pur non essendo efficaci al 100%, è disponibile anche un vaccino che permette la protezione da diversi sierotipi del virus, questa forma di prevenzione può prevenire oltre il 90% delle forme tumorali associate all'HPV,[23]l'HPV è uno dei principali fattori di rischio per il tumore della cervice.[24]
Note
[modifica|modifica wikitesto]- ^Hpv e cervicocarcinoma,suepicentro.iss.it.URL consultato il 17 ottobre 2017.
- ^Ian H. Frazer, J. Thomas Cox e Edward John Mayeaux,Advances in prevention of cervical cancer and other human papillomavirus-related diseases,inThe Pediatric Infectious Disease Journal,vol. 25, 2 Suppl, febbraio 2006, pp. S65–81, quiz S82,DOI:10.1097/01.inf.0000196485.86376.46.URL consultato il 17 ottobre 2017.
- ^Capitolo 19, Papillomavirus e polyomavirus,inSherris, Microbiologia medica, Settima edizione,p. 355.
- ^Collins et al.,Interactions with Pocket Proteins Contribute to the Role of Human Papillomavirus Type 16 E7 in the Papillomavirus Life Cycle,Journal of virology, 79 (23), p. 14.769-80, 2005
- ^Tsutsumi K et al.,Expression of human papillomavirus (HPV) gene in HPV-positive laryngeal tumors and activity of the HPV long control region in cultured normal laryngeal epithelial cells,Nippon Jibiinkoka Gakkai Kaiho, 96(5), p. 767-73.
- ^Papillomavirus,suemedicine.medscape.com,eMedicine, 2007.URL consultato il 16 agosto 2009.
- ^Muñoza N, Castellsaguéb X, Berrington de Gonzálezc A, Gissmann L,Chapter 1: HPV in the etiology of human cancer,inVaccine,vol. 24, n. 3, 2006, pp. S1–S10,DOI:10.1016/j.vaccine.2006.05.115,PMID16949995.
- ^HUMAN PAPILLOMAVIRUSES HPV types 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 and 66 (Group 1) - HPV 6 and HPV 11 (Group 2B)(PDF), sumonographs.iarc.fr,IARC, 2006.URL consultato il 16 agosto 2009(archiviato dall'url originaleil 9 dicembre 2008).
- ^Vaccination to prevent and treat cervical cancer.Hum Pathol. 2004 Aug;35(8):971.
- ^https://link.springer.com/article/10.1007/s13631-014-0048-0
- ^Heck DV et al.,Efficiency of binding the retinoblastoma protein correlates with the transforming capacity of the E7 oncoproteins of the human papillomaviruses,Proceeding of the National Academy of Sciences of the United States of America, 89 (10), p. 4442-46, 1992.
- ^DonnamedPapilloma virus e gravidanza(archiviato dall'url originaleil 2 ottobre 2009).
- ^AIRC - Associazione Italiana per la Ricerca sul Cancro,HPV test « Esami medici | AIRC,suAIRC.URL consultato il 28 febbraio 2018.
- ^Administrator,Il Nuovo Programma di Screening con il Test HPV sostituisce il Pap-test,sugisci.it.URL consultato il 13 settembre 2019.
- ^Mario Poljak, Boštjan J. Kocjan e Anja Oštrbenk,Commercially available molecular tests for human papillomaviruses (HPV): 2015 update,inJournal of Clinical Virology: The Official Publication of the Pan American Society for Clinical Virology,76 Suppl 1, 2016-3, pp. S3–S13,DOI:10.1016/j.jcv.2015.10.023.URL consultato il 13 settembre 2019.
- ^Anna Söderlund-Strand, Carina Eklund e Levent Kemetli,Genotyping of human papillomavirus in triaging of low-grade cervical cytology,inAmerican Journal of Obstetrics and Gynecology,vol. 205, n. 2, 2011-8, pp. 145.e1–6,DOI:10.1016/j.ajog.2011.03.056.URL consultato il 13 settembre 2019.
- ^Anna Söderlund-Strand, Lennart Kjellberg e Joakim Dillner,Human papillomavirus type-specific persistence and recurrence after treatment for cervical dysplasia,inJournal of Medical Virology,vol. 86, n. 4, 2014-4, pp. 634–641,DOI:10.1002/jmv.23806.URL consultato il 13 settembre 2019.
- ^Due normalisti realizzano il primo test al mondo per la diagnostica del Papilloma virus disponibile direttamente in farmacia,sunormalenews.sns.it,6 settembre 2019.URL consultato il 7 settembre 2019(archiviatoil 7 settembre 2019).
- ^Primo test del Papillomavirus in farmacia, è italiano,suadnkronos.com,AdnKronos.com, 7 settembre 2019.URL consultato il 7 settembre 2019(archiviatoil 7 settembre 2019).
- ^Papilloma virus, ora c'è il test in farmacia,sulanazione.it,La Nazione,7 settembre 2019.URL consultato il 7 settembre 2019(archiviatoil 7 settembre 2019).
- ^(EN) Bonazza, Deborah, Avian, A., Biagi, C. e Bussani, Rossana; DAL CIN, Elisa; Giudici, Fabiola; Ippodrino, R.; Marini, Bruna,Human Papillomavirus genotyping in oropharingeal squamous cell carcinoma, without DNA extraction through EasyPAP direct HPV DNA test,inPathologica,vol. 109, Fasc. 3, 2017, p. 337.URL consultato il 7 settembre 2019(archiviatoil 7 settembre 2019).,Presentato al Congresso di Anatomia Patologica dello SIAPEC-IAP, svoltosi aNapoli, dal 12 al 14 ottobre 2017.URL consultato il 22 settembre 2019(archiviato dall'url originaleil 7 settembre 2019)..
- ^Lorenza Masè,Ladymed, il kit che rivoluziona il modo di scoprire il Papilloma Virus(PDF), inIl Piccolo,Trieste, 26 maggio 2018, p. 16.URL consultato il 7 settembre 2019(archiviatoil 7 settembre 2019).
- ^Campagna di comunicazione sulla vaccinazione anti-HPV
- ^Tumore della cervice uterina
Bibliografia
[modifica|modifica wikitesto]- Patrick R. Murray,Microbiologia medica,Roma, EMSI, 2008,ISBN978-88-86669-56-6.
- Gianni Bonadonna, Gioacchino Robustelli Della Cuna, Pinuccia Valgussa,Medicina oncologica,8ª ed., Milano, Elsevier Masson, 2007,ISBN978-88-214-2814-2.
- Patrizia Marini,http://www.microbiology5.org/microbiology5/book/757-766.pdf.
Voci correlate
[modifica|modifica wikitesto]- Biopsia
- Cervarix
- Cidofovir
- Citologia
- Colposcopia
- Epidermodisplasia verruciforme
- Gardasil
- Papilloma
- Pap test
- Peniscopia
Altri progetti
[modifica|modifica wikitesto] Wikimedia Commonscontiene immagini o altri file suvirus del papilloma umano
Wikimedia Commonscontiene immagini o altri file suvirus del papilloma umano
Collegamenti esterni
[modifica|modifica wikitesto]- (EN)human papillomavirus,suEnciclopedia Britannica,Encyclopædia Britannica, Inc.
| Controllo di autorità | Thesaurus BNCF5361·LCCN(EN)sh85097679·GND(DE)4219886-0·BNE(ES)XX529073(data)·BNF(FR)cb120821523(data)·J9U(EN,HE)987007563274305171 |
|---|

