Trifluoruro di boro
| Trifluoruro di boro | |
|---|---|
 | |
 | |
| NomeIUPAC | |
| trifluoruro di boro | |
| Caratteristiche generali | |
| Formula brutaomolecolare | BF3 |
| Massa molecolare(u) | 67,81 |
| Aspetto | gas incolore |
| Numero CAS | |
| Numero EINECS | 231-569-5 |
| PubChem | 6356 |
| SMILES | B(F)(F)F |
| Proprietà chimico-fisiche | |
| Densità(g/l, inc.s.) | 2,178 |
| Temperatura di fusione | −126 °C (147 K) |
| Temperatura di ebollizione | −100,3 °C (172,9 K) |
| Proprietà termochimiche | |
| ΔfH0(kJ·mol−1) | −1137 |
| S0m(J·K−1mol−1) | 254,12 |
| C0p,m(J·K−1mol−1) | 50,46 |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
  
| |
| pericolo | |
| Frasi H | 280-314-330-EUH014 |
| Consigli P | 260-280-284-305+351+338-310-410+403[1] |
Iltrifluoruro di boro(noto cometrifluoro-boranonella vecchia nomenclatura) è ilcomposto chimicodi formula.È un gas incolore etossico,di odore pungente, che forma fumi bianchi in aria umida. È unacido di Lewise un reagente versatile per la preparazione di altri composti diboro.
Struttura e legami
[modifica|modifica wikitesto]I trialogenuri di boro sono composti molecolari monomerici, a differenza dei trialogenuri di alluminio. Miscele di alogenuri diversi scambiano molto rapidamente gli alogeni:
La reazione procede presumibilmente attraverso la formazione didimeriinstabili. A causa di questa reazione, i composti con alogeni misti non si possono ottenere in forma pura.
La geometria dellamolecolaè trigonale planare. La simmetriaè in accordo con le previsioni della teoriaVSEPR.Benché contenga tre legami covalenti polari, la molecola hamomento dipolarenullo in virtù dell'alta simmetria.è una tipica molecola elettron-deficiente, come avvalorato dal fatto che reagisce facilmente conbasi di Lewis.
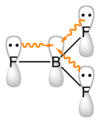
Nei trialogeno compostila distanza di legame tra boro e alogeno è più piccola di quella che ci si aspetterebbe per un legame singolo;[2]questo è stato interpretato con la presenza di un apprezzabilecontributo πal legame. Come mostrato nella figura, è facile invocare una sovrapposizione tra un orbitaledell'atomo di boro centrale con una combinazione dei tre orbitalicon la stessa orientazione presenti sugli atomi difluoro.[2]
Sintesi
[modifica|modifica wikitesto]è preparato industrialmente trattando a caldo ossido di boro o borati confluoritee conacido solforicoconcentrato:[3]
In laboratorio si può produrreper decomposizione termica del tetrafluoroborato di diazonio (reazione di Schiemann):[4]
Acidità di Lewis e reazioni collegate
[modifica|modifica wikitesto]Il trifluoruro di boro è un acido di Lewis molto versatile e forma addotti con basi di Lewis comefluoruriedeteri:
L'anionetetrafluoroborato() è comunemente impiegato come anione non coordinante. L'addotto con l'etere etilico è un liquido comodo da maneggiare e di conseguenza è largamente utilizzato in laboratorio come fonte di.
Confronti di acidità di Lewis
[modifica|modifica wikitesto]Tutti e tre i trialogenuri di boro,() formano addotti stabili con semplici basi di Lewis. La loro acidità relativa può essere stimata confrontando l'esotermicità delle reazioni di formazione degli addotti. Da queste misure si è ricavato il seguente ordine di acidità di Lewis:
- (acido di Lewis più forte)
Questo andamento è comunemente attribuito alla quantità di contributo π al legame che va perso nel passare dalla forma planare della molecolaalla forma tetraedrica nell'addotto formato,[5]quantità che varia nell'ordine:
- (diventa più facilmente tetraedrico)
I criteri per valutare le forze relative del legame π non sono però del tutto chiari.[2]
Una possibile interpretazione considera che, essendo l'atomo di fluoro più piccolo di quello di bromo, la coppia elettronica dell'orbitaledel fluoro può dare maggiore sovrapposizione con l'orbitalevuoto del boro. Di conseguenza, inil contributoal legame è maggiore rispetto a.
In un'altra interpretazione, la minor acidità di Lewis diè attribuita alla relativa debolezza del legame che si forma nell'addotto.[6][7]
Idrolisi
[modifica|modifica wikitesto]Il trifluoruro di boro reagisce con l'acqua in modo incompleto, formandotetrafluoroboratieacido borico.
Gli altri alogenuri sono invece completamente idrolizzati in acqua, senza formare lo ione tetraedrico.Ad esempio:
Precauzioni per l'impiego
[modifica|modifica wikitesto]Il trifluoruro di boro è corrosivo. I contenitori per il trifluoruro di boro devono essere fatti di metalli adatti comeacciaio inossidabile,monele hastelloy. In presenza di umidità corrode l'acciaio, anche inossidabile. Reagisce con lepoliammidi,mentrepolitetrafluoroetilene,policlorotrifluoroetilene,polivinildenfluoruroepolipropileneresistono in modo soddisfacente. Ilgrassousato per lubrificare le apparecchiature deve essere a base difluorocarburi,dato chereagisce con i grassi a base idrocarburica.[8]
Nella maggior parte dei casiè utilizzato come acido di Lewis. Gli usi principali sono:
- reazioni di acilazione e alchilazione diFriedel-Crafts.Queste reazioni non sono propriamente catalitiche, dato cheviene consumato. Ad esempio:
- reazioni dipolimerizzazionedi composti insaturi come glialcheni
- reazioni diisomerizzazionedi idrocarburi saturi e insaturi
- crackingdegli idrocarburi nell'industria petrolifera
- reazioni diesterificazionee condensazione
- sintesi di altri composti di boro comeboranie borati
- sintesi di additivi perlubrificanti
- drogaggiodi tipo P nella fabbricazione disemiconduttori
- rilevazione di neutroni termici usato come gas del contatore proporzionale sfruttando l'alta sezione d'urto di assorbimento del boro con i neutroni a bassa energia.
Note
[modifica|modifica wikitesto]- ^Sigma Aldrich; rev. del 05.12.2012
- ^abcGreenwood, N. N.; A. Earnshaw (1997). Chemistry of the Elements, 2nd Edition, Oxford:Butterworth-Heinemann.ISBN 0-7506-3365-4.
- ^Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001.ISBN 0-12-352651-5.
- ^Flood, D. T. (1943). "Fluorobenzene".Org. Synth.2:295.
- ^Cotton, F. A.; Wilkinson, G.; Murillo, C. A.; Bochmann, M. (1999). Advanced Inorganic Chemistry (6th Edn.) New York: Wiley-Interscience.ISBN 0-471-19957-5.
- ^Group V Chalcogenide Complexes of Boron TrihalidesBoorman, P. M.; Potts, D. Canadian. Journal of Chemistry (Rev. can. chim.) volume 52, (1974) pp 2016-2020
- ^T. Brinck, J. S. Murray and P. Politzer,A computational analysis of the bonding in boron trifluoride and boron trichloride and their complexes with ammonia,inInorg. Chem.,vol. 32, n. 12, 1993, pp. 2622–2625,DOI:10.1021/ic00064a008.
- ^Boron trifluoride,inGas Encyclopedia,Air Liquide.URL consultato il 4 marzo 2009(archiviato dall'url originaleil 6 dicembre 2006).
Altri progetti
[modifica|modifica wikitesto] Wikimedia Commonscontiene immagini o altri file suTrifluoruro di boro
Wikimedia Commonscontiene immagini o altri file suTrifluoruro di boro
Collegamenti esterni
[modifica|modifica wikitesto]- https://www.osha.gov/dts/chemicalsampling/data/CH_221700.html
- https://web.archive.org/web/20090310182250/http://www.cdc.gov/niosh/ipcsneng/neng0231.html
- National Pollutant Inventory - Boron and compounds fact sheet,sunpi.gov.au.URL consultato il 4 marzo 2009(archiviato dall'url originaleil 9 febbraio 2006).
- National Pollutant Inventory - Fluoride and compounds fact sheet,sunpi.gov.au.URL consultato il 4 marzo 2009(archiviato dall'url originaleil 16 gennaio 2006).
- WebBook page for BF3,suwebbook.nist.gov.URL consultato il 4 marzo 2009(archiviato dall'url originaleil 13 dicembre 2020).
| Controllo di autorità | LCCN(EN)sh2007010028·GND(DE)4146382-1·J9U(EN,HE)987007551902605171 |
|---|