Virginiamicina
| Virginiamicina | |
|---|---|
 | |
 | |
| Caratteristiche generali | |
| Formula brutaomolecolare | C71H84N10O17 |
| Massa molecolare(u) | 1349,48 |
| Numero CAS | |
| Numero EINECS | 234-244-6 |
| Codice ATC | D06 |
| PubChem | 11979535 |
| DrugBank | DBDB11476 |
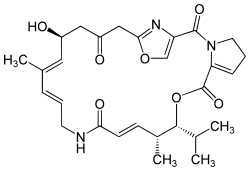
| SMILES | CC1C=CC(=O)NCC=CC(=CC(CC(=O)CC2=NC(=CO2)C(=O)N3CCC=C3C(=O)OC1C(C)C)O)C |
| Indicazioni di sicurezza | |
Lavirginiamicina(conosciuta anche con la siglaSKF-7988) è un complessoantibioticostreptograminico, simile allapristinamicina,utilizzato per trattare infezioni da germiGram-positivi,[1]costituito per l'80% circa da virginiamicina M1 (fattore M1 o pristinamicina IIA) e per il 20% circa da virginiamicina S1 (fattore S), prodotti dalla crescita diStreptomyces virginiae,Streptomyces loidensis,Streptomyces mitakaensis,Streptomyces pristina-spiralis,Streptomyces ostreogriseuse altri.[2]
Caratteristiche strutturali e fisiche
[modifica|modifica wikitesto]Il complesso antibiotico si presenta come una polvere amorfa bianca moderatamente solubile in acqua e in acidi diluiti. Facilmente solubile insoluzioniacquose alcaline apHsuperiore a 9,5 con rapida inattivazione. È solubile inoltre inmetanolo,alcool,acetone,etile acetato,cloroformioebenzene.Praticamente insolubile inligroina.
Farmacodinamica
[modifica|modifica wikitesto]La virginiamicina è un antibiotico streptograminico (macrolide), più precisamente unasinergistina(un termine generico che indica un gruppo di sostanze antibiotiche isolati da ceppi di Streptomyces, le quali consistono di diverse fazioni che agiscono in sinergia fra loro), che esercita la sua attività legandosi alla subunità ribosomiale 50S delle cellule batteriche e, interferendo con le normali funzioniribosomiali,causa inibizione dellasintesi proteica.[3][4][5] Il complesso antibiotico presenta uno spettro antibatterico simile a quello dell'eritromicinache comprendestafilococchi,anche resistenti ad altri antibiotici, alcuni streptococchi epneumococchi.Risultano sensibili all'azione dell'antibiotico ancheNeisseria gonorrhoeae,Bordetella pertussis,MycoplasmaeHaemophilus influenzae. L'attività della virginiamicina sembra essere dovuta principalmente alla componente M1, ad eccezione dell'azione nei confronti delBacillus subtilische sarebbe imputabile alla componente S1.
Spesso si manifesta resistenza crociata con altri macrolidi,streptograminae antibioticilincosamidici.[6]
Farmacocinetica
[modifica|modifica wikitesto]A seguito di somministrazione per via orale la virginiamicina è rapidamente assorbita daltratto gastrointestinale,anche se in modo incompleto (circa il 15-18% della dose ingerita). L'assorbimento risulta ridotto in presenza di cibo. La concentrazione plasmatica massima (Cmax) di 1 µg/ml viene raggiunta circa 4 ore dopo l'assunzione di una dose orale di 500 mg. L'antibiotico si distribuisce ampiamente neitessuti biologici,in particolare nelfegato,polmoni,cute,intestino,e nei fluidi organici, ma non è in grado di oltrepassare labarriera ematoencefalica.Anche nell'espettoratosi ritrovano concentrazioni rilevanti di farmaco. Il legame di virginiamicina con leproteine plasmaticheraggiunge il 70-80% circa. La molecola presenta un'emivitaplasmatica di circa 5 ore. La miscela antibiotica è metabolizzata a livello dellaghiandola epaticae viene escreta principalmente attraverso labile.Di una dose somministrata solo il 15% circa viene ritrovato nelleurinenell'arco di 24 ore. Non si manifestano fenomeni di accumulo.[7]
Usi clinici
[modifica|modifica wikitesto]La virginiamicina viene impiegata nel trattamento di infezioni sostenute da microorganismi sensibili (in particolare cocchigram-positivi), specialmente quando sono molto gravi e resistenti ad altri antibiotici.
La molecola viene utilizzata per via orale principalmente in campo otorinolaringoiatrico e stomatologico e nel trattamento di infezioni broncopolmonari, genito-urinarie (soprattutto a carico dellaprostata) o che interessano lacute,leossae learticolazioni.
Per via topica è usata soprattutto nella cura delle infezioni stafilococciche (foruncolosi,impetigine,sicosi,pustolesuperficiali) e nella prevenzione delle infezioni in chirurgia e traumatologia.
L'antibiotico in Europa è stato utilizzato per più di 20 anni in agricoltura e zootecnia come additivo nella preparazione di alimenti per animali. Il suo uso per questi scopi è stato oggi vietato in tutta l'Unione europeain quanto si ritiene vi siano ormai sufficienti fondamenti scientifici relativi all'esistenza di un nesso tra l'impiego della virginiamicina per questi usi e lo sviluppo nell'uomo della resistenza alle streptogramine, in particolare si pensa che la gran parte dei ceppi circolanti di Enterococcus faecium resistenti (SREF) derivi da questi usi.[8][9][10][11]
Effetti collaterali
[modifica|modifica wikitesto]Durante il trattamento con virginiamicina sono stati segnalati diversieffetti collateralia livello gastrointestinale, e in particolaredispepsia,nauseaevomito.Sono stati anche riportati casi di alterazione nella visione dei colori eipersensibilitàseguiti da manifestazioni qualiprurito,orticaria,rash cutaneoeeczema.[12]
Controindicazioni
[modifica|modifica wikitesto]L'antibiotico è controindicato in soggetti con ipersensibilità nota, ingravidanza,nei neonati e durante l'allattamento.Si consiglia di evitare l'esposizione ai raggi solari durante la terapia, dal momento che si può verificare fotosensibilizzazione.
Dosi terapeutiche
[modifica|modifica wikitesto]Nei soggetti adulti l'antibiotico viene somministrato per via orale alla dose di 2-3 g al giorno e, in caso di infezioni gravi, alla dose di 4 g al giorno. Nei bambini sono somministrate dosi pari a 50–100 mg/kg/die. L'antibiotico può essere applicato anche localmente in forma di polvere al 2% o di unguento allo 0,5%.
Note
[modifica|modifica wikitesto]- ^F. Le Goffic,Structure activity relationships in lincosamide and streptogramin antibiotics.,inJ Antimicrob Chemother,16 Suppl A, Lug 1985, pp. 13-21,PMID3932299.
- ^B. Boon,[Virginiamycin. Composition and analysis],inProc. Soc. Anal. Chem.,vol. 10, 1973, pp. 29-30, PMID.
- ^M. Di Giambattista, G. Chinali; C. Cocito,The molecular basis of the inhibitory activities of type A and type B synergimycins and related antibiotics on ribosomes.,inJ Antimicrob Chemother,vol. 24, n. 4, Ott 1989, pp. 485-507,PMID2515187.
- ^M. Di Giambattista, E. Nyssen; A. Pecher; C. Cocito,Affinity labeling of the virginiamycin S binding site on bacterial ribosome.,inBiochemistry,vol. 29, n. 39, Ott 1990, pp. 9203-11,PMID2125475.
- ^R. Parfait, MP. de Béthune; C. Cocito,A spectrofluorimetric study of the interaction between virginiamycin S and bacterial ribosomes.,inMol Gen Genet,vol. 166, n. 1, Ott 1978, pp. 45-51,PMID105239.
- ^J. Duval,Evolution and epidemiology of MLS resistance.,inJ Antimicrob Chemother,16 Suppl A, Lug 1985, pp. 137-49,PMID3932300.
- ^B. Boon, M. Gilbert; F. Lamy,[Study of plasma and urinary levels of virginiamycin in humans].,inTherapie,vol. 28, n. 2, pp. 367-77,PMID4588002.
- ^LA. Cox, DA. Popken,Quantifying human health risks from virginiamycin used in chickens.,inRisk Anal,vol. 24, n. 1, febbraio 2004, pp. 271-88,DOI:10.1111/j.0272-4332.2004.00428.x,PMID15028017.
- ^DL. Smith, JA. Johnson; AD. Harris; JP. Furuno; EN. Perencevich; JG. Morris,Assessing risks for a pre-emergent pathogen: virginiamycin use and the emergence of streptogramin resistance in Enterococcus faecium.,inLancet Infect Dis,vol. 3, n. 4, aprile 2003, pp. 241-9,PMID12679267.
- ^JR. Hayes, DD. Wagner; LL. English; LE. Carr; SW. Joseph,Distribution of streptogramin resistance determinants among Enterococcus faecium from a poultry production environment of the USA.,inJ Antimicrob Chemother,vol. 55, n. 1, gennaio 2005, pp. 123-6,DOI:10.1093/jac/dkh491,PMID15574480.
- ^I. Klare, C. Konstabel; D. Badstübner; G. Werner; W. Witte,Occurrence and spread of antibiotic resistances in Enterococcus faecium.,inInt J Food Microbiol,vol. 88, n. 2-3, Dic 2003, pp. 269-90,PMID14597000.
- ^J. Laroche, C. Laroche,[Modification of color vision caused by use of normal therapeutic doses of certain drugs].,inAnn Pharm Fr,vol. 30, n. 6, Giu 1972, pp. 433-44,PMID4404761.