Mentolo
| Mentolo | |
|---|---|
 | |
 | |
| NomeIUPAC | |
| (1R,2S,5R)-2-isopropil-5-metilcicloesanolo | |
| Nomi alternativi | |
| (-)-mentolo | |
| Caratteristiche generali | |
| Formula brutaomolecolare | C10H20O |
| Massa molecolare(u) | 156,27 g/mol |
| Aspetto | solido cristallino incolore |
| Numero CAS | (-)-mentolo |
| Numero EINECS | 218-690-9 |
| PubChem | 16666 |
| DrugBank | DBDB00825 |
| SMILES | CC1CCC(C(C1)O)C(C)C |
| Proprietà chimico-fisiche | |
| Densità(g/cm3,inc.s.) | 0,89 |
| Potere rotatorio specifico | [𝛼]20D= –50 (etanolo, 10%) |
| Solubilitàinacqua | 0,397 g/L |
| Temperatura di fusione | 41 -45 °C (314-318 K) |
| Temperatura di ebollizione | 212 °C (485 K) |
| Indicazioni di sicurezza | |
| Punto di fiamma | 96 °C (~369 K) |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 315 |
| Consigli P | [1] |
Ilmentolo(o(-)-mentolo) è unalcolchirale.Atemperatura ambientesi presenta come un solido bianco dall'odorecaratteristico. È un compostoirritante.
Estratto dall'olio essenziale dellamenta piperita,ha potere rinfrescante ed è usato per confezionareprofumi,farmacied altri preparati.[2]
Storia
[modifica|modifica wikitesto]Il mentolo fu scoperto più di duemila anni fa inGiappone,sebbene la menta piperita, da cui è ottenuto, venisse già usata nell'antichità comeerba medicinaledaEgizi,GrecieRomani.
InOccidente,il mentolo è stato isolato nel 1771 daHieronymus David Gaubius.
Struttura
[modifica|modifica wikitesto]Appartiene alla classe deiterpenoidi(è un monoterpenoide) e, a differenza di altri composti della stessa classe (es.limoneneecarvone), è presente in natura solo undiastereoisomerodegli otto possibili.
Il 2-isopropil-5-metil-cicloesanolo è una molecola dotata di 3 centrichirali,che portano a 8 diversistereoisomeri:di questi otto, quattro sono formediastereoisomere,conosciute con il nome di mentolo,neomentolo,isomentoloeneoisomentolo.Non esistendo un centro di inversione o unpiano di simmetria,nessuna delle forme è unaformameso,cosicché ognuno dei quattro diastereoisomeri ha un corrispondenteenantiomero.Tuttavia l'unica forma che possiede un effetto rinfrescante è l'isomero (1R-2S-5R), mentre gli altri isomeri non mostrano tale effetto.[3]
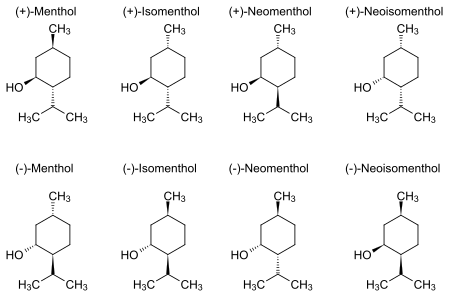
Il (-)-mentolo è il più stabile delle quattro forme: infatti presenta una configurazione "a sedia", con i sostituenti in posizione equatoriale che protendono verso l'esterno, e con il gruppo isopropile in posizione trans rispetto al gruppo alcol e metile. Questa disposizione relativa dei gruppi minimizza il loro reciprocoingombro sterico;negli altri stereoisomeri l'ingombro sterico reciproco tra i gruppi è maggiore.
Caratteristiche
[modifica|modifica wikitesto]
Il mentolo si presenta sotto forma dicristalliaghiformi incolori dal caratteristico odore di menta. È scarsamente solubile in acqua (circa 0,05%), mentre è molto solubile incloroformio,alcolioeteri.[4]
Come tutti i diastereoisomeri, gli isomeri del mentolo hanno la stessaformula brutae legami chimici, ma differiscono per l'orientazione spaziale dei sostituenti degli atomi di carboniostereogeniciC1, C2 e C5; di conseguenza, hanno proprietà chimiche molto simili, ma differiscono nella capacità di legare altre molecolechirali,come quelle presenti nei recettori delsistema nervoso:questo fa sì che ogni isomero abbia odore e gusto diverso dagli altri.
- (1R,2S,5R)-(-)-mentolo: molto rinfrescante, dolce, intenso sapore di menta.
- (1S,2R,5S)-(+)-mentolo: leggera sensazione di freddo, debole gusto alla menta con note erbacee.
- (1R,2R,5S)-(-)-neomentolo: odore stantio, gusto di menta, fresco.
- (1S,2S,5R)-(+)-neomentolo: leggermente fresco e rinfrescante gusto di menta.
- (1R,2S,5S)-(-)-isomentolo: debolmente rinfrescante, odore di canfora.
- (1S,2R,5R)-(+)-isomentolo: odore di canfora, fresco.
- (1S,2S,5S)-(-)-neoisomentolo: lieve potere rinfrescante, odore stantio e canforaceo.
- (1R,2R,5R)-(+)-neoisomentolo: molto poco rinfrescante, note erbacee.
Il mentolo reagisce come un normale alcol secondario. Può venir ossidato da agenti come l'acido cromico, diventando unchetone(il mentone) e in altre condizioni l'ossidazione può portare alla rottura dell'anello.
Il mentolo può facilmente essere disidratato per formare principalmente il 3-mentene.
Produzione
[modifica|modifica wikitesto]Il mentolo è uno deimonoterpenoididella menta, in cui viene prodotto perbiosintesi.Il componente (+)-pulegone è l'intermedio chiave di questa sintesi, in quanto può essereossidatoamentofuranooppure essereridottoa (+)-mentone o (+)-isomentone, che a sua volta per riduzione viene convertito in mentolo eacetato di mentile.
Data la grande richiesta di mentolo[5][6],oltre all'estrazione dalla menta piperita sono state messe a punto varie vie sintetiche per produrlo[3].
Una via sintetica parte dalcitronellale,il quale in seguito ad unaciclizzazioneinterna genera l'isopulegolo, il quale viene poiidrogenatoa mentolo; tuttavia la ciclizzazione del citronellale porta anche alla formazione degli altristereoisomeri,in quanto la reazione non è diastereoselettiva.
L'idrogenazione dal mircene
[modifica|modifica wikitesto]Un team guidato daRyōji Noyori,il quale verrà poi insignito delpremio Nobelproprio per queste ricerche, sviluppò un processo che, partendo dalmircene,permette di ottenere isopulegolo che viene idrogenato a mentolo. Si producono con questo processo via circa 3500 tonnellate annue.

Il mircene viene inizialmente attaccato dalladietilamminain presenza dilitioper formare un'amminaallilica. Successivamente uncatalizzatoreasimmetrico a base dirodioisomerizza il doppio legame allilico portando alla formazione di un'enammina,la quale subisce idrolisi per dare il (R)-citronellale. Il citronellale, in presenza di unacido di Lewis(zinco bromuro) ciclizza a (-)-isopulegolo che viene infine idrogenato a (1R,2S,5R)-(-)-mentolo.[6][3]
Il passaggio chiave è l'isomerizzazione catalitica del doppio legame che avviene in presenza di rodio legato a un legante asimmetrico (il S-BINAP), che permette di portare selettivamente verso l'enantiomero R.
Il processo Haarmann-Reimer
[modifica|modifica wikitesto]Un processo alternativo, noto come processo Haarmann-Reimer sintetizza iltimolodam-cresoloepropilene.[3][6][7]

Il timolo viene poiidrogenatoper dare la miscela dei vari stereoisomeri del mentolo. Questa miscela viene sottoposta adistillazione frazionataper estrarre il mentolo racemo, il quale viene fatto reagire conbenzoato di metileper dare il benzoato di mentile. Il (-)-mentolo viene quindi ottenuto per cristalizzazione frazionata, idrolisi dell'estere e ricristalizzazione con una purezza finale del 90%.
Altre tecniche
[modifica|modifica wikitesto]Altre strategie di sintesi prevedono l'uso di (-)-piperitone, 3-carene, (+)-pulegone, limonene.[6]
Applicazioni
[modifica|modifica wikitesto]Il mentolo viene usato in diversi prodotti.
In medicina viene utilizzato per alleviaremal di gola,come analgesico per ridurre lievi dolori comecrampi,mal di testaestrappi muscolari,essendo il mentolo un debole agonista deirecettori k-oppioidi.Inoltre è usato come decongestionante ed è presente in certi prodotti usati per curare scottature ederitemi solari.Lo si può trovare neiprodotti cosmetici.
Inapicolturasi è dimostrato efficace nella lotta contro laVarroa destructor.
Viene usato come additivo nellesigaretteper ridurre l'irritazione alla gola provocata dal fumo, ed in prodotti per l'igiene orale, comedentifriciecollutori,e comeadditivo alimentare(gomme da masticaree caramelle).
Secondo uno studio condotto da alcuni ricercatori dell'Università di Padova,stimola le cellule deltessuto adiposobianco inducendole a consumare igrassiproducendo calore.[8]Si pensa che il tessuto adiposo sia dotato di recettori di temperatura indipendenti dalsistema nervosoe che quindi venga indotto un aumento di temperatura con conseguente accelerazione delmetabolismoche permetterebbe il dimagrimento; questo meccanismo è ancora oggetto di studio nella comunità scientifica.
Infine può essere utilizzato per stimolare lalacrimazione,tecnica sfruttata dagli attori per piangere nelle scene in cui ciò è richiesto.[9]
Note
[modifica|modifica wikitesto]- ^scheda del (1R,2S,5R)-(-)-mentolo suSigma Aldrich
- ^(EN)menthol | Definition, Structure, & Uses,suEncyclopedia Britannica.URL consultato il 12 aprile 2020.
- ^abcd(EN) Johannes Panten e Horst Surburg,Ullmann's Encyclopedia of Industrial Chemistry,Wiley-VCH Verlag GmbH & Co. KGaA, 26 novembre 2015, pp. 1–55,DOI:10.1002/14356007.t11_t01,ISBN978-3-527-30673-2.URL consultato il 12 aprile 2020.
- ^(EN) PubChem,l-Menthol,supubchem.ncbi.nlm.nih.gov.URL consultato il 12 aprile 2020.
- ^New Process for Menthol Production:: News:: ChemistryViews,suchemistryviews.org.URL consultato il 12 aprile 2020.
- ^abcd(EN)6: Strategies in (-)-Menthol Synthesis,suChemistry LibreTexts,20 novembre 2014.URL consultato il 12 aprile 2020.
- ^(EN) Bernd Schäfer,Menthol: Minze versus Tagasako-Prozess,inChemie in unserer Zeit,vol. 47, n. 3, 2013-06, pp. 174–182,DOI:10.1002/ciuz.201300599.URL consultato il 12 aprile 2020.
- ^https:// unipd.it/sites/unipd.it/files/20140124b.pdf
- ^(EN) Ashlee Robbins, Masayuki Kurose e Barbara J. Winterson,Menthol Activation of Corneal Cool Cells Induces TRPM8-Mediated Lacrimation but Not Nociceptive Responses in Rodents,inInvestigative Ophthalmology & Visual Science,vol. 53, n. 11, 1º ottobre 2012, pp. 7034–7042,DOI:10.1167/iovs.12-10025.URL consultato il 10 dicembre 2020.
Voci correlate
[modifica|modifica wikitesto]Altri progetti
[modifica|modifica wikitesto] Wikimedia Commonscontiene immagini o altri file sumentolo
Wikimedia Commonscontiene immagini o altri file sumentolo
Collegamenti esterni
[modifica|modifica wikitesto]- (EN) Leroy G. Wade,menthol,suEnciclopedia Britannica,Encyclopædia Britannica, Inc.
| Controllo di autorità | LCCN(EN)sh85083726·GND(DE)4378972-9·BNF(FR)cb137450553(data)·J9U(EN,HE)987007565556905171 |
|---|
