Alkeny
Alkeny–organicznezwiązki chemicznez grupywęglowodorów nienasyconych,w których występuje jedno podwójnewiązanie chemicznemiędzy atomami węgla (C=C)[1].Razem ze związkami, które posiadają dwa lub więcej wiązań podwójnych (polienami,takimi jakdieny,trienyitd.) oraz z analogami pierścieniowymi (cykloalkenamiicyklopolienami) tworzą grupęolefin[2].Mają więcejizomerówi są bardziej aktywne niżalkany.Wraz ze zwiększającą się długościąłańcucha węglowegomaleje ich reaktywność. Można je otrzymać z ropy naftowej, a w laboratorium w reakcji eliminacjifluorowcazhalogenków alkilowychlub przezdehydratacjęalkoholi.Ich wzór ogólny toC
nH
2n.
Nazewnictwo
[edytuj|edytuj kod]Nazwy alkenów są tworzone z nazw odpowiednich alkanów. Z nazwy alkanu posiadającego ten sam szkielet węglowy usuwa się końcówkę-ani dodaje końcówkę-en,przed którą umieszcza sięlokant,wskazujący przy którym atomie węgla występuje podwójne wiązanie. Na przykład:
Lokant można pominąć, gdy jest on równy 1 (wtedy, gdy wiązanie podwójne występuje na początku szkieletu węglowego).
Nazewnictwodienówi polienów jest tworzone analogicznie z odpowiednio większą liczbą lokantów i końcówką-dien,-trien,-tetraenitd. Na przykład:
W literaturze spotyka się też nazewnictwo, które różni się od nomenklaturyIUPACtym, że lokanty występują przed nazwą. Przykładowo:
- 2-heksen; 1,3-butadien.
Izomeria
[edytuj|edytuj kod]Alkeny o większej liczbie atomów węgla niżpropenmogą istnieć w kilku formachizomerycznychna skutek rozgałęzienia łańcucha węglowego, zmiany umiejscowieniapodwójnych wiązańchemicznych i występowaniu zjawiskaizomerii geometrycznej.Eteni propen nie posiadają izomerów, abutenma ich 4.
Otrzymywanie
[edytuj|edytuj kod]Alkeny otrzymuje się poprzezeliminacjęcząstki nieorganicznej zhalogenopochodnych alkanów(dehydrohalogenacja) lubalkoholi(dehydratacja), wkrakingu,bądź reakcjiuwodornieniaalkinów.
- Dehydratacja alkoholi. Reakcję prowadzi się w podwyższonej temperaturze w obecnościkatalizatorakwasowego, np.tlenku glinulubkwasu siarkowego[3].W przypadku, gdy możliwe jest powstawanie różnych izomerów, produktem głównym jest ten, w którym wiązanie wielokrotne występuje między atomami węgla uboższymi w wodór[3](reguła Zajcewa,obowiązuje także dla dehydrohalogenacji)[4].
- Deaminacjaamin(eliminacja Hofmanna), w wyniku której otrzymuje się alkeny o położeniu wiązania podwójnego przeciwnie do reguły Zajcewa[5].
- Dehydrohalogenacja halogenoalkanów w środowisku zasadowym w podwyższonej temperaturze, np. wobeczasady potasowej[6].
- Reakcja wicynalnych (tj. zawierających atomy halogenu w pozycjach sąsiednich) dihalogenoalkanów zcynkiem[7].
- Otrzymywanie na skalę przemysłową z wykorzystaniem metodykrakowaniawyższych alkanów[8].
- Wropach naftowychwystępują w nieznacznych ilościach, toteż większość alkenów stosowanych w przemyśle pochodzi z przeróbki (krakinguniskociśnieniowego, tzw. olefinowego) różnych frakcji ropy, główniebenzyny ciężkiej.
Charakterystyczne reakcje
[edytuj|edytuj kod]Alkeny są trwałymi związkami, które jednak są bardziej reaktywne odalkanów. Podlegają one m.in.: reakcjompolimeryzacjiwinylowej oraz reakcjomaddycjinp.: przyłączania gazowegochloru,chlorowodoru,wody.
Przykładowa reakcja addycji chloru do etenu:
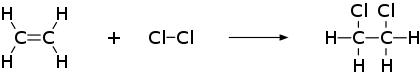
Alkeny o większej ilości wiązań podwójnych
[edytuj|edytuj kod]Alkeny z dwoma podwójnymi wiązaniami todieny.Alkeny z więcej niż dwoma wiązaniami podwójnymi (trieny, tetraeny itd.) są ogólnie nazywanepolienami. Dieny można podzielić na:
- allenyzwane też dienami skumulowanymi, w których wiązania podwójne sąsiadują ze sobą,
- dieny sprzężone, w których wiązania podwójne oddzielone są jednym wiązaniem pojedynczym,
- dieny z izolowanym układem wiązań podwójnych, w których występują co najmniej 2 wiązania pojedyncze pomiędzy wiązaniami podwójnymi.
Zobacz też
[edytuj|edytuj kod]Przypisy
[edytuj|edytuj kod]- ↑Alkeny,[w:]A.D.McNaught,A.Wilkinson,Compendium of Chemical Terminology (Gold Book),S.J. Chalk (akt.),International Union of Pure and Applied Chemistry,wyd. 2, Oxford: Blackwell Scientific Publications, 1997,DOI:10.1351/goldbook.A00224,ISBN0-9678550-9-8(ang.).
- ↑Olefins,[w:]A.D.McNaught,A.Wilkinson,Compendium of Chemical Terminology (Gold Book),S.J. Chalk (akt.),International Union of Pure and Applied Chemistry,wyd. 2, Oxford: Blackwell Scientific Publications, 1997,DOI:10.1351/goldbook.O04281,ISBN0-9678550-9-8(ang.).
- ↑abMorrison i Boyd 1985 ↓,s. 211–222.
- ↑Morrison i Boyd 1985 ↓,s. 559.
- ↑Morrison i Boyd 1985 ↓,s. 849–851.
- ↑Morrison i Boyd 1985 ↓,s. 199–203.
- ↑Morrison i Boyd 1985 ↓,s. 199.
- ↑Morrison i Boyd 1985 ↓,s. 197.
Bibliografia
[edytuj|edytuj kod]- Robert T.Morrison,Robert N.Boyd,Chemia organiczna,t. 1, Warszawa:PWN,1985,ISBN83-01-04166-8.
