Granica faz
Granica faz,powierzchnia międzyfazowa,granica międzyfazowa– granica międzyfazamiukładudwufazowego (ciecz–ciało stałe,ciecz–gaz,ciało stałe–gaz, ciało stałe–ciało stałe, dwie ciecze niemieszające się), na której następuje szybka zmianafizykochemicznychwłaściwości układu (często określana jako skokowa)[1].
Wewnętrzne granice faz w stopach metali
[edytuj|edytuj kod]Gdy obie sąsiadujące fazy sąciałami krystalicznymi(na przykład fazy wstopach metali,tworzące ichstrukturę) wyróżnia się typy wewnętrznych granic o różnejkoincydencji(zgodności położenia atomów) obusieci krystalicznych[2][3]:

- granice koherentne – zgodność położenia wszystkich węzłów obu sieci
- granice półkoherentne (semikoherentne) – część węzłów wspólnych (duża liczbadefektów sieci krystalicznychw okolicy ich spojenia)
- granice niekoherentne – węzły granicy faz znacznie przemieszczone względem położeń charakteryzujących obie sieci (zerwanie spójności, konsekwencją jest największeumocnienie metalu)
Granice koherentne lub semikoherentne występują na przykład między siecią przesyconegoroztworu stałegowęgla w sieciγ-Fe(austenitszczątkowy) amartenzytem,powstającym w czasiehartowaniastali.


Wzrost liczby wewnętrznych naprężeń sieci w otoczeniu granic międzyfazowych powoduje spadekplastycznościmetalu. Zmniejsza też odporność nakorozję elektrochemiczną,ponieważ zdefektowane granice faz mają mniejszypotencjałniż ich uporządkowane wnętrze (sąanodamiogniwkorozji międzykrystalicznej).
Inne granice faz (przykłady)
[edytuj|edytuj kod]Wiedza na temat powierzchni międzyfazowych ciało stałe–ciecz, ciało stałe–gaz, ciecz–ciecz, ciecz–gaz wchodzi w zakrestermodynamikiikinetykiprzemian fazowych.Stanowi teoretyczną podstawęadsorpcji,absorpcji,krystalizacji,destylacji(parowania i skraplania),ekstrakcji.Procesy te prowadzą do ustalenia się stanurównowagi dynamicznejmiędzy graniczącymi fazami. Występują między nimi warstwyamorficzne,na przykład fazy o pośrednich wartościach stężenia składników graniczących faz.
Granice ciało stałe–gaz i ciało stałe–ciecz
[edytuj|edytuj kod]
Graniczne warstwy przejściowe o różnej grubości powstają między powierzchnią ciał stałych i cieczą lub gazem w układach, w których zachodzą na przykład:
- przemiany fazowe(np. w czasie powstawania zarodkówkrystalizacjiobszar przejściowy obejmuje przypowierzchniową warstewkę cieczy i zewnętrzną warstwę rosnącego kryształu)
- procesy wymiany masy między fazami, między innymidyfuzja,adsorpcja, absorpcja (np. w przypadku procesu adsorpcji z cieczy na powierzchni ciała stałego stężenia składników w ciekłej „fazie objętościowej” są inne niż w fazie powierzchniowej – większe lub mniejsze – co wyraża się przez dodatni lub ujemny „nadmiar powierzchniowy”;grubość fazy powierzchniowej odpowiada często kilku średnicom cząsteczek adsorbatu).
Granice ciecz–ciecz i ciecz–gaz
[edytuj|edytuj kod]


Granice ciecz–ciecz i ciecz–gaz występują w układach, w których zachodzą na przykład:
- parowanieiskraplanie
- absorpcjaidesorpcja
- powstawanie warstwniemieszających się cieczylubemulsji
Charakterystycznym przykładem fazy powierzchniowej jest warstwa cieczy, znajdująca się między dwoma ciekłym fazami objętościowymi o różnych właściwościach, np. określonych wartościach stężeń składników. W fazie powierzchniowej stężenia tych składników monotonicznie rosną lub maleją w miarę przemieszczania się punktu od fazy pierwszej do drugiej (amorfizm).
Najważniejszą rolę wbiologii,odgrywają bardziej ostre granice między roztworami (np.cytoplazma,płyn zewnątrzkomórkowy,błona komórkowa). Powstawanie i trwałość granic między roztworami wodnymi icieczami niepolarnymi(np.tłuszcze) jest często związana z obecnością związków o właściwościachamfifilowych,między innymifosfolipidówlubglikolipidów.Takie związki samorzutnie gromadzą się na powierzchni roztworów wodnych, tworząc uporządkowane warstwy, w których są skierowane grupąhydrofilowąw kierunku wody. Mechaniczne wstrząsanie może wówczas prowadzić do utworzenialiposomów,zbudowanych analogicznie dobłony komórkowejwszystkich organizmów żywych. Analogiczne zjawiska umożliwiają stabilizacjęemulsji.
W niektórych układach ciecz–ciecz trwałośćkoloidówjest związana z powstawaniem na granicy fazpodwójnej warstwy elektrycznej(np. koloidy liofobowe, mleko). Takie warstwy powstają również w procesiepolaryzacjibłony komórkowejneuronów.
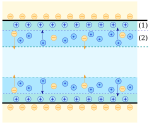
Międzyfazowe warstwy graniczne o charakterystycznym, amorficznym rozkładzieładunków elektrycznych(jonów) powstają również na powierzchni znajdujących się welektroliciecząstek stałych lub pęcherzyków gazu.
Przypisy
[edytuj|edytuj kod]- ↑Encyklopedia techniki; Metalurgia.T. Metalurgia. Katowice: Wydawnictwo „Śląsk”, 1978, s. 186.
- ↑Encyklopedia techniki, Materiałoznawstwo.T. Materiałoznawstwo. Warszawa: PWN, 1969, s. 263–264.
- ↑Defekty (defekty liniowe, defekty powierzchniowe).[w:]Fizyka; Rzeczywista struktura materii[on-line]. oen.dydaktyka.agh.edu.pl. [dostęp 2016-03-21].
Bibliografia
[edytuj|edytuj kod]- Zjawiska powierzchniowe. W: S Bursa:Chemia fizyczna.Warszawa: PWN, 1979.ISBN83-01-00152-6.
- P.W. Atkins:Chemia fizyczna.Warszawa: PWN, 2001.ISBN83-01-13502-6.
- J. Ościk:Adsorpcja.Warszawa: PWN, 1973.ISBN83-01-00554-8.
