Kwasy karboksylowe
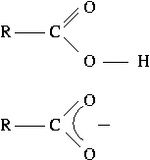
Kwasy karboksylowe– grupaorganicznychzwiązków chemicznychzawierającagrupę karboksylową.
Atomwodoruw grupie karboksylowej może się łatwo odszczepiać w formiejonu wodorowego,co zgodnie zteorią Arrheniusanadaje tym związkom charakterkwasowy:
- RCOOH + H
2O ⇄ RCOO−
+ H
3O+
Kwasy karboksylowe tworzą chętniewiązania wodorowez grupąaminową,hydroksylowąi innymi.
Kwasy karboksylowe z krótkimigrupami alkilowymisą dobrze rozpuszczającymi się w wodzie cieczami o ostrym, nieprzyjemnymzapachuitoksycznychwłaściwościach. Wraz ze wzrostem długości grupy alkilowej wzrastatemperatura topnieniatych kwasów (prawidłowość tę widać dla kwasów wyższych niżkwas heksanowy[1]). Kwasy karboksylowe zawierające poniżej 10 atomów węgla są cieczami w temperaturze pokojowej, a zawierające 10 lub więcej atomów węgla, ciałami stałymi. Kwasy monokarboksylowe zawierające 4–28 atomów węgla o prostym łańcuchu noszą nazwękwasów tłuszczowych(czasem pojęcie kwasów tłuszczowych rozszerza się na wszystkie alifatyczne niecykliczne kwasy karboksylowe)[2].
Otrzymywanie
[edytuj|edytuj kod]Kwasy karboksylowe otrzymuje się zwykle w reakcjach utleniania odpowiednichalkoholilubaldehydów:

Dogodnymi metodami otrzymywania kwasów karboksylowych są równieżhydrolizanitrylii dekarboksylacja kwasów dikarboksylowych.
Charakterystyczne reakcje
[edytuj|edytuj kod]Kwasy karboksylowe ulegają takim samym reakcjom jak zwykłe kwasy nieorganiczne. Tworzą onesolezzasadaminieorganicznymi i organicznymi. Reagują również zalkoholamitworzącestry.Estry kwasów tłuszczowych zglicerynąnazywane sątłuszczami.
Tworzenie chlorków kwasowych
[edytuj|edytuj kod]W wyniku reakcji ztrichlorkiem fosforu(PCl3) lubchlorkiem tionylu(SOCl2) przechodzą wchlorki kwasowe:

Odwadnianie
[edytuj|edytuj kod]Inną charakterystyczną reakcją dla kwasów karboksylowych jest reakcja odwadniania, w wyniku której powstajebezwodnik kwasowy:

Redukcja do alkoholi
[edytuj|edytuj kod]Pod wpływemtetrahydroglinianu litukwasy karboksyloweredukują siędo odpowiednich alkoholi. W pierwszym etapie tej reakcji tworzy się kompleksowa sól kwasu karboksylowego:

W dalszych etapach następują kolejne przeniesienia anionów wodorkowych od glinu do atomu węgla grupy karboksylowej, przy czym anion karboksylanowy redukuje się najpierw do aldehydu, a następnie doalkoholanu:

Otrzymany alkoholan poddaje się następniehydroliziew celu wydzielenia wolnego alkoholu:

Ważniejsze kwasy karboksylowe
[edytuj|edytuj kod]Kwasy monokarboksylowe
[edytuj|edytuj kod]- kwas mrówkowy
- kwas octowy
- kwas propionowy
- kwas masłowy
- kwas walerianowy
- kwas pelargonowyCH3(CH2)7COOH.
Aromatyczne z innymi grupami funkcyjnymi, np.hydroksykwasy
Aromatyczne
Z innymi grupami funkcyjnymi
Inne kwasy karboksylowe
[edytuj|edytuj kod]Trikarboksylowe z innymi grupami funkcyjnymi
Zobacz też
[edytuj|edytuj kod]Przypisy
[edytuj|edytuj kod]- ↑Robert T. Morrison, Robert N. Boyd:Chemia organiczna.T. 1. Warszawa:PWN,1985, s. 668.ISBN83-01-04166-8.
- ↑Fatty acids,[w:]A.D.McNaught,A.Wilkinson,Compendium of Chemical Terminology (Gold Book),S.J. Chalk (akt.),International Union of Pure and Applied Chemistry,wyd. 2, Oxford: Blackwell Scientific Publications, 1997,DOI:10.1351/goldbook.F02330,ISBN0-9678550-9-8(ang.).
