Powłoka elektronowa


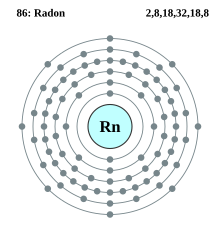
Powłoka elektronowa– zbiórstanów kwantowycho tej samej wartościgłównej liczby kwantowej.
Wchemiiza powłokę elektronową wokół danegoatomuuważa się zbiórorbitali atomowychmających tę samą główną liczbę kwantowąn.Kolejnym wartościomnprzypisane są kolejne powłoki: K, L, M, N, O, P i Q. Powłoki składają się z różnej liczby podpowłok elektronowych, odpowiadających określonym rodzajom orbitali atomowych:
- K – jedenorbitals– może pomieścić maksymalnie 2elektrony
- L – jedensi 3orbitalep– może pomieścić maksymalnie 8 elektronów
- M – jedens,3pi 5d– może pomieścić maksymalne 18 elektronów
- N – jedens,3p,5di 7f– może pomieścić maksymalne 32 elektrony
- itd.
| Symbol powłoki | główna liczba kwantowan |
2n2 (maksymalna liczba elektronów) |
podpowłoki |
|---|---|---|---|
| K | 1 | 2 | s |
| L | 2 | 8 | s, p |
| M | 3 | 18 | s, p, d |
| N | 4 | 32 | s, p, d, f |
| O | 5 | 50 | s, p, d, f, g |
| P | 6 | 72 | s, p, d, f, g, h |
| Q | 7 | 98 | s, p, d, f, g, h, i |
Maksymalna liczba elektronów na podpowłokach (zgodnie ze wzoremn= 4l+ 2, gdzieltopoboczna liczba kwantowa):
- s (l= 0): 2 elektrony
- p (l= 1): 6 elektronów
- d (l= 2): 10 elektronów
- f (l= 3): 14 elektronów
- g (l= 4): 18 elektronów
- h (l= 5): 22 elektrony
- i (l= 6): 26 elektronów
Wbrew informacjom podawanym przez niektóre źródła, nie wszystkiegazy szlachetnemają całkowicie zapełnione powłoki elektronowe. Np.argonma w powłoce M zapełnione podpowłoki s i p, nie ma natomiast elektronów d. Maksymalnie zapełniona powłoka elektronowa nie musi być energetycznie korzystna – pierwsze odstępstwo od tej zasady obserwuje się dla atomupotasu,w którym ostatni elektron wchodzi na podpowłokę 4s, a nie 3d. Jest tak dlatego, że przy dużych liczbach atomowych wzrasta rola oddziaływania spin-orbital w porównaniu zoddziaływaniami elektrostatycznymi[1].
Zobacz też[edytuj|edytuj kod]
Przypisy[edytuj|edytuj kod]
- ↑Hermann Haken,Hans Christoph Wolf:Atomy i kwanty. Wprowadzenie do współczesnej spektroskopii atomowej.Warszawa: PWN, 1997, s. 362–367.ISBN83-01-12135-1.
Bibliografia[edytuj|edytuj kod]
- Adam Bielański:Chemia ogólna i nieorganiczna.Warszawa: Państwowe Wydaw. Naukowe, 1981, s. 81–89.ISBN83-01-02626-X.
