Linus Pauling
Linus Carl Pauling(Portland,28 de fevereirode1901—Big Sur,19 de agostode1994) foi umquímico quânticoebioquímicodosEstados Unidos.Também é reconhecido comocristalógrafo,biólogo moleculare pesquisador médico.
Pauling é amplamente reconhecido como um dos principais químicos doséculo XX.Foi pioneiro na aplicação daMecânica Quânticaem química e, em 1954, foi galardoado com oNobel de Químicapelo seu trabalho relativo à natureza dasligações químicas.Também efetuou importantes contribuições relativas à determinação daestrutura de proteínasecristais,sendo considerado um dos fundadores da Biologia Molecular. Durante as suas investigações esteve perto de descobrir a estrutura em hélice dupla doADN,descoberta essa efectuada mais tarde porJames WatsoneFrancis Crick,em 1953.
É ainda referenciado como sendo um académico versátil, devido à sua intervenção e perícia em campos diversos como aquímica inorgânica,química orgânica,metalurgia,imunologia,anestesiologia,psicologiaeradioatividade.
Pauling recebeu oNobel da Pazde 1962, pela sua campanha contra ostestes nuclearese é a única personalidade a ter recebido dois Prémios Nobel não compartilhados. As outras personalidades que receberam dois Prémios Nobel foramMarie Curie(Física e Química),John Bardeen(ambos emFísica),Frederick Sanger(ambos emQuímica) eBarry Sharpless(ambos em Química). Mais tarde na sua carreira científica, advogou o uso em maiores proporções, em dietas, devitamina Ce outros nutrientes. Generalizou as suas ideias nesta área com vista a definirMedicina Ortomolecular,que ainda é vista comométodo não ortodoxopela Medicina convencional. Pauling popularizou as suas ideias, análises, pesquisa e visões em vários livros de sucesso, mas controversos, sobre a temática da vitamina C e Medicina Ortomolecular.
Juventude[editar|editar código-fonte]

Nascido no noroeste dos Estados Unidos, filho de Hermann Heinrich William Pauling (1876-1910), de ascendênciaalemã,e de Lucy Isabelle Darling (1881-1926).[1]Os Pauling, de acordo comJohn Simmons,pertenciam a uma família peculiar; a tia de Linus chamava-se Stella "Dedos" Darling e era uma conhecida arrombadora de cofres.[2]Seu pai era umfarmacêuticoque, sem ter êxito comercial, fez que a sua família percorresse diferentes lugares do estado do Oregon.[1]Quando o seu pai morreu, em 1910, Lucy Isabelle teve que criar sozinha Linus e as suas duas irmãs, Pauline (1901-2003) e Frances Lucille (1904-1973). A família voltaria mais tarde a reinstalar-se em Portland.[1]
Durante a infância, Linus foi um leitor voraz, tanto que o seu pai chegou a escrever para um periódico local, pedindo sugestões de livros para mantê-lo ocupado.[1]Um dos seus amigos, Lloyd Jeffress, tinha um pequeno laboratório químico na sua habitação; e as experiências levadas a cabo neste laboratório despertaram o interesse de Pauling em se tornar umengenheiro químico.[1]
Durante os seus estudos no ensino médio, Pauling continuava com as experiências de química, buscando a maioria dos materiais e equipamentos utilizados em uma fábrica abandonada que existia perto do local onde o seu avô tinha trabalhado como guarda noturno.[1]
As más classificações que Pauling obteve emhistória dos Estados Unidosimpediram-no de obter, nessa altura, o seu diploma de ensino médio. A escola concedeu-lhe o diploma quarenta e cinco anos mais tarde, depois de ter ganho os seus dois Prémios Nobel.[1]
Estudos[editar|editar código-fonte]

Em 1917, Pauling ingressou na Universidade Agrícola do Oregon ( "OAC", denominada atualmente deUniversidade Estadual do Oregon), emCorvallis.Paralelamente aos seus estudos, Linus Pauling teve que trabalhar a tempo inteiro, devido às suas necessidades financeiras. Entre os empregos que teve, encontram-se o de distribuidor de leite, projeccionista numcinemae como trabalhador num estaleiro naval. No começo do seu segundo ano de estudos, Pauling propôs-se a encontrar emprego em Portland para poder ajudar financeiramente a sua mãe. Na mesma altura, na Universidade, propuseram-lhe que aceitasse uma cátedra dequímica analíticaquantitativa (um curso que ele mesmo acabava de concluir como estudante), que lhe permitiria, ao mesmo tempo, continuar os seus estudos.
Durante os seus dois últimos anos na OAC, Pauling estudou o trabalho deLewiseLangmuirsobre aconfiguração electrónicadosátomos,assim como a forma como estes se ligavam para formarmoléculas.Neste momento, decidiu seguir uma carreira de investigação, concentrando-se na compreensão da relação da estrutura atómica da matéria com as suas propriedades físicas e químicas, o que o levaria a converter-se num dos pioneiros da química quântica. Na OAC, teve a oportunidade de realizar as suas primeiras investigações respeitantes ao efeito que umcampo magnéticoexerce sobre a orientação de um cristal deferro.
Pauling gradou-se comoBachelor of Science,em 1922, na área deengenharia química.Imediatamente, procurou continuar os estudos com uma pós-graduação noInstituto de Tecnologia da Califórnia(Caltech) emPasadena.Em busca dodoutoramento,Pauling investigou a utilização dadifração de raios-X,na determinação dasestrutura dos cristais.Durante os seus três anos em Caltech, Pauling publicou sete artigos sobre a estrutura cristalina dos minerais. O primeiro deles foi publicado na revistaJournal of the American Chemical Society,e tratava a estrutura damolibdenita,MoS2.[3]Linus Pauling recebeu o doutoramentosumma cum laudeem 1925.
A 17 de Junho de 1923, Pauling casou-se com Ava Helen Miller, com quem teve três filhos e uma filha. O casal tinha-se conhecido na OAC, quando Pauling cursava o último ano de estudos. Miller foi aluna de Pauling no curso "Química para estudantes de Economia Doméstica".[4]
Carreira científica[editar|editar código-fonte]
Início[editar|editar código-fonte]
Tendo em vista a conclusão do seu doutoramento, Pauling recebeu uma bolsa daFundação Guggenheim,que lhe permitiu viajar para aEuropa,onde estudou sob a orientação deArnold SommerfeldemMunique,Niels BohremCopenhagaeErwin SchrödingeremZurique.Durante a sua estadia na OAC, Pauling tinha-se familiarizado com o trabalho dos três cientistas, pioneiros da química quântica. Teve ainda a oportunidade de presenciar um dos primeiros estudos, baseados em química quântica, sobre as ligações da molécula dehidrogénio.A investigação foi realizada porWalter HeitlereFritz London.Pauling consagrou os seus anos na Europa a esta área, e decidiu torná-la a matéria principal das suas investigações futuras. Quando Pauling voltou aos Estados Unidos em 1927, obteve a posição deProfessor assistentede química teórica em Caltech.
Os primeiros cinco anos da carreira de Pauling, decorridos em Caltech, foram muito produtivos, tendo aplicado a mecânica quântica ao estudo de átomos e moléculas, no seguimento de seus estudos sobre cristais, utilizando a difração deraios X.Neste período, Pauling publicou cerca de cinquenta artigos, e criou as cinco regras de Pauling, desenvolvidas para determinar a estrutura molecular dos cristais complexos. Em 1929, foi nomeadoProfessor associado,e no ano seguinte recebeu o título deProfessor.
Em 1930, Pauling teve uma estadia de verão na Europa, durante a qual trabalhou no instituto de Arnold Sommerfeld. Nesse período, Pauling viu a possibilidade de utilizar oselectrõespara os estudos de difração, tal como tinha usado, para o mesmo efeito, os raios X. No seu regresso, construiu um aparelho de difração electrónica, auxiliado pelo estudante L. O. Brockway. O aparelho foi utilizado para estudar a estrutura molecular de um grande número de substâncias químicas. Em 1931, Pauling recebeu oPrémio Langmuir,outorgado pelaAmerican Chemical Society,pelo trabalho científico mais significativo, realizado por um investigador com menos de 30 anos.
Em 1932, Pauling concebeu a noção deelectronegatividade.Utilizando diversas propriedades das moléculas, especialmente o seumomento dipolare a energia necessária para romper as ligações químicas, estabeleceu aescala de Pauling,útil para a previsão da natureza das ligações químicas. A escala atribui um valor de electronegatividade à maioria doselementos químicos.Este valor resulta da medida da força com que os átomos de uma molécula se atraem entre si. Nesse mesmo ano, Pauling publicou o que é considerado o seu artigo mais importante, em que desenvolve o novo conceito dehibridizaçãodas orbitais atómicas, e realiza uma análise do carácter tetravalente docarbono.
Pauling desenvolveu uma forte amizade comRobert Oppenheimer,daUniversidade da Califórnia(Berkeley), que deslocava-se regularmente a Caltech como investigador e professor. Oppenheimer e Pauling planejaram trabalhar em conjunto na investigação das ligações químicas. Oppenheimer efectuaria os cálculos matemáticos e Pauling interpretaria os resultados. No entanto, os planos não se desenvolveram por completo, pois Pauling começou a suspeitar que o seu amigo se estava a aproximar demasiado da sua esposa, Ava Helen. Numa ocasião em que Pauling estava ausente a trabalhar, Oppenheimer convidou Ava Helen a encontrar-se com ele noMéxico.Ela recusou o convite de imediato, tendo avisado o seu marido. Este incidente, e a indolência com que Ava Helen o tomou, levaram Pauling a pôr fim à relação com o cientista de Berkeley, criando uma fria tensão que durou para o resto das suas vidas. Mais tarde, Oppenheimer propôs a Pauling a chefia na área de química doProjecto Manhattan.Pauling recusou a proposta, argumentando que erapacifista.
A natureza da ligação química[editar|editar código-fonte]
No início dadécada de 1930,Pauling começou a publicar as suas investigações sobre a natureza da ligação química, que levou, depois, à edição do seu famoso livro de textoThe Nature of the Chemical Bond,publicado em 1939. Este livro é considerado um dos mais importantes trabalhos de química jamais publicados. Pode-se ter uma ideia da sua influência bastando recordar que nos primeiros trinta anos após a sua primeira edição, o livro foi citado mais de 16 mil vezes por outros autores, o que faz dele a investigação mais citada como referência no meio científico. As investigações nesta área valeram a Pauling oNobel de Químicade 1954,"pelas suas investigações sobre a natureza da ligação química e suas aplicações na determinação da estrutura das substâncias complexas".

Como parte das suas investigações sobre a natureza da ligação química, Pauling criou o conceito dehibridizaçãodas orbitais atómicas. Amecânica quânticautiliza o número quânticolpara determinar o número máximo deelectrõesem cada orbital (denominando as orbitais com as letrass,p,d,f,geh); Pauling observou que para descrever a ligação química nas moléculas, é preferível construir funções que são uma mistura destas orbitais. Por exemplo, as orbitais2se2pde um átomo de carbono, podem-se combinar para formar quatro orbitais equivalentes, chamadasorbitais híbridas sp³.Estas orbitais híbridas podem descrever melhor a existência de compostos como ometano,de geometriatetraédrica.De forma similar, a orbital2spode combinar-se com duas orbitais2p,formando três orbitais equivalentes, chamadosorbitais híbridos sp²,sendo que a terceira orbital2pnão se hibridiza. Esta estrutura permite descrever oscompostos insaturados,como oetileno.
Pauling estava também interessado em compreender a relação entre asligações iónicas,em que os electrões são transferidos de um átomo para outro, e asligações covalentes,em que ambos os átomos fornecem electrões. Pauling demonstrou que estes dois tipos de ligação são, na realidade, casos extremos, e que a maioria das ligações químicas são na realidade uma combinação de ligação iónica com covalente. É nesta temática onde a noção deelectronegatividadeé especialmente útil, pois a diferença entre as electronegatividades dos átomos participantes numa ligação é a medida mais adequada para prever o grau de ionicidade de uma ligação.

Ainda na área das ligações químicas, o terceiro tema estudado por Pauling incidia na compreensão e descrição da estrutura doscompostos aromáticos;especialmente obenzeno(C6H6), o composto mais simples dentro dos aromáticos.
A estrutura do benzeno sempre havia sido motivo de controvérsia entre os cientistas, pois não era clara a forma como seis átomos de carbono e seis de hidrogénio poderiam conectar-se, satisfazendo todo o seu potencial de ligação.[5]Até essa altura, a melhor descrição sobre a dita estrutura, era a formulada pelo químicoalemãoFriedrich Kekulé.Kekulé descrevia o benzeno como a transição rápida entre duas estruturas em que havia alternância de posição das ligações simples e duplas. Pauling propôs uma estrutura intermédia, baseada na mecânica quântica, que considera uma sobreposição das duas estruturas de Kekulé. Posteriormente, este fenómeno recebeu o nome deressonância(ou mesomeria).
De certo modo, a ressonância é análoga ao fenómeno de hibridização das orbitais atómicas, já que consiste na combinação de várias estruturas electrónicas: nela, as orbitais de diferentes átomos de carbono combinam-se para formar asorbitais moleculares.
Estrutura do núcleo atômico[editar|editar código-fonte]
A 16 de Setembro de 1952, Linus Pauling começou um novo caderno de apontamentos com as palavras "Decidi atacar o problema da estrutura do núcleo".[6]Treze anos depois, Pauling publicou o seu modelo de núcleo atómico nas revistasScienceeProc. Natl. Acad. Sci.[7]Durante as seguintes três décadas, Pauling continuou a publicar artigos baseados no dito modelo.
No entanto, poucos livros de texto modernos referem este modelo. O modelo dá uma perspectiva única sobre a forma como cadeias de núcleos podem formar estruturas, de acordo com a mecânica quântica. Em 2006, Norman D. Cook, na sua revisão sobre vários modelos de estrutura atómica, disse sobre o modelo de Pauling que "leva a uma construção sensata dos núcleos e tem uma lógica inerentemente difícil de negar....no entanto....os teóricos nucleares não aprofundaram a ideia, e o modelo de Pauling não entrou no comum da investigação atómica teórica", não concluindo que o modelo de Pauling fora substituído por um modelo superior, mas simplesmente ignorado.
As cadeias de Pauling, incluem osisótoposdeutério,hélioetrítio.Os núcleos eram descritos como cadeias departículas alfa,o que é frequente para núcleos leves. Pauling tentou descrever a estrutura nuclear a partir dossólidos platónicos,em vez de partir de um modelo de partículas baseado noprincípio de exclusão de Pauli,mais tradicional. Foi por vezes dito que estas investigações teriam recebido maior atenção da comunidade científica se tivessem sido levadas a cabo por um cientista menos famoso; mais certo era que Pauling estava a tentar, de forma inovadora, entender o trabalho deMaria Goeppert-Mayer,efectuado no fim dadécada de 1940,respeitante à estrutura do núcleo atómico.
Investigações em biologia molecular[editar|editar código-fonte]
Em meados dadécada de 1930,Pauling interessou-se por uma nova disciplina científica. No início da sua carreira, havia manifestado falta de interesse pelo estudo das moléculas biológicas. No entanto, enquanto esteve em Caltech, teve oportunidade de relacionar-se com biólogos de renome, comoThomas Hunt Morgan,Theodosius Dobzhansky,Calvin BridgeseAlfred Sturtevant,que o levaram a mudar de opinião. Começou, então, a estudar estas moléculas, graças a uma bolsa de estudo daFundação Rockefeller.Os seus primeiros trabalhos no tema incidiram sobre a estrutura dahemoglobina.Pauling propôs que a estrutura da hemoglobina se altera em função do ganho ou perda de um átomo deoxigéniopela molécula. Na sequência desta observação, Linus Pauling decidiu estudar de forma mais precisa a estrutura dasproteínas,utilizando adifração de raios-X,mas a estrutura proteica mostrou ser muito mais difícil de determinar usando esta técnica, em comparação com a estrutura dos cristais de minerais estudados anteriormente. Nesta década, ocristalógrafobritânicoWilliam Astburytinha obtido bons resultados usando raios-X, mas quando Pauling tentou reinterpretar as suas observações, em 1937, com auxílio damecânica quântica,não o conseguiu.
Foram necessários onze anos até que Pauling compreendesse a origem do problema. A sua análise matemática estava correta, mas os resultados de Astbury foram obtidos de tal maneira que as proteínas estavam inclinadas em relação às posições esperadas. Para explicar esta discrepância, Pauling propôs um modelo molecular da hemoglobina, no qual os átomos estavam posicionados em hélice, e aplicou esta ideia às proteínas em geral.
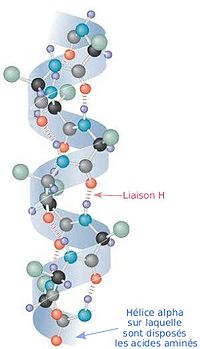
Em 1951, com base nas estruturas dosaminoácidose dospéptidos,e considerando a natureza planar daligação peptídica,Pauling e seus colegas propuseram que a estrutura secundária das proteínas era baseada naalfa-hélicee nafolha-beta.Esta conclusão exemplifica a capacidade de Pauling para pensar de maneira não convencional, pois a assumpção central da proposta radicava no facto de uma volta de hélice poder conter um número não inteiro de aminoácidos.
No seguimento, Pauling sugeriu uma estrutura helicoidal para oácido desoxirribonucleico(ADN), ainda que o seu modelo tivesse alguns erros, incluindo a proposição de grupos neutros de fosfato, ideia que estava em conflito com a natureza ácida, e não neutra, do ADN.[8]Sir Lawrence Braggdecepcionou-se, ao saber que Pauling tinha ganho a corrida para a descoberta da alfa-hélice. A equipa de Bragg tinha cometido um erro fundamental, ao não considerar a natureza planar da ligação peptídica. Quando nosLaboratórios Cavendishse soube que Pauling trabalhava com os modelos moleculares da estrutura do ADN,James WatsoneFrancis Crickforam autorizados a propor um modelo estrutural da molécula de ADN, utilizando material não publicado, dos investigadoresMaurice WilkinseRosalind Elsie Franklin,doKing's College.Em 1953, Watson e Crick propuseram a estrutura, ainda hoje considerada correta, para a dupla hélice do ADN, o que lhes valeria oNobel de Fisiologia ou Medicinade 1962. Um dos obstáculos que Pauling enfrentou durante a sua investigação foi a impossibilidade de consultar as fotografias de alta qualidade de difração do ADN que Franklin tinha efectuado. Quando Pauling as tentou ver num congresso em Inglaterra, o seu passaporte foi retido peloDepartamento de Estadodos Estados Unidos, sob a suspeita de ter simpatias pelo comunismo.[9]
Durante este período, Pauling também estudou as reacçõesenzimáticas.Encontra-se entre os primeiros cientistas que demonstraram que as enzimas atuam estabilizando osestados de transiçãodas reacções químicas, o que é fundamental para a compreensão do seu mecanismo de ação. Pauling está também entre os primeiros que propuseram que osanticorposse ligam aosantigéniosgraças a uma compatibilidade das suas estruturas. Seguindo a mesma ordem de ideias, escreveu um artigo juntamente comMax Delbrück,um físico convertido em biólogo, onde sugeria que a replicação do ADN é devida à complementaridade, e não à similitude, como tinha sido sugerido por outros cientistas. O modelo de Watson e Crick viria a corroborar esta ideia. Por outra parte, Pauling contribuiu também, juntamente com outros investigadores, para o fabrico de anticorpos artificiais, e para um substituto doplasma sanguíneo.
Genética molecular[editar|editar código-fonte]
Em Novembro de 1949, juntamente com Harvey Itano, S. J. Singer e Ibert Wells, Pauling publicou na revistaSciencea primeira prova da relação entre uma doença humana e uma alteração numa proteína específica.[10]Utilizando a técnica deelectroforese,demonstraram que ahemoglobinasofrera modificações em pacientes comanemia falciforme,e que pacientes que eram propensos a este tipo de anemia, sem tê-la desenvolvido, tinham dois tipos de hemoglobina: modificada e não modificada. Esta publicação foi a primeira demonstração de que ahereditariedade mendelianadeterminava as propriedades físicas específicas das proteínas e não apenas a sua presença ou ausência, marcando assim os primeiros passos dagenética molecular.
Automóvel elétrico[editar|editar código-fonte]

Nos finais dadécada de 1950,Pauling começou a interessar-se pelo problema dapoluição atmosféricae particularmente pelo fenômeno dosmog,que tinha vindo a crescer na cidade deLos Angeles.Nesta época, a maioria dos cientistas pensavam que osmogse devia às emissões dasrefinariase indústrias químicas. Graças aos trabalhos de Pauling,Arie Haagen-Smite outros investigadores de Caltech, demonstrou-se que o principal responsável do smog eram as emissões dos automóveis. Pouco tempo depois desta descoberta, começou a trabalhar no desenvolvimento de um automóvel elétrico que fosse funcional, mas barato. Para isso, uniu os seus esforços com os engenheiros da empresaEureka Williams,com vista ao desenvolvimento do primeiro automóvel eléctrico de velocidade controlável, oHenney Kilowatt.Depois de ter trabalhado no sistema depropulsão,Pauling demonstrou que osacumuladoresclássicos não podiam proporcionar uma potência suficiente para fazer os motores eléctricos comparáveis aosmotores de combustão interna.Também previu que oHenney Kilowattseria pouco popular, devido à baixa velocidade que alcançava e à sua reduzida autonomia. Dirigiu-se, então, à empresa Eureka Williams para pedir que detivessem o projeto até que se desenvolvesse uma bateria mais potente. A empresa preferiu fazer o lançamento, que conduziu a um fracasso comercial.
Medicina e vitaminas[editar|editar código-fonte]
Depois de ultrapassar os quarenta anos de idade, em 1941, Pauling descobriu que estava afetado por uma forma grave dadoença de Bright,uma enfermidade renal potencialmente mortal, considerada incurável pela medicina da época. Com a ajuda do doutor Thomas Addis, de Stanford, Pauling conseguiu controlar a doença seguindo uma dieta pobre emproteínase semsal,algo fora do comum para a época. Addis também receitava a todos os seus pacientes maiores consumos devitaminasesais mineraise Pauling não foi uma excepção.
Em finais dadécada de 1950,Pauling investigou a ação dasenzimassobre as funçõescerebrais.Pensava que as doenças mentais poderiam ser causadas, em parte, por disfunções enzimáticas. Quando em 1965 leu "A terapia deniacinaem psiquiatria ", publicação deAbram Hoffer,deu-se conta de que as vitaminas podiam ter importantes efeitosbioquímicosno organismo, para além dos relacionados com a prevenção de doenças provocadas por deficiência vitamínica. Em 1968, Pauling publicou na revistaScienceo seu mais importante artigo nesta área: "Psiquiatria ortomolecular [....]" (PMID 5641253), em que inventou a palavraortomolecularpara descrever o conceito de controlo da concentração dos compostos presentes no corpo humano, no sentido de prevenir e tratar doenças. As ideias aí apresentadas constituíram a base daMedicina Ortomolecular,fortemente criticada pelos profissionais da medicina tradicional.[11][12]
Nos anos seguintes, as investigações de Pauling sobre avitamina Cforam fonte de controvérsias, e alguns consideraram-nas fruto de charlatanismo.[13]Em 1966, Irwin Stone desenvolveu o conceito de cura à base de altas doses de vitamina C. Depois deste desenvolvimento, Pauling começou a tomar vários gramas da vitamina (3 gramas por dia, segundo algumas fontes[14]) para prevenir osresfriados.Entusiasmado com os resultados, interessou-se pela literatura sobre o tema, e em 1970 publicou "Vitamin C and the Common Cold"(" A vitamina C e o resfriado comum "). No ano seguinte, Pauling iniciou uma extensa colaboração com ooncologistabritânicoEwan Cameron,[15]trabalhando sobre o uso da vitamina C por via intravenosa ou por via oral em doentes decancroem fase terminal.
Cameron e Pauling escreveram vários artigos e um livro de divulgação chamado "A vitamina C e o cancro", descrevendo as suas observações. Ainda que os resultados parecessem ser favoráveis, a campanha de publicidade negativa de que foi alvo, minou-lhe a credibilidade e as suas investigações durante muitos anos.
Desde as suas campanhas de luta contra os testes nucleares, na década de 1950, até às suas investigações em Biologia Ortomolecular, Pauling sempre esteve na corda bamba. Em 1985, Pauling ficou sem apoio, tanto financeiro institucional, como dos seus colegas. Não obstante, Pauling colaborou com o médico Abram Hoffer no desenvolvimento de uma dieta que incluía a vitamina C em altas doses, como um tratamento complementar contra o cancro.
A ideia que Pauling promoveu, de elevar as doses de vitamina C de forma prolongada para prevenir várias doenças, sempre foram causa de controvérsia (QuackWatch,[16]Plos,[17]WebMD[18]), não impedindo, no entanto, que estudos posteriores voltassem a abordar o tema. Alguns médicos foram chamados para uma reavaliação cuidadosa do papel da vitamina C,[19]especialmente na forma intravenosa para o tratamento do cancro,[20][21]que continua também a ser controverso[22]e alvo de novas investigações.[23]
Em 1973, Linus Pauling fundou, juntamente com dois colegas seus, o Instituto de Medicina Ortomolecular em Menlo Park. Neste instituto, cujo nome foi alterado, de seguida, paraInstituto Linus Pauling de Ciência e Medicina,Pauling continuou a dirigir investigações sobre a vitamina C, mas também manteve o seu interesse em trabalhos de química e física teórica, até à sua morte em 1994. Durante os seus últimos anos de vida, interessou-se particularmente no possível papel que a vitamina C teria na prevenção daarterioesclerose,tendo publicado três artigos sobre o uso da vitamina C e dalisina,usadas para o alívio daangina de peito.Em 1996, dois anos depois da sua morte, o instituto mudou as suas instalações para Corvallis (Oregon), para formar parte da Universidade Estadual do Oregon. No instituto realizam-se investigações sobremicronutrientes,fitonutrientes e outras maneiras de prevenir e tratar doenças através da dieta humana.
Devido à sua insistência em promover o uso da Vitamina C para finalidades carentes de evidência científica de eficácia, Pauling é algumas vezes citado como um dos exemplares de casos daDoença do Nobel.[24][25][26]
Ativismo político[editar|editar código-fonte]
Pauling não exercera qualquer ativismo político até àSegunda Guerra Mundial,mas este conflito mundial mudou a sua vida profundamente, tornando-se ativista pela paz. Por altura do início doProjecto Manhattan,que levaria ao fabrico da primeirabomba atómica,Pauling recebeu uma oferta de Robert Oppenheimer, para encabeçar o departamento de química do projecto. Pauling recusou a proposta. Em 1946, juntou-se aoComité Emergencial de Cientistas Atómicos,dirigido porAlbert Einstein.A missão deste comité era alertar o público para os perigos associados ao desenvolvimento de armas nucleares. O ativismo de Pauling levou ao confisco de seu passaporte em 1952, quando se dirigia para um congresso emLondres.O passaporte foi restaurado em 1954, pouco antes de se deslocar aEstocolmo,a fim de receber o Prémio Nobel. No ano seguinte, Linus Pauling assinou oManifesto Russell-Einstein,juntando o seu nome ao deBertrand Russell,Albert Einstein e outros oito cientistas e intelectuais, que apelavam para a busca de soluções pacíficas durante aGuerra Fria.
Dois anos depois, Pauling redigiu uma petição com o biólogoBarry Commoner.Este tinha estudado a presença deestrôncio-90radioativonosdentes de leitede crianças dos Estados Unidos, concluindo que ostestes nuclearesna atmosfera tinham riscos para a saúde pública, em forma de precipitação radioativa. Também participou num debate público com o físico atómicoEdward Teller,sobre os riscos reais demutações genéticasprovocadas por estas precipitações.
Em 1958, Pauling e a sua esposa apresentaram, perante aOrganização das Nações Unidasuma carta assinada por mais de 11 mil cientistas, pedindo a suspensão dos testes nucleares. A pressão da opinião pública conduziu a uma moratória relativa a teste nucleares de superfície, seguida pela assinatura doTratado de Interdição Parcial de Ensaios Nucleares,por 113 países, em 5 de Agosto de 1963. Entre os subscritores, estavamJohn F. Kennedypelos Estados Unidos eNikita KhrushchovpelaUnião Soviética.O tratado entrou em vigor em Outubro desse ano. Logo após, Pauling recebeu oNobel da Pazde 1962 (o prémio foi reservado para que a data de entrega coincidisse com a data de entrada em vigor do tratado).
....a Linus Pauling, que desde 1946 tem advogado incessantemente, não somente contra os testes nucleares, nem somente contra a proliferação das armas nucleares, nem somente contra o seu uso; mas contra qualquer forma de resolver os conflitos internacionais pela via bélica.— Descrição do Prémio, pelo Comité Nobel Norueguês
Quando foi anunciado o prémio, o Departamento de Química de Caltech, ciente das suas visões políticas, não lhe endereçou qualquer tipo de congratulação. Contrariamente, o Departamento de Biologia ofereceu-lhe uma pequena festa, demonstrando assim a sua simpatia pelo seu trabalho sobre mutações induzidas por radiação. A desaprovação institucional relacionada com o ativismo de Pauling, motivou que este renunciasse do seu posto em Caltech, no ano de 1964. Depois disso, veio a trabalhar naUniversidade da Califórnia(San Diego), de 1967 a 1969 e mais tarde naUniversidade de Stanford,de 1969 a 1973.
Muitos dos detractores de Pauling apreciavam o seu trabalho científico, mas estavam em desacordo com a sua posição política, chegando a vê-lo como um ingénuo porta-voz do comunismo soviético. Em 1955, Pauling foi ordenado a comparecer diante do Subcomité de Segurança Interior do Senado, que o descreveu como "a personalidade científica número um, relacionada com virtualmente todas as atividades importantes da ofensiva pacifista-comunista que existe neste país". Pauling voltou a apresentar-se a este subcomité por várias vezes mais, em especial quando enviou a sua petição contra os testes nucleares. A revistaLifedescreveu o Nobel da Paz atribuído a Pauling como "um estranho insulto da Noruega". Em 1970, Pauling recebeu oPrémio Lenin da Paz,naURSS.
Até ao fim da sua vida, Pauling fez-se valer da sua notoriedade como personalidade pública, para protestar contra os conflitos armados, incluindo aguerra do Vietname.Foi também um crítico do intervencionismo dos Estados Unidos naAmérica Latina,especialmente naNicarágua.
Prêmios e distinções[editar|editar código-fonte]
O prêmio mais notável recebido por Linus Pauling foi oPrêmio Nobel,recebendo o deQuímicade 1954 e o daPazde 1962. Para além de Pauling, só mais três pessoas o receberam em mais de uma ocasião. Pauling, contudo, foi o único a tê-lo recebido individualmente das duas vezes. Para além do Nobel, foi várias vezes distinguido ao longo da sua carreira, entre as quais cabe destacar:
- 1931 Prêmio Langmuir, pelaAmerican Chemical Society
- 1933 Membro daUnited States National Academy of Sciences
- 1936 Membro daAmerican Philosophical Society
- 1946 Medalha Gibbs, pelaAmerican Chemical Society,secção deChicago
- 1947 Medalha Davy, pelaRoyal Society
- 1947 Membro daRoyal Society,Londres
- 1951 Medalha Lewis, pelaAmerican Chemical Society,secção deCalifórnia
- 1952 Medalha Pasteur, pelaSociedade Bioquímica de França
- 1954Nobel de Química
- 1956 Medalha Avogadro, pelaAcademia Italiana de Ciências
- 1960 Homem do Ano, segundo a revistaTime
- 1962 Prêmio Gandhi da Paz
- 1962Nobel da Paz
- 1970Prémio Lenine da Paz
- 1974Medalha Nacional de Ciências
- 1977Medalha de Ouro Lomonossov,outorgada pelaAcademia de Ciências da Rússia
- 1979 Primeiro agraciado com oPrêmio em Ciências Químicas NASpelaAcademia Nacional de Ciências dos Estados Unidos
- 1984Medalha PriestleypelaAmerican Chemical Society
Legado[editar|editar código-fonte]

A contribuição de Linus Pauling para o desenvolvimento científico noséculo XXé de especial importância. Pauling integrou uma lista com os vinte maiores cientistas de todos os tempos, segundo a revista britânicaNew Scientist.Pauling é, a par deAlbert Einstein,a única personalidade do século XX a aparecer na dita lista. Gautam R. Desiraju, autor deEnsaio do Milénio,na revistaNature(PMID 11100703), descreveu Pauling como um dos maiores pensadores e visionários do milénio, juntamente comGalileu,Newtone Einstein.[27]Outro aspecto de relevo em Pauling é a diversidade de suas investigações. Pauling moveu-se em diversas áreas, fazendo contribuições importantes emMecânica Quântica,Química Quântica,Química Inorgânica,Química Orgânica,Bioquímica,Biologia MoleculareMedicina,trazendo contribuições especialmente significativas nas fronteiras entre as ditas áreas. As suas investigações sobre a natureza das ligações químicas marcaram o início da Química Quântica, e muitos conceitos inovadores, como a hibridização de orbitais atómicas e a electronegatividade, fazem parte das bases da Química moderna, ainda que a teoria da hibridização fosse substituída pela teoria de orbitais moleculares deRobert Mulliken.Ainda que a teoria de Pauling falhasse ao não descrever quantitativamente algumas das características moleculares, como a naturezaparamagnéticado oxigénio, ou a cor dos compostosorganometálicos,a sua simplicidade fez com que perdurasse nos livros de química. O trabalho de Pauling sobre a estrutura cristalina contribuiu para o avanço na predição e entendimento das estruturas dos minerais. As suas descobertas sobre aalfa-hélicee afolha-betaestabeleceram a base para a compreensão e estudo da estrutura das proteínas. Na sua época, Pauling era comumente chamado depai da Biologia Molecular.Desde a altura em que Pauling entendeu que aanemia falciformeera uma enfermidade com bases moleculares, abriram-se as portas para o exame das mutações genéticas a um nível molecular.
Ainda que grande parte da comunidade científica não comungasse com as conclusões de Pauling nas suas investigações médicas a respeito do consumo de vitaminas, a participação de Pauling na polémica levou o público a sensibilizar-se para a importância do consumo de vitaminas e minerais na prevenção de doenças. A firme posição de Pauling nesta controvérsia, ajudou também a redobrar os esforços que outros investigadores dedicaram a este campo, incluindo os que laboram no Instituto Linus Pauling, onde uma dezena de investigadores e académicos exploram a importância dos micronutrientes na saúde humana.
Publicações[editar|editar código-fonte]
Livros[editar|editar código-fonte]
- ——; Wilson, E. B. (1985) [1935].Introduction to Quantum Mechanics with Applications to Chemistry.[S.l.]: Reimpresso porDover Publications.ISBN978-0-486-64871-2
- —— (1939).The Nature of the Chemical Bond and the Structure of Molecules and Crystals.[S.l.]:Cornell University Press
- —— (1947).General Chemistry: An Introduction to Descriptive Chemistry and Modern Chemical Theory.[S.l.]: W. H. Freeman
- Revisado e ampliado em 1947, 1953 e 1970. Reimpresso porDover Publicationsem 1988.
- ——; Hayward, Roger (1964).The Architecture of Molecules.Proceedings of the National Academy of Sciences of the United States of America.51.San Francisco: Freeman. pp. 977–84.ISBN978-0-7167-0158-3.PMC300194
 .PMID16591181.doi:10.1073/pnas.51.5.977
.PMID16591181.doi:10.1073/pnas.51.5.977
- —— (1958).No more war!.[S.l.]: Dodd, Mead & Co.ISBN978-1-124-11966-3
- —— (1977).Vitamin C, the Common Cold and the Flu.[S.l.]: W.H. Freeman.ISBN978-0-7167-0360-0
- —— (1987).How to Live Longer and Feel Better.[S.l.]: Avon.ISBN978-0-380-70289-3
- Cameron, E.;—— (1993).Cancer and Vitamin C: A Discussion of the Nature, Causes, Prevention, and Treatment of Cancer With Special Reference to the Value of Vitamin C.[S.l.]: Camino.ISBN978-0-940159-21-1
- —— (1998).Linus Pauling On Peace: A Scientist Speaks Out on Humanism and World Survival.[S.l.]: Rising Star Press.ISBN978-0-933670-03-7
- Hoffer, Abram; —— (2004).Healing Cancer: Complementary Vitamin & Drug Treatments.Toronto: CCNM Press.ISBN978-1-897025-11-6
- Ikeda, Daisaku; —— (2008).A Lifelong Quest for Peace: A Dialogue.Richard L. Gage (ed., trans.). Londres: I. B. Tauris.ISBN978-1-84511-889-1
Artigos[editar|editar código-fonte]
- —— (1927). «The Theoretical Prediction of the Physical Properties of Many-Electron Atoms and Ions. Mole Refraction, Diamagnetic Susceptibility, and Extension in Space».Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences.114(767): 181–211.Bibcode:1927RSPSA.114..181P.doi:10.1098/rspa.1927.0035

- —— (1929). «The Principles Determining the Structure of Complex Ionic Crystals».Journal of the American Chemical Society.51(4): 1010–1026.doi:10.1021/ja01379a006
- —— (1931). «The Nature of the Chemical Bond. I. Application of Results Obtained from the Quantum Mechanics and from a Theory of Paramagnetic Susceptibility to the Structure of Molecules».Journal of the American Chemical Society.53(4): 1367–1400.doi:10.1021/ja01355a027
- —— (1931). «The Nature of the Chemical Bond. II. The One-Electron Bond and the Three-Electron Bond».Journal of the American Chemical Society.53(9): 3225–3237.doi:10.1021/ja01360a004
- —— (1932). «The Nature of the Chemical Bond. III. The Transition from One Extreme Bond Type to Another».Journal of the American Chemical Society.54(3): 988–1003.doi:10.1021/ja01342a022
- —— (1932). «The Nature of the Chemical Bond. IV. The Energy of Single Bonds and the Relative Electronegativity of Atoms».Journal of the American Chemical Society.54(9): 3570–3582.doi:10.1021/ja01348a011
- ——; Wheland, G. W. (1933).«The Nature of the Chemical Bond. V. The Quantum-Mechanical Calculation of the Resonance Energy of Benzene and Naphthalene and the Hydrocarbon Free Radicals»(PDF).The Journal of Chemical Physics.1(6). 362 páginas.Bibcode:1933JChPh...1..362P.doi:10.1063/1.1749304.Cópia arquivada(PDF)em 9 de outubro de 2022
- —— (1935). «The Structure and Entropy of Ice and of Other Crystals with Some Randomness of Atomic Arrangement».Journal of the American Chemical Society.57(12): 2680–2684.doi:10.1021/ja01315a102
- —— (1940). «A Theory of the Structure and Process of Formation of Antibodies*».Journal of the American Chemical Society.62(10): 2643–2657.doi:10.1021/ja01867a018
- —— (1947). «Atomic Radii and Interatomic Distances in Metals».Journal of the American Chemical Society.69(3): 542–553.doi:10.1021/ja01195a024
- ——; Itano, H. A.;Singer, S. J.;Wells, I. C. (1949). «Sickle Cell Anemia, a Molecular Disease».Science.110(2865): 543–548.Bibcode:1949Sci...110..543P.PMID15395398.doi:10.1126/science.110.2865.543
- ——; Corey, R. B.;Branson, H. R.(1951).«The structure of proteins: Two hydrogen-bonded helical configurations of the polypeptide chain».Proceedings of the National Academy of Sciences.37(4): 205–11.Bibcode:1951PNAS...37..205P.PMC1063337
 .PMID14816373.doi:10.1073/pnas.37.4.205
.PMID14816373.doi:10.1073/pnas.37.4.205
Bibliografia[editar|editar código-fonte]
- Cruz-Garritz, D., Chamizo, J.A., Garritz, A.Estructura atómica.Addison-Wesley Iberoamericana, Wilmington, EE.UU., 1987.ISBN 0-201-64018-X
- Hager, Thomas.Force of Nature: The Life of Linus Pauling.Simon & Schuster, 1995.ISBN 0-684-80909-5
- Hager, Thomas.Linus Pauling and the Chemistry of Life,Oxford University Press, 2000.ISBN 0-19-513972-0
- Mead, Clifford; Hager, T.Linus Pauling: Scientist and Peacemaker,Oregon State University Press, 2001.ISBN 0-87071-489-9
- Marinacci, Barbara (ed.).Linus Pauling in His Own Words: Selections from His Writings, Speeches, and Interviews,Touchstone Books, 1995.ISBN 0-684-81387-4
- Goertzel, T., et al.Linus Pauling: A Life in Science and Politics,HarperCollins Publishers, 1996.ISBN 0-465-00673-6
- Serafini, A.Linus Pauling: A Man and His Science,iUniverse, 2000.ISBN 0-595-00101-7
- Bouguerra, Mohamed Larbi (dir.),Linus Pauling,Berlin, 2002.ISBN 2-7011-2658-4
Referências
- ↑abcdefgBiografia de Linus Pauling,em Nobelprize.org
- ↑Barth, John Simmons (2010).Os 100 Maiores Cientistas da História5ª ed. Rio de Janeiro - RJ: DIFEL. 115 páginas
- ↑The crystal structure of molybdeniteJ. Am. Chem. Soc.,45,6,pp. 1466–1471, 1923.
- ↑Cronologia da vida de Pauling,pela Universidade Estatal de Oregon.
- ↑O carbono tem a capacidade de formar quatro ligações de cada vez. Matematicamente, não se encontrava o mecanismo pelo qual seis átomos de carbono, que têm uma capacidade total de formar 24 ligações, se poderiam unir a seis átomos de hidrogénio, que têm uma capacidade de formar apenas seis ligações no total.
- ↑Facsimile do caderno.
- ↑Facsímile da publicação na revistaProc. Natl. Acad. SciArquivado em9 de julho de 2007, noWayback Machine., 54,4,pp. 989-994, 1965.
- ↑Descrição do modeloArquivado em18 de março de 2007, noWayback Machine..
- ↑Este evento marcou o início da época conhecida comoMacartismo,nos Estados Unidos.
- ↑Pauling, L. et al.Science110,543-8 (1949)PMID 15395398
- ↑Cassileth BR.Alternative medicine handbook: the complete reference guide to alternative and complementary therapies.W.W. Norton & Co., Nova York, 1998:67.
- ↑«"Vitamin Therapy, Megadose / Orthomolecular Therapy "Servicios de Salud Provincial de la Columbia Británica, 2000».Consultado em 10 de julho de 2007.Arquivado dooriginalem 2 de fevereiro de 2007
- ↑Barrett, Stephen.The Dark Side of Linus Pauling's Legacy(O lado obscuro do legado de Linus Pauling).
- ↑Dunitz, J. D. (1 de novembro de 1996).«Linus Carl Pauling. 28 February 1901-19 August 1994».Biographical Memoirs of Fellows of the Royal Society(em inglês).42(0): 316-338.doi:10.1098/rsbm.1996.0020
- ↑Publicaciones de Cameron, en doctoryourself.com.
- ↑Owebsitequackwatch.orgapresentou uma análise de Charles W. Marshall, de 1997, negando os efeitos da vitamina C.
- ↑PlosArquivado em27 de abril de 2006, noWayback Machine.publica um estudoaustralianode 2005, que confirma os efeitos benéficos da vitamina C.
- ↑WebMD,num estudo de 2007, mostra os efeitos curativos que a vitamina C têm sobre as células imunitárias.
- ↑Padayattyet al.,na revistaCanadian Medical Association Journal (CMAJ),Março de 2006Arquivado em6 de fevereiro de 2010, noWayback Machine..
- ↑As publicações nowebsitedo centroThe Bright Spot For HealthArquivado em9 de fevereiro de 2007, noWayback Machine.mostram que a vitamina C teve efeitos positivos na luta contra o cancro.
- ↑Artigo naNational Academy of Sciences,a favor do uso da vitamina C como arma contra as células cancerígenas.
- ↑Resumo da controvérsia.
- ↑Estudos em progresso.
- ↑Basterfield, Candice;Lilienfeld, Scott;Bowes, Shauna; Costello, Thomas (2020).«The Nobel disease: When intelligence fails to protect against irrationality».Skeptical Inquirer.44:32–37.Consultado em 6 de agosto de 2021
- ↑Gorski, David(18 de agosto de 2008).«High dose vitamin C and cancer: Has Linus Pauling been vindicated?».Science Based Medicine.sciencebasedmedicine.org.Consultado em 13 de maio de 2020
- ↑Gorski, David(4 de junho de 2012).«Luc Montagnier and the Nobel Disease».Science Based Medicine.sciencebasedmedicine.org.Consultado em 13 de maio de 2020
- ↑Desiraju, G.R.Nature408,407 (2000)PMID 11100703
Ligações externas[editar|editar código-fonte]
- Linus Pauling(em inglês) noMathematics Genealogy Project
- Publicações científicas selecionadas, em formato PDF
- «Perfil no sítio oficial do Nobel de Química 1954»(em inglês)
- «Perfil no sítio oficial do Nobel da Paz 1962»(em inglês)
| Precedido por Hermann Staudinger |
Nobel de Química 1954 |
Sucedido por Vincent du Vigneaud |
| Precedido por Dag Hammarskjöld |
Nobel da Paz 1962 |
Sucedido por Comitê Internacional da Cruz Vermelhae Federação Internacional das Sociedades da Cruz Vermelha e do Crescente Vermelho |
- Nascidos em 1901
- Mortos em 1994
- Linus Pauling
- Nobel da Paz
- Laureados dos Estados Unidos com o Nobel
- Nobel de Química
- Medalha Nacional de Ciências
- Presidentes da American Chemical Society
- Professores do Instituto de Tecnologia da Califórnia
- Químicos inorgânicos
- Químicos dos Estados Unidos
- Bioquímicos dos Estados Unidos
- Químicos do século XX
- Ateus dos Estados Unidos
- Humanistas dos Estados Unidos
- Pacifistas dos Estados Unidos
- Biofísicos dos Estados Unidos
- Pessoas na medicina alternativa
- Norte-americanos de ascendência alemã
- Naturais de Portland (Oregon)
- Pessoa do Ano
- Membros da Academia Nacional de Ciências dos Estados Unidos



