Hidroxid de sodiu
| Hidroxid de sodiu | |
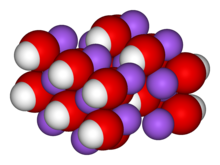 | |
| Denumiri | |
|---|---|
| Alte denumiri | leșie, sodă caustică |
| Identificare | |
| Număr CAS | 1310-73-2 |
| ChEMBL | CHEMBL2105794 |
| PubChemCID | 14798 |
| Informații generale | |
| Formulă chimică | NaOH |
| Aspect | substanțăsolidă,de culoarealbă |
| Masă molară | 39,997 g/mol |
| Proprietăți | |
| Densitate | 2,130 g/cm3 |
| Starea de agregare | solidă |
| Punct de topire | 322°C |
| Punct de fierbere | 1.388 °C |
| Solubilitate | ușor solubil înapă,1260 g/l (20 °C) |
| Presiune de vapori | 13 Pa (618 °C) |
| Sunt folosite unitățileSIși condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modificădate/text | |
Hidroxidul de sodiu(denumit șisodă causticăsauleșie) este obazăanorganicăcuformula chimicăNaOH. Ca formă de agregare este un corp solid, higroscopic, de culoare albă, fiind format dintr-uncationdesodiuși unanionhidroxid.
Soda caustică este o substanță puternic alcalină și caustică (pH=14 la c=1 mol/l), iar prin contactul cu pielea cauzează arsuri chimice severe. Este foarte solubilă înapășihigroscopică,absorbind umiditatea șidioxidul de carbondin atmosferă. Formează diverșihidrațicu formula NaOH·nH
2O.[2]
Reacționează cudioxidul de carbondin aer, rezultândcarbonat de sodiu,din această cauză soda caustică se păstrează în vase închise ermetic, pentru a evita contactul cu aerul sau umezeala.
Hidroxidul de sodiu este utilizat în foarte multe procese industriale, câteva exemple fiind: fabricareahârtiei,textilelor,săpunurilorșidetergenților.În anul 2004, producția la nivel mondial a fost de aproximativ 60 milioane detone,iar cererea a fost de 51 milioane de tone.[3]
Utilizări[modificare|modificare sursă]
- Hidroxidul de sodiu este folosit în cantități mari în multe industrii, mai ales ca solvent apos alături dehidroxidul de potasiu.
Este folosit pentru:
- Obținerea decelulozășihârtiedinlemnsau paie,
- Produse chimice și materiale plastice,
- Fabricarea desăpunșidetergenți,
- Fabricarea coloranților,
- Sinteza unor fibre textile artificiale,
- Mercerizareabumbacului(bumbacul devine mai mătăsos, ușor de colorat, mai rezistent
- Obținerea dealuminiu(prelucrarea bauxitei).

- Curățarea de ulei, grăsimi,petrol
- Rafinarea chimică auleiuluialimentar
- Sinteza chimică a diferitelor produse ca:hipoclorit de sodiu,fosfat de sodiu,sulfit de sodiu,aluminat de sodiu
- Sinteza deacid formic
- Producerea apei demineralizate: pentru a reglementa pH-ul și de a regenera schimbul de ioni staționari în rășini la tratarea apei.
- În electronică: producerea plăcilor conductoare (ca. 10g/l bei 20 °C)
- Este parte componentă a substanțelor de curățare a conductelor
- Proprietatea caustică e folosit în tratarea plăcilor de cupru pentru producătorii de modele
- Curățarea recipientelor din oțel sau metal inoxidabil
- Îndepărtarea coloranților
- În 1883 a fost fabricată olocomotivăcu aburi cu sodă fără folosireafocului
- În industria agro-alimentară se utilizează la curățarea instalațiilor (circuite, sticlă), modificareaamidonului,peeling chimic etc. Este, de asemenea, unaditiv alimentar(E524[4]), plus servește caregulator de aciditate[5]și este utilizat într-o gamă largă de produse[6].
- Producția mondială în 1998 a fost de aprox. 45 de milioane de tone. Hidroxidul de sodiu este solventul cel mai frecvent utilizat în laborator.
- Soda poate fi folosită pentru stocarea energiei solare în formă chimică. Ca efect, reacția dintre sodiu și apă este puternicexotermă.Soda diluată încă o dată, este utilizată pentru energia solară doar pentru a evapora apa și a reveni la starea inițială.
- Soda mai este utilizată ca reactiv pentru teste chimice. Într-adevăr, în prezența anumitor cationi metalici, hidroxidul de sodiu se precipită într-o anumită culoare.
Proprietăți fizico-chimice[modificare|modificare sursă]
- Substanță leșioasă
- Puternic electrolit favorizând electroliza apei
- Se dizolvă în substanțele polare degajându-se căldură de diluare
- Neutralizează acizii formând sărurile corespunzătoare radicalului ns
- Reacționează cu clorul, producând hipoclorit de sodiu (soluție diluată și rece) sau clorat de sodiu (soluție fierbinte concentrată):
- la rece
- la cald
Producerea[modificare|modificare sursă]
- Prin substituție acarbonatului de sodiucuhidroxid de calciu,rezultând hidroxid de sodiu șicarbonat de calciu:
Carbonatul de calciu mai puțin solubil va fi separat prin filtrare, în soluție rămânând numai soda caustică.
- Prinelectrolizădinclorură de sodiu(NaCl) -> leșie(NaOH) șiclor
- Procedeul industrial (de producere, purificare și concentrare a Na(OH):
- Metoda amalgam
- Metoda diafragmei
- Metoda membranei
- În laborator se poate obține direct din sodiu și apă:
- După procesul de condensare se obține soda caustică:
Vezi și[modificare|modificare sursă]
Referințe[modificare|modificare sursă]
- ^„Hidroxid de sodiu”,SODIUM HYDROXIDE(în engleză),PubChem,accesat în
- ^P. R. Siemens, William F. Giauque (1969): "Entropies of the hydrates of sodium hydroxide. II. Low-temperature heat capacities and heats of fusion of NaOH·2H2O and NaOH·3.5H2O".Journal of Physical Chemistry,volume 73, issue 1, pages 149–157.doi:10.1021/j100721a024
- ^Cetin Kurt, Jürgen Bittner (), „Sodium Hydroxide”,Ullmann's Encyclopedia of Industrial Chemistry,Weinheim: Wiley-VCH,doi:10.1002/14356007.a24_345.pub2
- ^Parlamentul EuropeanșiConsiliul Europei().„Directiva 95/2/CE despre aditivii alimentari cât și despre coloranți și despre îndulcitori”.Jurnalul official al Uniunii Europene.pp. 1–56. 95/2/CE.Accesat în.Parametru necunoscut
|no=ignorat (ajutor). - ^Codex alimentarius,ed. ().„Clasificarea și Sistemul de Numerotare Internațional pentru aditivi alimentari”.http://www.codexalimentarius.net.CAC/GL 361989. p. 1-35. Codex_Alimentarius. Arhivat dinoriginalla.Accesat în.Legătură externa în
|site=(ajutor). - ^engleză{{{1}}}Comisia Codex Alimentarius (2008).„Updated up to the 31st Session of the Codex Alimentarius Commission for Sodium hydroxide (524)”.http://www.codexalimentarius.net.GSFA Online. Codex Alimentarius. codex-gfsa-256. Arhivat dinoriginalla 2015-09-23.Accesat în10 martie2008.Verificați datele pentru:
|access-date=(ajutor);Legătură externa în|site=(ajutor)
Legături externe[modificare|modificare sursă]
| |||||







