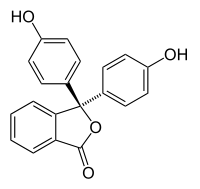
Fenolftalein
| Fenolftalein | |||
|---|---|---|---|
| |||
| IUPAC ime |
| ||
| Identifikacija | |||
| CAS registarski broj | 77-09-8 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | C20H14O4 | ||
| Molarna masa | 318.32 g mol−1 | ||
| Gustina | 1.277 g cm−3,at 32 °C | ||
| Tačka topljenja |
262.5 °C | ||
| Tačka ključanja |
N/A | ||
| Rastvorljivostuvodi | Nerastvoran | ||
| Rastvorljivostu Drugi rastvarači | Nerastvoran ubenzenu,veoma rastvoran uetanoluietru,u manjoj meri uDMSO | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose nastandardno stanje (25 °C, 100 kPa)materijala | |||
| Infobox references | |||
Fenolftaleinjehemijsko jedinjenjesaformulomC20H14O4.On se često označava sa "HIn"ili"phph".Često se koristi utitracijama,on je bezbojan ukiselimrastvorima i roze ubaznimrastorima.[1]Ako je koncentracija indikatora posebno jaka, on može da izgleda ljubičasto.
U jakim baznim rastvorima, fenolftalein roze boja podleže prilično sporoj reakciji izbleđavanja i on ponovo postaje bezbojan. Ovaj molekul ima četiri forme:
| Vrste | In+ | H2In | In2− | In(OH)3− |
|---|---|---|---|---|
| Struktura |  |
 |
 |

|
| Model |  |
 |
 |

|
| pH | <0 | 0−8.2 | 8.2−12.0 | >12.0 |
| Uslovi | jako kiselo | kiselo ili blizo-neutralnom | bazno | jako bazno |
| Boja | narandžasta | bezbojno | roze | bezbojno |
| Slika |  |
 |
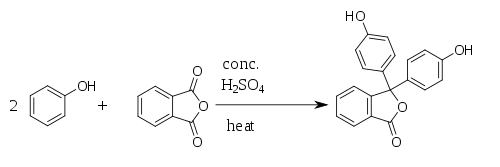
Fenolftalein se sintetiše kondenzacijomftalnog anhidridasa dva ekvivalentafenolapod kiselim uslovima. Ovu reakciju je otkrio1871.godineAdolf fon Bajer.
Fenolftaleinjeindikatorkoji menja boju u odnosu na sredinu. Ako je sredinakisela,on neće promeniti boju (ostaće bezbojan), a ako je sredinabazna,menjaće boju uljubičasto.
| Fenolftalein(pH indikator) | ||
| ispod pH 8.2 | iznad pH 10.0 | |
| bezbojan | ⇌ | fuksija |
Fenolftalein je bio korišten duže od jednog veka kaolaksativ,ali se sad uklanja sa tržišta laksativa[2]zbog zabrinutosti okokarcinogenosti.[3][4]
- ↑Rajković M. B. i saradnici (1993).Analitička hemija.Beograd: Savremena administracija.
- ↑Spiller, Ha; Winter, Ml; Weber, Ja; Krenzelok, Ep; Anderson, Dl; Ryan, Ml (May 2003), „Skin breakdown and blisters from senna-containing laxatives in young children”,The Annals of pharmacotherapy37(5): 636–9,DOI:10.1345/aph.1C439,ISSN1060-0280,PMID12708936
- ↑June K. Dunnick and James R. Hailey (November 1, 1996),„Phenolphthalein Exposure Causes Multiple Carcinogenic Effects in Experimental Model Systems”,Cancer Research56(21): 4922–4926,PMID8895745
- ↑Tice, Rr; Furedi-Machacek, M; Satterfield, D; Udumudi, A; Vasquez, M; Dunnick, Jk (1998), „Measurement of micronucleated erythrocytes and DNA damage during chronic ingestion of phenolphthalein in transgenic female mice heterozygous for the p53 gene.”,Environmental and molecular mutagenesis31(2): 113–24,DOI:10.1002/(SICI)1098-2280(1998)31:2<113::AID-EM3>3.0.CO;2-N,ISSN0893-6692,PMID9544189
