Lipidi

Lipidi(masti)sujedinjenjalepe supstancevodi,a rastvorna u organskimrastvaračima.Biološkisu veoma značajna jedinjenja. Oni su osnovna komponenta biološkihmembranai utiču na njihovu propustljivost, učestvuju u predajunervihimpulsa,stvaraju kontakte međućelijama,čine energetske rezerve, štiteorganizamod mehaničkih povreda i formiraju termoizolacionu sloj.
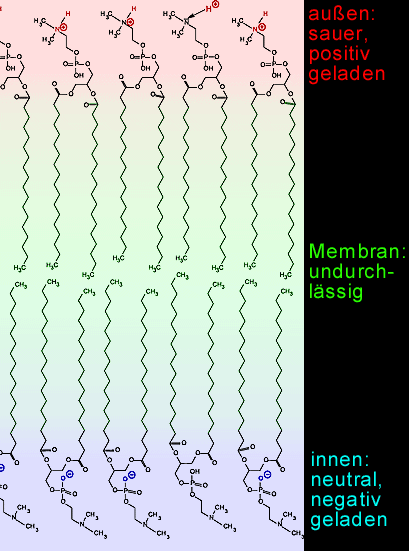
Zbog specifične hemijske strukture, lipidi se sastoje od nepolarnog i polarnog dela.
Lipide karakterizira velika grupa raznorodnih jedinjenja sa zajedničkom odlikom – nerastvorljivost u vodi, a rastvorljivosti u organskim otapalima:benzolu,hloroformu,acetonu,vrelomalkoholu.Inače u biljnim i životinjskim organizmima učestvtvuju kao gradivne i rezervne matetije. Umetabolizmulipida značajnu ulogu ima aktiviranasirćetna kiselina(ili acetil-koenzim-acetil-KoA). Prema strukturnoj organizaciji, masti se dijele na:
- proste i
- složene masti.[4]
Prosti lipidi su estri trihidroksilnog alkohola (glicerola) i masnih kiselina (oleinske, pamitinske i stearinske). Čvrste n1asti (loj) čini spoj glicerola sa zasićenom palmitinskom (C16H36O2) iii stearinskom (C18H36O2) kiselinom. Za razliku od njih, u sastav tečnih masti ili ulja ulazi oleinska (C17H34O2). Proste masti sa vodom tvore nestabilne emulzije.
Zagrijavanjem masti u prisustvu lužina (NaOHiliKOH) dolazi do saponifikacije, čime se dobijaju jedinjenjasapuna(koja su topiva u vodi). Procesom saponifikacije masti se razgrađuju na glicerol i masne kiseline. Uvođenjemvodikau nezasićene masne kiseline (procesomhidrogenizacije), one prelaze u zasićene sa izmijenjenim mirisom i okusom. Zahvaljujući primjeni ovog postupka, u industriji se razvio postupak pravljenja margarina i biljnog masla.
Lipidi, kao rezervnu organsku tvar, karaktetizira velika energetska vrijednost, a počinju se trošiti samno u nedostatku glukoze. Zato se suvišakugljikohidratau organizmu pretvara u masti i skladišti u različitim organima (kod životinja, npr. najčešće se odlažuu potkožno). Takav slučaj je posebno značajan kod ptica selica i zivotinja sa sezonskom dinmnikom zimskog sna.
Voskovi,za razliku od glicetida, umjesto glicerola sadrže dugolančane jednovalentne alkohole. Poredalkohola,sadrže i više masne kiseline. Zastupljeni su u biljkama i životinjama. Nisu rastvorljivi u vodi, već u organskim otapalima. Među poznatijim supstancmna ove skupine su: pčelinji vosak, spermacet ilanolin.
U složene lipide ubrajaju sefosfolipidi,glikolipidiilipoproteini.Izgrađene su od glicerola, masnih kiselina i fosforne kiseline.[4]
Od poznatijih fosfolipida, najčešći sulecitin,kefalin,plazmalogeni lizofosfolipid. Fosfolipidi čine temeljnu kotmponentu žive ćelijske membrane i ostalih ćelijskih uldopina. Odvijanje normalnih životnih procesa u organizmu, vezano je za specificne funkcije složenih lipida. Tako je za kontrahiranje glatke muskulature neophodan medijatoracetilholin.On takoder ima poseban značaj u podraživanju parasimpatičkih nerava, te snižavanju krvnog pritiska. Fosfolipidi takoder učestvuju u penneabilnosti ćelijske (žive) membrane, posebno pri prijenosu jona Na+ i K, u srčanotn mišiču (miokardu), dok od nekih drugih zavisi permeabilnost membranemitohondrija. Lizofosfatidi izazivaju hemolizu (razgradnju)eritrocita.U zmijskom otrovu nalazi se fosfolipaza A, zbog čega nakon ujeda dolazi do hemolize eritrocita.
Glikolipidi obuhvataju cerebrozide, gangliozide, sulfatide itd. Cerebrozidi su prvi put izolirani iz mozga (cerebrum), po čemu su i dobili ime. Gangliozidi su izolirani iz ganglijskih ćelija mozga (sive mase). Sulfatidi su jedinjenja složenih lipida izolirana izjetreibubrega,a relativno visokim sadržajetn ovih glikolipida obogaćen je imozak.Sva ova jedinjenja u organizmima životinja imaju vrlo specifične i značajne funkcije.[4]
Prosti lipidisusupstancečiji semolekulisastoje samo od ostatakamasnih kiselinaialkohola(najčešćeglicerola). Ovde spadaju masti iulja(trigliceridi) ivoskovi.
Složeni lipidiuključuju derivatefosforne kiseline(fosfolipidi) i lipide koji sadrže ostatkeugljenih hidrata(glikolipidi). Ovde spadaju isteroidi.
Ako se životinjska ili biljnatkivatretiraju organskim rastvaračima, deo će se rastvoriti. Komponente rastvora se nazivaju lipidi. Lipidna frakcija sadrži supstance različitih tipova.
Masne kiseline spadaju u alifatičnekarboksilnee kiseline.Iz lipida je izolovano više od 70 raznih masnih kiselina. Dele se nazasićeneinezasićene.Prirodne masne kiseline sadrže paran brojCatoma,a niz nije razgranat, već je normalan. Ispod su nabrojane neke od najvažnijih masnih kiselina (masne se zovu zato što se nalaze u mastima):
- Maslačna kiselina(butanska): CH3(CH2)2COOH ili C4:0
- Kapronska kiselina(heksanska): CH3(CH2)4COOH ili C6:0
- Kaprilna kiselina(oktanska): CH3(CH2)6COOH ili C8:0
- Kaprinska kiselina(dekadska): CH3(CH2)8COOH ili C10:0
- Laurinska kiselina(dodekadska): CH3(CH2)10COOH ili C12:0
- Miristinska kiselina(tetradekadska): CH3(CH2)12COOH ili C14:0
- Palmitinska kiselina(heksadekadska): CH3(CH2)14COOH ili C16:0
- Stearinska kiselina(oktadekadska): CH3(CH2)16COOH ili C18:0
Najvažnije prirodne masne kiseline sadrže 16 ili 18 C atoma. Nezasićene masne kiseline obično sadrže dvostruke veze između C9 i C10. Ostale dvostruke veze nisu konjugovane i nalaze se prema CH3- kraju niza. Imajucis- konfiguraciju, a veoma retkotrans.Masne kiseline sa većim brojem C atoma su praktično nerastvorne u vodi. NjihoveNaiK- soli se zovusapuni.One obrazujumiceleu vodi kod kojih he negativan COO- kraj okrenut ka vodi, a nepolaran C- niz je okrenut ka unutrašnjosti micele. U celini micele su naelektrisane negativno i u rastvoru ostaju suspendovane jer se međusobno odbijaju.
Neutralne masti (gliceridi) (acilgliceridi)suestriglicerola (glicerina) i masnih kiselina. U odnosu na broj estarskih veza u molekulu razlikuju semonogliceridi,digliceridiitrigliceridi(odnosno, monoacilglicerini, diacilglicerini i triacilglicerini).
Masti se u organizmima nalaze kao protoplazmatične masti (u određenoj količini) i kao rezervne masti (u neodređenoj količini). Osnovnu masu masti čine trigliceridi. Ako su sva tri kiselinska ostatka ista, prosti trigliceridi (na primer, tripalmatin), a ako su ostaci od od različitih kiselina, mešoviti trigliceridi. Kod davanja naziva, cifre ukazuju na kome se C atomu nalazi odgovarajući kiselinski ostatak (na primer. 1-oleo-2-pal-mitostearin).
Ukoliko su kiselinski ostaci duži, utoliko raste itačka topljenja.Ako su kiseline nezasićene, tačka topljenja sa brojem dvostrukih veza opada. Životinjske masti sadrže znatnu količinu zasićenih masnih kiselina (naročitostearinskuipalmitinsku) pa su na sobnojtemperaturičvrste. Ako se u molekulu nalazi dosta nezasićenih kiselina to su onda ulja, koja su na sobnoj temperaturi tečna (maslinovo ulje,sojino,suncokretovo,uljeuljane repice). Mast kod ljudi ima tačku topljenja 15 C i sadrži 70% oleinske kiseline.
Gliceridi raguju kao estri, a posebno je važna reakcijahidrolize,pri čemu se izdvaja glicerin i masne kiseline. Hidroliza se može vršitienzimskiili dejstvomkiselinailibaza.Bazna hidroliza sanatrijum hidroksidom(NaOH) ili sakalijum hidroksidom(KOH) se koristi za proizvodnju sapuna (reakcijasaponifikacije,sapo-sapun).
Masti sadrže razne primese koje se uklanjaju, a zaostaje tzv. neutralna mast. Ona se karakteriše:
- jodnim brojem (broj gramajodakoga vezuje 100 g masti pod određenim uslovima i koji karakteriše stepen nezasićenosti. Jodni broj svinjske masti je 46-66, a maslinovog ulja oko 85).
- kiselinski broj (broj mg KOH potreban zaneutralizaciju1 g masti i koji ukazuje na količinu slobodnih masnih kiselina u masti).
- saponifikacioni broj (broj mg KOH potreban za neutralizaciju svih kiselina – i slobodnih i vezanih u trigliceride – u 1 g masti).
Voskovisu estri viših masnih kiselina i viših alkohola sa 20 do 70 C atoma u molekulu. Oni se nalaze u sastavu masti koja pokrivakožu,vunu,perje.Kod biljaka su 80% svih lipida voskovi koji stvaraju zaštitni sloj na površini biljke i štite je odispravanjavode.
Prirodni vosak (pčelinji,lanolin) pored pomenutih estara sadrži i malu količinu slobodnih masnih kiselina, nekih alkohola iugljovodonika,sa 20-35 C atoma u molekulu.
Fosfolipidi ili fosfatidise dele naglicerofosfolipideisfingolipide.
Glicerofosfolipidesu derivati fosfatidne kiseline i sadrže glicerol, masne kiseline, fosfatidnu kiselinu iazotnajedinjenja. Njihova opšta formula je:
gde su R i R' ostaci viših masnih kiselina, a R "je ostatak nekog azotnog jedinjenja ifosforne kiseline.
Jedan deo molekula (R i R') je jako hidrofoban, a drugi deo je hidrofilan (negativnonaelektrisanjeu fosfornoj kiselini i pozitivno naelektrisanje azotnogjedinjenja– R "). Od svih lipida glicerofosfolipidi su najpolarniji, a u vodenoj sredini se nalazi u oblikumicela.Ima nekoliko grupa glicerofosfolipida:
- Fosfatidilholini, lecitinisadrže glicerol, više masne kiseline, fosfornu kiselinu iholin:
- Fosfatidiletanolamini, kefaliniumesto holina sadržeetanolamin:
Gornje dve grupe su glavna lipidna komponenta membrane ćelija.
- Fosfatidilserinikao azotna jedinjenja sadrže ostatak serina:
Od masnih kiselina koje ulaze u sastav glicerofosfolipida najčešće su stearinska, palmitinska, oleinska i linolenska. Pri njihovoj hidrolizi (otrovkobre) izdavaja se ostatak nezasićene masne kiseline, a preostalo jedinjenje ima jakohemolitičkodejstvo.
Sfingolipidine sadrže glicerol već alkoholsfingozin:
Najčešće su sfingomijelini koji se nalaze u membranama ćelija i to posebnonervih.Hidrolizom daju jedan molekul masne kiseline, jedan molekul nezasićenog dvovalentnog alkohola sfingozina, jedan molekul azotnog jedinjenja (najčešće holina) i jedan molekul fosforne kiseline. Hemijska formula sfingomijelina data je ispod:
Polarni deo je naelektrisan i pozitivno (holin) i negativno (ostatak fosforne kiseline), a ostali deo molekula je nepolaran.
Glikolipidisu složeni lipidi koji sadrže ostatakugljenih hidrata(najčešćeD-galaktoze). Bitni su za rad bioloških membrana. Nalaze se umozguikrvi.Dele se ne dve grupe:
- Cerebrozidisadržeheksozu(čestoD-galaktozu) vezanuetarskomvezom sa sfingozinom, a sadrže i neku masnu kiselinu sa 24 C atoma (lignocerinska,cerebronska):
Mnogo cerebrozida se nalazi u membranama nervnih ćelija.
- Gangliozidihidrolizom daju višu masnu kiselinu, sfingozin, D-glukozu, D-galaktozu kao i derivateaminošećera:N-acetilglukozaminiN-acetilneuraminsku kiselinu.Nalaze se pretežno u sivoj kori mozga i membranama nervih ćelija.
Svi gore pomenuti lipidi spadaju u saponifikujuće lipide jer pri njihovoj baznoj hidrolizi nastaju sapuni. Postoje i lipidi koji se ne hidrolizuju uz oslobađanje masnih kiselina. U tu grupu spadajusteroidi.
Eukariotske ćelije su kompartmentalizovane uorganeleobavijene membranama, koje vrše različite biološke funkcije.Glicerofosfolipidisu glavna strukturna komponentabioloških membrana,kao što sućelijska membranai intraćelijske membraneorganela;u životinjskim ćelijama membrane fizički odvajajuintraćelijskekomponente od ekstracelularnog okruženja. Glicerofosfolipidi suamfipatičkimolekuli (sadržehidrofobneihidrofilneregione) koji imaju glicerolno jezgro vezano sa dve masne kiselineestarskimvezama, i za jednu „čeonu “grupu putemfosfatneestarske veze. Dok su glicerofosfolipidi glavne komponente bioloških membrana, druge negliceridne lipidne komponente kao što susfingomijelinisteroli(uglavnomholesterolu životinjskim ćelijskim membranama) su isto tako prisutni u biološkim membranama.[5]Kod biljki i algi galaktozildiacilgliceroli[6]i sulfohinovozildiacilglicerol,[7]kojima nedostaje fosfatna grupa, su važne komponente membranahloroplastai srodnih organela i najzastupljeniji su lipidi u fotosintetičkim tkivima, uključujući ona kod viših biljki, algi i pojedinih bakterija.
Najveća lipidna komponenta biljnetilakoidnemembrane je monogalaktozil diglicerid (MGDG) koji obično ne formira dvosloj, dok su fosfolipidi prisutni u manjoj meri. Uprkos toj jedinstvenoj lipidnoj kompoziciji, za hloroplastne tilakoidne membrane je putem magnetne rezonance i elektronske mikroskopije pokazano da sadrže dinamičku lipidni dvoslojnu matricu.[8]
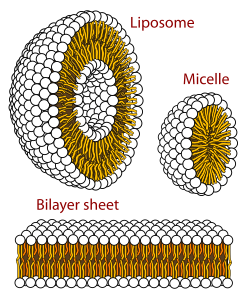
Biološka membrana je formalamelarne fazelipidnog dvosloja.Formiranje lipidnog dvosloja je energetski preferentan proces kad su gore opisaniglicerofosfolipidiu vodenom okruženju.[9]To je poznato kao hidrofobni efekat. U vodenoj sredini, polarne glave lipida se poravnavaju ka polarnom, vodenom okruženju, dok hidrofobni repovi minimizuju svoj kontakt sa vodom i grupišu se zajedno, formirajućivezikule;u zavisnosti odkoncentracijelipida, ta biofizička interakcija može da dovede do formiranjamicela,lipozoma,ililipidnih dvosloja.Drugi oblici agregacije su isto tako primećeni i formiraju deo polimorfizmaamfifilnog(lipidnog) ponašanja.Fazno ponašanjeje oblast izučavanja u okvirubiofizikei predmet je tekućih akademskih istraživanja.[10][11]Micele i dvoslojevi se formiraju u polarnom medijumu procesu poznatom kaohidrofobni efekat.[12]Pri rastvaranju lipofilne ili amfifilne supstance u polarnoj sredini, polarni molekuli (i.e., voda u vodenim rastvorima) postaju u većoj meri uređeni oko rastvorene lipofilne supstance, pošto polarni molekuli ne mogu da formirajuvodonične vezesa lipofilnim oblastimaamfifila.Stoga u vodenom okruženju, molekuli vode formiraju uređene "klatratne"kaveze oko rastvorenih lipofilnih molekula.[13]
Organizovanje lipida uprotoćelijskemembrane je ključni korak u modelimaabiogeneze,porekla života.[14]
Trigliceridi,uskladišteni uadipoznom tkivu,su glavna forma energetskog skladišta kod životinja i biljki.Adipocit,ili masna ćelija, je dizajniran za kontinuiranu sintezu i razlaganje triglicerida kod životinja, pri čemu se razlaganje uglavnom aktivira enzimima senzitivnim nahormone,lipazama.[15]Kompletna oksidacijamasnih kiselinapruža visok kalorijski sadržaj, oko 9kcal/g,u poređenju sa 4 kcal/g za razlaganjeugljenih hidrataiproteina.Migratorne ptice mogu da lete preko velikih rastojanja bez konzumiranja hrate koristeći energiju sačuvanu u obliku triglicerida kao gorivo za svoj let.[16]
Zadnjih godina je postalo jasno da jelipidna signalizacijavitalni deoćelijske signalizacije.[17][18]Lipidna signalizacija se može odvijati putem aktivacijeG protein spregnutihilinuklearnih receptora,i članovi nekoliko različitih kategorija lipida su identifikovani kao signalni molekuli ićelijski glasnici.[19]Među njima susfingozin-1-fosfat,sfingolipid izveden iz keramida koji je potentan glasnički molekul koji učestvuje u regulaciji kalcijumske mobilizacije,[20]u ćelijskom rastu, i apoptozi;[21]diacilglicerol(DAG) ifosfatidilinozitolfosfati (PIP), koji učestvuju u kalcijumom posredovanoj aktivacijiproteinske kinaze C;[22]prostaglandini,koji su jedan od tipova iz masnih kiselina izvedenih eikosanoida koji učestvuju uinflamacijiiimunosti;[23]steroidni hormoni kao što suestrogen,testosteronikortizol,koji modulišu domaćinove funkcije reprodukcije, metabolizma i krvnog pritiska; ioksisterolikao što je 25-hidroksi-holesterol koji jeagonistjetrenog X receptora.[24]Poznato je da fosfatidilserinski lipidi učestvuju u signalizaciji fagocitoze apoptotičkih ćelija i/ili delova ćelija. Oni ostvaruju taj cilj tako što su izloženi na ekstracelularnom licu ćelijske membrane nakon inaktivacije flipaza koje ih ekskluzivno postavljaju na citozolnu stranu i aktivacije skramblaza, koje izokreću orijentaciju fosfolipida. Nakon toga druge ćelije prepoznaju fosfatidilserine i fagocitoziraju ćelije ili ćelijske fragmente koji ih izlažu.[25]
Vitamini rastvorni u mastima (A,D,EiK) – koji su na izoprenu bazirana jedinjenja – su esenicjalni nutrijenti koji se čuvaju u jetri i masnim tkivima, sa raznovrsnim opsegom funkcija.Acil-karnitiniučestvuju u transportu i metabolizmu masnih kiselina „u i iz “mitohondrija, gde oni podležubeta oksidacijii.[26]Poliprenoli i njihovi fosforilisani derivati takođe imaju važnu transportne uloge, u tom slučaju u transportuoligosaharidakroz membrane. Poliprenolni fosfatni šećeri i poliprenolni difosfatni šećeri uzimaju učešća u reakcijama glikozilacije izvan citoplazme, u biosintezi ekstracelularnih polisaharida (na primer,peptidoglikanskojpolimerizaciji kod bakterija), i u N-glikozilacijieukariotskih proteina.[27][28]Kardiolipinisu potklasa glicerofosfolipida koji sadrže četiri acilna lanca i tri glicerolne grupe, koja je posebno izobilna u unutrašnjoj mitohondrijskoj membrani.[29][30]Smatra se da oni aktiviraju enizme koji učestvuju uoksidativnoj fosforilaciji.[31]Lipidi isto tako formiraju osnovu steroidnih hormona.[32]
Glavni prehrambeni lipidi kod ljudi i životinja su biljni trigliceridi, steroli, i membranski fosfolipidi. Procesom lipidnog metabolizma se sintetišu i degradiraju uskladišteni lipidi i proizvode se strukturni i funkcionalni lipidi karakteristični za pojedinačna tkiva.
Kod životinja, kad postoji višak ponude prehrambenih ugljenih hidrata, suvišni ugljeni hidrati se konvertuju u trigliceride. Taj proces obuhvata sintezu masnih kiselina iz acetil-KoA i esterifikaciju masnih kiselina radi produkcije triglicerida. Ovaj proces se nazivalipogeneza.[33]Masne kiseline se formirajusintezom masnih kiselina,kojom se polimerizuju i zatim redukuju acetil-KoA jedinice. Acilni lanci masnih kiselina se produžavaju ciklusom reakcija koje dodaju acetil grupu, redukuju je do alkohola,dehidratišualkohol doalkenskegrupe i zatim se ponovo vrši redukcija doalkanskegrupe. Enzimi masno kiselinske biosinteze se dele u dve grupe, kod životinja i gljiva sve reakcije sinteze masnih kiselina se izvode posredstvom jednog multifunkcionalnog proteina,[34]dok u biljnimplastidimai bakterijama zasebni enzimi vrše svaki korak tog procesa.[35][36]Masne kiseline se mogu naknadno konvertovati do triglicerida koji se pakuju ulipoproteinimai izlučuju iz jetre.
Sinntezanezasićenih masnih kiselineobuhvata reakcijudesaturacije,pri čemu se dvostruka veza uvodi u masni acilni lanac. Na primer, kod ljudi, desaturacijastearinske kiselineposredstvom enzimastearoil-CoA desaturaza-1proizvodioleinsku kiselinu.Dvostruko nezasićena masna kiselinalinoleinska kiselina,kao i trostruko nezasićenaα-linoleinska kiselinase ne mogu sintetisati u tkivima sisara, i stoga suesencijalne masne kiselinei moraju se unositi kao hrana.[37]
Trigliceridna sinteza se odvija uendoplazmatičnom retikulumuputem metaboličkih puteva u kojima se acilne grupe u masnim acil-KoA molekulima prenose na hidroksine grupe glicerol-3-fosfata i diacilglicerola.[38]
Terpeniiizoprenoidi,uključujućikarotenoide,se formiraju putem pravljenja i modifikacijeizoprenskihjedinica iz reaktivnih prekursoraizopentenil pirofosfataidimetilalil pirofosfata.[39]Ti prekursori mogu da budu napravljeni na različite načine. Kod životinja iarheja,mevalonatni putemse formiraju ta jedinjenja iz acetil-KoA,[40]dok se u biljkama i bakterijama unemevalonatnom putukoriste pyruvat igliceraldehid 3-fosfatkao supstrati.[39][41]Jedna važna reakcija koja koristi te aktivirane izoprenske donore jesteroidna biosinteza.Ovde se izoprenske jedinice spajaju da bi se formiraoskvaleni zatim se savijaju da bi nastala grupa prstenova koji sačinjavajulanosterol.[42]Lanosterol se može dalje konvertovati u druge steroide kao što jeholesteroliergosterol.[42][43]
Beta oksidacijaje metabolički proces kojim se masne kiseline razlažu umitohondrijamai/ili uperoksizomimada bi se formiraoacetil-KoA.Najvećim delom, masne kiseline se oksiduju putem mehanizma koji je sličan sa, mada ne i identičan sa, reverznim procesom sinteze masnih kiselina. Drugim rečima, dvougljenični fragmenti se uklanjaju sekvencijalno sa karboksilnog kraja kiseline nakon korakadehidrogenacije,hidracije,ioksidacijeuz formiranjebeta-keto kiseline,koje se odvajatiolizom.Acetil-KoA se zatim ultimatno konvertuje uATP,CO2,i H2O koristećiciklus limunske kiselineilanac elektronskog transporta.Ciklus limunske kiseline može da počne od acetil-KoA kad se masnoća razlaže radi energije, ako je prisutno malo ili je odsutna glukoza. Energetski prinos od kompletne oksidacije masne kiseline palmitata je 106 ATP.[44]Za degradaciju nezasićenih i neparnih masnih kiselina neophodni su dodatni enzimatski procesi.
- ↑Maitland, Jr Jones (1998).Organic Chemistry.W W Norton & Co Inc (Np). str. 139.ISBN978-0-393-97378-5.
- ↑Stryeret al.,p. 328.
- ↑Stryeret al.,p. 330.
- ↑4,04,14,2Međedović S., Maslić E., Hadžiselimović R. (2002).Biologija 2..Svjetlost, Sarajevo.ISBN9958-10-222-6.
- ↑Stryeret al.,pp. 329–331.
- ↑Heinz E. (1996). "Plant glycolipids: structure, isolation and analysis", pp. 211–332 inAdvances in Lipid Methodology,Vol. 3. W.W. Christie (ed.). Oily Press, Dundee.ISBN978-0-9514171-6-4
- ↑Hölzl G, Dörmann P. (2007). „Structure and function of glycoglycerolipids in plants and bacteria”.Progress in Lipid Research46(5): 225–243.DOI:10.1016/j.plipres.2007.05.001.PMID17599463.
- ↑Yashroy RC. (1990). „Magnetic resonance studies of dynamic organisation of lipids in chloroplast membranes”.Journal of Biosciences15(4): 281–288.DOI:10.1007/BF02702669.
- ↑Stryeret al.,pp. 333–334.
- ↑van Meer G, Voelker DR, Feigenson GW. (2008).„Membrane lipids: where they are and how they behave”.Nature Reviews Molecular Cell Biology9(2): 112–124.DOI:10.1038/nrm2330.PMC2642958.PMID18216768.
- ↑Feigenson GW. (2006).„Phase behavior of lipid mixtures”.Nature Chemical Biology2(11): 560–563.DOI:10.1038/nchembio1106-560.PMC2685072.PMID17051225.
- ↑Wiggins PM. (1990).„Role of water in some biological processes”.Microbiological Reviews54(4): 432–449.PMC372788.PMID2087221.
- ↑Raschke TM, Levitt M. (2005).„Nonpolar solutes enhance water structure within hydration shells while reducing interactions between them”.Proceedings of the National Academy of Sciences of the United States of America102(19): 6777–6782.DOI:10.1073/pnas.0500225102.PMC1100774.PMID15867152.
- ↑Segré D, Ben-Eli D, Deamer D, Lancet D. (2001).„The Lipid World”(PDF).Origins of Life and Evolution of Biospheres31(1–2): 119–145.DOI:10.1023/A:1006746807104.PMID11296516.Arhivirano izoriginalana datum 2008-09-11.Pristupljeno 2015-05-03.
- ↑Brasaemle DL. (2007).„Thematic review series: adipocyte biology. The perilipin family of structural lipid droplet proteins: stabilization of lipid droplets and control of lipolysis”.Journal of Lipid Research48(12): 2547–2559.DOI:10.1194/jlr.R700014-JLR200.PMID17878492.
- ↑Stryeret al.,p. 619.
- ↑Wang X. (2004). „Lipid signaling”.Current Opinion in Plant Biology7(3): 329–236.DOI:10.1016/j.pbi.2004.03.012.PMID15134755.
- ↑Dinasarapu AR, Saunders B, Ozerlat I, Azam K, Subramaniam S. (2011).„Signaling gateway molecule pages—a data model perspective”.Bioinformatics27(12): 1736–1738.DOI:10.1093/bioinformatics/btr190.PMC3106186.PMID21505029.
- ↑Eyster KM. (2007). „The membrane and lipids as integral participants in signal transduction”.Advances in Physiology Education31(1): 5–16.DOI:10.1152/advan.00088.2006.PMID17327576.
- ↑Hinkovska-Galcheva V, VanWay SM, Shanley TP, Kunkel RG. (2008). „The role of sphingosine-1-phosphate and ceramide-1-phosphate in calcium homeostasis”.Current Opinion in Investigational Drugs9(11): 1191–1205.PMID18951299.
- ↑Saddoughi SA, Song P, Ogretmen B. (2008).„Roles of bioactive sphingolipids in cancer biology and therapeutics”.Subcellular Biochemistry.Subcellular Biochemistry49:413–440.DOI:10.1007/978-1-4020-8831-5_16.ISBN978-1-4020-8830-8.PMC2636716.PMID18751921.
- ↑Klein C, Malviya AN. (2008). „Mechanism of nuclear calcium signaling by inositol 1,4,5-trisphosphate produced in the nucleus, nuclear located protein kinase C and cyclic AMP-dependent protein kinase”.Frontiers in Bioscience13(13): 1206–1226.DOI:10.2741/2756.PMID17981624.
- ↑Boyce JA. (2008). „Eicosanoids in asthma, allergic inflammation, and host defense”.Current Molecular Medicine8(5): 335–349.DOI:10.2174/156652408785160989.PMID18691060.
- ↑Bełtowski J. (2008). „Liver X receptors (LXR) as therapeutic targets in dyslipidemia”.Cardiovascular Therapy26(4): 297–316.DOI:10.1111/j.1755-5922.2008.00062.x.PMID19035881.
- ↑Biermann M, Maueröder C, Brauner JM,Chaurio R, Janko C, Herrmann M, Muñoz LE. (2013). „Surface code—biophysical signals for apoptotic cell clearance”.Physical Biology10(6): 065007.DOI:10.1088/1478-3975/10/6/065007.PMID24305041.
- ↑Indiveri, C; Tonazzi, A; Palmieri, F (1991). „Characterization of the unidirectional transport of carnitine catalyzed by the reconstituted carnitine carrier from rat liver mitochondria”.Biochimica et biophysica acta1069(1): 110-6.PMID1932043.
- ↑Parodi AJ, Leloir LF. (1979). „The role of lipid intermediates in the glycosylation of proteins in the eucaryotic cell”.Biochimica et Biophysica Acta559(1): 1–37.DOI:10.1016/0304-4157(79)90006-6.PMID375981.
- ↑Helenius A, Aebi M. (2001). „Intracellular functions of N-linked glycans”.Science291(5512): 2364–2369.DOI:10.1126/science.291.5512.2364.PMID11269317.
- ↑Nowicki M, Frentzen M. (2005). „Cardiolipin synthase ofArabidopsis thaliana”.FEBS Letters579(10): 2161–2165.DOI:10.1016/j.febslet.2005.03.007.PMID15811335.
- ↑Gohil VM, Greenberg ML. (2009).„Mitochondrial membrane biogenesis: phospholipids and proteins go hand in hand”.Journal of Cell Biology184(4): 469–472.DOI:10.1083/jcb.200901127.PMC2654137.PMID19237595.
- ↑Hoch FL. (1992). „Cardiolipins and biomembrane function”.Biochimica et Biophysica Acta1113(1): 71–133.DOI:10.1016/0304-4157(92)90035-9.PMID10206472.
- ↑SteroidsArhivirano2011-10-23 naWayback Machine-u.Elmhurst.edu. Retrieved on 2013-10-10.
- ↑Stryeret al.,p. 634.
- ↑Chirala S, Wakil S. (2004).„Structure and function of animal fatty acid synthase”.Lipids39(11): 1045–1053.DOI:10.1007/s11745-004-1329-9.PMID15726818.
- ↑White SW, Zheng J, Zhang YM, Rock CO. (2005).„The structural biology of type II fatty acid biosynthesis”.Annual Review of Biochemistry74:791–831.DOI:10.1146/annurev.biochem.74.082803.133524.PMID15952903.
- ↑Ohlrogge J, Jaworski J. (1997). „Regulation of fatty acid synthesis”.Annual Review of Plant Physiology and Plant Molecular Biology48:109–136.DOI:10.1146/annurev.arplant.48.1.109.PMID15012259.
- ↑Stryeret al.,p. 643.
- ↑Stryeret al.,pp. 733–739.
- ↑39,039,1Kuzuyama T, Seto H. (2003). „Diversity of the biosynthesis of the isoprene units”.Natural Product Reports20(2): 171–183.DOI:10.1039/b109860h.PMID12735695.
- ↑Grochowski L, Xu H, White R. (2006).„Methanocaldococcus jannaschiiuses a modified mevalonate pathway for biosynthesis of isopentenyl diphosphate”.Journal of Bacteriology188(9): 3192–3198.DOI:10.1128/JB.188.9.3192-3198.2006.PMC1447442.PMID16621811.
- ↑Lichtenthaler H. (1999). „The 1-dideoxy-D-xylulose-5-phosphate pathway of isoprenoid biosynthesis in plants”.Annual Review of Plant Physiology and Plant Molecular Biology50:47–65.DOI:10.1146/annurev.arplant.50.1.47.PMID15012203.
- ↑42,042,1Schroepfer G. (1981).„Sterol biosynthesis”.Annual Review of Biochemistry50:585–621.DOI:10.1146/annurev.bi.50.070181.003101.PMID7023367.
- ↑Lees N, Skaggs B, Kirsch D, Bard M. (1995).„Cloning of the late genes in the ergosterol biosynthetic pathway ofSaccharomyces cerevisiae—a review”.Lipids30(3): 221–226.DOI:10.1007/BF02537824.PMID7791529.
- ↑Stryeret al.,pp. 625–626.
- Grupa autora (2006). Nenad Ugrešić. ur.Farmakoterapijski vodič 3.Beograd. ISSN 1451-4680.Arhiviranoiz originala na datum 2011-07-15.Pristupljeno 2021-08-30.
- Darinka Koraćević, Gordana Bjelaković, Vidosava Đorđević.Biohemija.Savremena administracija.ISBN978-86-387-0622-8.
- Šerban, Nada M. (2010).Biologija 1.Beograd: ZUNS. str. 11.ISBN978-86-17-17585-4.
- Bhagavan NV (2002).Medical Biochemistry.San Diego: Harcourt/Academic Press.ISBN978-0-12-095440-7.
- Devlin TM (1997).Textbook of Biochemistry: With Clinical Correlations(4th izd.). Chichester: John Wiley & Sons.ISBN978-0-471-17053-2.
- Stryer L, Berg JM, Tymoczko JL (2007).Biochemistry(6th izd.). San Francisco: W.H. Freeman.ISBN978-0-7167-8724-2.
- van Holde KE, Mathews CK (1996).Biochemistry(2nd izd.). Menlo Park, California: Benjamin/Cummings Pub. Co.ISBN978-0-8053-3931-4.
- Georg Löffler, Petro E. Petrides:Biochemie und Pathobiochemie.Springer, Berlin 2003,ISBN3-540-42295-1
- Florian Horn, Isabelle Moc, Nadine Schneider:Biochemie des Menschen.Thieme, Stuttgart 2005,ISBN3-13-130883-4
- Charles E. Mortimer, Ulrich Müller:Chemie.Thieme, Stuttgart 2003,ISBN3-13-484308-0
- F.D. Gunstone, J.L. Harwood, F.B. Padley:The Lipid Handbook.Chapman and Hall, London New - York 1986,ISBN0-412-24480-2.
- O.W. Thiele:Lipide, Isoprenoide mit Steroiden.G. Thieme Verlag, Stuttgart 1979,ISBN3-13-576301-3.
- Robert C. Murphy:Mass Spectrometry of Lipids,Handbook of Lipid Research Vol. 7, Plenum Press, New York and London, 1993,ISBN0-306-44361-9
- Julian N. Kanfer and Sen-itiroh Hakomori, Sphingolipid Biochemistry, vol. 3 of Handbook of Lipid Research (1983)
- Dennis E. Vance and Jean E. Vance (eds.), Biochemistry of Lipids and Membranes (1985).
- Donald M. Small, The Physical Chemistry of Lipids, vol. 4 of Handbook of Lipid Research (1986).
- Robert B. Gennis, Biomembranes: Molecular Structure and Function (1989)
- Charles R. Scriver, Arthur L. Beaudet, William S. Sly, and David Valle, The Metabolic and Molecular Bases of Inherited Disease (1995).
- Gunstone, F. D. Fatty acids and lipid chemistry. — London: Blackie Academic and Professional, 1996. 252 pp.
- Robert M. Bell, John H. Exton, and Stephen M. Prescott (eds.), Lipid Second Messengers, vol. 8 of Handbook of Lipid Research (1996).
- Christopher K. Mathews, K.E. van Holde, and Kevin G. Ahern, Biochemistry, 3rd ed. (2000).
- Alberts, B., et al. (2004) «Essential Cell Biology, 2nd Edition.» Garland Science.ISBN0-8153-3480-X
- Solomon, Eldra P., et. al. (2005) «Biology, 7th Edition.» Thomson, Brooks/Cole.
- «Advanced Biology — Principles and Applications.» C.J. Clegg and D.G. Mackean.ISBN0-7195-7670-9
- Fahy E. et al. A comprehensive classification system for lipids // J. Lipid. Res. 2005. V. 46, № 5. P. 839—861.
- ApolloLipids - Provides dyslipidemia and cardiovascular disease prevention and treatment information as well as continuing medical education programs.Arhivirano2005-07-20 naWayback Machine-u
- Lipids, Membranes and Vesicle Trafficking - The Virtual Library of Biochemistry and Cell Biology
- The Lipid library - provides information on the chemistry, analysis and biochemistry of lipids
- LIPID MAPS: LIPID Metabolites and Pathways Strategy
- IUPAC glossary entry for the lipid class of moleculeswhat is IUPAC?
- "A comprehensive classification system for lipids"Arhivirano2010-08-24 naWayback Machine-u
- CCMDWeb, a lipid health educational resource on global risk reduction for dyslipidemia and cardiovascular disease as well as online CME programs.Arhivirano2007-09-12 naWayback Machine-u
- European Federation for the Science and Technology of Lipids
- Genomics of Lipid-Associated Disorders(Seite der Technischen Universität Graz, u. a. mit einer Fülle von Lipid-Stoffwechselwegen)